名校
解题方法
1 . Ⅰ.下图为工业合成氨的流程图:
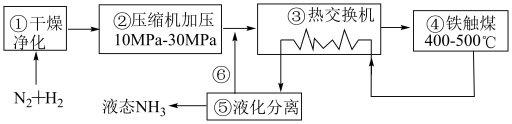
(1)⑥循环利用的物质是___________ ,①的气体若不进化,容易造成的问题是___________
(2)上述流程中能增加反应速率的是___________ ,能提高原料转化率的是___________ 。(填数字编号)
Ⅱ.某兴趣小组为研究“不同条件”对化学平衡的影响情况,进行了如下实验:(反应起始的温度和体积均相同):
(3)则:
___________  、
、
___________  (填“>”、“=”或“<”)
(填“>”、“=”或“<”)

(1)⑥循环利用的物质是
(2)上述流程中能增加反应速率的是
Ⅱ.某兴趣小组为研究“不同条件”对化学平衡的影响情况,进行了如下实验:(反应起始的温度和体积均相同):
| 序号 | 起始投入量 | 平衡转化率 | ||
 |  |  | ||
| ①恒温恒容 |  |  | 0 |  |
| ②绝热恒容 |  |  | 0 |  |
| ③恒温恒压 |  |  | 0 |  |
(3)则:

 、
、
 (填“>”、“=”或“<”)
(填“>”、“=”或“<”)
您最近一年使用:0次
名校
解题方法
2 . 工业上通过将CO、CO2与氢气反应,实现碳中和。
(1)已知反应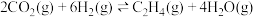
 ,在恒容密闭条件下,该反应达平衡时各组分的浓度随温度变化的曲线如图所示(某些曲线只画出了部分),回答下列问题:
,在恒容密闭条件下,该反应达平衡时各组分的浓度随温度变化的曲线如图所示(某些曲线只画出了部分),回答下列问题:
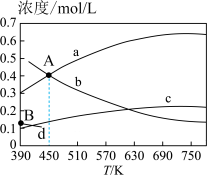
①该反应的平衡常数表达式为___________ 。
②图中曲线b、c分别表示的是平衡时___________ 和___________ 的浓度变化。
③已知坐标A(450,0.4),B(390,0.13),求450K时该反应的K=___________ 。(列出带数值的计算表达式即可,不需要算最终结果)
(2)用CO和H2合成CH3OH的反应为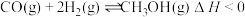 ,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图所示:
,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图所示:
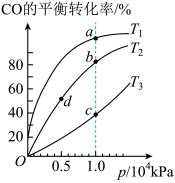
①图中T1、T2、T3的大小关系为___________ 。
②图中b、c点逆反应速率的大小关系为___________ 。
③图中b、c、d点平衡常数的大小关系为___________ 。
④若忽略坐标上的数值,横坐标表示温度,T1、T2、T3分别用P1、P2、P3替换,则纵坐标可以表示___________ ,P1、P2、P3的大小关系为___________ 。
(1)已知反应
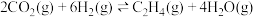
 ,在恒容密闭条件下,该反应达平衡时各组分的浓度随温度变化的曲线如图所示(某些曲线只画出了部分),回答下列问题:
,在恒容密闭条件下,该反应达平衡时各组分的浓度随温度变化的曲线如图所示(某些曲线只画出了部分),回答下列问题:
①该反应的平衡常数表达式为
②图中曲线b、c分别表示的是平衡时
③已知坐标A(450,0.4),B(390,0.13),求450K时该反应的K=
(2)用CO和H2合成CH3OH的反应为
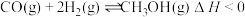 ,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图所示:
,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图所示:
①图中T1、T2、T3的大小关系为
②图中b、c点逆反应速率的大小关系为
③图中b、c、d点平衡常数的大小关系为
④若忽略坐标上的数值,横坐标表示温度,T1、T2、T3分别用P1、P2、P3替换,则纵坐标可以表示
您最近一年使用:0次
2023高三·全国·专题练习
3 . 无色气体N2O4是一种强氧化剂,为重要的火箭推进剂之一。N2O4与NO2相互转化的热化学方程式为N2O4(g)⇌2NO2(g) ΔH=+24.4 kJ/mol。
(1)将一定量N2O4投入固定容积的真空容器中,下列现象能说明反应达到平衡的是_______ (填字母)。
a.v正(N2O4)=2v逆(NO2)
b.体系颜色不变
c.气体平均相对分子质量不变
d.气体密度不变
(2)达到平衡后,保持体积不变,升高温度,再次达到平衡时,混合气体颜色_______ (填“变深”“变浅”或“不变”),判断理由是_______ 。
(3)平衡常数K可用反应体系中气体物质分压表示,即K表达式中用平衡分压代替平衡浓度,分压=总压×物质的量分数[例如:p(NO2)=p总×x(NO2)]。写出上述反应平衡常数表达式:Kp=_______ (用p总、各气体物质的量分数x表示);影响Kp的因素为_______ 。
(4)真空密闭容器中充入一定量N2O4,维持总压强p0恒定,在温度为T时,平衡时N2O4的分解百分率为α。保持温度不变,向密闭容器中充入等量的N2O4,维持总压强在2p0条件下分解,则平衡时N2O4的分解百分率为_______ (用α表示)。
(1)将一定量N2O4投入固定容积的真空容器中,下列现象能说明反应达到平衡的是
a.v正(N2O4)=2v逆(NO2)
b.体系颜色不变
c.气体平均相对分子质量不变
d.气体密度不变
(2)达到平衡后,保持体积不变,升高温度,再次达到平衡时,混合气体颜色
(3)平衡常数K可用反应体系中气体物质分压表示,即K表达式中用平衡分压代替平衡浓度,分压=总压×物质的量分数[例如:p(NO2)=p总×x(NO2)]。写出上述反应平衡常数表达式:Kp=
(4)真空密闭容器中充入一定量N2O4,维持总压强p0恒定,在温度为T时,平衡时N2O4的分解百分率为α。保持温度不变,向密闭容器中充入等量的N2O4,维持总压强在2p0条件下分解,则平衡时N2O4的分解百分率为
您最近一年使用:0次
名校
4 . 硝酸广泛用于化肥、化纤、医药、染料、橡胶等的制造,在国防工业、冶金工业、印染工业以及其他工业部门中,也是不可缺少的重要的化学试剂。
(1)工业生产中未直接在一个设备中将 催化氧化至
催化氧化至 ,而设计了两步氧化,中间经过热交换器降温,这样做的目的除了节约能源,还有
,而设计了两步氧化,中间经过热交换器降温,这样做的目的除了节约能源,还有_____ 目的;
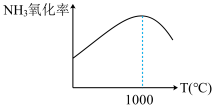
(2)实验发现,单位时间内 的氧化率[
的氧化率[ ]会随着温度的升高先增大后减小(如图所示),分析1000℃后
]会随着温度的升高先增大后减小(如图所示),分析1000℃后 的氧化率减小的可能原因
的氧化率减小的可能原因_____
(3) 的反应历程如下:
的反应历程如下:
反应Ⅰ: (快)
(快) 


反应Ⅱ: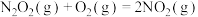 (慢)
(慢) 

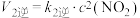
①一定条件下,反应 达到平衡状态,平衡常数
达到平衡状态,平衡常数
_____ (用含 、
、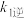 、
、 、
、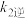 的代数式表示);
的代数式表示);
②已知反应速率常数k随温度升高而增大,则升高温度后 增大的倍数
增大的倍数_____ 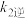 增大的倍数(填“大于”“小于”或“等于”)。
增大的倍数(填“大于”“小于”或“等于”)。
(Ⅱ)工业上也可以直接由 合成
合成 ,其中最关键的步骤为
,其中最关键的步骤为 ,利用现代手持技术传感器可以探究压强对该平衡的影响。
,利用现代手持技术传感器可以探究压强对该平衡的影响。
在恒定温度和标准压强条件下,往针筒中充入一定体积的 气体后密封并保持活塞位置不变。分别在
气体后密封并保持活塞位置不变。分别在 、
、 时迅速移动活塞后并保持活塞位置不变,测定针筒内气体压强变化如图所示。
时迅速移动活塞后并保持活塞位置不变,测定针筒内气体压强变化如图所示。

(4)有关该过程说法正确的是_____
a.E、H两点对应的 的体积分数较大的为E点
的体积分数较大的为E点
b.B向里快速推注射器活塞,E向外快速拉注射器活塞
c.B、C、D三点正反应速率最大的是B点
d.C点时体系的颜色比D点深X
(5)下列表述能表示该反应已达平衡的是_____ (填序号)
a.活塞位置不变时,针管中的压强不再改变
b.针管内各物质的物质的量相等
c.针管内气体的平均摩尔质量不再改变
d.针管中温度、压强不变时,管内气体的密度不再改变
(6)求D点
_____ (不必化成小数)
(7)图像中C、E两点气体平均摩尔质量最大的点为_____ (填代号)。
(1)工业生产中未直接在一个设备中将
 催化氧化至
催化氧化至 ,而设计了两步氧化,中间经过热交换器降温,这样做的目的除了节约能源,还有
,而设计了两步氧化,中间经过热交换器降温,这样做的目的除了节约能源,还有(2)实验发现,单位时间内
 的氧化率[
的氧化率[ ]会随着温度的升高先增大后减小(如图所示),分析1000℃后
]会随着温度的升高先增大后减小(如图所示),分析1000℃后 的氧化率减小的可能原因
的氧化率减小的可能原因
(3)
 的反应历程如下:
的反应历程如下:反应Ⅰ:
 (快)
(快) 


反应Ⅱ:
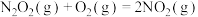 (慢)
(慢) 

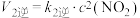
①一定条件下,反应
 达到平衡状态,平衡常数
达到平衡状态,平衡常数
 、
、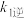 、
、 、
、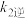 的代数式表示);
的代数式表示);②已知反应速率常数k随温度升高而增大,则升高温度后
 增大的倍数
增大的倍数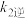 增大的倍数(填“大于”“小于”或“等于”)。
增大的倍数(填“大于”“小于”或“等于”)。(Ⅱ)工业上也可以直接由
 合成
合成 ,其中最关键的步骤为
,其中最关键的步骤为 ,利用现代手持技术传感器可以探究压强对该平衡的影响。
,利用现代手持技术传感器可以探究压强对该平衡的影响。在恒定温度和标准压强条件下,往针筒中充入一定体积的
 气体后密封并保持活塞位置不变。分别在
气体后密封并保持活塞位置不变。分别在 、
、 时迅速移动活塞后并保持活塞位置不变,测定针筒内气体压强变化如图所示。
时迅速移动活塞后并保持活塞位置不变,测定针筒内气体压强变化如图所示。
(4)有关该过程说法正确的是
a.E、H两点对应的
 的体积分数较大的为E点
的体积分数较大的为E点b.B向里快速推注射器活塞,E向外快速拉注射器活塞
c.B、C、D三点正反应速率最大的是B点
d.C点时体系的颜色比D点深X
(5)下列表述能表示该反应已达平衡的是
a.活塞位置不变时,针管中的压强不再改变
b.针管内各物质的物质的量相等
c.针管内气体的平均摩尔质量不再改变
d.针管中温度、压强不变时,管内气体的密度不再改变
(6)求D点

(7)图像中C、E两点气体平均摩尔质量最大的点为
您最近一年使用:0次
名校
解题方法
5 . (一)一种工业制硝酸的方法经历下列几个步骤:
4NH3(g)+5O2(g) 4NO(g)+6H2O(g) △H1<0
4NO(g)+6H2O(g) △H1<0
2NO(g)+O2(g) 2NO2(g) △H2<0
2NO2(g) △H2<0
3NO2(g)+H2O(l)=NO(g)+2HNO3(aq) △H3<0
已知:NO在1000℃以上会发生分解反应。
(1)工业生产中未直接在一个设备中将NH3催化氧化至NO2,而设计了两步氧化,中间经过热交换器降温,这样做的目的除了节约能源,还有________ 的目的。
(2)实验发现,单位时间内NH3的氧化率[n(NO)生成/n(NH3)原料]会随着温度的升高先增大后减小(如图所示),分析1000℃后NH3的氧化率减小的主要原因是________ 。

(3)2NO(g)+O2(g) 2NO2(g)的反应历程如下:
2NO2(g)的反应历程如下:
反应I:2NO(g) N2O2(g)(快) △H1<0 v1正=k1正•c²(NO) v1逆=k1逆•c(N2O2);
N2O2(g)(快) △H1<0 v1正=k1正•c²(NO) v1逆=k1逆•c(N2O2);
反应II:N2O2(g)+O2(g) 2NO2(g)(慢) △H2<0 v2正=k2正•c(N2O2)•c(O2) v2逆=k2逆•c2(NO2)。
2NO2(g)(慢) △H2<0 v2正=k2正•c(N2O2)•c(O2) v2逆=k2逆•c2(NO2)。
①一定条件下,反应2NO(g)+O2(g) 2NO2(g)达到平衡状态,平衡常数K=
2NO2(g)达到平衡状态,平衡常数K=________ (用含k1正、k1逆、k2正、k2逆的代数式表示)。
②已知反应速率常数k随温度升高而增大,则升高温度后k2正增大的倍数________ k2逆增大的倍数(填“大于”“小于”或“等于”)。
(二)工业上也可以直接由N2O4合成HNO3,其中最关键的步骤为2NO2(g) N2O4(g),利用现代手持技术传感器可以探究压强对该平衡的影响。
N2O4(g),利用现代手持技术传感器可以探究压强对该平衡的影响。
在恒定温度和标准压强条件下,往针筒中充入一定体积的NO2气体后密封并保持活塞位置不变。分别在t1、t2时迅速移动活塞后并保持活塞位置不变,测定针筒内气体压强变化如图所示。
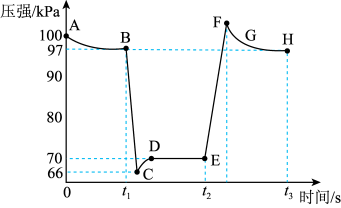
(4)有关该过程说法正确的是________ 。
a.E、H两点对应的的NO2体积分数较大的为E点
b.B向里快速推注射器活塞,E向外快速拉注射器活塞
c.B、C、D三点正反应速率最大的是B点
d.C点时体系的颜色比D点深
e.图像中C、E两点气体平均摩尔质量最大的点为C
(5)求B点NO2的转化率为________ 。
4NH3(g)+5O2(g)
 4NO(g)+6H2O(g) △H1<0
4NO(g)+6H2O(g) △H1<02NO(g)+O2(g)
 2NO2(g) △H2<0
2NO2(g) △H2<03NO2(g)+H2O(l)=NO(g)+2HNO3(aq) △H3<0
已知:NO在1000℃以上会发生分解反应。
(1)工业生产中未直接在一个设备中将NH3催化氧化至NO2,而设计了两步氧化,中间经过热交换器降温,这样做的目的除了节约能源,还有
(2)实验发现,单位时间内NH3的氧化率[n(NO)生成/n(NH3)原料]会随着温度的升高先增大后减小(如图所示),分析1000℃后NH3的氧化率减小的主要原因是

(3)2NO(g)+O2(g)
 2NO2(g)的反应历程如下:
2NO2(g)的反应历程如下:反应I:2NO(g)
 N2O2(g)(快) △H1<0 v1正=k1正•c²(NO) v1逆=k1逆•c(N2O2);
N2O2(g)(快) △H1<0 v1正=k1正•c²(NO) v1逆=k1逆•c(N2O2);反应II:N2O2(g)+O2(g)
 2NO2(g)(慢) △H2<0 v2正=k2正•c(N2O2)•c(O2) v2逆=k2逆•c2(NO2)。
2NO2(g)(慢) △H2<0 v2正=k2正•c(N2O2)•c(O2) v2逆=k2逆•c2(NO2)。①一定条件下,反应2NO(g)+O2(g)
 2NO2(g)达到平衡状态,平衡常数K=
2NO2(g)达到平衡状态,平衡常数K=②已知反应速率常数k随温度升高而增大,则升高温度后k2正增大的倍数
(二)工业上也可以直接由N2O4合成HNO3,其中最关键的步骤为2NO2(g)
 N2O4(g),利用现代手持技术传感器可以探究压强对该平衡的影响。
N2O4(g),利用现代手持技术传感器可以探究压强对该平衡的影响。在恒定温度和标准压强条件下,往针筒中充入一定体积的NO2气体后密封并保持活塞位置不变。分别在t1、t2时迅速移动活塞后并保持活塞位置不变,测定针筒内气体压强变化如图所示。

(4)有关该过程说法正确的是
a.E、H两点对应的的NO2体积分数较大的为E点
b.B向里快速推注射器活塞,E向外快速拉注射器活塞
c.B、C、D三点正反应速率最大的是B点
d.C点时体系的颜色比D点深
e.图像中C、E两点气体平均摩尔质量最大的点为C
(5)求B点NO2的转化率为
您最近一年使用:0次
名校
解题方法
6 . 我国在第75届联合国大会上正式提出了2030年实现碳达峰、2060年实现碳中和的目标,所以研发利用二氧化碳技术,降低空气中二氧化碳含量成为重要的任务。
Ⅰ.化石燃料的燃烧产生大量的二氧化碳。已知25℃时,相关物质的摩尔燃烧焓数据如表:
(1)则25℃时H2(g)和C(石墨,s)生成C2H2(l)的热化学方程式为________ 。
Ⅱ.二氧化碳甲烷化反应合成替代天然气,是利用二氧化碳的技术之一。
甲烷化主反应:CO2(g)+4H2(g) CH4(g)+2H2O(g) △H=-165kJ•mol-1
CH4(g)+2H2O(g) △H=-165kJ•mol-1
副反应:i.CO(g)+3H2(g) CH4(g)+H2O(g) ΔH1=_______。
CH4(g)+H2O(g) ΔH1=_______。
ii.CO2(g)+H2(g) CO(g)+H2O(g) △H2=+41.2kJ•mol-1;
CO(g)+H2O(g) △H2=+41.2kJ•mol-1;
iii.CO2(g)+2H2(g) C(s)+2H2O(g) △H3=-90kJ•mol-1;
C(s)+2H2O(g) △H3=-90kJ•mol-1;
iv.C(s)+H2O(g) CO(g)+H2(g) △H4=+131.3kJ•mol-1。
CO(g)+H2(g) △H4=+131.3kJ•mol-1。
(2)反应i的ΔH1=_______ ,该反应在_______ (填“高温”或“低温”)条件下能够自发进行反应。
(3)在恒温恒容的密闭容器中,关于反应iii叙述正确的是_______ 。
(4)某容器中加入一定量的CO2和H2,保持温度和压强不变的情况下,达平衡后再向该容器中注入Ar稀释,反应iii的化学平衡将_______ (填“正向移动”“逆向移动”或“不移动”),平衡时,CO2的分压p(CO2)_______ (填“增大”、“减小”或“不变”,下同)。
(5)以4molH2和1molCO2为初始原料,在催化剂(Ni/xMg)作用下保持总压为P0时,若只发生反应4H2(g)+CO2(g) CH4(g)+2H2O(g),不同温度下在相同时间测得CO2的转化率如图所示。
CH4(g)+2H2O(g),不同温度下在相同时间测得CO2的转化率如图所示。
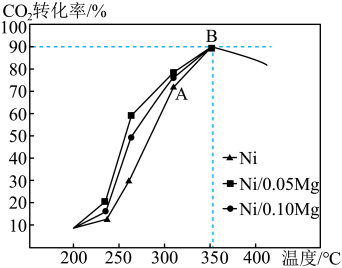
①B点的平衡常数KP=________ 。
②由图像可知,影响该催化剂活性的因素有________ 。
Ⅰ.化石燃料的燃烧产生大量的二氧化碳。已知25℃时,相关物质的摩尔燃烧焓数据如表:
| 物质 | H2(g) | C(石墨,s) | C2H2(l) |
| 摩尔燃烧焓ΔH(kJ•mol-1) | -285.8 | -393.5 | -1299.5 |
(1)则25℃时H2(g)和C(石墨,s)生成C2H2(l)的热化学方程式为
Ⅱ.二氧化碳甲烷化反应合成替代天然气,是利用二氧化碳的技术之一。
甲烷化主反应:CO2(g)+4H2(g)
 CH4(g)+2H2O(g) △H=-165kJ•mol-1
CH4(g)+2H2O(g) △H=-165kJ•mol-1副反应:i.CO(g)+3H2(g)
 CH4(g)+H2O(g) ΔH1=_______。
CH4(g)+H2O(g) ΔH1=_______。ii.CO2(g)+H2(g)
 CO(g)+H2O(g) △H2=+41.2kJ•mol-1;
CO(g)+H2O(g) △H2=+41.2kJ•mol-1;iii.CO2(g)+2H2(g)
 C(s)+2H2O(g) △H3=-90kJ•mol-1;
C(s)+2H2O(g) △H3=-90kJ•mol-1;iv.C(s)+H2O(g)
 CO(g)+H2(g) △H4=+131.3kJ•mol-1。
CO(g)+H2(g) △H4=+131.3kJ•mol-1。(2)反应i的ΔH1=
(3)在恒温恒容的密闭容器中,关于反应iii叙述正确的是
| A.用CO2、H2、H2O表示的速率之比为1:2:2可以作为判断化学平衡的依据 |
| B.容器中气体的压强不变时,不能作为平衡的判断依据 |
| C.容器内的气体密度不变可以作为平衡的判断依据 |
| D.使用催化剂不能改变平衡转化率 |
(4)某容器中加入一定量的CO2和H2,保持温度和压强不变的情况下,达平衡后再向该容器中注入Ar稀释,反应iii的化学平衡将
(5)以4molH2和1molCO2为初始原料,在催化剂(Ni/xMg)作用下保持总压为P0时,若只发生反应4H2(g)+CO2(g)
 CH4(g)+2H2O(g),不同温度下在相同时间测得CO2的转化率如图所示。
CH4(g)+2H2O(g),不同温度下在相同时间测得CO2的转化率如图所示。
①B点的平衡常数KP=
②由图像可知,影响该催化剂活性的因素有
您最近一年使用:0次
名校
7 . 2023年全国政府工作报告指出,推动重点领域节能降碳减污。萨巴蒂尔反应提出,电解水生成的氢气与宇航员呼出的二氧化碳在催化剂作用下生成水和甲烷,而水可循环使用,可用于太空生命保障。
(1)一定温度下,在恒容密闭容器发生4H2(g)+CO2(g) CH4(g)+2H2O(g)反应。
CH4(g)+2H2O(g)反应。
①能说明该反应达到平衡状态的是________ (填字母)。
A.H2的浓度保持不变
B.断开1molC=O键的同时生成4mol的C-H键
C.气体平均相对分子质量一定
D.v(CO2)=v(CH4)
②已知容器的容积为10L,初始加入2molCO2和6molH2,反应平衡后测得CO2的转化率为40%,则该反应的平衔常数为________ (只列出计算式即可)。
③保持温度和容积不变,再加入1molCO2(g)和3molH2(g),此时,CO2的转化率________ (填“>”“<”或“=”)40%。
(2)工业上可以利用H2和CO2合成乙醇,其反应为:6H2(g)+2CO2(g) C2H5OH(g)+3H2O(g)。将等物质的量的H2和CO2充入一刚性容器中,测得平衡时C2H5OH的体积分数随温度和压强的变化关系如图所示。
C2H5OH(g)+3H2O(g)。将等物质的量的H2和CO2充入一刚性容器中,测得平衡时C2H5OH的体积分数随温度和压强的变化关系如图所示。
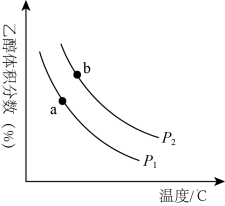
①压强P1________ P2(填“>”、“<”或“=”,下同)。判断依据是_______ 。
②a、b两点的平衡常数Ka________ Kb。
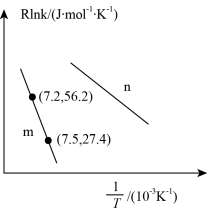
③已知Arhenius经验公式为Rlnk=- +C(Ea为活化能,k为速率常数,R和C为常数),为探究m、n两种催化剂的催化效率,进行了实验探究,依据实验数据获得如图所示曲线。在n催化剂作用下,该反应的活化能Ea
+C(Ea为活化能,k为速率常数,R和C为常数),为探究m、n两种催化剂的催化效率,进行了实验探究,依据实验数据获得如图所示曲线。在n催化剂作用下,该反应的活化能Ea________ J•mol-1。从图中信息获知催化效率较高的催化剂是________ (填“m”或“n”)。
(1)一定温度下,在恒容密闭容器发生4H2(g)+CO2(g)
 CH4(g)+2H2O(g)反应。
CH4(g)+2H2O(g)反应。①能说明该反应达到平衡状态的是
A.H2的浓度保持不变
B.断开1molC=O键的同时生成4mol的C-H键
C.气体平均相对分子质量一定
D.v(CO2)=v(CH4)
②已知容器的容积为10L,初始加入2molCO2和6molH2,反应平衡后测得CO2的转化率为40%,则该反应的平衔常数为
③保持温度和容积不变,再加入1molCO2(g)和3molH2(g),此时,CO2的转化率
(2)工业上可以利用H2和CO2合成乙醇,其反应为:6H2(g)+2CO2(g)
 C2H5OH(g)+3H2O(g)。将等物质的量的H2和CO2充入一刚性容器中,测得平衡时C2H5OH的体积分数随温度和压强的变化关系如图所示。
C2H5OH(g)+3H2O(g)。将等物质的量的H2和CO2充入一刚性容器中,测得平衡时C2H5OH的体积分数随温度和压强的变化关系如图所示。
①压强P1
②a、b两点的平衡常数Ka
③已知Arhenius经验公式为Rlnk=-
 +C(Ea为活化能,k为速率常数,R和C为常数),为探究m、n两种催化剂的催化效率,进行了实验探究,依据实验数据获得如图所示曲线。在n催化剂作用下,该反应的活化能Ea
+C(Ea为活化能,k为速率常数,R和C为常数),为探究m、n两种催化剂的催化效率,进行了实验探究,依据实验数据获得如图所示曲线。在n催化剂作用下,该反应的活化能Ea
您最近一年使用:0次
名校
解题方法
8 . 氨气是重要的化工原料,在国民经济中占重要地位。工业合成氨的反应为
 。
。
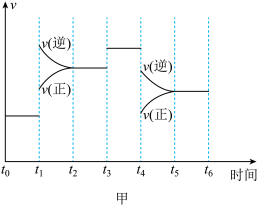
(1)图甲表示合成氨反应在某段时间 中反应速率与时间的曲线图,
中反应速率与时间的曲线图, 、
、 、
、 时刻分别改变某一外界条件,则在下列达到化学平衡的时间段中,
时刻分别改变某一外界条件,则在下列达到化学平衡的时间段中, 的体积分数最小的一段时间是
的体积分数最小的一段时间是___________ (填字母)。 时刻改变的条件是
时刻改变的条件是___________ 。
A. B.
B. C.
C. D.
D.
(2)在773 K时,分别将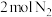 和
和 充入一个固定容积为1 L的密闭容器中,随着反应的进行,气体混合物中
充入一个固定容积为1 L的密闭容器中,随着反应的进行,气体混合物中 、
、 与反应时间t的关系如表所示:
与反应时间t的关系如表所示:
①该温度下,此反应的平衡常数
___________ 。
②该温度下,若向同容积的另一容器中投入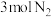 和
和 ,则达到平衡时
,则达到平衡时 的转化率将
的转化率将___________ (填“变大”、“变小”或“不变”)。
③该温度下,若向同容积的另一容器中投入的 、
、 、
、 的浓度分别为
的浓度分别为 、
、 、
、 ,则此时
,则此时
___________  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
④由表中的实验数据计算得到“浓度—时间”的关系可用图乙中的曲线表示,表示 的曲线是
的曲线是___________ 。在此温度下,若起始充入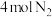 和
和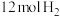 ,则反应刚达到平衡时,表示
,则反应刚达到平衡时,表示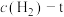 的曲线上相应的点为
的曲线上相应的点为___________ 。


 。
。(1)图甲表示合成氨反应在某段时间
 中反应速率与时间的曲线图,
中反应速率与时间的曲线图, 、
、 、
、 时刻分别改变某一外界条件,则在下列达到化学平衡的时间段中,
时刻分别改变某一外界条件,则在下列达到化学平衡的时间段中, 的体积分数最小的一段时间是
的体积分数最小的一段时间是 时刻改变的条件是
时刻改变的条件是
A.
 B.
B. C.
C.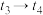 D.
D.
(2)在773 K时,分别将
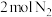 和
和 充入一个固定容积为1 L的密闭容器中,随着反应的进行,气体混合物中
充入一个固定容积为1 L的密闭容器中,随着反应的进行,气体混合物中 、
、 与反应时间t的关系如表所示:
与反应时间t的关系如表所示:| t/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
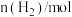 | 6.00 | 4.50 | 3.60 | 3.30 | 3.03 | 3.00 | 3.00 |
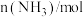 | 0 | 1.00 | 1.60 | 1.80 | 1.98 | 2.00 | 2.00 |

②该温度下,若向同容积的另一容器中投入
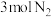 和
和 ,则达到平衡时
,则达到平衡时 的转化率将
的转化率将③该温度下,若向同容积的另一容器中投入的
 、
、 、
、 的浓度分别为
的浓度分别为 、
、 、
、 ,则此时
,则此时
 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。④由表中的实验数据计算得到“浓度—时间”的关系可用图乙中的曲线表示,表示
 的曲线是
的曲线是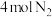 和
和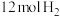 ,则反应刚达到平衡时,表示
,则反应刚达到平衡时,表示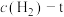 的曲线上相应的点为
的曲线上相应的点为
您最近一年使用:0次
名校
9 . 合成氨是人类科学技术上的一项重大突破,其反应原理为N2(g)+3H2(g) 2NH3(g) ΔH=-92.4kJ·mol-1.。一种工业合成氨的简式流程如图1所示:
2NH3(g) ΔH=-92.4kJ·mol-1.。一种工业合成氨的简式流程如图1所示:

步骤Ⅱ中制氢气的原理如下:
①CH4(g)+H2O(g) CO(g)+3H2(g) ΔH=+206.4kJ·mol-1
CO(g)+3H2(g) ΔH=+206.4kJ·mol-1
②CO(g)+H2O(g) CO2(g)+H2(g) ΔH=-41.2kJ·mol-1
CO2(g)+H2(g) ΔH=-41.2kJ·mol-1
(1)对于反应①,一定可以提高平衡体系中H2的百分含量,且能加快反应速率的措施是___________。
(2)图2表示500 ℃、60.0 MPa条件下,原料气投料比与平衡时NH3体积分数的关系。根据图中a点数据计算H2的平衡体积分数:___________ 。

(3)合成氨反应中正反应速率v正=k正c(N2)•c3(H2),逆反应速率v逆=k逆c2(NH3),k正、k逆为速率常数。平衡常数K与温度的关系如图。

①表示正反应的平衡常数K与温度变化的曲线为___________ (填L1或L2)。
②平衡时,合成氨反应的平衡常数K=___________ (用k正、k逆表示)。
(4)上述流程图中,使合成氨放出的能量得到充分利用的主要步骤是(填序号)___________ 。简述本流程中提高合成氨原料总转化率的方法:___________ (写出2条即可)。
(5)合成氨工业中,原料气(N2、H2及少量的CO、NH3的混合气)在进入合成塔前常用醋酸二氨合铜溶液来吸收原料气中的CO,其反应是[Cu(NH3)2CH3COO]+CO+NH3 [Cu(NH3)3]CH3COO·CO(正反应为放热反应)。必须除去原料气中CO的原因是
[Cu(NH3)3]CH3COO·CO(正反应为放热反应)。必须除去原料气中CO的原因是___________ 。
(6)相同温度下,有体积相同的甲、乙两个恒容密闭容器,甲容器中充入1 g N2和1 g H2,乙容器中充入2 g N2和2 g H2,分别进行合成氨反应。下列叙述中正确的是___________
 2NH3(g) ΔH=-92.4kJ·mol-1.。一种工业合成氨的简式流程如图1所示:
2NH3(g) ΔH=-92.4kJ·mol-1.。一种工业合成氨的简式流程如图1所示:
步骤Ⅱ中制氢气的原理如下:
①CH4(g)+H2O(g)
 CO(g)+3H2(g) ΔH=+206.4kJ·mol-1
CO(g)+3H2(g) ΔH=+206.4kJ·mol-1②CO(g)+H2O(g)
 CO2(g)+H2(g) ΔH=-41.2kJ·mol-1
CO2(g)+H2(g) ΔH=-41.2kJ·mol-1(1)对于反应①,一定可以提高平衡体系中H2的百分含量,且能加快反应速率的措施是___________。
| A.降低压强 | B.增大水蒸气浓度 | C.加入催化剂 | D.升高温度 |

(3)合成氨反应中正反应速率v正=k正c(N2)•c3(H2),逆反应速率v逆=k逆c2(NH3),k正、k逆为速率常数。平衡常数K与温度的关系如图。

①表示正反应的平衡常数K与温度变化的曲线为
②平衡时,合成氨反应的平衡常数K=
(4)上述流程图中,使合成氨放出的能量得到充分利用的主要步骤是(填序号)
(5)合成氨工业中,原料气(N2、H2及少量的CO、NH3的混合气)在进入合成塔前常用醋酸二氨合铜溶液来吸收原料气中的CO,其反应是[Cu(NH3)2CH3COO]+CO+NH3
 [Cu(NH3)3]CH3COO·CO(正反应为放热反应)。必须除去原料气中CO的原因是
[Cu(NH3)3]CH3COO·CO(正反应为放热反应)。必须除去原料气中CO的原因是(6)相同温度下,有体积相同的甲、乙两个恒容密闭容器,甲容器中充入1 g N2和1 g H2,乙容器中充入2 g N2和2 g H2,分别进行合成氨反应。下列叙述中正确的是___________
| A.化学反应速率:乙>甲 | B.平衡后N2的浓度:乙>甲 |
| C.H2的平衡转化率:甲>乙 | D.平衡后混合气体中H2的体积分数:乙>甲 |
您最近一年使用:0次
名校
10 . 雾霾中含有颗粒物(PM2.5)、氮氧化物(NOx)、CO等多种污染物。
(1)NO在空气中存在如下反应:2NO(g)+O2(g) 2NO2(g),上述反应分两步完成即反应I和反应Ⅱ,其反应历程如下图所示:(纵坐标从下到上依次是:E1、E2、E3、E4、E5)。反应I和反应Ⅱ中,一个是快反应,会快速建立平衡状态,而另一个是慢反应。
2NO2(g),上述反应分两步完成即反应I和反应Ⅱ,其反应历程如下图所示:(纵坐标从下到上依次是:E1、E2、E3、E4、E5)。反应I和反应Ⅱ中,一个是快反应,会快速建立平衡状态,而另一个是慢反应。

①反应2NO(g)+O2(g) 2NO2(g)的ΔH
2NO2(g)的ΔH___________ 0(填“>”、“<”或“=”)。
②决定2NO(g)+O2(g) 2NO2(g)反应速率的是
2NO2(g)反应速率的是___________ (填“反应I”或“反应Ⅱ”);快反应的正反应活化能为___________ kJ/mol(用含E1~E5的代数式表示)。
③T1℃下一密闭容器中充入一定量的NO2,发生反应2NO(g)+O2(g) 2NO2(g),测得NO2浓度随时间变化的曲线如图所示。前5秒内O2的平均生成速率为
2NO2(g),测得NO2浓度随时间变化的曲线如图所示。前5秒内O2的平均生成速率为___________ ;

④对于③中的反应体系达平衡后,若降低温度,再次达平衡后,混合气体的平均相对分子质量___________ 。(填“增大”、“减小”或“不变”);对于③中的反应体系达平衡后,若在恒温恒容条件下,追加NO2,再次达平衡后,NO2的体积分数___________ (填“增大”、“减小”或“不变”)。
(2)将一定量N2O4气体充入恒容的密闭容器中,控制反应温度为T1,发生的反应为:N2O4(g) 2NO2(g) △H>0,t时刻反应达到平衡,混合气体平衡总压强为P,N2O4的平衡转化率为80%,则反应N2O4(g)
2NO2(g) △H>0,t时刻反应达到平衡,混合气体平衡总压强为P,N2O4的平衡转化率为80%,则反应N2O4(g) 2NO2(g)的平衡常数Kp=
2NO2(g)的平衡常数Kp=___________ (用平衡分压代替平衡浓度,分压=总压×物质的量分数)。
(1)NO在空气中存在如下反应:2NO(g)+O2(g)
 2NO2(g),上述反应分两步完成即反应I和反应Ⅱ,其反应历程如下图所示:(纵坐标从下到上依次是:E1、E2、E3、E4、E5)。反应I和反应Ⅱ中,一个是快反应,会快速建立平衡状态,而另一个是慢反应。
2NO2(g),上述反应分两步完成即反应I和反应Ⅱ,其反应历程如下图所示:(纵坐标从下到上依次是:E1、E2、E3、E4、E5)。反应I和反应Ⅱ中,一个是快反应,会快速建立平衡状态,而另一个是慢反应。
①反应2NO(g)+O2(g)
 2NO2(g)的ΔH
2NO2(g)的ΔH②决定2NO(g)+O2(g)
 2NO2(g)反应速率的是
2NO2(g)反应速率的是③T1℃下一密闭容器中充入一定量的NO2,发生反应2NO(g)+O2(g)
 2NO2(g),测得NO2浓度随时间变化的曲线如图所示。前5秒内O2的平均生成速率为
2NO2(g),测得NO2浓度随时间变化的曲线如图所示。前5秒内O2的平均生成速率为
④对于③中的反应体系达平衡后,若降低温度,再次达平衡后,混合气体的平均相对分子质量
(2)将一定量N2O4气体充入恒容的密闭容器中,控制反应温度为T1,发生的反应为:N2O4(g)
 2NO2(g) △H>0,t时刻反应达到平衡,混合气体平衡总压强为P,N2O4的平衡转化率为80%,则反应N2O4(g)
2NO2(g) △H>0,t时刻反应达到平衡,混合气体平衡总压强为P,N2O4的平衡转化率为80%,则反应N2O4(g) 2NO2(g)的平衡常数Kp=
2NO2(g)的平衡常数Kp=
您最近一年使用:0次



