1 . 下列关于2SO2(g)+O2(g) 2SO3(g) ∆H=-197kJ∙mol-1的说法正确的是
2SO3(g) ∆H=-197kJ∙mol-1的说法正确的是
 2SO3(g) ∆H=-197kJ∙mol-1的说法正确的是
2SO3(g) ∆H=-197kJ∙mol-1的说法正确的是| A.该反应的∆S>0 |
| B.根据∆G,高温条件下反应可以自发进行 |
| C.生产过程中将SO3分离出去,逆反应速率减慢 |
| D.其他条件不变,增大压强,平衡右移,平衡常数增大 |
您最近一年使用:0次
2022-09-21更新
|
222次组卷
|
2卷引用:云南省楚雄天人中学2021-2022学年高二上学期12月月考化学试题(A卷)
名校
2 . 下列反应一定属于非自发进行的是
| A.N2(g)+2O2(g)=2NO2(g) △H=+67.7kJ/mol |
| B.CaCO3(s)=CaO(s)+CO2(g) △H=+1921.8kJ/mol |
| C.C6H12O6(s)+6O2(g)=6CO2(g)+6H2O(l) △H=-2804kJ/mol |
| D.2CO(g)+O2(g)=2CO2(g) △H=-566kJ/mol |
您最近一年使用:0次
2022-09-14更新
|
501次组卷
|
6卷引用:云南省文山州麻栗坡县2021-2022学年高二上学期期中测试化学试题
10-11高二上·吉林·阶段练习
名校
解题方法
3 . 知道了某过程有自发性之后,则
| A.可判断出过程的方向 | B.可确定过程是否一定会发生 |
| C.可预测过程发生完成的快慢 | D.可判断过程的热效应 |
您最近一年使用:0次
2022-07-09更新
|
484次组卷
|
29卷引用:2011-2012学年云南省蒙自县文澜高级中学高二上学期期中考试化学试卷
(已下线)2011-2012学年云南省蒙自县文澜高级中学高二上学期期中考试化学试卷云南省屏边县第一中学2019-2020学年高二上学期12月月考化学试题云南省陇川县民族中学2019-2020学年高二上学期期末考试化学试题云南省曲靖市富源县第六中学2019-2020学年高二上学期期末考试化学试题(已下线)2010年吉林省东北师大附中高二上学期第一次月考(化学)(已下线)2011-2012年山东省莒南县三中高二上学期期中考试化学试卷(已下线)2011-2012学年陕西师大附中高二年级第一学期期中考试化学试卷(已下线)2012年人教版高中化学选修4 2.4化学反应进行的方向练习卷(已下线)2012-2013学年广东省汕头市金山中学高二上学期期末考试化学试卷(已下线)2013-2014学年陕西省岐山县高二上学期期中质量检测理科化学试卷(已下线)2015安徽望江中学同步课时练(人教选修4)2.4化学反应进行的方向(已下线)2014-2015学年湖南省娄底市高二上学期期中联考化学试卷2016-2017学年黑龙江省大庆市杜蒙县高二上月考一化学卷河北省承德市第一中学2017-2018学年高二上学期第一次月考化学试题(已下线)2019年9月24日 《每日一题》选修4—— 自发过程与自发反应福建省厦门外国语学校2019-2020学年高二上学期期中考试化学试题山西省阳泉市2019-2020学年高二上学期期末考试化学试题(已下线)2.2.1 化学反应的方向(基础练)——2020-2021学年高二化学上学期十分钟同步课堂专练(苏教版选修4)(已下线)2.3 化学反应的方向(练习)-2020-2021学年上学期高二化学同步精品课堂(新教材人教版选择性必修1)人教版(2019)高二选择性必修第一册 第二章 化学反应速率与化学平衡 第三节 化学反应的方向 教材帮(已下线)2.2.1 化学反应的方向(备作业)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1)(已下线)2.3 化学反应进行的方向——同步学习必备知识第三节 化学反应的方向第1节 化学反应的方向(已下线)2011-2012学年陕西省师大附中高一下学期期末考试化学试卷2016届黑龙江省牡丹江一中高三上学期10月月考化学试卷(已下线)考点24 化学反应的方向-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)考点24 化学反应的方向(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)上海市向明中学 2023-2024学年高三上学期9月质量监控化学试题
4 . 下列说法正确的是
A.恒温恒压下, 且 且 的反应一定不能自发进行 的反应一定不能自发进行 |
| B.非自发的反应一定可以通过改变条件使其成为自发反应 |
| C.相同物质的量的同种物质气态时熵值最小,固态时熵值最大 |
D.反应 在室温下可自发进行,则该反应的 在室温下可自发进行,则该反应的 |
您最近一年使用:0次
2022-07-08更新
|
315次组卷
|
3卷引用:云南省昆明市寻甸县2022-2023学年高二上学期期中考试化学试题
云南省昆明市寻甸县2022-2023学年高二上学期期中考试化学试题广西钦州市2021-2022学年高二下学期期末考试化学试题(已下线)2.3 化学反应的方向-2022-2023学年高二化学上学期课后培优分级练(人教版2019选择性必修1)
名校
解题方法
5 . 合成氨反应为:N2(g)+3H2(g) 2NH3(g) △H=-92.4kJ·mol-1。下列说法正确的是
2NH3(g) △H=-92.4kJ·mol-1。下列说法正确的是
 2NH3(g) △H=-92.4kJ·mol-1。下列说法正确的是
2NH3(g) △H=-92.4kJ·mol-1。下列说法正确的是| A.合成氨反应在任何温度下都能自发 |
| B.1molN2与过量H2充分反应放热92.4kJ |
| C.合成氨实际生产中选择高压和低温 |
| D.将氨液化分离,可促进平衡正移及循环利用氮气和氢气 |
您最近一年使用:0次
2022-06-25更新
|
382次组卷
|
4卷引用:云南省昆明一中教育集团2023届高二升高三诊断性考试化学试题
云南省昆明一中教育集团2023届高二升高三诊断性考试化学试题(已下线)2.4 化学反应的调控-2022-2023学年高二化学上学期课后培优分级练(人教版2019选择性必修1)福建省莆田第二十五中学2022-2023学年高二上学期期中考试化学试题【精品卷】2.4 化学反应的调控课堂例题-人教版2023-2024学年选择性必修1
名校
6 .  与
与 重整技术是获得合成气(CO、
重整技术是获得合成气(CO、 )、实现碳中和的重要途径之一。在一定条件下,向密闭容器中通入物质的量均为
)、实现碳中和的重要途径之一。在一定条件下,向密闭容器中通入物质的量均为 的
的 和
和 ,发生反应:
,发生反应: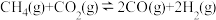 ,测得平衡时
,测得平衡时 的转化率与温度、压强的关系如图所示[已知气体分压(p)=总压×物质的量分数,用平衡分压代替平衡浓度可得到平衡常数
的转化率与温度、压强的关系如图所示[已知气体分压(p)=总压×物质的量分数,用平衡分压代替平衡浓度可得到平衡常数 ]:
]:
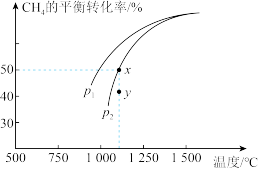
下列说法错误的是
 与
与 重整技术是获得合成气(CO、
重整技术是获得合成气(CO、 )、实现碳中和的重要途径之一。在一定条件下,向密闭容器中通入物质的量均为
)、实现碳中和的重要途径之一。在一定条件下,向密闭容器中通入物质的量均为 的
的 和
和 ,发生反应:
,发生反应: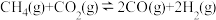 ,测得平衡时
,测得平衡时 的转化率与温度、压强的关系如图所示[已知气体分压(p)=总压×物质的量分数,用平衡分压代替平衡浓度可得到平衡常数
的转化率与温度、压强的关系如图所示[已知气体分压(p)=总压×物质的量分数,用平衡分压代替平衡浓度可得到平衡常数 ]:
]:
下列说法错误的是
A.该反应的 、 、 |
B.y点 的生成速率小于氢气的消耗速率 的生成速率小于氢气的消耗速率 |
C.x点对应温度下该反应的平衡常数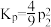 |
| D.随着温度升高,对平衡限度的影响温度大于压强 |
您最近一年使用:0次
2022-06-15更新
|
177次组卷
|
3卷引用:云南省临沧市第一中学2022-2023学年高二上学期期中考试化学试题
7 . 钛(Ti)及其合金是理想的高强度、低密度结构材料。以钛渣(主要成分为 ,含少量V、Si和Al的氧化物杂质)为原料,制备金属钛的工艺流程如下:
,含少量V、Si和Al的氧化物杂质)为原料,制备金属钛的工艺流程如下:
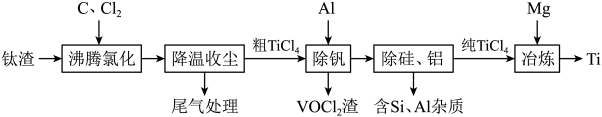
已知“降温收尘”后,粗 中含有的几种物质的沸点:
中含有的几种物质的沸点:
回答下列问题:
(1)已知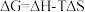 ,
, 的值只决定于反应体系的始态和终态,忽略
的值只决定于反应体系的始态和终态,忽略 、
、 随温度的变化。若
随温度的变化。若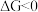 ,则该反应可以自发进行。根据下图判断:
,则该反应可以自发进行。根据下图判断: 时,下列反应不能自发进行的是_______。
时,下列反应不能自发进行的是_______。
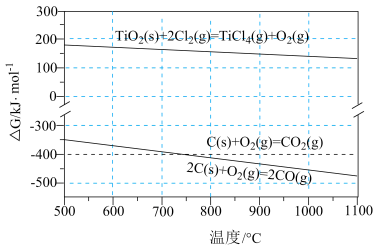
(2) 与C、
与C、 ,在
,在 的沸腾炉中充分反应后,混合气体中各组分的分压如下表:
的沸腾炉中充分反应后,混合气体中各组分的分压如下表:
①该温度下, 与C、
与C、 反应的总化学方程式为
反应的总化学方程式为_______ ;
②随着温度升高,尾气中 的含量升高,原因是
的含量升高,原因是_______ 。
(3)“除钒”过程中的化学方程式为_______ ;“除硅、铝”过程中,分离 中含
中含 、
、 杂质的方法是
杂质的方法是_______ 。
(4)“除钒”和“除硅、铝”的顺序_______ (填“能”或“不能”)交换,理由是_______ 。
(5)下列金属冶炼方法与本工艺流程中加入 冶炼
冶炼 的方法相似的是_______。
的方法相似的是_______。
 ,含少量V、Si和Al的氧化物杂质)为原料,制备金属钛的工艺流程如下:
,含少量V、Si和Al的氧化物杂质)为原料,制备金属钛的工艺流程如下:
已知“降温收尘”后,粗
 中含有的几种物质的沸点:
中含有的几种物质的沸点:| 物质 |  |  |  |  |
沸点/ | 136 | 127 | 57 | 180 |
(1)已知
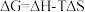 ,
, 的值只决定于反应体系的始态和终态,忽略
的值只决定于反应体系的始态和终态,忽略 、
、 随温度的变化。若
随温度的变化。若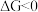 ,则该反应可以自发进行。根据下图判断:
,则该反应可以自发进行。根据下图判断: 时,下列反应不能自发进行的是_______。
时,下列反应不能自发进行的是_______。
A. | B. |
C. | D. |
 与C、
与C、 ,在
,在 的沸腾炉中充分反应后,混合气体中各组分的分压如下表:
的沸腾炉中充分反应后,混合气体中各组分的分压如下表:| 物质 |  |  |  |  |
分压 | 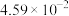 | 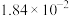 |  |  |
 与C、
与C、 反应的总化学方程式为
反应的总化学方程式为②随着温度升高,尾气中
 的含量升高,原因是
的含量升高,原因是(3)“除钒”过程中的化学方程式为
 中含
中含 、
、 杂质的方法是
杂质的方法是(4)“除钒”和“除硅、铝”的顺序
(5)下列金属冶炼方法与本工艺流程中加入
 冶炼
冶炼 的方法相似的是_______。
的方法相似的是_______。| A.高炉炼铁 | B.电解熔融氯化钠制钠 | C.铝热反应制锰 | D.氧化汞分解制汞 |
您最近一年使用:0次
2022-06-10更新
|
11480次组卷
|
19卷引用:云南省开远市第一中学校2022-2023学年高二下学期5月月考化学试题
云南省开远市第一中学校2022-2023学年高二下学期5月月考化学试题福建省厦门第一中学2023-2024学年高二上学期期中考试化学试题河南省周口恒大中学2023-2024学年高二上学期12月月考化学试题2022年新高考湖南化学高考真题(已下线)2022年湖南卷高考真题变式题(15-19)(已下线)专题14 化学反应原理综合题-2022年高考真题模拟题分项汇编(已下线)专题16 工艺流程题-三年(2020-2022)高考真题分项汇编(已下线)考点24 化学反应的方向-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)2022年湖北省高考真题变式题16-19(已下线)2022年海南省高考真题变式题15-19(已下线)易错点08 金属材料-备战2023年高考化学考试易错题(已下线)专题29 无机化工流程综合分析-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)第一部分 二轮专题突破 大题突破3 无机化工流程题题型研究(已下线)题型38 基于金属元素的工艺流程题(已下线)专题18 工艺流程题(已下线)专题18 工艺流程题(已下线)专题13 工艺流程综合题-2023年高考化学真题题源解密(新高考专用)(已下线)专题13 工艺流程综合题-2023年高考化学真题题源解密(全国通用)(已下线)考点47 无机工艺流程(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)
名校
8 . 以NaCl为原料,可制取Na、Na2O2、NaOH和Na2CO3等。Na2CO3,可用侯氏制碱法制取,主要涉及如下反应:
N2(g)+3H2(g) 2NH3(g) ΔH=-92.4kJ·mol-1
2NH3(g) ΔH=-92.4kJ·mol-1
NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl
2NaHCO3 Na2CO3+CO2↑+H2O
Na2CO3+CO2↑+H2O
对于反应N2(g)+3H2(g) 2NH3(g),下列说法正确的是
2NH3(g),下列说法正确的是
N2(g)+3H2(g)
 2NH3(g) ΔH=-92.4kJ·mol-1
2NH3(g) ΔH=-92.4kJ·mol-1NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl
2NaHCO3
 Na2CO3+CO2↑+H2O
Na2CO3+CO2↑+H2O对于反应N2(g)+3H2(g)
 2NH3(g),下列说法正确的是
2NH3(g),下列说法正确的是| A.该反应的ΔS>0 |
B.该反应的平衡常数可表示为 |
C.其他条件相同,增大 ,H2转化率减小 ,H2转化率减小 |
| D.使用催化剂能降低该反应的焓变 |
您最近一年使用:0次
2022-05-07更新
|
554次组卷
|
7卷引用:云南省曲靖市会泽实验高级中学校2022-2023学年高二下学期3月月考(二)化学试题
云南省曲靖市会泽实验高级中学校2022-2023学年高二下学期3月月考(二)化学试题江苏省南京市2022届高三下学期第二次(5月)模拟考试化学试题(已下线)2022年江苏卷高考真题变式题1-13江苏省高邮市第一中学2022-2023学年高三上学期阶段测试一化学试题(已下线)江苏省2022年普通高中学业水平选择性考试变式题(选择题6-10)江苏省常州市八校2022-2023学年高三上学期10月联合调研化学试题(已下线)选择题1-5
名校
9 . 以煤为原料可合成一系列燃料。回答下列问题:
(1)向1L恒容密闭容器中加入2mol CO、4mol H2,在适当的催化剂作用下,发生反应:2CO(g)+4H2(g) CH3OCH3(l)+H2O(l) △H=+71kJ·mol-l
CH3OCH3(l)+H2O(l) △H=+71kJ·mol-l
①该反应_______ 自发进行(填“能”、“不能”或“无法判断”);
②下列叙述能说明此反应达到平衡状态的是_______ 。
a.混合气体的平均相对分子质量保持不变
b.CO和H2的转化率相等
c.CO和H2的体积分数保持不变
d.混合气体的密度保持不变
e.1mol CO生成的同时有1mol O-H 键断裂
(2)CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H<0,在一定条件下,某反应过程中部分数据如下表:
CH3OH(g)+H2O(g) △H<0,在一定条件下,某反应过程中部分数据如下表:
①0~10min内,用H2O(g)表示的化学反应速率v(H2O)=_______ mol/(L ·min)。
②T1℃,该反应的平衡常数K=_______ (用分数表示),平衡时H2的转化率是_______ 。
③在其它条件不变的情况下,若30min时改变温度为T2℃,再次平衡时H2的物质的量为3.2mol,则T1_______ T2(填“>”“<”或“=”),理由是_______ ; 在其他条件不变的情况下,若30min时向容器中再充入1mol CO2(g)和1mol H2O(g),则平衡_______ 移动(填“正向”、“逆向”或“不”)。
(1)向1L恒容密闭容器中加入2mol CO、4mol H2,在适当的催化剂作用下,发生反应:2CO(g)+4H2(g)
 CH3OCH3(l)+H2O(l) △H=+71kJ·mol-l
CH3OCH3(l)+H2O(l) △H=+71kJ·mol-l①该反应
②下列叙述能说明此反应达到平衡状态的是
a.混合气体的平均相对分子质量保持不变
b.CO和H2的转化率相等
c.CO和H2的体积分数保持不变
d.混合气体的密度保持不变
e.1mol CO生成的同时有1mol O-H 键断裂
(2)CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H<0,在一定条件下,某反应过程中部分数据如下表:
CH3OH(g)+H2O(g) △H<0,在一定条件下,某反应过程中部分数据如下表:| 反应条件 | 反应时间 | CO2/mol | H2/mol | CH3OH/mol | H2O/mol |
| 恒温恒容(T1℃、2L) | 0min | 2 | 6 | 0 | 0 |
| 10min | 4.5 | ||||
| 20min | 1 | ||||
| 30min | 1 |
②T1℃,该反应的平衡常数K=
③在其它条件不变的情况下,若30min时改变温度为T2℃,再次平衡时H2的物质的量为3.2mol,则T1
您最近一年使用:0次
名校
10 . NOx是造成大气污染的主要物质,工业上脱硝有多种方法。利用碳还原NO的反应为2NO(g)+C(s)  N2(g)+CO2(g)。回答下列问题:
N2(g)+CO2(g)。回答下列问题:
(1)该反应在常温下可以自发进行,则反应的△H_______ (填“>”“<”或“=”)0。
(2)在一定温度下,向甲、乙、丙三个恒容密闭容器中加入一定量的NO和足量的焦炭,反应过程中测得各容器中c(NO)(mol·L-1)随时间(s)的变化如下表所示。(已知:三个容器的反应温度分别为T甲=400℃、T乙=400℃、T丙=a℃)
丙容器的反应温度a_______ (填“>” “<”或“=”)400。
(3)已知:8NH3(g)+6NO2 (g) 7N2(g)+ 12H2O(l) △H< 0,相同条件下,在2 L密闭容器内,选用不同的催化剂进行反应,产生N2的量随时间的变化关系如图所示。
7N2(g)+ 12H2O(l) △H< 0,相同条件下,在2 L密闭容器内,选用不同的催化剂进行反应,产生N2的量随时间的变化关系如图所示。

①该反应活化能Ea(A)、Eb(B)、Ec(C)由小到大的顺序是_______ ,理由是_______ 。
②下列说法不正确的是_______ (填标号)。
a.使用催化剂A达平衡时,△H值更大
b.升高温度可使容器内气体颜色加深
c.单位时间内形成N- H键与O- H键的数目相等时,说明反应已经达到平衡
d.若在恒容绝热的密闭容器中反应,当平衡常数不变时,说明反应已经达到平衡
 N2(g)+CO2(g)。回答下列问题:
N2(g)+CO2(g)。回答下列问题:(1)该反应在常温下可以自发进行,则反应的△H
(2)在一定温度下,向甲、乙、丙三个恒容密闭容器中加入一定量的NO和足量的焦炭,反应过程中测得各容器中c(NO)(mol·L-1)随时间(s)的变化如下表所示。(已知:三个容器的反应温度分别为T甲=400℃、T乙=400℃、T丙=a℃)
| 时间 | 0s | 10 s | 20 s | 30 s | 40 s |
| 甲 | 2.00 | 1.50 | 1.10 | 0.80 | 0.80 |
| 乙 | 1.00 | 0.80 | 0.65 | 0.53 | 0. 45 |
| 丙 | 2. 00 | 1.45 | 1. 00 | 1. 00 | 1. 00 |
(3)已知:8NH3(g)+6NO2 (g)
 7N2(g)+ 12H2O(l) △H< 0,相同条件下,在2 L密闭容器内,选用不同的催化剂进行反应,产生N2的量随时间的变化关系如图所示。
7N2(g)+ 12H2O(l) △H< 0,相同条件下,在2 L密闭容器内,选用不同的催化剂进行反应,产生N2的量随时间的变化关系如图所示。
①该反应活化能Ea(A)、Eb(B)、Ec(C)由小到大的顺序是
②下列说法不正确的是
a.使用催化剂A达平衡时,△H值更大
b.升高温度可使容器内气体颜色加深
c.单位时间内形成N- H键与O- H键的数目相等时,说明反应已经达到平衡
d.若在恒容绝热的密闭容器中反应,当平衡常数不变时,说明反应已经达到平衡
您最近一年使用:0次



