1 . 回答下列问题:
(1)工业制胆矾时,将粗制CuO粉末(含杂质FeO、Fe2O3)慢慢加入适量的稀H2SO4中完全溶解,除去杂质离子后,再蒸发结晶可得纯净的胆矾晶体。已知:pH≥9.6时,Fe2+以Fe(OH)2的形式完全沉淀;pH≥6.4时,Cu2+以Cu(OH)2的形式完全沉淀;pH接近4时,Fe3+以Fe(OH)3的形式完全沉淀。回答下列问题:
①为除去溶液中的Fe2+,可先加入_______ ,(从下面四个选项选择,填字母)将Fe2+氧化为Fe3+,反应的离子方程式为_______ ,然后加入适量的_______ ,(从下面四个选项选择,填字母)调整溶液的pH使Fe3+转化为Fe(OH)3沉淀。
A.CuO B.Cl2 C.Cu(OH)2 D.H2O2
②甲同学怀疑调整至溶液pH=4是否能达到除去Fe3+而不损失Cu2+的目的,乙同学认为可以通过计算确定,他查阅有关资料得到如下数据,常温下Fe(OH)3的溶度积Ksp=1×10-38,Cu(OH)2的溶度积Ksp=3×10-20,通常认为残留在溶液中的离子浓度小于1×10-5mol·L-1时就认为沉淀完全,设溶液中CuSO4的浓度为3mol·L-1,则Cu(OH)2开始沉淀时溶液的pH为_______ ,Fe3+完全沉淀时溶液的pH为_______ ,通过计算即可确定上述方案是否可行。
(2)在微电子工业中NF3常用作氮化硅的蚀刻剂,工业上通过电解含NH4F等的无水熔融物生产NF3,其电解原理如图所示。
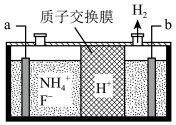
①H+向_______ (填“左”或“右”)移动。
②写出a电极的电极反应式:_______ 。
(1)工业制胆矾时,将粗制CuO粉末(含杂质FeO、Fe2O3)慢慢加入适量的稀H2SO4中完全溶解,除去杂质离子后,再蒸发结晶可得纯净的胆矾晶体。已知:pH≥9.6时,Fe2+以Fe(OH)2的形式完全沉淀;pH≥6.4时,Cu2+以Cu(OH)2的形式完全沉淀;pH接近4时,Fe3+以Fe(OH)3的形式完全沉淀。回答下列问题:
①为除去溶液中的Fe2+,可先加入
A.CuO B.Cl2 C.Cu(OH)2 D.H2O2
②甲同学怀疑调整至溶液pH=4是否能达到除去Fe3+而不损失Cu2+的目的,乙同学认为可以通过计算确定,他查阅有关资料得到如下数据,常温下Fe(OH)3的溶度积Ksp=1×10-38,Cu(OH)2的溶度积Ksp=3×10-20,通常认为残留在溶液中的离子浓度小于1×10-5mol·L-1时就认为沉淀完全,设溶液中CuSO4的浓度为3mol·L-1,则Cu(OH)2开始沉淀时溶液的pH为
(2)在微电子工业中NF3常用作氮化硅的蚀刻剂,工业上通过电解含NH4F等的无水熔融物生产NF3,其电解原理如图所示。

①H+向
②写出a电极的电极反应式:
您最近一年使用:0次
2022-01-18更新
|
47次组卷
|
2卷引用:湖南省岳阳市临湘市2021-2022学年高二上学期期末教学质量检测化学试题
名校
解题方法
2 . 钴酸锂电池的正极材料含有钴酸锂(LiCoO2)、铝箔及少量铁等,其通过如下图流程可回收铝、钴、锂。请回答下列问题:
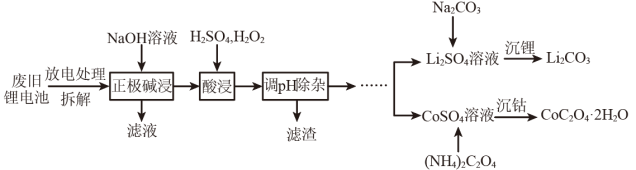
(1) 中Co的化合价为
中Co的化合价为_______ 。
(2)钴酸锂电池放电总反应为: ,则其负极的电极反应式为
,则其负极的电极反应式为_______ 。
(3)“酸浸”时Co、Li元素的浸出率随温度的变化如图所示:
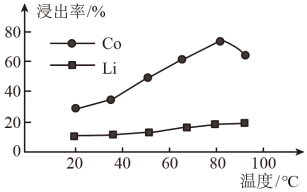
“酸浸”的适宜温度约为_______ ℃[所填数据限整数],若酸浸主要反应的化学方程式为:
 ,则上述反应过程中消耗的氧化剂与还原剂物质的量之比为
,则上述反应过程中消耗的氧化剂与还原剂物质的量之比为_______ 。
(4)“调pH除杂”的目的是使 沉淀完全[即
沉淀完全[即 ],则常温下应控制
],则常温下应控制
_______ [保留到小数点后1位,另外已知常温时 的
的 为
为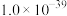 ]。
]。
(5)沉锂的离子反应方程式为_______ 。
(6)准确称取4.575g的 样品,在空气中加热分解获取金属氧化物,固体样品的剩余质量随温度的变化如下图所示(已知385℃及以上残留固体均为金属氧化物),请写出B处物质与浓盐酸反应的化学方程式
样品,在空气中加热分解获取金属氧化物,固体样品的剩余质量随温度的变化如下图所示(已知385℃及以上残留固体均为金属氧化物),请写出B处物质与浓盐酸反应的化学方程式_______ 。

(1)
 中Co的化合价为
中Co的化合价为(2)钴酸锂电池放电总反应为:
 ,则其负极的电极反应式为
,则其负极的电极反应式为(3)“酸浸”时Co、Li元素的浸出率随温度的变化如图所示:

“酸浸”的适宜温度约为

 ,则上述反应过程中消耗的氧化剂与还原剂物质的量之比为
,则上述反应过程中消耗的氧化剂与还原剂物质的量之比为(4)“调pH除杂”的目的是使
 沉淀完全[即
沉淀完全[即 ],则常温下应控制
],则常温下应控制
 的
的 为
为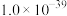 ]。
]。(5)沉锂的离子反应方程式为
(6)准确称取4.575g的
 样品,在空气中加热分解获取金属氧化物,固体样品的剩余质量随温度的变化如下图所示(已知385℃及以上残留固体均为金属氧化物),请写出B处物质与浓盐酸反应的化学方程式
样品,在空气中加热分解获取金属氧化物,固体样品的剩余质量随温度的变化如下图所示(已知385℃及以上残留固体均为金属氧化物),请写出B处物质与浓盐酸反应的化学方程式
您最近一年使用:0次
2022-01-17更新
|
295次组卷
|
2卷引用:湖南省岳阳市岳阳县2021-2022学年高三上学期入学考试化学试题
名校
解题方法
3 . 某温度下,分别向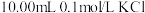 和
和 溶液中滴加
溶液中滴加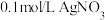 溶液,滴加过程中
溶液,滴加过程中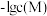 (M为
(M为 或
或 )与
)与 溶液体积(V)的变化关系如图所示(忽略溶液体积变化)。下列说法
溶液体积(V)的变化关系如图所示(忽略溶液体积变化)。下列说法不正确 的是
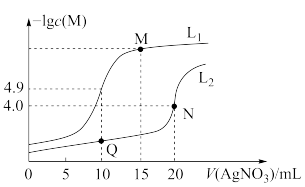
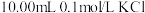 和
和 溶液中滴加
溶液中滴加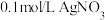 溶液,滴加过程中
溶液,滴加过程中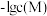 (M为
(M为 或
或 )与
)与 溶液体积(V)的变化关系如图所示(忽略溶液体积变化)。下列说法
溶液体积(V)的变化关系如图所示(忽略溶液体积变化)。下列说法
A.曲线 表示 表示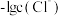 与 与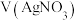 的变化关系 的变化关系 |
B.M点溶液中: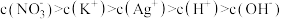 |
C.该温度下,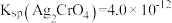 |
D.相同实验条件下,若改为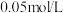 的 的 和 和 溶液,则曲线 溶液,则曲线 中N点移到Q点 中N点移到Q点 |
您最近一年使用:0次
2022-01-11更新
|
1357次组卷
|
19卷引用:湖南省岳阳市第一中学2023届高三下学期第七次月考化学试题
湖南省岳阳市第一中学2023届高三下学期第七次月考化学试题2020届高三化学化学二轮复习——常考题型:沉淀溶解平衡的曲线分析【精编25题】福建省厦门市2020届高三毕业班五月质量检查理综化学试题福建省厦门市2020届高三高考化学模拟(5月份)理综化学试题(已下线)专题10 水溶液中的离子平衡-2020年高考真题和模拟题化学分项汇编河北省石家庄市2019届高三毕业班模拟考试(一)化学试题湖南省邵阳市2021-2022学年高三上学期第一次联考化学试题福建省福州第三中学2021-2022学年高三上学期第六次质量检测化学试题(已下线)专项13 水溶液中的离子平衡-备战2022年高考化学阶段性新题精选专项特训(全国卷)(3月期)广东省广州市第六中学2022届高三第三次模拟考试化学试题(已下线)第24讲 沉淀溶解平衡(练)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)化学(湖南A卷)-学易金卷:2023年高考化学第一次模拟考试卷(已下线)化学(湖北A卷)-学易金卷:2023年高考第一次模拟考试卷(已下线)化学(山东B卷)-学易金卷:2023年高考第一次模拟考试卷湖南省长沙市明达中学2022-2023学年高三下学期2月月考化学试题(已下线)第八章 水溶液中的离子反应与平衡 第53讲 沉淀溶解平衡图像的分析(已下线)2022年福建省高考真题变式题(选择题6-10)(已下线)第5讲 难溶电解质的溶解平衡陕西省西安交通大学附属中学2023-2024年高二上学期第一次月考化学试题
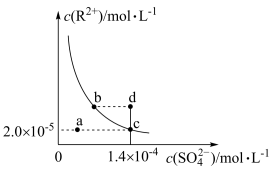
4 . 常温下某盐 在水中的溶解平衡曲线如图所示,下列说法错误的是
在水中的溶解平衡曲线如图所示,下列说法错误的是
 在水中的溶解平衡曲线如图所示,下列说法错误的是
在水中的溶解平衡曲线如图所示,下列说法错误的是
A.a点体系中存在平衡: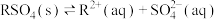 |
B.d点对应的体系中,分散质粒子直径大于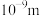 |
C.b、c两点均为 的饱和溶液 的饱和溶液 |
D.常温下 |
您最近一年使用:0次
2021-11-06更新
|
135次组卷
|
3卷引用:湖南省岳阳市岳阳县第一中学2021-2022学年高二下学期期末考试试题
名校
解题方法
5 . 请回答下列问题。
(1)用重铬酸钾法(一种氧化还原滴定法)可测定产物Fe3O4中的二价铁含量。若需配制浓度为0.01000mol•L-1的K2Cr2O7标准溶液240mL,应准确称取K2Cr2O7的质量是___________ g[保留4位有效数字,已知M(K2Cr2O7)=294.0g•mol-1]。
(2)金属表面处理、皮革鞣制、印染等都可能造成铬污染。六价铬比三价铬毒性高,更易被人体吸收且在体内蓄积。工业上处理酸性含Cr2O 废水的方法如下:
废水的方法如下:
①向含Cr2O 的酸性废水中加入FeSO4溶液,使Cr2O
的酸性废水中加入FeSO4溶液,使Cr2O 全部转化为Cr3+。写出该反应的离子方程式:
全部转化为Cr3+。写出该反应的离子方程式:___________ 。
②调节溶液的pH,使Cr3+完全沉淀。实验室粗略测定溶液pH的方法为___________ ;25℃,若调节溶液的pH=8,则溶液中残余Cr3+的物质的量浓度为___________ mol/L。(已知25℃时,Ksp[Cr(OH)3]=6.3×10-31)
(3)Na2S2O3是重要的化工原料,易溶于水,在中性或碱性环境中稳定。
测定产品(Na2S2O3•5H2O)纯度
准确称取Wg产品,用适量蒸馏水溶解,以淀粉做指示剂,用0.1000mol/L碘的标准溶液滴定,反应原理为:2S2O +I2=S4O
+I2=S4O +2I-。
+2I-。
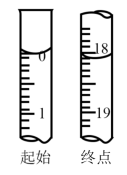
①滴定至终点时,溶液颜色的变化:由___________ 色变为___________ 色。
②滴定起始和终点的液面位置如图,则消耗点的标准溶液体积为18.10mL,产品的纯度为(设Na2S2O3•5H2O的相对分子质量为M)___________ 。
(1)用重铬酸钾法(一种氧化还原滴定法)可测定产物Fe3O4中的二价铁含量。若需配制浓度为0.01000mol•L-1的K2Cr2O7标准溶液240mL,应准确称取K2Cr2O7的质量是
(2)金属表面处理、皮革鞣制、印染等都可能造成铬污染。六价铬比三价铬毒性高,更易被人体吸收且在体内蓄积。工业上处理酸性含Cr2O
 废水的方法如下:
废水的方法如下:①向含Cr2O
 的酸性废水中加入FeSO4溶液,使Cr2O
的酸性废水中加入FeSO4溶液,使Cr2O 全部转化为Cr3+。写出该反应的离子方程式:
全部转化为Cr3+。写出该反应的离子方程式:②调节溶液的pH,使Cr3+完全沉淀。实验室粗略测定溶液pH的方法为
(3)Na2S2O3是重要的化工原料,易溶于水,在中性或碱性环境中稳定。
测定产品(Na2S2O3•5H2O)纯度
准确称取Wg产品,用适量蒸馏水溶解,以淀粉做指示剂,用0.1000mol/L碘的标准溶液滴定,反应原理为:2S2O
 +I2=S4O
+I2=S4O +2I-。
+2I-。
①滴定至终点时,溶液颜色的变化:由
②滴定起始和终点的液面位置如图,则消耗点的标准溶液体积为18.10mL,产品的纯度为(设Na2S2O3•5H2O的相对分子质量为M)
您最近一年使用:0次
6 . 已知相同温度下, 。某温度下,饱和溶液中
。某温度下,饱和溶液中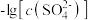 、
、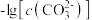 、与
、与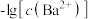 的关系如图所示。
的关系如图所示。
 。某温度下,饱和溶液中
。某温度下,饱和溶液中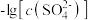 、
、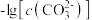 、与
、与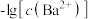 的关系如图所示。
的关系如图所示。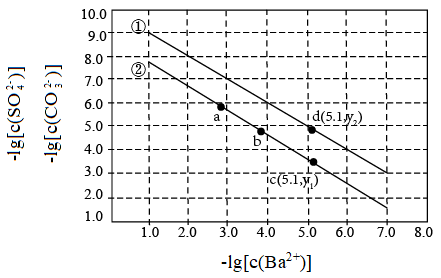
A.曲线①代表 的沉淀溶解曲线 的沉淀溶解曲线 |
B.该温度下 的 的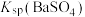 值为 值为 |
C.加适量 固体可使溶液由a点变到b点 固体可使溶液由a点变到b点 |
D. 时两溶液中 时两溶液中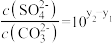 |
您最近一年使用:0次
2021-06-11更新
|
25707次组卷
|
71卷引用:湖南省岳阳市华容县普通高中2023届高三新高考适应性考试化学试题
湖南省岳阳市华容县普通高中2023届高三新高考适应性考试化学试题2021年高考全国甲卷化学真题重庆市缙云教育联盟2020-2021学年高二下学期期末质量检测化学试题(已下线)第八章能力提升检测卷(精练)-2022年高考化学一轮复习讲练测(已下线)考点26 难溶电解质的溶解平衡-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)课时45 难溶电解质的溶解平衡-2022年高考化学一轮复习小题多维练(全国通用)湖南省邵阳邵东市第一中学2022届高三上学期第一次月考化学试题河北省石家庄市第一中学2021-2022学年高二上学期10月月考化学试卷(已下线)第24讲 沉淀溶解平衡(讲)— 2022年高考化学一轮复习讲练测(新教材新高考)辽宁省东北育才学校2021-2022学年高二上学期期中考试化学试题河北省石家庄市第二中学2022届高三上学期11月第三次考试化学试题(已下线)2021年高考全国甲卷化学试题变式题(已下线)专题27 难溶电解质的溶解平衡(热点讲义)-2022年高三毕业班化学常考点归纳与变式演练(已下线)3.4.2 沉淀溶解平衡的应用-2021-2022学年高二化学课后培优练(人教版选修4)(已下线)专题12 水溶液中的离子平衡-备战2022年高考化学学霸纠错(全国通用)(已下线)第八单元 水溶液中的离子平衡(B卷 真题滚动练)-2022年高考化学一轮复习单元滚动双测卷(新高考地区专用)浙江省绍兴市诸暨中学2021-2022学年高二上学期期中考试(实验班)化学试题浙江省绍兴市诸暨中学2021-2022学年高二上学期期中考试(平行班)化学试题(已下线)解密10 水溶液中的离子平衡(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)专题13 水溶液中的离子平衡-2022年高考化学二轮复习重点专题常考点突破练(已下线)专题07 电解质溶液—2022年高考化学二轮复习讲练测(全国版)-练习山东省泰安市2021-2022学年高三下学期3月一模考试化学试题福建省三明第一中学2021-2022学年高二上学期第二次月考化学试题吉林省长春市2022届高三质量监测线上考试(三)理综化学试题(已下线)卷11 溶液中的离子平衡-【小题小卷】冲刺2022年高考化学小题限时集训(全国卷专用)(已下线)卷09 水溶液中的离子平衡-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)(已下线)【奋进985】08-备战2022年高考化学名校进阶模拟卷(通用版)云南省丽江市第一高级中学2021-2022学年高二下学期4月月考化学试题(已下线)押全国卷理综第12题 水溶液中的离子平衡-备战2022年高考化学临考题号押题(全国卷)(已下线)回归教材重难点07 图像数据和结果的分析-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)(已下线)回归教材重难点04 水溶液中的离子平衡-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)河南省商丘市五校2021-2022学年高二下学期5月联考化学试题(已下线)专题6 Ksp专练(已下线)专题10水溶液中的离子平衡-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题10水溶液中的离子平衡-五年(2018~2022)高考真题汇编(全国卷)黑龙江省饶河县高级中学2021-2022学年上学期期末考试化学试题(已下线)考点29 沉淀溶解平衡-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第33练 沉淀溶解平衡-2023年高考化学一轮复习小题多维练(全国通用)云南省玉溪市通海县第一中学2021-2022学年高二上学期期末考试化学试题第三章 综合拔高练(已下线)微专题39 水溶液中平衡图像的拓展与探析-备战2023年高考化学一轮复习考点微专题(已下线)第24讲 沉淀溶解平衡(讲)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)微专题42 四大平衡常数的计算与应用-备战2023年高考化学一轮复习考点微专题江苏省海安市立发中学2022-2023学年高三上学期学情检测卷(二)化学试题辽宁省沈阳市五校协作体2022-2023学年高二上学期期中考试化学试题(已下线)专题06 水溶液中的离子平衡(讲)-2023年高考化学二轮复习讲练测(新高考专用)广东省华南师范大学附属中学2022-2023学年高二上学期阶段检测化学B卷试题吉林省长春市第二实验中学2022-2023学年高二上学期期末考试化学试题湖南省株洲市第二中学2022-2023学年高二上学期期中考试化学试题湖南省株洲九方中学2022-2023学年高二上学期期中考试化学试题湖南省株洲市第八中学2022-2023学年高二上学期期中考试化学试题(已下线)专题22 沉淀溶解平衡及图像分析-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)第一部分 二轮专题突破 题型专攻4 电解质溶液各类图像的分析(已下线)第八章 水溶液中的离子反应与平衡 第53讲 沉淀溶解平衡图像的分析(已下线)题型142 有关沉淀溶解平衡图像江西省赣州市重点中学九校联盟2022-2023学年高二下学期第一次月考化学试题(已下线)素养卷05 电解质溶液中微粒变化图像题-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)(已下线)题型27 沉淀溶解平衡常数及其应用图象(已下线)专题16 水溶液中的离子平衡(已下线)专题16 水溶液中的离子平衡(已下线)专题09 水溶液中的离子平衡-2023年高考化学真题题源解密(新高考专用)黑龙江省齐齐哈尔市讷河市第二中学等3校2022-2023学年高二下学期开学考试化学试题微专题(12) 电解质溶液中的两类特殊图像微专题(九)——沉淀溶解平衡曲线(已下线)考点29 沉淀溶解平衡(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)考点4 沉淀溶解平衡 (核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)广东省广州市真光中学2023-2024学年高二上学期12月月考化学试题山东省菏泽市鄄城县第一中学2023-2024学年高三上学期1月月考化学试题山东省青岛第一中学2023-2024学年高二上学期第二次月考化学试卷云南省大理白族自治州实验中学2021-2022学年高二上学期10月月考化学试题福建省福建师范大学附属中学2023-2024学年高三上学期开学考化学试题
名校
7 . 2020年6月比亚迪正式发布采用磷酸铁锂技术的刀片电池,大幅度提高了电动汽车的续航里程,可媲美特斯拉。以硫铁矿(主要成分是FeS2,含少量Al2O3、SiO2和Fe3O4)为原料制备LiFePO4的流程如下:
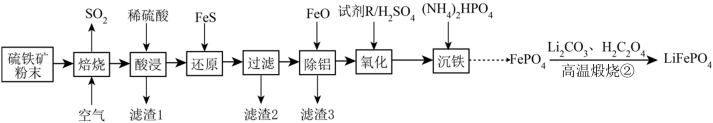
已知几种金属离子沉淀的pH如表所示:
请回答下列问题:
(1)“酸浸”需要适当加热,但温度不宜过高,其原因是___________ 。灼烧滤渣3得到固体的主要成分是___________ (写出化学式)。
(2)用FeS还原Fe3+的目的是___________ ,加入FeO的作用是___________ (用离子反应方程式表示)。
(3)试剂R宜选择___________ (填字母)。
A.高锰酸钾 B.稀硝酸 C.双氧水 D.次氯酸钠
(4)常温下,Ksp(FePO4)=1.3×10-22,“沉铁”中为了使c(Fe3+)≤1×10-5 mol·L-1,c(PO )最小为
)最小为___________ mol·L-1。
(5)写出“高温煅烧②”中由FePO4制备LiFePO4的化学方程式:___________ 。

已知几种金属离子沉淀的pH如表所示:
| 金属氢氧化物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
| 开始沉淀的pH | 2.3 | 7.5 | 4.0 |
| 完全沉淀的pH | 4.1 | 9.7 | 5.2 |
(1)“酸浸”需要适当加热,但温度不宜过高,其原因是
(2)用FeS还原Fe3+的目的是
(3)试剂R宜选择
A.高锰酸钾 B.稀硝酸 C.双氧水 D.次氯酸钠
(4)常温下,Ksp(FePO4)=1.3×10-22,“沉铁”中为了使c(Fe3+)≤1×10-5 mol·L-1,c(PO
 )最小为
)最小为(5)写出“高温煅烧②”中由FePO4制备LiFePO4的化学方程式:
您最近一年使用:0次
2021-03-27更新
|
515次组卷
|
3卷引用:湖南省岳阳市2021届高三二模考试化学试题
19-20高三·江苏苏州·期末
名校
8 . 黄铁矿(主要成分FeS2),在空气中会被缓慢氧化,氧化过程如图所示。下列说法不正确的是


| A.发生反应a时,0.05 mol FeS2被氧化时消耗标准状况下氧气的体积大约3.92 L |
| B.为了验证b过程反应后溶液中含Fe2+,可选用KSCN溶液和氯水 |
C.c发生反应的离子方程式为:14Fe3++FeS2+8H2O=15Fe2++2 +16H+ +16H+ |
| D.已知25 ℃时,Ksp[Fe(OH)3]=2.79×10-39,则该温度下d反应的逆反应的平衡常数为K=2.79×103 |
您最近一年使用:0次
名校
解题方法
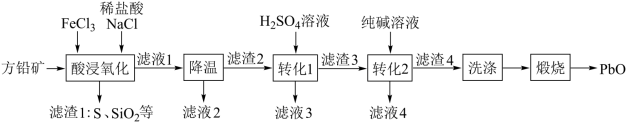
9 . 纳米级PbO是大规模集成电路(IC)制作过程中的关键性基础材料。一种以方铅矿(含PbS及少量Fe2O3、MgO、SiO2等)为原料制备PbO的工艺流程如图:
已知:[PbCl4]2-(aq) PbCl2(s)+2Cl-(aq) ΔH<0
PbCl2(s)+2Cl-(aq) ΔH<0
回答下列问题:
(1)“酸浸氧化”过程中被氧化的元素是:______ ,该过程需要加热,其目的是______ 。FeCl3与PbS发生反应生成[PbCl4]2-的离子方程式为______ 。
(2)检验滤液1中存在Fe2+,可取样后滴加少量______ 溶液(填化学式),观察到有蓝色沉淀析出。
(3)“降温”步骤中析出的晶体主要是______ (填化学式);滤液2中的金属阳离子有Na+、Fe3+、______ 。(填离子符号)
(4)要实现PbSO4转化为PbCO3,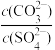 的最小值为
的最小值为______ 。(Ksp(PbCO3)=7.4×10-14、Ksp(PbSO4)=1.6×10-8)(保留两位有效数字)
(5)“煅烧”时,PbCO3发生反应的化学方程式为______ 。

已知:[PbCl4]2-(aq)
 PbCl2(s)+2Cl-(aq) ΔH<0
PbCl2(s)+2Cl-(aq) ΔH<0回答下列问题:
(1)“酸浸氧化”过程中被氧化的元素是:
(2)检验滤液1中存在Fe2+,可取样后滴加少量
(3)“降温”步骤中析出的晶体主要是
(4)要实现PbSO4转化为PbCO3,
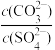 的最小值为
的最小值为(5)“煅烧”时,PbCO3发生反应的化学方程式为
您最近一年使用:0次
2021-03-13更新
|
707次组卷
|
3卷引用:湖南省岳阳市2021-2022学年高三教学质量监测(三)化学试题
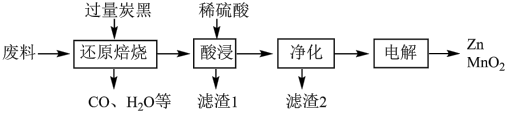
10 . 锰是重要的合金材料和催化剂,在工农业生产和科技领域有广泛的用途。利用某工业废料[含MnO2、MnOOH、Zn(OH)2及少量Fe]制备Zn和MnO2的一种工艺流程如图所示:
已知:
①MnO能溶于酸,且Mn2+在酸性条件下比较稳定,pH高于5.5时易被O2氧化。
②室温下,Ksp[Mn(OH)2]=10-13,Ksp[Fe(OH)3]=10-38,Ksp[Zn(OH)2]=10-17(当离子浓度≤10-5mol·L-1可认为沉淀完全)
下列说法错误的是

已知:
①MnO能溶于酸,且Mn2+在酸性条件下比较稳定,pH高于5.5时易被O2氧化。
②室温下,Ksp[Mn(OH)2]=10-13,Ksp[Fe(OH)3]=10-38,Ksp[Zn(OH)2]=10-17(当离子浓度≤10-5mol·L-1可认为沉淀完全)
下列说法错误的是
| A.加入过量炭黑主要作用是将MnO2、MnOOH转化为MnO |
| B.“酸浸”时,不可以用浓盐酸代替稀硫酸 |
| C.“净化”时,溶液中Mn2+、Zn2+的浓度约为0.1mol·L-1,调节pH的合理范围是3≤pH<8 |
| D.“电解”时,阳极产物制得MnO2,阴极制得Zn,余下电解质溶液经处理可循环使用 |
您最近一年使用:0次
2021-01-06更新
|
1143次组卷
|
8卷引用:湖南省岳阳县一中2022届高三年级入学考试化学试题
湖南省岳阳县一中2022届高三年级入学考试化学试题山东省寿光现代中学2021届高三上学期1月月考化学试题(已下线)解密10 水溶液中离子反应(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(已下线)解密10 水溶液中离子反应(分层训练)-【高频考点解密】2021年高考化学二轮复习讲义+分层训练(浙江专版)(已下线)热点8 无机化工流程分析(选择题)-2021年高考化学【热点·重点·难点】专练(山东专用)湖南省新高考联盟2021届高三下学期3月提升检测化学(A)试题(已下线)专题13 水溶液中的离子平衡-2022年高考化学二轮复习重点专题常考点突破练重庆市第一中学校2021-2022学年高三3月月考化学试题



