1 . (1)联氨( )是二元弱碱,在水中的电离方程式与氨相似,联氨第一步电离反应的平衡常数值为
)是二元弱碱,在水中的电离方程式与氨相似,联氨第一步电离反应的平衡常数值为______ 。(已知: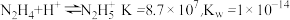 ),联氨与硫酸形成的酸式盐的化学式为
),联氨与硫酸形成的酸式盐的化学式为_______ 。
(2)0.20mol/L的小苏打溶液中各离子浓度由小到大的顺序是___ 。
(3)如图所示为二元酸H2A溶液中各微粒的物质的量分数(δ)随溶液pH的变化曲线(25°C)。
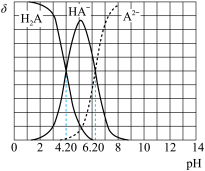
H2A的电离平衡常数 =
=_________ ,溶液pH=7时,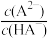 =
=_______ 。
 )是二元弱碱,在水中的电离方程式与氨相似,联氨第一步电离反应的平衡常数值为
)是二元弱碱,在水中的电离方程式与氨相似,联氨第一步电离反应的平衡常数值为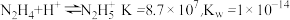 ),联氨与硫酸形成的酸式盐的化学式为
),联氨与硫酸形成的酸式盐的化学式为(2)0.20mol/L的小苏打溶液中各离子浓度由小到大的顺序是
(3)如图所示为二元酸H2A溶液中各微粒的物质的量分数(δ)随溶液pH的变化曲线(25°C)。

H2A的电离平衡常数
 =
=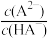 =
=
您最近一年使用:0次
名校
解题方法
2 . (1)pH相同的下列物质的溶液①(NH4)2SO4;②NH4HSO4;③NH4NO3,铵根离子浓度由小到大的顺序是__________ (填序号)。
(2)同浓度的下列溶液:①HCl;②NH4Cl;③Na2CO3;④NaHCO3,其中pH由大到小的顺序是______________ 。
(3)物质的量浓度相同的①盐酸、②硫酸溶液、元③醋酸(CH3COOH)溶液各100mL分别与足量的Zn反应,在相同的条件下,产生H2的体积分别为V1、V2、V3,它们由大到小的顺序是___________ 。
(4)等体积的CH3COOH与NaOH溶液反应后溶液中存在c(Na+)<c(CH3COO-),该溶液呈______ 性(填“酸”、“碱”或“中”),反应前c(NaOH)_____ c(CH3COOH)(填“>”“<”或“=”)
(5)在化学分析中采用K2CrO4为指示剂,以AgNO3标准溶液滴定溶液中Cl-,利用Ag+与 生成砖红色沉淀,指示到达滴定终点。当溶液中Cl-恰好沉淀完全(浓度等于1.0×10-5mol/L)时,溶液中c(Ag+)为
生成砖红色沉淀,指示到达滴定终点。当溶液中Cl-恰好沉淀完全(浓度等于1.0×10-5mol/L)时,溶液中c(Ag+)为____ mol/L,此时溶液中c(CrO42-)等于_____ mol/L。(已知Ag2CrO4、AgCl的Ksp分别为2.0×10-12和2.0×10-10)。
(2)同浓度的下列溶液:①HCl;②NH4Cl;③Na2CO3;④NaHCO3,其中pH由大到小的顺序是
(3)物质的量浓度相同的①盐酸、②硫酸溶液、元③醋酸(CH3COOH)溶液各100mL分别与足量的Zn反应,在相同的条件下,产生H2的体积分别为V1、V2、V3,它们由大到小的顺序是
(4)等体积的CH3COOH与NaOH溶液反应后溶液中存在c(Na+)<c(CH3COO-),该溶液呈
(5)在化学分析中采用K2CrO4为指示剂,以AgNO3标准溶液滴定溶液中Cl-,利用Ag+与
 生成砖红色沉淀,指示到达滴定终点。当溶液中Cl-恰好沉淀完全(浓度等于1.0×10-5mol/L)时,溶液中c(Ag+)为
生成砖红色沉淀,指示到达滴定终点。当溶液中Cl-恰好沉淀完全(浓度等于1.0×10-5mol/L)时,溶液中c(Ag+)为
您最近一年使用:0次
2020-11-07更新
|
1001次组卷
|
4卷引用:安徽省六安市第一中学2020-2021学年高二上学期第一次段考化学试题
安徽省六安市第一中学2020-2021学年高二上学期第一次段考化学试题(已下线)第3章 水溶液中的离子反应与平衡(能力提升卷)-【高效检测】2021-2022学年高二化学章末测试卷(人教版2019选择性必修1)天津市第一中学2022-2023学年高二上学期月考化学试题辽宁省铁岭市昌图县第一高级中学2023-2024学年高二上学期9月考试化学试题
3 . (1)已知某温度时,KW=1.0×10-12 ,Na2CO3溶液的水解常数Kh=2.0×10-3,则当溶液中c(HCO )∶c(CO
)∶c(CO )=2∶1时,试求该溶液的pH=
)=2∶1时,试求该溶液的pH=______ 。
(2)已知25 ℃时,NH3·H2O的电离平衡常数Kb=1.8×10-5,该温度下1 mol·L-1的NH4Cl溶液中c(H+)=____________ mol·L-1。(已知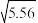 ≈2.36)
≈2.36)
(3)25 ℃时,H2SO3 HSO
HSO +H+的电离常数Ka=1×10-2,则该温度下NaHSO3水解反应的平衡常数Kh=
+H+的电离常数Ka=1×10-2,则该温度下NaHSO3水解反应的平衡常数Kh=________________ ,若向NaHSO3溶液中加入少量的I2,则溶液中 将
将________ (填“增大”“减小”或“不变”)。
(4)已知常温下CN-的水解常数Kh=1.61×10-5。
①常温下,含等物质的量浓度的HCN与NaCN的混合溶液显_____ (填“酸”“碱”或“中”)性,c(CN-)________ (填“>”“<”或“=”)c(HCN)。该溶液中各离子浓度由大到小的顺序为____________ 。
②常温下,若将c mol·L-1盐酸与0.62 mol·L-1KCN溶液等体积混合后恰好得到中性溶液,则c=________ (小数点后保留4位数字)。
 )∶c(CO
)∶c(CO )=2∶1时,试求该溶液的pH=
)=2∶1时,试求该溶液的pH=(2)已知25 ℃时,NH3·H2O的电离平衡常数Kb=1.8×10-5,该温度下1 mol·L-1的NH4Cl溶液中c(H+)=
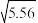 ≈2.36)
≈2.36)(3)25 ℃时,H2SO3
 HSO
HSO +H+的电离常数Ka=1×10-2,则该温度下NaHSO3水解反应的平衡常数Kh=
+H+的电离常数Ka=1×10-2,则该温度下NaHSO3水解反应的平衡常数Kh= 将
将(4)已知常温下CN-的水解常数Kh=1.61×10-5。
①常温下,含等物质的量浓度的HCN与NaCN的混合溶液显
②常温下,若将c mol·L-1盐酸与0.62 mol·L-1KCN溶液等体积混合后恰好得到中性溶液,则c=
您最近一年使用:0次
2020-10-15更新
|
978次组卷
|
3卷引用:安徽省阜阳市太和第一中学2020-2021学年高二上学期10月月考化学试题
安徽省阜阳市太和第一中学2020-2021学年高二上学期10月月考化学试题(已下线)全册综合检测(一)-2020-2021学年高二化学选择性必修1同步单元AB卷(新教材鲁科版)安徽省桐城中学2020-2021学年高二上学期12月月考化学试题
名校
解题方法
4 . (1)已知100℃时,水的离子积常数为1×10-12,将此温度下pH=1的H2SO4溶液aL与pH=11的NaOH溶液bL混合,若所得混合液pH=2,则a:b=______ 。
(2)0.1mol/L NaHS溶液显碱性,则c(S2﹣)_____ c(H2S)(填“>”,“<”或“=”)。
(3)常温下,向0.2mol/L的H2S溶液中逐滴滴入0.2mol/L NaOH溶液至中性,此时溶液中以下所示关系一定正确的是_____ 。
A c(H+)•c(OH﹣)=1×10﹣14 B c(Na+)=c(HS﹣)+2c(S2﹣)
C c(Na+)>c(HS﹣)+c(S2﹣)+c(H2S) D c(H2S)>c(S2﹣)
(4)Na2S溶液中存在多种平衡,写出其物料守恒:_______ 。
(5)已知Ka(HA)>Ka(HB)。现有温度、物质的量浓度和体积均相同的NaA和NaB两种溶液,若前者溶液中所有离子数目为n1,后者的所有离子数目为n2, 则n1______ n2。(填>、=或<)
(2)0.1mol/L NaHS溶液显碱性,则c(S2﹣)
(3)常温下,向0.2mol/L的H2S溶液中逐滴滴入0.2mol/L NaOH溶液至中性,此时溶液中以下所示关系一定正确的是
A c(H+)•c(OH﹣)=1×10﹣14 B c(Na+)=c(HS﹣)+2c(S2﹣)
C c(Na+)>c(HS﹣)+c(S2﹣)+c(H2S) D c(H2S)>c(S2﹣)
(4)Na2S溶液中存在多种平衡,写出其物料守恒:
(5)已知Ka(HA)>Ka(HB)。现有温度、物质的量浓度和体积均相同的NaA和NaB两种溶液,若前者溶液中所有离子数目为n1,后者的所有离子数目为n2, 则n1
您最近一年使用:0次
解题方法
5 . 按要求填空。
(1)AlCl3溶液呈_____ 性(填“酸”“中”或“碱”),原因是_______ (用离子方程式表示)。把AlCl3溶液蒸干、灼烧,最后得到的主要固体产物是______ (写化学式)。实验室在保存AlCl3溶液时,常在溶液中加少量的________ ,以抑制其水解。
(2)25℃时,将pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后溶液呈____ 性(填“酸”“中”或“碱”)。
(3)已知0.1 mol·L-1的NaHSO3溶液pH=5,则溶液中离子浓度从大到小关系为______ 。
(4)常温下,将pH=12的Ba(OH)2溶液aL和pH=2的盐酸bL混合后pH=11,则a∶b的值为________ 。
(5)常温下,a mol/L的盐酸与b mol/L 的氨水等体积混合后溶液呈中性,则Kb(NH3·H2O)=_____ (用含a、b的代数式表示) 。
(1)AlCl3溶液呈
(2)25℃时,将pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后溶液呈
(3)已知0.1 mol·L-1的NaHSO3溶液pH=5,则溶液中离子浓度从大到小关系为
(4)常温下,将pH=12的Ba(OH)2溶液aL和pH=2的盐酸bL混合后pH=11,则a∶b的值为
(5)常温下,a mol/L的盐酸与b mol/L 的氨水等体积混合后溶液呈中性,则Kb(NH3·H2O)=
您最近一年使用:0次
2020-10-13更新
|
217次组卷
|
2卷引用:浙江省苍南县金乡卫城中学2020-2021学年高二上学期第一次月考化学试题
解题方法
6 . 室温下,已知: 的电离平衡常数
的电离平衡常数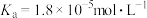 ;
; 的电离平衡常数
的电离平衡常数 、
、 ,回答下列问题:
,回答下列问题:
(1)室温时,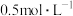 的醋酸溶液中由醋酸电离出的
的醋酸溶液中由醋酸电离出的 约是由水电离出的
约是由水电离出的 的
的________ 倍。
(2)室温时, 的水解平衡常数
的水解平衡常数
________ , 溶液中的各离子浓度由大到小的顺序为
溶液中的各离子浓度由大到小的顺序为________________ 。若向 溶液中加入少量
溶液中加入少量 ,则溶液中
,则溶液中 将
将________ (填“增大”“减小”或“不变”)。
(3)室温时, 溶液的
溶液的
________ 。
 的电离平衡常数
的电离平衡常数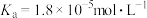 ;
; 的电离平衡常数
的电离平衡常数 、
、 ,回答下列问题:
,回答下列问题:(1)室温时,
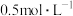 的醋酸溶液中由醋酸电离出的
的醋酸溶液中由醋酸电离出的 约是由水电离出的
约是由水电离出的 的
的(2)室温时,
 的水解平衡常数
的水解平衡常数
 溶液中的各离子浓度由大到小的顺序为
溶液中的各离子浓度由大到小的顺序为 溶液中加入少量
溶液中加入少量 ,则溶液中
,则溶液中 将
将(3)室温时,
 溶液的
溶液的
您最近一年使用:0次
解题方法
7 . 室温下,有下列溶液:
(1)0.2mol·L-1HR溶液与0.1mol·L-1NaOH溶液等体积混合,测得混合溶液pH<7,则说明在相同条件下HR的电离程度_____ NaR的水解程度(填“>”、“<”或“=”),混合溶液中各离子浓度的大小顺序为_________ 。
(2)pH=3的0.1mol·L−1NH4Al(SO4)2溶液中c( )+c(NH3·H2O)
)+c(NH3·H2O)____ c(Al3+)+c[Al(OH)3](填“﹥”、“﹤”或“=”);2c( )-c(
)-c( )-3c(Al3+)=
)-3c(Al3+)=_________ mol·L−1(填准确数值)。
(3)已知:Ksp[Cu(OH)2]=2.2×10-20、Ksp[Fe(OH)3]=4.0×10-38、Ksp[Mn(OH)2]=2.1×10-13。若某溶液中c(Cu2+)=2.2mol·L-1、c(Fe3+)=0.008mol·L-1、c(Mn2+)=0.21mol·L-1,向其中逐滴加入稀氨水,先生成的沉淀是_____ (填化学式);为尽可能多地回收铜,而不让锰析出,所得滤液的pH最大值为_____ 。
(1)0.2mol·L-1HR溶液与0.1mol·L-1NaOH溶液等体积混合,测得混合溶液pH<7,则说明在相同条件下HR的电离程度
(2)pH=3的0.1mol·L−1NH4Al(SO4)2溶液中c(
 )+c(NH3·H2O)
)+c(NH3·H2O) )-c(
)-c( )-3c(Al3+)=
)-3c(Al3+)=(3)已知:Ksp[Cu(OH)2]=2.2×10-20、Ksp[Fe(OH)3]=4.0×10-38、Ksp[Mn(OH)2]=2.1×10-13。若某溶液中c(Cu2+)=2.2mol·L-1、c(Fe3+)=0.008mol·L-1、c(Mn2+)=0.21mol·L-1,向其中逐滴加入稀氨水,先生成的沉淀是
您最近一年使用:0次
解题方法
8 . 散尾葵是城市盆栽的常见景观植物,其营养液为 KNO3、Mg(NO3)2、FeCl3组成的混合液,2L该混合液中部分离子浓度大小如图所示,回答下列问题:

(1)该混合液中c( -)=
-)=__________ mol•L-1。
(2)该混合液中,KNO3的物质的量为________ mol,FeCl3的质量为______ g。
(3)将该混合液加水稀释至10L,稀释后溶液中Fe3+的物质的量浓度为__ mol•L-1。
(4)向该混合液中加入足量 NaOH 溶液,可得到沉淀的物质的量为________ mol。
(5)向该混合液中加入足量铁粉,溶液可增重________________ g。

(1)该混合液中c(
 -)=
-)=(2)该混合液中,KNO3的物质的量为
(3)将该混合液加水稀释至10L,稀释后溶液中Fe3+的物质的量浓度为
(4)向该混合液中加入足量 NaOH 溶液,可得到沉淀的物质的量为
(5)向该混合液中加入足量铁粉,溶液可增重
您最近一年使用:0次
解题方法
9 . 电解质在水溶液中存在各种行为,如电离、水解等,依据所学知识回答下列问题:
(1)t℃时,纯水中c(H+)=1×10-6mol·L-1,该温度下,pH=10的NaOH溶液的物质的量浓度为___ 。
(2)25℃时,相同物质的量浓度的下列溶液中:①NaCl②NH3·H2O③H2SO4④(NH4)2SO4,其中水的电离程度由大到小顺序为___ (填标号)。
(3)25℃时,将amol·L-1的醋酸和bmol·L-1的氢氧化钠溶液等体积混合后,溶液的pH=7,则a___ b(填“>”“<”或“=”)。
(1)t℃时,纯水中c(H+)=1×10-6mol·L-1,该温度下,pH=10的NaOH溶液的物质的量浓度为
(2)25℃时,相同物质的量浓度的下列溶液中:①NaCl②NH3·H2O③H2SO4④(NH4)2SO4,其中水的电离程度由大到小顺序为
(3)25℃时,将amol·L-1的醋酸和bmol·L-1的氢氧化钠溶液等体积混合后,溶液的pH=7,则a
您最近一年使用:0次
2020-05-16更新
|
102次组卷
|
2卷引用:福建省宁德市2019-2020学年高二上学期期末考试化学试题
解题方法
10 . 按要求填空:
(1)Cr(OH)3在溶液中存在以下沉淀溶解平衡:Cr(OH)3(s)⇌Cr3+(aq)+3OH-(aq)。常温下,Cr(OH)3溶度积Ksp=1.0×10-32,要使c(Cr3+)完全沉淀,溶液的pH应调至______ 。
(2)25℃时,向水的电离平衡体系中加入少量碳酸钠固体,得到pH为11的溶液,其水解方程式为_________ ,由水电离出的c(OH-)=________ mol·L-1。
(3)在100℃下,将pH=3的硫酸溶液和pH=10的NaOH溶液混合,若要使混合后溶液的pH=7,则硫酸溶液和NaOH溶液的体积比约为_____ 。
(1)Cr(OH)3在溶液中存在以下沉淀溶解平衡:Cr(OH)3(s)⇌Cr3+(aq)+3OH-(aq)。常温下,Cr(OH)3溶度积Ksp=1.0×10-32,要使c(Cr3+)完全沉淀,溶液的pH应调至
(2)25℃时,向水的电离平衡体系中加入少量碳酸钠固体,得到pH为11的溶液,其水解方程式为
(3)在100℃下,将pH=3的硫酸溶液和pH=10的NaOH溶液混合,若要使混合后溶液的pH=7,则硫酸溶液和NaOH溶液的体积比约为
您最近一年使用:0次



