名校
1 . 草酸镍晶体( )可用于制镍催化剂。工业上用废镍催化剂(主要成分为Al2O3、Ni、Fe、SiO2、CaO)制备草酸镍晶体的一种工艺流程如图所示:
)可用于制镍催化剂。工业上用废镍催化剂(主要成分为Al2O3、Ni、Fe、SiO2、CaO)制备草酸镍晶体的一种工艺流程如图所示:

已知:
①相关金属离子生成氢氧化物沉淀的pH如下表(开始沉淀的pH按金属离子浓度为 计算):
计算):
② ,
,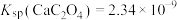 。
。
回答下列问题:
(1)基态镍原子的价层电子排布式为___________ 。
(2)试剂X可以是___________ ,
(3)调节pH的范围是___________ 。
(4)滤渣1的成分是___________ (写化学式),加入适量NH4F溶液的目的是___________ 。
(5)“沉镍”的离子方程式为___________ 。
(6)称取一定质量某镀镍试剂,配成100mL溶液,溶液中存在的离子为 、
、 、
、 ;准确量取10.00mL溶液,用
;准确量取10.00mL溶液,用 的EDTA标准溶液滴定其中的
的EDTA标准溶液滴定其中的 ,消耗EDTA标准溶液25.00mL。已知M2+为金属阳离子,与EDTA反应的方程式为:M2++EDTA4-=MEDTA2-。
,消耗EDTA标准溶液25.00mL。已知M2+为金属阳离子,与EDTA反应的方程式为:M2++EDTA4-=MEDTA2-。
①配制EDTA标准溶液需要注意蒸馏水的水质,水中若含 、
、 会使滴定时消耗的EDTA的体积
会使滴定时消耗的EDTA的体积___________ (填“偏大”“不变”或“偏小”)。
②该镀镍试剂中 的物质的量浓度为
的物质的量浓度为___________ mol/L。
 )可用于制镍催化剂。工业上用废镍催化剂(主要成分为Al2O3、Ni、Fe、SiO2、CaO)制备草酸镍晶体的一种工艺流程如图所示:
)可用于制镍催化剂。工业上用废镍催化剂(主要成分为Al2O3、Ni、Fe、SiO2、CaO)制备草酸镍晶体的一种工艺流程如图所示:
已知:
①相关金属离子生成氢氧化物沉淀的pH如下表(开始沉淀的pH按金属离子浓度为
 计算):
计算):| 金属离子 | 开始沉淀的pH | 沉淀完全的pH |
 | 1.1 | 3.2 |
 | 5.8 | 8.8 |
 | 3.0 | 5.0 |
 | 6.7 | 9.5 |
 ,
,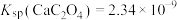 。
。回答下列问题:
(1)基态镍原子的价层电子排布式为
(2)试剂X可以是
(3)调节pH的范围是
(4)滤渣1的成分是
(5)“沉镍”的离子方程式为
(6)称取一定质量某镀镍试剂,配成100mL溶液,溶液中存在的离子为
 、
、 、
、 ;准确量取10.00mL溶液,用
;准确量取10.00mL溶液,用 的EDTA标准溶液滴定其中的
的EDTA标准溶液滴定其中的 ,消耗EDTA标准溶液25.00mL。已知M2+为金属阳离子,与EDTA反应的方程式为:M2++EDTA4-=MEDTA2-。
,消耗EDTA标准溶液25.00mL。已知M2+为金属阳离子,与EDTA反应的方程式为:M2++EDTA4-=MEDTA2-。①配制EDTA标准溶液需要注意蒸馏水的水质,水中若含
 、
、 会使滴定时消耗的EDTA的体积
会使滴定时消耗的EDTA的体积②该镀镍试剂中
 的物质的量浓度为
的物质的量浓度为
您最近一年使用:0次
2 . 向AgCl饱和溶液(有足量AgCl固体)中滴加氨水,发生反应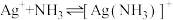 和
和 ,
,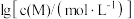 与
与 的关系如下图所示(其中M代表
的关系如下图所示(其中M代表 、
、 、[Ag(NH3)]+或
、[Ag(NH3)]+或 )。
)。
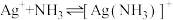 和
和 ,
,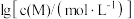 与
与 的关系如下图所示(其中M代表
的关系如下图所示(其中M代表 、
、 、[Ag(NH3)]+或
、[Ag(NH3)]+或 )。
)。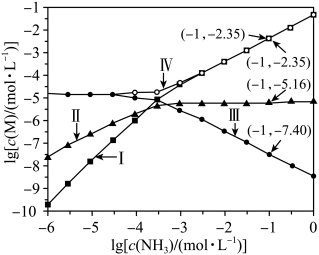
A.曲线IV可视为AgCl溶解度随 浓度变化曲线 浓度变化曲线 |
B.反应 的平衡常数K的值为 的平衡常数K的值为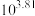 |
| C.c(NH3)=0.01mol·L-1时,溶液中c([Ag(NH3)2]+)>c([Ag(NH3)]+)>c(Ag+) |
D.AgCl的溶度积常数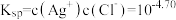 |
您最近一年使用:0次
名校
解题方法
3 . 由下列实验操作及现象能得出相应结论的是
| 实验操作 | 现象 | 结论及解释 | |
| A | 向KBr、KI混合溶液中依次加入少量氯水和CCl4,振荡,静置 | 溶液分层,下层呈紫红色 | 氧化性:Cl2>Br2>I2 |
| B | 在火焰上灼烧搅拌过某无色溶液的玻璃棒 | 火焰出现黄色 | 溶液中含Na元素 |
| C | 用pH计测定pH:①NaHCO3溶液 ②CH3COONa溶液 | pH:①>②; | H2CO3酸性弱于CH3COOH |
| D | 向盛有少量Mg(OH)2沉淀的试管中 加入适量饱和NH4Cl溶液,振荡 | 白色沉淀溶解 |  结合OH-使Mg(OH)2沉淀溶解平衡向右移动 结合OH-使Mg(OH)2沉淀溶解平衡向右移动 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-06-21更新
|
290次组卷
|
4卷引用:四川省成都市新都区2022-2023学年高三上学期期末摸底测试理科综合化学试题
名校
解题方法
4 . 铟(In)是一种稀散金属,常与其他金属矿石伴生,回收氧化锌烟尘(主要成分是ZnO,还含少量PbO、FeS、FeSiO3、 In2O3、 In2S3等)中的金属铟的工艺流程如下:
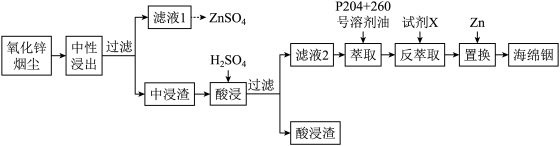
已知:室温下,金属离子开始沉淀和完全沉淀的pH如表所示。
回答下列问题:
(1)In2O3中In的化合价是_______________________ 。
(2)“中性浸出”的过程为:先加入稀硫酸和适量氧化剂MnO2氧化酸浸氧化锌烟尘,反应结束前半个小时加入CaO调整pH=5.0~5.2。
①FeSiO3与稀H2SO4反应的化学方程式为____________________________________________ 。
②氧化酸浸过程中,In2S3中的硫元素被MnO2氧化为 ,该反应的离子方程式为
,该反应的离子方程式为____________________ 。
③氧化剂用量对中性浸出效果的影响如图所示。最佳氧化剂用量为_________________ 。
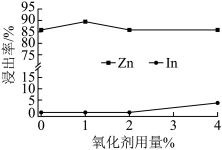
④“中浸渣”的主要成分为In(OH)3、________________ 。 (写化学式)
(3)萃取时,发生反应In3+ +3H2A2 In(HA2)3 +3H+,H2A2代表有机萃取剂。
In(HA2)3 +3H+,H2A2代表有机萃取剂。
①反萃取时,宜选用的试剂X为_____________________ (写化学式)
②实验室进行萃取和反萃取时,均需要使用的玻璃仪器有_________________________ 。
(4)“置换”后的滤液可返回________________________ (填“滤液 1”或“滤液2”)中利用。
(5)“置换”时锌粉的利用率为90%,若想获得6.9 kg海绵铟,需要使用锌粉___ _kg (结果保留1位小数)

已知:室温下,金属离子开始沉淀和完全沉淀的pH如表所示。
金属离子 | Fe3+ | Fe2+ | In3+ |
开始沉淀pH(离子浓度为0.1mol·L-1时) | 1.3 | 6 | 3 |
完全沉淀pH | 2.7 | 8 | 4.3 |
(1)In2O3中In的化合价是
(2)“中性浸出”的过程为:先加入稀硫酸和适量氧化剂MnO2氧化酸浸氧化锌烟尘,反应结束前半个小时加入CaO调整pH=5.0~5.2。
①FeSiO3与稀H2SO4反应的化学方程式为
②氧化酸浸过程中,In2S3中的硫元素被MnO2氧化为
 ,该反应的离子方程式为
,该反应的离子方程式为③氧化剂用量对中性浸出效果的影响如图所示。最佳氧化剂用量为

④“中浸渣”的主要成分为In(OH)3、
(3)萃取时,发生反应In3+ +3H2A2
 In(HA2)3 +3H+,H2A2代表有机萃取剂。
In(HA2)3 +3H+,H2A2代表有机萃取剂。①反萃取时,宜选用的试剂X为
②实验室进行萃取和反萃取时,均需要使用的玻璃仪器有
(4)“置换”后的滤液可返回
(5)“置换”时锌粉的利用率为90%,若想获得6.9 kg海绵铟,需要使用锌粉
您最近一年使用:0次
名校
解题方法
5 . 回答下列问题
(1)写出过量Mg(OH)2固体放入水中溶解形成饱和溶液时的溶解平衡表达式________________________________ ,向有Mg(OH)2沉淀的溶液中加入过量浓NH4Cl,溶液变澄清,相关反应的化学方程式为____________________________ ,已知室温时饱和的Mg(OH)2溶液的pH=10,则Mg(OH)2的溶度积为___________ 。
(2)明矾是KAl(SO4)2·12H2O,其溶液中离子浓度由大到小的顺序______________________ ;向明矾溶液中逐渐滴入Ba(OH)2 溶液至SO 离子恰好沉淀完全时,溶液的显
离子恰好沉淀完全时,溶液的显_______ 性(填酸、碱、中),离子反应的总方程式:_________________________________________________ 。
(3)为配制SbCl3溶液,取少量SbCl3固体,加2mL~3mL水溶解,此时却会产生白色沉淀Sb2O3,写出此时反应的化学方程式为:___________________________ ,故在配制SbCl3溶液时应加少量____________ 。
(1)写出过量Mg(OH)2固体放入水中溶解形成饱和溶液时的溶解平衡表达式
(2)明矾是KAl(SO4)2·12H2O,其溶液中离子浓度由大到小的顺序
 离子恰好沉淀完全时,溶液的显
离子恰好沉淀完全时,溶液的显(3)为配制SbCl3溶液,取少量SbCl3固体,加2mL~3mL水溶解,此时却会产生白色沉淀Sb2O3,写出此时反应的化学方程式为:
您最近一年使用:0次
6 . 化学与生产生活密切相关,下列说法错误的是
| A.工业使用的碳纤维属于新型有机高分子材料 |
| B.科研上可以用Na2S作废水中Cu2+的沉淀剂 |
| C.硫酸是工业生产过磷酸钙肥料的原料之一 |
| D.葡萄糖可以用于食品加工和合成补钙药物 |
您最近一年使用:0次
名校
解题方法
7 . 根据下列实验操作,现象和结论都正确的是
| 实验操作 | 现象 | 结论 | |
| A | 等体积、pH=3的两种酸HA和HB,分别与足量Zn反应 | HA放出的氢气多 | 酸性:HA<HB |
| B | 向AgNO3溶液中依次滴加NaCl、KI溶液 | 依次出现白色、黄色沉淀 | 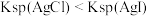 |
| C | 用pH试纸测定NaCl与NaF溶液的pH | 前者小于后者 | 非金属性:F<Cl |
| D | 用pH试纸测定饱和新制氯水的pH | pH试纸变红色 | 饱和新制氯水呈酸性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-05-15更新
|
281次组卷
|
2卷引用:四川省绵阳南山中学2023-2024学年高二下学期入学考试化学试题
名校
8 . 某温度下,Ksp(MnS)=2×10-13,Ksp(PbS)=2×10-28,生产中用MnS作为沉淀剂除去工业废水中Pb2+,其反应原理为Pb2+(aq)+MnS(s) PbS(s)+Mn2+(aq)。下列说法正确的是
PbS(s)+Mn2+(aq)。下列说法正确的是
 PbS(s)+Mn2+(aq)。下列说法正确的是
PbS(s)+Mn2+(aq)。下列说法正确的是| A.该反应的平衡常数K=1015 |
| B.PbS悬浊液中:c(Pb2+)=1×10-14mol•L-1 |
| C.该反应达平衡时c(Mn2+)=c(Pb2+) |
| D.其他条件不变,使平衡体系中c(Mn2+)增大,则c(Pb2+)减小 |
您最近一年使用:0次
2023-05-11更新
|
330次组卷
|
5卷引用:四川省广元市苍溪中学校2023-2024学年高二上学期12月月考化学试题
名校
9 . 某温度下,向 溶液中滴加
溶液中滴加 溶液,滴加过程中溶液中
溶液,滴加过程中溶液中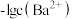 与
与 溶液体积
溶液体积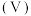 的关系如图所示,已知
的关系如图所示,已知 。下列说法正确的是
。下列说法正确的是
 溶液中滴加
溶液中滴加 溶液,滴加过程中溶液中
溶液,滴加过程中溶液中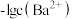 与
与 溶液体积
溶液体积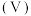 的关系如图所示,已知
的关系如图所示,已知 。下列说法正确的是
。下列说法正确的是
| A.溶液b点可以通过升高温度到达c点 |
B.该温度下 |
C.b点溶液中: |
D.若把 溶液换成等浓度 溶液换成等浓度 溶液,则曲线变为Ⅱ 溶液,则曲线变为Ⅱ |
您最近一年使用:0次
2023-05-04更新
|
454次组卷
|
4卷引用:四川省绵阳南山中学2023-2024学年高二上学期12月月考化学试题
10 . 常温下,金属离子(Mn+)浓度的负对数pM[pM=-lgc(Mn+)]随溶液pH变化关系如图所示。当c(Mn+)≤10-6mol/L时认为该金属离子已沉淀完全,下列叙述正确的是
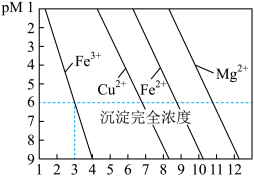

| A.常温下,Mg(OH)2的溶解度比Cu(OH)2的溶解度小 |
| B.常温下,Fe(OH)3的溶度积常数为1.0×10-39 |
| C.除去含Cu2+溶液中的少量Fe2+,可加入适量H2O2后控制溶液3≤pH<7 |
| D.能通过调节溶液pH的方法分步沉淀Mg2+和Fe2+ |
您最近一年使用:0次
2023-04-29更新
|
470次组卷
|
4卷引用:四川省绵阳市南山中学2022-2023学年高二下学期期中考试化学试题



