解题方法
1 . 下列说法中,正确的是
| A.难溶电解质达到沉淀溶解平衡时,保持温度不变增加难溶电解质的量,平衡向溶解方向移动 |
| B.难溶电解质都是弱电解质 |
C.室温下, 在水中的溶解度大于在饱和 在水中的溶解度大于在饱和 溶液中的溶解度 溶液中的溶解度 |
D.在白色 沉淀上滴加 沉淀上滴加 溶液,沉淀变黑,说明 溶液,沉淀变黑,说明 比 比 更难溶于水 更难溶于水 |
您最近一年使用:0次
2 . 物质在水中可能存在电离平衡、盐的水解平衡和沉淀溶解平衡,请回答:
(1)泡沫灭火剂包括Al2(SO4)3 溶液(约1mol/L ), NaHCO3溶液(约1mol/L )及起泡剂,使用时发生反应的离子方程式为_______ 。
(2)t℃时,某稀硫酸溶液中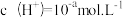 ,
,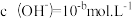 ,已知:
,已知: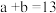 ,该温度下水的离子积常数 KW 的数值为
,该温度下水的离子积常数 KW 的数值为_______ 。
(3)含等物质的量的 NaHC2O4 和 Na 2C2O4 的溶液物料守恒式为_______ 。
(4)已知25℃时部分弱电解质的电离平衡常数数据如下表:
pH 相同的①CH3COONa 溶液、② NaClO溶液、③ NaHCO3溶液、④ NaOH 溶液,其物质的量浓度由大到小的顺序为_______ 。
(5)某溶液只含Cu2+、Fe2+、Fe3+三种金属离子,且三种离子沉淀时的pH 如下表所示:
为制备CuCl2·3H2O,除去Cu2+、Fe2+、Fe3+离子应该先加入_______ ,然后再加入_______ ,调节pH 范围为_______ 。
(1)泡沫灭火剂包括Al2(SO4)3 溶液(约1mol/L ), NaHCO3溶液(约1mol/L )及起泡剂,使用时发生反应的离子方程式为
(2)t℃时,某稀硫酸溶液中
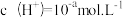 ,
,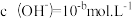 ,已知:
,已知: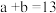 ,该温度下水的离子积常数 KW 的数值为
,该温度下水的离子积常数 KW 的数值为(3)含等物质的量的 NaHC2O4 和 Na 2C2O4 的溶液物料守恒式为
(4)已知25℃时部分弱电解质的电离平衡常数数据如下表:
| 化学式 | CH3COOH | H2CO3 | HClO | |
| 平衡常数 | 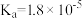 | 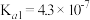 | 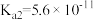 | 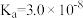 |
(5)某溶液只含Cu2+、Fe2+、Fe3+三种金属离子,且三种离子沉淀时的pH 如下表所示:
| 金属离子 | Fe3+ | Fe2+ | Cu2+ | |
| pH | 氢氧化物开始沉淀 | 1.9 | 7.0 | 4.7 |
| 氢氧化物完全沉淀 | 3.2 | 9.0 | 6.7 | |
您最近一年使用:0次
名校
解题方法
3 . 以硅藻土为载体的五氧化二钒( )是接触法生产硫酸的催化剂。从废矾催化剂中回收
)是接触法生产硫酸的催化剂。从废矾催化剂中回收 既避免污染环境又有利于资源综合利用。废钒催化剂的主要成分为
既避免污染环境又有利于资源综合利用。废钒催化剂的主要成分为
以下是一种废钒催化剂回收工艺路线:

回答下列问题:
(1)“酸浸”时 转化为
转化为 ,反应的离子方程式为
,反应的离子方程式为______ ,同时 转化成
转化成 。
。
(2)“废渣1”的主要成分是______ 。
(3)“氧化”中欲使3mol的 变为
变为 ,则需要氧化剂
,则需要氧化剂 至少为
至少为______ mol。
(4)“中和”作用之一是使钒以 形式存在于溶液中,将Al和Fe元素转化为难溶物。“废渣2”中含有
形式存在于溶液中,将Al和Fe元素转化为难溶物。“废渣2”中含有______ 。
(5)“离子交换”和“洗脱”可简单表示为 (ROH为强碱性阴离子交换树脂)。为了提高洗脱效率,淋洗液应该呈
(ROH为强碱性阴离子交换树脂)。为了提高洗脱效率,淋洗液应该呈______ 性(填“酸”、“碱”或“中”)。
(6)“流出液”中阳离子最多的是______ 。
(7)“沉钒”得到偏钒酸铵( )沉淀,写出“煅烧”中发生反应的化学方程式
)沉淀,写出“煅烧”中发生反应的化学方程式______ 。
 )是接触法生产硫酸的催化剂。从废矾催化剂中回收
)是接触法生产硫酸的催化剂。从废矾催化剂中回收 既避免污染环境又有利于资源综合利用。废钒催化剂的主要成分为
既避免污染环境又有利于资源综合利用。废钒催化剂的主要成分为| 物质 |  |  |  |  |  |  |
| 质量分数/% | 2.2~2.9 | 2.8~3.1 | 22~28 | 60~65 | 1~2 | <1 |

回答下列问题:
(1)“酸浸”时
 转化为
转化为 ,反应的离子方程式为
,反应的离子方程式为 转化成
转化成 。
。(2)“废渣1”的主要成分是
(3)“氧化”中欲使3mol的
 变为
变为 ,则需要氧化剂
,则需要氧化剂 至少为
至少为(4)“中和”作用之一是使钒以
 形式存在于溶液中,将Al和Fe元素转化为难溶物。“废渣2”中含有
形式存在于溶液中,将Al和Fe元素转化为难溶物。“废渣2”中含有(5)“离子交换”和“洗脱”可简单表示为
 (ROH为强碱性阴离子交换树脂)。为了提高洗脱效率,淋洗液应该呈
(ROH为强碱性阴离子交换树脂)。为了提高洗脱效率,淋洗液应该呈(6)“流出液”中阳离子最多的是
(7)“沉钒”得到偏钒酸铵(
 )沉淀,写出“煅烧”中发生反应的化学方程式
)沉淀,写出“煅烧”中发生反应的化学方程式
您最近一年使用:0次
解题方法
4 . 高纯硫酸锰作为合成镍钴锰三元正极材料的原料,工业上可由天然二氧化锰粉与硫化锰矿(还含 、
、 、
、 、
、 、
、 、
、 等元素的氧化物)制备,工艺如图所示。回答下列问题:
等元素的氧化物)制备,工艺如图所示。回答下列问题:

相关金属离子[起始浓度为 ]形成氢氧化物沉淀的
]形成氢氧化物沉淀的 范围如表:
范围如表:
(1)“滤渣1”含有 和
和___________ 。
(2)“氧化”中添加适量的 的作用是将
的作用是将 氧化为
氧化为 ,写出该反应的离子方程式为
,写出该反应的离子方程式为___________ 。
(3)调 范围为4.7~6,滤渣2成分的化学式为
范围为4.7~6,滤渣2成分的化学式为___________ 。
(4)“除杂1”的目的是除去 和
和 ,“滤渣3”的主要成分是
,“滤渣3”的主要成分是___________ 。
(5)“除杂2”的目的是生成 沉淀除去
沉淀除去 。若溶液酸度过高,
。若溶液酸度过高, 沉淀不完全,原因是
沉淀不完全,原因是___________ (从沉淀溶解平衡角度解释)。
(6)写出“沉锰”的离子方程式___________ 。
 、
、 、
、 、
、 、
、 、
、 等元素的氧化物)制备,工艺如图所示。回答下列问题:
等元素的氧化物)制备,工艺如图所示。回答下列问题:
相关金属离子[起始浓度为
 ]形成氢氧化物沉淀的
]形成氢氧化物沉淀的 范围如表:
范围如表:| 金属离子 | Mn2+ | Fe2+ | Fe3+ | Al3+ | Mg2+ | Zn2+ | Ni2+ |
| 开始沉淀的pH | 8.1 | 6.3 | 1.5 | 3.4 | 8.9 | 6.2 | 6.9 |
| 沉淀完全的pH | 10.1 | 8.3 | 2.8 | 4.7 | 10.9 | 8.2 | 8.9 |
(1)“滤渣1”含有
 和
和(2)“氧化”中添加适量的
 的作用是将
的作用是将 氧化为
氧化为 ,写出该反应的离子方程式为
,写出该反应的离子方程式为(3)调
 范围为4.7~6,滤渣2成分的化学式为
范围为4.7~6,滤渣2成分的化学式为(4)“除杂1”的目的是除去
 和
和 ,“滤渣3”的主要成分是
,“滤渣3”的主要成分是(5)“除杂2”的目的是生成
 沉淀除去
沉淀除去 。若溶液酸度过高,
。若溶液酸度过高, 沉淀不完全,原因是
沉淀不完全,原因是(6)写出“沉锰”的离子方程式
您最近一年使用:0次
解题方法
5 . 火法炼铜中产生的白烟尘常含ZnO、 、CuO、CdO、
、CuO、CdO、 、PdO等,其中Cu、Zn、Pb、Cd等是潜在的金属资源,As有潜在环境威胁,可综合利用变废为宝,流程如下:
、PdO等,其中Cu、Zn、Pb、Cd等是潜在的金属资源,As有潜在环境威胁,可综合利用变废为宝,流程如下:

(1)溶解度:

 (填“>”“<”或“=”)。在浸出液中,砷元素主要以
(填“>”“<”或“=”)。在浸出液中,砷元素主要以 的形式存在,写出“酸浸”生成
的形式存在,写出“酸浸”生成 的化学方程式
的化学方程式(2)表1和表2是在其他条件一定时,铁铜摩尔置换比[
 ]、温度分别对铜的置换率和品位(矿石中所含某种金属或有用成分的多少)的影响,浸出液置换铜的最佳
]、温度分别对铜的置换率和品位(矿石中所含某种金属或有用成分的多少)的影响,浸出液置换铜的最佳 比值是
比值是表1  对铜置换率和品味的影响
对铜置换率和品味的影响
| 置换率/% | Cu品位/% |
1.2 | 74.87 | 51.22 |
1.4 | 92.17 | 72.82 |
1.6 | 99.92 | 72.08 |
表2温度对铜置换率和品味的影响
温度/℃ | 置换率/% | Cu品位/% |
30 | 99.92 | 72.08 |
60 | 99.93 | 70.34 |
80 | 99.86 | 69.98 |
(3)随着pH增大,沉砷率将
(4)金属活动性顺序为Zn>Cd>Cu,“电解”主要回收到的金属中,首先析出的是
您最近一年使用:0次
名校
6 . 下列实验对应的反应方程式书写正确的是
A.泡沫灭火器原理:2Al3++3 +3H2O=2Al(OH)3 ↓+ 3CO2↑ +3H2O=2Al(OH)3 ↓+ 3CO2↑ |
B.FeS除去废水中的Hg2+:FeS(s) + Hg2+(aq)  Fe2+(aq) + HgS(s) Fe2+(aq) + HgS(s) |
C.用铁电极电解饱和食盐水:2Cl-+2H2O 2OH-+H2↑+Cl2↑ 2OH-+H2↑+Cl2↑ |
D.Fe2(SO4)3溶液中加入足量Ba(OH)2溶液:Fe3++ +Ba2++3OH-=Fe(OH)3↓+BaSO4↓ +Ba2++3OH-=Fe(OH)3↓+BaSO4↓ |
您最近一年使用:0次
2024-02-07更新
|
234次组卷
|
3卷引用:四川省成都石室中学2023-2024学年高二上学期期中考试化学试卷
名校
解题方法
7 . 相关物质的溶度积常数见下表(25℃):
下列有关说法不正确的是
| 物质 | Mg(OH)2 | CH3COOAg | AgCl | Ag2CrO4 |
 | 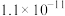 | 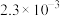 |  | 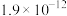 |
| A.浓度均为0.2mol/L的AgNO3溶液和CH3COONa溶液等体积混合一定产生CH3COOAg沉淀 |
| B.在其他条件不变的情况下,向饱和AgCl溶液中加入NaCl溶液,Ksp(AgCl)不变 |
| C.0.11mol/L的MgCl2溶液中加入氨水产生Mg(OH)2沉淀时溶液的pH为9 |
| D.将0.001mol/L的AgNO3溶液滴入0.001mol/L的KCl和0.001mol/L的K2CrO4混合溶液中,先产生Ag2CrO4沉淀 |
您最近一年使用:0次
名校
8 . 下列说法中正确的是
| A.钡中毒患者可尽快使用苏打溶液洗胃,随即导泻使Ba2+转化为BaCO3而排出 |
B.珊瑚虫从海水中获取Ca2+和HCO ,经反应形成石灰石(CaCO3)外壳,逐渐形成珊瑚 ,经反应形成石灰石(CaCO3)外壳,逐渐形成珊瑚 |
C.泡沫灭火器原理3CO +2Al3++3H2O=2Al(OH)3 +3CO2 +2Al3++3H2O=2Al(OH)3 +3CO2 |
| D.使用含氟牙膏预防龋齿利用了盐类水解的原理 |
您最近一年使用:0次
名校
解题方法
9 . 纳米铁酸锰(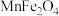 ,具有磁性)在光、电子、催化等领域应用广泛。实验室可采用共沉淀法制备纳米铁酸锰,步骤如下:
,具有磁性)在光、电子、催化等领域应用广泛。实验室可采用共沉淀法制备纳米铁酸锰,步骤如下:
步骤1:按 ,称取
,称取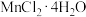 和
和 于烧杯中,加入200mL的蒸馏水,搅拌,形成混合溶液;
于烧杯中,加入200mL的蒸馏水,搅拌,形成混合溶液;
步骤2:配制浓度为 的NaOH溶液,并加热至沸腾;
的NaOH溶液,并加热至沸腾;
步骤3:将步骤1的混合液加热至80℃,剧烈搅拌下于10s内加入沸腾的130mL的NaOH溶液中,然后将该溶液倒入仪器X中回流,于90℃恒温晶化1h;
步骤4:反应结束后,将铁酸锰晶体粒子分离出来,依次用蒸馏水、乙醇洗涤干燥后,即得到黑色具有磁性的铁锰酸。
回答下列问题:
(1)步骤2所配NaOH溶液的物质的量浓度为___________  。配制过程中,下列仪器不需要用到的是
。配制过程中,下列仪器不需要用到的是___________ (填字母)。___________ 。
②回流时的加热方式为___________ 。
③写出形成铁酸锰反应的离子方程式:___________ 。
(3)步骤4分离出铁酸锰的简单方法是___________ ,检验蒸馏水将铁酸锰洗涤干净的操作是___________ ,乙醇洗涤的目的是___________ 。
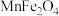 ,具有磁性)在光、电子、催化等领域应用广泛。实验室可采用共沉淀法制备纳米铁酸锰,步骤如下:
,具有磁性)在光、电子、催化等领域应用广泛。实验室可采用共沉淀法制备纳米铁酸锰,步骤如下:步骤1:按
 ,称取
,称取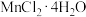 和
和 于烧杯中,加入200mL的蒸馏水,搅拌,形成混合溶液;
于烧杯中,加入200mL的蒸馏水,搅拌,形成混合溶液;步骤2:配制浓度为
 的NaOH溶液,并加热至沸腾;
的NaOH溶液,并加热至沸腾;步骤3:将步骤1的混合液加热至80℃,剧烈搅拌下于10s内加入沸腾的130mL的NaOH溶液中,然后将该溶液倒入仪器X中回流,于90℃恒温晶化1h;
步骤4:反应结束后,将铁酸锰晶体粒子分离出来,依次用蒸馏水、乙醇洗涤干燥后,即得到黑色具有磁性的铁锰酸。
回答下列问题:
(1)步骤2所配NaOH溶液的物质的量浓度为
 。配制过程中,下列仪器不需要用到的是
。配制过程中,下列仪器不需要用到的是

②回流时的加热方式为
③写出形成铁酸锰反应的离子方程式:
(3)步骤4分离出铁酸锰的简单方法是
您最近一年使用:0次
2024-01-22更新
|
110次组卷
|
4卷引用:四川省内江市第三中学2023-2024学年高三1月月考理综试卷-高中化学
名校
10 . 工业.上用菱锰矿( )[含
)[含 、
、 、
、 等杂质]为原料制取二氧化锰,其流程示意图如下:
等杂质]为原料制取二氧化锰,其流程示意图如下:
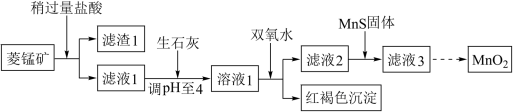
已知生成氢氧化物沉淀的 :
:
注:金属离子的起始浓度为
回答下列问题:
(1) 元素在周期表中位置是
元素在周期表中位置是__________ ,属于__________ 区元素(选填“s”、“p”、“d”或s")。
(2)含杂质的菱锰矿使用前需将其粉碎,主要目的是___________ ;盐酸溶解 的化学方程式是
的化学方程式是____________________ 。
(3)向溶液1中加入双氧水时,反应的离子方程式是______________________________ 。
(4)滤液2中加入稍过量的难溶电解质 ,以除去
,以除去 ,反应的离子方程式是
,反应的离子方程式是____________________ 。
(5)将 转化为
转化为 的一种方法是氧化法。其具体做法是用酸化的
的一种方法是氧化法。其具体做法是用酸化的 溶液将
溶液将 氧化,该反应的离子方程式:
氧化,该反应的离子方程式: __________
 。
。
(6)将 转化为
转化为 的另一种方法是电解法。
的另一种方法是电解法。
①生成 的电极反应式是
的电极反应式是______________________________ 。
②若在上述 溶液中加入一定量的
溶液中加入一定量的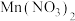 粉末,则无
粉末,则无 产生。其原因是
产生。其原因是____________________ 。
 )[含
)[含 、
、 、
、 等杂质]为原料制取二氧化锰,其流程示意图如下:
等杂质]为原料制取二氧化锰,其流程示意图如下:
已知生成氢氧化物沉淀的
 :
:
|
|
|
| |
开始沉淀时 | 8.3 | 6.3 | 2.7 | 4.7 |
完全沉淀时 | 9.8 | 8.3 | 3.7 | 6.7 |

回答下列问题:
(1)
 元素在周期表中位置是
元素在周期表中位置是(2)含杂质的菱锰矿使用前需将其粉碎,主要目的是
 的化学方程式是
的化学方程式是(3)向溶液1中加入双氧水时,反应的离子方程式是
(4)滤液2中加入稍过量的难溶电解质
 ,以除去
,以除去 ,反应的离子方程式是
,反应的离子方程式是(5)将
 转化为
转化为 的一种方法是氧化法。其具体做法是用酸化的
的一种方法是氧化法。其具体做法是用酸化的 溶液将
溶液将 氧化,该反应的离子方程式:
氧化,该反应的离子方程式:  。
。(6)将
 转化为
转化为 的另一种方法是电解法。
的另一种方法是电解法。①生成
 的电极反应式是
的电极反应式是②若在上述
 溶液中加入一定量的
溶液中加入一定量的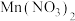 粉末,则无
粉末,则无 产生。其原因是
产生。其原因是
您最近一年使用:0次







