解题方法
1 . 某元素X的激发态原子的电子排布式为1s22s22p63s13p3,则该元素基态原子的电子排布式为_______ ,其最高价氧化物属于_______ 晶体;Z原子的核电荷数为33,其在元素周期表中的位置是_______ ,属于_______ 区的元素。
您最近一年使用:0次
解题方法
2 . 如表列出了①~⑦七种元素在周期表中的位置:
请按要求回答下列问题:
(1)元素③的原子结构示意图是___________ ,以上元素的最高价氧化物形成的水化物酸性最强的是___________ (填分子式)。
(2)②、③、⑥三种元素的原子形成的简单离子半径由大到小的顺序排列为___________ (用离子符号表示);②、③两种元素的最高价氧化物对应的水化物碱性由弱到强的顺序是___________ (用化学式表示)。
(3)向元素②的单质与水反应后的溶液中加入元素④的单质,发生反应的化学方程式为___________ 。
(4)②和⑦按原子个数比1∶1形成离子化合物的电子式___________ 。
(5)设计一个实验比较②与③的金属性强弱___________ 。
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 二 | ① | ⑦ | ||||||
| 三 | ② | ③ | ④ | ⑤ | ⑥ |
请按要求回答下列问题:
(1)元素③的原子结构示意图是
(2)②、③、⑥三种元素的原子形成的简单离子半径由大到小的顺序排列为
(3)向元素②的单质与水反应后的溶液中加入元素④的单质,发生反应的化学方程式为
(4)②和⑦按原子个数比1∶1形成离子化合物的电子式
(5)设计一个实验比较②与③的金属性强弱
您最近一年使用:0次
3 . (1)下列状态的镁中,电离最外层一个电子所需能量最大的是________ (填标号)。
A.[Ne] B.[Ne]
B.[Ne] C.[Ne]
C.[Ne] D.[Ne]
D.[Ne]
(2)Sm的价层电子排布式为4f66s2,Sm3+价层电子排布式为________ 。
(3)Cu2+基态核外电子排布式为__________________ 。
(4)Mn位于元素周期表中第四周期________ 族,基态Mn原子核外未成对电子有________ 个。
(5)丙酮( )分子中碳原子轨道的杂化类型是
)分子中碳原子轨道的杂化类型是_____ 、______ 。
(6)在[Ni(NH3)6]2+中Ni2+与NH3之间形成的化学键称为________ ,提供孤电子对的成键原子是___________ 。
A.[Ne]
 B.[Ne]
B.[Ne] C.[Ne]
C.[Ne] D.[Ne]
D.[Ne]
(2)Sm的价层电子排布式为4f66s2,Sm3+价层电子排布式为
(3)Cu2+基态核外电子排布式为
(4)Mn位于元素周期表中第四周期
(5)丙酮(
 )分子中碳原子轨道的杂化类型是
)分子中碳原子轨道的杂化类型是(6)在[Ni(NH3)6]2+中Ni2+与NH3之间形成的化学键称为
您最近一年使用:0次
名校
4 . 如表是周期表中的一部分,根据A~I在周期表中的位置,用元素符号或化学式回答下列问题:
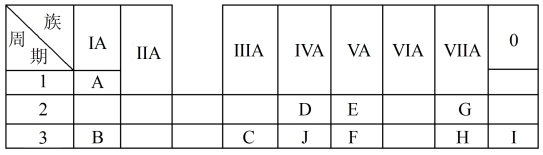
(1)表中元素,化学性质最不活泼的是___ ,只有负价而无正价的元素是___ 。
(2)最高价氧化物的水化物酸性最强的是___ ,呈两性的是___ 。
(3)A分别与E、G、H形成的化合物中,最稳定的是___ 。
(4)在B、C、E、F中,原子半径最大的是___ 。
(5)B、H两种元素所形成的化合物所含的化学键类型为___ 。
(6)写出C的最高价氧化物与H的氢化物之间反应的离子方程式:__ 。
(7)写出B与C两种元素的最高价氧化物对应的水化物相互反应的化学方程式:___ 。

(1)表中元素,化学性质最不活泼的是
(2)最高价氧化物的水化物酸性最强的是
(3)A分别与E、G、H形成的化合物中,最稳定的是
(4)在B、C、E、F中,原子半径最大的是
(5)B、H两种元素所形成的化合物所含的化学键类型为
(6)写出C的最高价氧化物与H的氢化物之间反应的离子方程式:
(7)写出B与C两种元素的最高价氧化物对应的水化物相互反应的化学方程式:
您最近一年使用:0次
5 . 下表是元素周期表的一部分,针对表中的①~⑨九种元素,填写下列空白:

(1)在这些元素中,化学性质最不活泼的是______ (填具体元素符号,下同)。
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是______ ,碱性最强的化合物的化学式是______ 。
(3)最高价氧化物是两性氧化物的元素是______ ;写出它的氧化物与氢氧化钠反应的离子方程式______ 。
(4)用电子式表示元素④与⑥形成的化合物:______ ,该化合物属于______ (填“共价”或“离子”)化合物。

(1)在这些元素中,化学性质最不活泼的是
(2)在最高价氧化物的水化物中,酸性最强的化合物的化学式是
(3)最高价氧化物是两性氧化物的元素是
(4)用电子式表示元素④与⑥形成的化合物:
您最近一年使用:0次
2021-04-01更新
|
179次组卷
|
4卷引用:新疆昌吉教育共同体2020-2021学年高一下学期期中考试化学试题
名校
6 . 下表为元素周期表的一部分:
回答下列有关问题:
(1)上表中原子半径最小的元素是_______ (填元素符号)。
(2)表中所列元素中,最活泼的金属元素是_______ (填元素符号,下同),最活泼的非金属元素是_______ ,最不活泼的元素是_______ 。
(3)这些元素的最高价氧化物对应的水化物中,酸性最强的是_______ (填化学式,下同),碱性最强的是_______ ,呈两性的是_______ ,最不稳定的气态氢化物是_______ 。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
回答下列有关问题:
(1)上表中原子半径最小的元素是
(2)表中所列元素中,最活泼的金属元素是
(3)这些元素的最高价氧化物对应的水化物中,酸性最强的是
您最近一年使用:0次
2021-01-23更新
|
308次组卷
|
3卷引用:新疆巴楚县第一中学2020-2021学年高一年级下学期化学期中考试试题
新疆巴楚县第一中学2020-2021学年高一年级下学期化学期中考试试题吉林省松原市长岭县第三中学2020-2021学年高一上学期期末考试化学试题(已下线)人教必修第一册第4章第2节第1课时元素性质的周期性变化规律(课后)
名校
7 . 下列为元素周期表中的一部分,用化学式或元素符号回答下列问题。
(1)11种元素中,化学性质最不活泼的是__________ ,原子半径最小的是_________ 。
(2)①②⑤中,最高价氧化物的水化物,碱性最强的是___________ 。
(3)②③④中形成的简单离子半径由大到小的顺序是_________________ 。
(4)元素⑦的氢化物电子式为_______ ,该氢化物常温下和元素②的单质反应的离子方程式是________________ 。
(5)①和⑨的最高价氧化物对应的水化物化学式为__________ 和__________ 。①和⑨两元素形成化合物中化学键的类型为____________ ,该化合物灼烧时焰色为_________ ,该化合物的溶液与元素⑧的单质反应的离子方程式为__________________ 。
(6)①和⑤最高价氧化物对应的水化物相互反应的化学方程式为___________ 。
(7)⑧⑨⑪三种元素形成的气态氢化物最稳定的是_______ 。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ⑥ | ⑦ | ⑪ | |||||
| 3 | ① | ③ | ⑤ | ⑧ | ⑩ | |||
| 4 | ② | ④ | ⑨ |
(1)11种元素中,化学性质最不活泼的是
(2)①②⑤中,最高价氧化物的水化物,碱性最强的是
(3)②③④中形成的简单离子半径由大到小的顺序是
(4)元素⑦的氢化物电子式为
(5)①和⑨的最高价氧化物对应的水化物化学式为
(6)①和⑤最高价氧化物对应的水化物相互反应的化学方程式为
(7)⑧⑨⑪三种元素形成的气态氢化物最稳定的是
您最近一年使用:0次
2021-01-20更新
|
1827次组卷
|
6卷引用:新疆哈密市第八中学2019-2020学年高一下学期期中考试化学试题
新疆哈密市第八中学2019-2020学年高一下学期期中考试化学试题(已下线)专题07 物质结构与元素周期律-备战2021届高考化学二轮复习题型专练河南省新蔡县第一高级中学2020-2021学年高一下学期5月月考化学试题甘肃省金昌市第一中学2020-2021学年高一下学期期中考试化学(理)试题(已下线)专题17 化学键(限时精炼)-2022年高三毕业班化学常考点归纳与变式演练福建省政和县第二中学2022-2023学年高一下学期第一次月考化学试题
8 . 下表为元素周期表的一部分,请参照元素①~⑩在表中的位置,回答下列问题:

(1)元素⑩在周期表中的位置是______ ,⑦的原子结构示意图为______ 。
(2)④、⑤、⑥的简单离子半径由大到小的顺序为____ (用离子符号和“>”表示)。
(3)④⑧⑨的气态氢化物中,最稳定的是_____ (用化学式表示),最高价氧化物对应水化物中,酸性最强的是____ (用化学式表示)。
(4)⑤的最高价氧化物对应的水化物与⑦的最高价氧化物对应的水化物发生反应的离子方程式____________________________________ 。
(5)下列五种物质中,①H2O ②CO2 ③Na2O2 ④NaOH ⑤NaBr,
①只存在共价键的是______ ,只存在离子键的是_____ ,既存在离子键又存在共价键的是__ 。
②写出下列物质的电子式:CO2_________ ,NaOH___________ 。

(1)元素⑩在周期表中的位置是
(2)④、⑤、⑥的简单离子半径由大到小的顺序为
(3)④⑧⑨的气态氢化物中,最稳定的是
(4)⑤的最高价氧化物对应的水化物与⑦的最高价氧化物对应的水化物发生反应的离子方程式
(5)下列五种物质中,①H2O ②CO2 ③Na2O2 ④NaOH ⑤NaBr,
①只存在共价键的是
②写出下列物质的电子式:CO2
您最近一年使用:0次
2020-09-08更新
|
691次组卷
|
2卷引用:新疆呼图壁县第一中学2019-2020学年高一下学期期末考试化学试题
9 . 下表是元素周期表的一部分,针对表中的①~⑩种元素,填写下列空白:
(1)在这些元素中,化学性质最活泼的是___ ;化学性质最不活泼的是___ (填元素符号)。
(2)在最高价氧化物对应的水化物中,酸性最强的化合物的分子___ ,④和⑧结合的化合物的电子式是___ ,该化合物属于___ 化合物(填“共价”或“离子”)。
(3)③、⑥、⑦三种元素的原子半径由大到小的顺序是___ (用化学式表示),⑥、⑦、⑧三种元素的非金属性逐渐___ ,①、④、⑩三种元素原子还原性逐渐___ (填“增强”或“减弱”)。
| IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0族 | |
| 第二周期 | ① | ② | ③ | |||||
| 第三周期 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ||
| 第四周期 | ⑩ |
(2)在最高价氧化物对应的水化物中,酸性最强的化合物的分子
(3)③、⑥、⑦三种元素的原子半径由大到小的顺序是
您最近一年使用:0次
10 . 下表为元素周期表的一部分,请参照元素①-⑧在表中的位置,用化学用语回答下列问题:
(1)⑧的原子结构示意图为_________ ;
(2)②的气态氢化物分子的结构式为___________ ,②和⑦的气态氢化物的稳定性相比,其中较弱的是____ (用该氢化物的化学式表示);
(3)②、③的最高价含氧酸的酸性由强到弱的顺序是____ (填化学式);
(4)⑤、⑥元素的金属性强弱依次为___________ (填“增大”、“减小”或“不变”);
(5)④、⑤、⑥的形成的简单离子半径依次_________ (填“增大”、“减小”或“不变”);
(6)①、④、⑤元素可形成既含离子键又含共价键的化合物,写出它的电子式:_____ 。
族 周期 | IA | 0 | ||||||
1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
2 | ② | ③ | ④ | |||||
3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
(1)⑧的原子结构示意图为
(2)②的气态氢化物分子的结构式为
(3)②、③的最高价含氧酸的酸性由强到弱的顺序是
(4)⑤、⑥元素的金属性强弱依次为
(5)④、⑤、⑥的形成的简单离子半径依次
(6)①、④、⑤元素可形成既含离子键又含共价键的化合物,写出它的电子式:
您最近一年使用:0次
2020-05-18更新
|
521次组卷
|
2卷引用:新疆吐蕃市高昌区第二中学2019-2020学年高一下学期期末考试化学试题



