名校
解题方法
1 . 氨基酸是构成人体必备蛋白质的基础,某氨基酸的结构简式如图所示。下列有关说法正确的是
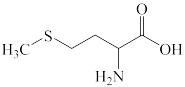

| A.第一电离能:O>N>C>H |
| B.基态氧原子的电子有8种空间运动状态 |
C.该分子中碳原子的杂化类型有sp、 和 和 |
| D.键的极性大小:N-H<O-H<F-H |
您最近一年使用:0次
2022-04-06更新
|
1553次组卷
|
7卷引用:天津市第三中学2022-2023学年高二下学期3月阶段性质量检测化学试题
名校
2 . 金属钛(Ti)被誉为“二十一世纪金属”,有“生物金属,海洋金属,太空金属”的美称,具有广泛的应用前景。回答下列问题:
(1)基态Ti原子的电子排布式为[Ar]___________ ,Ti原子核外有___________ 种空间运动状态不同的电子。
(2)Ti(BH4)2是一种储氢材料。BH 的空间构型是
的空间构型是___________ ,H、B、Ti的电负性由大到小的顺序为___________ 。
(3)锆(Zr)与钛(Ti)是同一副族的相邻元素,ZrCl4可以与乙二胺(H2NCH2CH2NH2)形成六配位化合物[ZrCl4(H2NCH2CH2NH2)]。
①乙二胺中,N原子的杂化方式为___________ 。
②1mol[ZrCl4(H2NCH2CH2NH2)]中含有σ键的物质的量为___________ mol。
③乙二胺形成配合物后,H-N-H键角将变大,原因是___________ 。
(4)钙钛矿(主要成分CaTiO3),晶胞结构如图所示,若阿伏加德罗常数的值为NA,晶体密度为ρg·cm-3,则相距最近的Ca和O之间的距离为___________ pm(列出计算式)。

(1)基态Ti原子的电子排布式为[Ar]
(2)Ti(BH4)2是一种储氢材料。BH
 的空间构型是
的空间构型是(3)锆(Zr)与钛(Ti)是同一副族的相邻元素,ZrCl4可以与乙二胺(H2NCH2CH2NH2)形成六配位化合物[ZrCl4(H2NCH2CH2NH2)]。
①乙二胺中,N原子的杂化方式为
②1mol[ZrCl4(H2NCH2CH2NH2)]中含有σ键的物质的量为
③乙二胺形成配合物后,H-N-H键角将变大,原因是
(4)钙钛矿(主要成分CaTiO3),晶胞结构如图所示,若阿伏加德罗常数的值为NA,晶体密度为ρg·cm-3,则相距最近的Ca和O之间的距离为

您最近一年使用:0次
2022-03-10更新
|
228次组卷
|
2卷引用:天津市滨海新区七所重点学校2021-2022学年高三下学期联考化学试题
名校
3 . 科学家通过观察金星的酸性云层,分析出金星存在磷化氢气体,从而推测金星可能存在生命的迹象。下列关于P元素的说法中,不正确 的是
| A.第一电离能:P<S | B.原子半径:S<P |
| C.非金属性:P<S | D.电负性:P<S |
您最近一年使用:0次
2022-03-10更新
|
812次组卷
|
7卷引用:天津市南开区2021-2022学年高二上学期期末考试化学试题
名校
4 . 短周期主族元素 、
、 、
、 、
、 原子序数依次增大,
原子序数依次增大, 元素的单质在自然界存在硬度很大的矿石,
元素的单质在自然界存在硬度很大的矿石, 原子最外层有
原子最外层有 个电子,
个电子, 元素的氧化物可做耐高温材料且其最高价氧化物的水化物是难溶于水的碱性物质,
元素的氧化物可做耐高温材料且其最高价氧化物的水化物是难溶于水的碱性物质, 与
与 同主族。下列叙述正确的是
同主族。下列叙述正确的是
 、
、 、
、 、
、 原子序数依次增大,
原子序数依次增大, 元素的单质在自然界存在硬度很大的矿石,
元素的单质在自然界存在硬度很大的矿石, 原子最外层有
原子最外层有 个电子,
个电子, 元素的氧化物可做耐高温材料且其最高价氧化物的水化物是难溶于水的碱性物质,
元素的氧化物可做耐高温材料且其最高价氧化物的水化物是难溶于水的碱性物质, 与
与 同主族。下列叙述正确的是
同主族。下列叙述正确的是A.原子最外层电子数由少到多的顺序: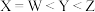 |
B.原子半径由大到小的顺序: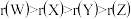 |
C.元素电负性由强到弱的顺序: |
D.元素的最简单气态氢化物的稳定性由强到弱的顺序: 、 、 、 、 |
您最近一年使用:0次
2022-03-10更新
|
221次组卷
|
2卷引用:天津市耀华中学2022届高三第二次模拟考化学试题
解题方法
5 . 回答下列问题:
(1)如图所示为元素周期表中氮元素部分信息,数据“14.01”表示的是____ ,氮元素原子核外有____ 个未成对电子,最外层有____ 种能量不同的电子。

(2)氮和磷是同主族元素,下列能说明二者非金属性相对强弱的是____ (填编号)。
a.NH3比PH3稳定性强 b.电负性数据:N3.0、P2.1
c.硝酸显强氧化性,磷酸不显强氧化性 d.氮气常温是气体,磷单质是固体
(3)2020年12月17日,我国“嫦娥五号”返回器携月壤成功着陆。研究发现,月壤中存在天然的铁、金、银、铅、锌、铜、锑、铼等矿物颗粒。
①要证明月壤中含有这些元素,可采用的方法是____ 。
②写出铜的基态原子的电子排布式____ 。
③周期表中,与铜位于同一周期的元素原子中最外层电子数与铜原子的相同的元素有____ (填元素符号)。
(1)如图所示为元素周期表中氮元素部分信息,数据“14.01”表示的是

(2)氮和磷是同主族元素,下列能说明二者非金属性相对强弱的是
a.NH3比PH3稳定性强 b.电负性数据:N3.0、P2.1
c.硝酸显强氧化性,磷酸不显强氧化性 d.氮气常温是气体,磷单质是固体
(3)2020年12月17日,我国“嫦娥五号”返回器携月壤成功着陆。研究发现,月壤中存在天然的铁、金、银、铅、锌、铜、锑、铼等矿物颗粒。
①要证明月壤中含有这些元素,可采用的方法是
②写出铜的基态原子的电子排布式
③周期表中,与铜位于同一周期的元素原子中最外层电子数与铜原子的相同的元素有
您最近一年使用:0次
名校
6 . 一种由短周期主族元素组成的化合物(如下图所示),具有良好的储氢性能,其中元素W、X、Y、Z的原子序数依次增大、且总和为24。下列有关叙述错误的是
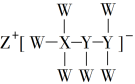
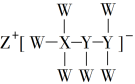
| A.该化合物中,W、X、Y之间均为共价键 |
| B.Z的单质既能与水反应,也可与甲醇反应 |
| C.W、X、Y、Z四种元素电负性Z<X<W<Y |
| D.X的氟化物XF3中原子均为8电子稳定结构 |
您最近一年使用:0次
2022-03-04更新
|
335次组卷
|
2卷引用:天津市部分区2021-2022学年高三上学期期末考试化学试题
7 . 根据所学化学知识回答下列问题:
(1)基态铁原子的价电子排布式为_______ 。基态硫原子的最外层电子排布的轨道表示式 为_______ 。
(2) 可以与
可以与 形成一系列不同配位数的红色配合物,所以常用KSCN溶液检验
形成一系列不同配位数的红色配合物,所以常用KSCN溶液检验 的存在,KSCN中四种元素的电负性最大的是
的存在,KSCN中四种元素的电负性最大的是_______ (用元素符号表示)。
(3) 中S的价层电子对数为
中S的价层电子对数为_______ , 的键角
的键角_______  的键角(填“>”、“<”或“=”)。
的键角(填“>”、“<”或“=”)。
(4)单质铜及镍都是由_______ 键形成的晶体;某镍铜合金的立方晶胞结构如下图所示。

晶胞中铜原子与镍原子的个数比为_______ 。
(5)SiC的晶体结构与晶体硅类似。SiC的晶体类型为_______ ,晶体中Si原子与Si-C键的数目之比为_______ 。
(1)基态铁原子的价电子排布式为
(2)
 可以与
可以与 形成一系列不同配位数的红色配合物,所以常用KSCN溶液检验
形成一系列不同配位数的红色配合物,所以常用KSCN溶液检验 的存在,KSCN中四种元素的电负性最大的是
的存在,KSCN中四种元素的电负性最大的是(3)
 中S的价层电子对数为
中S的价层电子对数为 的键角
的键角 的键角(填“>”、“<”或“=”)。
的键角(填“>”、“<”或“=”)。(4)单质铜及镍都是由

晶胞中铜原子与镍原子的个数比为
(5)SiC的晶体结构与晶体硅类似。SiC的晶体类型为
您最近一年使用:0次
名校
解题方法
8 . 短周期主族元素X、Y、Z、W原子序数依次增大,X原子核外有7个电子,基态Y原子无未成对电子,Z与X为同族元素,W最高价含氧酸为二元酸,下列说法正确的是
A.原子半径: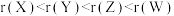 |
| B.元素Y、W的简单离子具有相同的电子层结构 |
| C.Z的最高价氧化物对应水化物的酸性比X的强 |
| D.电负性大小:Y<Z<W |
您最近一年使用:0次
2022-03-03更新
|
347次组卷
|
3卷引用:天津市南开区南开中学2021-2022学年高二上学期期末检测化学试题
名校
9 . 下列说法不正确的是
| A.从空间角度看,2s轨道比1s轨道大,其空间包含了1s轨道 |
B.s-s 键与s-p 键与s-p 键的电子云形状的对称性相同 键的电子云形状的对称性相同 |
| C.电负性大于1.8的为非金属,小于1.8的为金属 |
| D.共价键是原子间通过共用电子对所形成的相互作用 |
您最近一年使用:0次
10 . 下列各项叙述中,正确的是
| A.N、P、As的电负性随原子序数的增大而增大 |
| B.价电子排布为3d54s2的元素位于第四周期VA族,是p区元素 |
| C.2p和3p轨道形状均为哑铃形,能量也相等 |
D.氮原子的最外层电子排布图: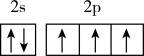 |
您最近一年使用:0次
2022-02-28更新
|
156次组卷
|
2卷引用:天津市第九十五中益中学校2021-2022学年高三上学期第二次月考化学试题



