名校
1 . 有关周期表和周期律的说法正确的是
| A.周期表p区所有元素,电子最后填入的能级均为p能级 |
| B.第二周期元素,电离能介于B和N之间的元素有1种 |
| C.周期表第14列元素形成化合物种类最多 |
| D.同一周期,第ⅡA族元素电负性大于第ⅢA族元素 |
您最近一年使用:0次
2023-02-11更新
|
711次组卷
|
9卷引用:天津市武清区城关中学、杨村第四中学、黄花店中学2022-2023学年高二下学期第一次阶段考化学试题
天津市武清区城关中学、杨村第四中学、黄花店中学2022-2023学年高二下学期第一次阶段考化学试题山东省济宁市2022-2023学年高二上学期期末考试化学试题山东省曹县第一中学2022-2023学年高二下学期2月月考化学试题广东省梅州市梅州五校2022-2023学年高二下学期4月期中联考化学试题河南省淮滨高级中学2022-2023学年高二下学期期中教学质量检测化学试题河北省邢台市重点高中联考2022-2023学年高二下学期6月月考化学试题广东番禺中学2022-2023学年高二下学期4月期中考试化学试题河南省信阳市第十高级中学2022-2023学年高二下学期期中教学质量检测化学试卷湖北省荆州市沙市中学2022-2023学年高二下学期2月月考化学试题
名校
2 . 如图是部分短周期元素的原子序数与其某种常见化合价的关系图,若用原子序数代表所对应的元素,则下列说法中,正确的是
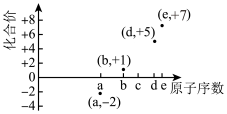

A.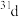 和 和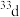 属于同种核素 属于同种核素 | B.第一电离能: ,电负性: ,电负性: |
C.最简单气态氢化物的稳定性: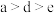 | D.a和b形成的化合物可能含共价键 |
您最近一年使用:0次
3 . 黑火药是中国古代四大发明之一,其爆炸反应为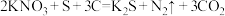 下列说法正确的是
下列说法正确的是
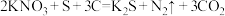 下列说法正确的是
下列说法正确的是A.半径: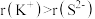 | B.第一电离能: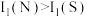 |
C.电负性: | D.酸性: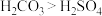 |
您最近一年使用:0次
名校
解题方法
4 . 含ⅥA族元素的化合物在研究和生产中有许多重要用途。回答下列问题:
(1)基态O原子电子占据最高能级的电子云轮廓图为_______ 形。
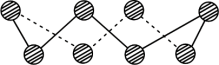
(2)S单质的常见形式为S8,其环状结构如图所示,S原子的杂化轨道类型是_______ 。
(3)Se的核外M层电子的排布式为_______ 。
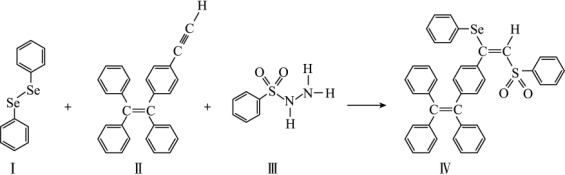
(4)关于物质I~Ⅳ,下列说法正确的有_______ 。
A.I中仅有σ键
B.I中的Se-Se键为非极性共价键
C.I易溶于水
D.II中碳原子的杂化轨道类型只有sp与sp2
E.I~Ⅳ含有的元素中,O电负性最大
(5)常温下CO2是气体而CS2是液体的原因是_______ 。
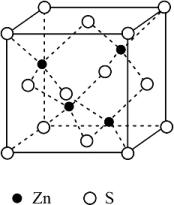
(6)立方ZnS晶体结构如图所示,S周围紧邻且等距的Zn有_______ 个。晶胞棱长为apm,密度为_______ gcm3(NA表示阿伏加德罗常数的值)。
(1)基态O原子电子占据最高能级的电子云轮廓图为
(2)S单质的常见形式为S8,其环状结构如图所示,S原子的杂化轨道类型是

(3)Se的核外M层电子的排布式为
(4)关于物质I~Ⅳ,下列说法正确的有

A.I中仅有σ键
B.I中的Se-Se键为非极性共价键
C.I易溶于水
D.II中碳原子的杂化轨道类型只有sp与sp2
E.I~Ⅳ含有的元素中,O电负性最大
(5)常温下CO2是气体而CS2是液体的原因是
(6)立方ZnS晶体结构如图所示,S周围紧邻且等距的Zn有

您最近一年使用:0次
解题方法
5 . 下列各组元素中,电负性依次减小的是
| A.F、N、O | B.Cl、C、 F | C.Cl、S、P | D.P、N、H |
您最近一年使用:0次
名校
6 . A、B、C、D、E、F、G是元素周期表前四周期常见元素,且原子序数依次增大,其相关信息如表所示,请用化学用语回答下列问题。
(1)写出元素G在周期表中的位置为_______ ,价电子排布式为_______ 。
(2)A、B、C三种元素的第一电离能由大到小为:_______ 。
(3)由A、B、C三种元素分别与氢元素形成的简单气态氢化物,键角由大到小的顺序为_______ 。
(4)D、E、F三种元素的电负性由大到小为:_______ 。
(5)电解D与F形成的化合物的水溶液在工业上有着重要应用,其电解的总反应化学方程式为_______ 。阴极产物为_______
(6)工业上冶炼单质E的化学反应方程式_______ 。
| A | 原子核外有6种不同运动状态的电子 |
| C | 基态原子中s电子总数与p电子总数相等 |
| D | 原子半径在同周期元素中最大 |
| E | 基态原子最外层电子排布式为3s23p1 |
| F | 基态原子的最外层p轨道有2个电子的自旋状态与其他电子的自旋状态相反 |
| G | 生活中使用最多的一种金属 |
(2)A、B、C三种元素的第一电离能由大到小为:
(3)由A、B、C三种元素分别与氢元素形成的简单气态氢化物,键角由大到小的顺序为
(4)D、E、F三种元素的电负性由大到小为:
(5)电解D与F形成的化合物的水溶液在工业上有着重要应用,其电解的总反应化学方程式为
(6)工业上冶炼单质E的化学反应方程式
您最近一年使用:0次
7 . 已知A、B、C、D、E为原子序数依次增大的前36号元素,A的2p轨道有3个电子;B是地壳中含量最多的元素;C元素的M层有一个电子;D元素形成的单质具有两性;E的基态原子的电子排布为[Ar]3d104S1。回答下列问题(用元素符号或化学式表示):
(1)A的最高能级电子云呈_______ 形,B的价层电子轨道表达式是_______ 。
(2)D的基态原子核外电子排布式为_______ 。
(3)A、B的第一电离能由小到大顺序是_______ (填元素符号)。
(4)B、C、D的电负性由小到大的顺序为_______ (填元素符号)。
(5)B、C、D的原子半径由小到大的顺序为_______ (填元素符号)。
(6)E在元素周期表中的位置_______ ,位于_______ 区。
(1)A的最高能级电子云呈
(2)D的基态原子核外电子排布式为
(3)A、B的第一电离能由小到大顺序是
(4)B、C、D的电负性由小到大的顺序为
(5)B、C、D的原子半径由小到大的顺序为
(6)E在元素周期表中的位置
您最近一年使用:0次
名校
解题方法
8 . 金属钛被誉为“二十一世纪金属”,有“生物金属,海洋金属,太空金属”的美称,具有广泛的应用前景。回答下列问题:
(1)钛在周期表中的位置_______ ,钛原子核外有_______ 种空间运动状态不同的电子,Ti2+电子占据的最高能层的电子排布式为_______ 。
(2)磷酸钛铝锂可用作锂离子电池的正极材料,PO 的空间构型是
的空间构型是_______ ,第一电离能介于Al、P之间的第三周期元素为_______ (填元素符号)。
(3)Ti(BH4)2是一种储氢材料,其中所含元素的电负性由小到大排列顺序为_______ ,B原子的杂化方式是_______ ,其中的BH 可由BH3和H-结合而成。BH
可由BH3和H-结合而成。BH 含有
含有_______ (填序号)
①σ键②π键③氢键④配位键 ⑤离子键
(4)TiO2在自然界中有三种同素异形态,即金红石型、锐钛型和斜钛型三种,其中金红石型是三种变体中最稳定的一种,其晶胞如图所示,该晶体的密度为_______ g·cm-3(设阿伏加德罗常数的值为NA,用含a、b、NA的代数式表示)。
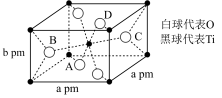
(1)钛在周期表中的位置
(2)磷酸钛铝锂可用作锂离子电池的正极材料,PO
 的空间构型是
的空间构型是(3)Ti(BH4)2是一种储氢材料,其中所含元素的电负性由小到大排列顺序为
 可由BH3和H-结合而成。BH
可由BH3和H-结合而成。BH 含有
含有①σ键②π键③氢键④配位键 ⑤离子键
(4)TiO2在自然界中有三种同素异形态,即金红石型、锐钛型和斜钛型三种,其中金红石型是三种变体中最稳定的一种,其晶胞如图所示,该晶体的密度为

您最近一年使用:0次
2023-01-11更新
|
505次组卷
|
3卷引用:天津市第四十七中学2022—2023学年高三上学期期末 阶段性学习检测化学试题
名校
解题方法
9 . 短周期主族元素X、Y、Z、W、M、N 的原子序数依次增大,X 核外电子只有 1 种运动状态,Y、W 的 2p 轨道均含有 2 个未成对电子,M 是与X 不同主族的金属元素,N 的氢氧化物具有两性,下列说法正确的是
| A.电负性:Z<Y<W |
| B.Y 的氢化物沸点不一定低于W 的氢化物 |
| C.第一电离能:M<N |
| D.N 的单质可以在高温下还原 M 的氧化物 |
您最近一年使用:0次
2023-01-06更新
|
622次组卷
|
5卷引用:天津市南开中学2022-2023学年高二上学期期末考试化学试题
10 . 根据原子结构与性质的相关知识,请回答下列问题:
(1)基态S原子电子占据最高能层的符号是______ ,最高能级的电子云轮廓图为______ 形。
(2)电负性As______ Se(填“大于”或“小于”)。
(3) 基态核外电子排布式为
基态核外电子排布式为______ ,基态磷原子的核外价电子排布图为______ 。
(4)铜元素在元素周期表中的位置是______ ,位于元素周期表的______ 区。
(5)C、N、O的第一电离能由大到小的顺序为______ 。
(6)已知 和
和 反应放热,且断开1molH−H键、1molO=O键、1molO−H键吸收的能量分别为
反应放热,且断开1molH−H键、1molO=O键、1molO−H键吸收的能量分别为 kJ、
kJ、 kJ、
kJ、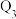 kJ,由此推知下列关系正确的是______(填选项字母)。
kJ,由此推知下列关系正确的是______(填选项字母)。
(1)基态S原子电子占据最高能层的符号是
(2)电负性As
(3)
 基态核外电子排布式为
基态核外电子排布式为(4)铜元素在元素周期表中的位置是
(5)C、N、O的第一电离能由大到小的顺序为
(6)已知
 和
和 反应放热,且断开1molH−H键、1molO=O键、1molO−H键吸收的能量分别为
反应放热,且断开1molH−H键、1molO=O键、1molO−H键吸收的能量分别为 kJ、
kJ、 kJ、
kJ、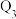 kJ,由此推知下列关系正确的是______(填选项字母)。
kJ,由此推知下列关系正确的是______(填选项字母)。A.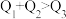 | B.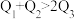 | C.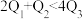 | D.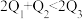 |
您最近一年使用:0次



