真题
名校
1 . 日光灯中用到的某种荧光粉的主要成分为3W3(ZX4)2·WY2。已知:X、Y、Z和W为原子序数依次增大的前20号元素,W为金属元素。基态X原子s轨道上的电子数和p轨道上的电子数相等,基态X、Y、Z原子的未成对电子数之比为2:1:3。下列说法正确的是
| A.电负性:X>Y>Z>W |
| B.原子半径:X<Y<Z<W |
| C.Y和W的单质都能与水反应生成气体 |
| D.Z元素最高价氧化物对应的水化物具有强氧化性 |
您最近一年使用:0次
2023-06-16更新
|
10995次组卷
|
25卷引用:天津市耀华中学2023-2024学年高三上学期第一次月考化学试题
天津市耀华中学2023-2024学年高三上学期第一次月考化学试题2023年高考湖南卷化学真题(已下线)专题07 元素周期表与元素周期律(已下线)专题07 元素周期表与元素周期律(已下线)专题07 元素周期表与元素周期律(已下线)2023年湖南卷高考真题变式题(选择题6-10)(已下线)考点07 元素周期律和元素周期表(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)第19讲元素周期律与元素周期表安徽省亳州市第二完全中学2022-2023学年高二下学期期末考试化学(A卷)试题(已下线)专题12 物质结构与性质(选择题)-2023年高考化学真题题源解密(新高考专用)(已下线)专题08 物质结构与性质 元素推断-2023年高考化学真题题源解密(全国通用)湖北省武汉市第六中学2023-2024学年高三上学期第一次月考化学试题江西省宜春市宜丰中学2023-2024学年高三上学期开学考试化学试题(已下线)考点18 元素周期律与元素周期表(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)福建省厦门第一中学2024届高三上学期10 月月考化学试题河北省迁安市2023-2024学年高三上学期期中考试化学试题福州市福州高级中学2023-2024学年高三上学期10月月考化学试题福建省厦门第一中学2024届高三上学期第一次月考化学试题重庆市第七中学校2023-2024学年高三上学期11月月考化学试卷北京市第二十中学2023-2024学年高三上学期10月月考化学试题(已下线)题型01 元素位-构-性推断-2024年高考化学答题技巧与模板构建(已下线)题型08 元素周期律推断-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)福建省福州高级中学2023-2024学年高三上学期第一阶段考试化学试卷山东省东营市第一中学2023-2024学年高二下学期开学收心考试化学试题(已下线)FHgkyldyjhx12
名校
解题方法
2 . 氢能是一种极具发展潜力的清洁能源,下列物质都是具有广阔应用前景的储氢材料。按要求回答下列问题:
(1)氢化钠( )是一种常用的储氢剂,遇水后放出氢气并生成一种碱,该反应的还原剂的电子式为
)是一种常用的储氢剂,遇水后放出氢气并生成一种碱,该反应的还原剂的电子式为___________ 。
(2)钛系贮氢合金中的钛锰合金具成本低,吸氢量大,室温下易活化等优点,基态钛的价层电子排布式为___________ 。
(3) (氨硼烷)具有很高的储氢容量及相对低的放氢温度(
(氨硼烷)具有很高的储氢容量及相对低的放氢温度(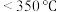 )而成为颇具潜力的化学储氢材料之一,它可通过环硼氮烷、
)而成为颇具潜力的化学储氢材料之一,它可通过环硼氮烷、 与
与 进行合成,则涉及的元素H、B、C、N、O电负性最大的是
进行合成,则涉及的元素H、B、C、N、O电负性最大的是___________ ,键角:
___________  (填“
(填“ ”或“
”或“ ”)。
”)。
(4)咔唑(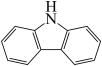 )是一种新型有机液体储氢材料,它的沸点比(
)是一种新型有机液体储氢材料,它的沸点比(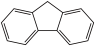 )的高,其主要原因是
)的高,其主要原因是___________ 。
(5)氢气的安全贮存和运输是氢能应用的关键,铁镁合金是目前已发现的储氢密度最高的储氢材料之一,其晶胞结构如图所示。
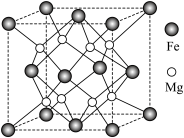
①距离 原子最近的
原子最近的 原子个数是
原子个数是___________ 。
②铁镁合金的化学式为___________ 。
③若该晶胞的晶胞边长为dnm,阿伏加德罗常数为NA,则该合金的密度为___________  。
。
④若该晶体储氢时, 分子在晶胞的体心和棱心位置,则含Mg 48g的该储氢合金可储存标准状况下
分子在晶胞的体心和棱心位置,则含Mg 48g的该储氢合金可储存标准状况下 的体积约为
的体积约为___________ L。
(1)氢化钠(
 )是一种常用的储氢剂,遇水后放出氢气并生成一种碱,该反应的还原剂的电子式为
)是一种常用的储氢剂,遇水后放出氢气并生成一种碱,该反应的还原剂的电子式为(2)钛系贮氢合金中的钛锰合金具成本低,吸氢量大,室温下易活化等优点,基态钛的价层电子排布式为
(3)
 (氨硼烷)具有很高的储氢容量及相对低的放氢温度(
(氨硼烷)具有很高的储氢容量及相对低的放氢温度(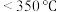 )而成为颇具潜力的化学储氢材料之一,它可通过环硼氮烷、
)而成为颇具潜力的化学储氢材料之一,它可通过环硼氮烷、 与
与 进行合成,则涉及的元素H、B、C、N、O电负性最大的是
进行合成,则涉及的元素H、B、C、N、O电负性最大的是
 (填“
(填“ ”或“
”或“ ”)。
”)。(4)咔唑(
 )是一种新型有机液体储氢材料,它的沸点比(
)是一种新型有机液体储氢材料,它的沸点比( )的高,其主要原因是
)的高,其主要原因是(5)氢气的安全贮存和运输是氢能应用的关键,铁镁合金是目前已发现的储氢密度最高的储氢材料之一,其晶胞结构如图所示。

①距离
 原子最近的
原子最近的 原子个数是
原子个数是②铁镁合金的化学式为
③若该晶胞的晶胞边长为dnm,阿伏加德罗常数为NA,则该合金的密度为
 。
。④若该晶体储氢时,
 分子在晶胞的体心和棱心位置,则含Mg 48g的该储氢合金可储存标准状况下
分子在晶胞的体心和棱心位置,则含Mg 48g的该储氢合金可储存标准状况下 的体积约为
的体积约为
您最近一年使用:0次
2023-05-25更新
|
342次组卷
|
3卷引用:天津市新华中学2023届高三二模化学试题
2023·湖北·模拟预测
名校
解题方法
3 . 五种短周期主族元素X、Y、Z、M、Q的原子序数依次增大,X的2p轨道半充满,Y的s能级电子数和p能级电子数相等, Z是至今发现的电负性最大的元素,M在元素周期表中处于周期序数等于族序数的位置,Q的单质被广泛用作半导体材料。下列叙述中不正确的是
| A.元素的第一电离能:X<Y<Z |
| B.气态氢化物的稳定性:X<Y<Z |
| C.气态氢化物分子的键角:Q>X>Y |
| D.最高价氧化物对应的水化物的酸性:X>Q>M |
您最近一年使用:0次
2023-05-11更新
|
955次组卷
|
8卷引用:化学(天津卷03)-2024年高考化学押题预测卷
(已下线)化学(天津卷03)-2024年高考化学押题预测卷湖北省名校2023届高三下学期5月适应性考试化学试题(已下线)第06练 元素“位—构—性”的综合推断 -2023年【暑假分层作业】高二化学(2024届一轮复习通用)广东省汕头市金山中学2023屇高三下学期三模化学试题福建省泉州第五中学2023届高三一模化学试题江西省新余市第一中学2023-2024学年高三上学期开学考试化学试题吉林省辽源市田家炳高中友好学校七十六届期末联考2023-2024学年高三上学期1月期末化学试题安徽省阜阳市第三中学2023-2024学年高二上学期1月期末化学试题
2023·全国·模拟预测
名校
解题方法
4 . 六方氮化硼(BN)被称为“白色石墨烯”,其纳米片可用于以乙烯-乙酸乙烯酯共聚物为基体的导热复合材料中。下列有关说法正确的是
| A.基态N原子中有2个未成对电子 | B.石墨烯中碳原子的杂化方式为 杂化 杂化 |
C.乙烯分子中 键和 键和 键个数之比为4∶1 键个数之比为4∶1 | D.BN中N的化合价为 价 价 |
您最近一年使用:0次
名校
解题方法
5 . 氢能是一种极具发展潜力的清洁能源,下列物质都是具有广阔应用前景的储氢材料。回答下列问题:
(1)氢化钠(NaH)是一种常用的储氢剂,遇水后放出氢气并生成一种碱,该反应的还原产物为_____ 。
(2)Ti-Fe合金室温下吸、放氢的速率快,Ti元素在周期表中的位置是____ 。
(3) (氨硼烷)具有很高的储氢容量及相对低的放氢温度(<350℃),是颇具潜力的化学储氢材料之一,它可通过环硼氮烷、
(氨硼烷)具有很高的储氢容量及相对低的放氢温度(<350℃),是颇具潜力的化学储氢材料之一,它可通过环硼氮烷、 与
与 进行合成。
进行合成。
① 中涉及的元素H、B、N电负性最大的是
中涉及的元素H、B、N电负性最大的是______ 。
②键角:
_____  (填“>”、“<”或“=”),原因是
(填“>”、“<”或“=”),原因是_______ 。
(4)Fe-Mg合金是目前已发现的储氢密度最高的储氢材料之一,其晶胞结构如图所示。
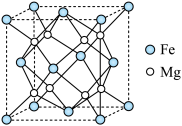
①距离Mg原子最近的Fe原子个数是___________ 。
②若该晶胞的棱长为anm,阿伏加德罗常数的值为 ,则该合金的密度为
,则该合金的密度为___________  。
。
③若该晶体储氢时, 分子在晶胞的体心和棱心位置,则含Mg48g的该储氢合金可储存标准状况下
分子在晶胞的体心和棱心位置,则含Mg48g的该储氢合金可储存标准状况下 的体积约为
的体积约为___________ L。
(1)氢化钠(NaH)是一种常用的储氢剂,遇水后放出氢气并生成一种碱,该反应的还原产物为
(2)Ti-Fe合金室温下吸、放氢的速率快,Ti元素在周期表中的位置是
(3)
 (氨硼烷)具有很高的储氢容量及相对低的放氢温度(<350℃),是颇具潜力的化学储氢材料之一,它可通过环硼氮烷、
(氨硼烷)具有很高的储氢容量及相对低的放氢温度(<350℃),是颇具潜力的化学储氢材料之一,它可通过环硼氮烷、 与
与 进行合成。
进行合成。①
 中涉及的元素H、B、N电负性最大的是
中涉及的元素H、B、N电负性最大的是②键角:

 (填“>”、“<”或“=”),原因是
(填“>”、“<”或“=”),原因是(4)Fe-Mg合金是目前已发现的储氢密度最高的储氢材料之一,其晶胞结构如图所示。

①距离Mg原子最近的Fe原子个数是
②若该晶胞的棱长为anm,阿伏加德罗常数的值为
 ,则该合金的密度为
,则该合金的密度为 。
。③若该晶体储氢时,
 分子在晶胞的体心和棱心位置,则含Mg48g的该储氢合金可储存标准状况下
分子在晶胞的体心和棱心位置,则含Mg48g的该储氢合金可储存标准状况下 的体积约为
的体积约为
您最近一年使用:0次
2023-03-30更新
|
830次组卷
|
2卷引用:天津市南开区2022-2023学年高三下学期质量检测(一)化学试题
名校
6 . 含主族元素N、F、Cl、As、Se等的某些化合物对工农业生产意义重大,下列说法正确的是
| A.N元素基态原子所有价电子的电子云轮廓图均为哑铃形 |
| B.Se元素基态原子的电子排布式为[Ar]4s24p4 |
| C.O、F、Cl电负性由大到小的顺序为F>Cl>O |
| D.第一电离能As>Se |
您最近一年使用:0次
2023-03-24更新
|
542次组卷
|
4卷引用:天津市武清区杨村第一中学2023-2024学年高三上学期第三次质量检测化学试题
名校
解题方法
7 . 下列与分子性质有关的说法正确的是
A.邻硝基苯酚( )的沸点高于对硝基苯酚( )的沸点高于对硝基苯酚( )是因为后者形成了分子间氢键 )是因为后者形成了分子间氢键 |
B. 的酸性强于 的酸性强于 是因为 是因为 的电负性大,使 的电负性大,使 中 中 极性强 极性强 |
C.C的电负性强于Si,所以 的熔沸点高于 的熔沸点高于 |
D.尿素 不溶于水,易溶于有机溶剂 不溶于水,易溶于有机溶剂 |
您最近一年使用:0次
2023-03-10更新
|
1246次组卷
|
7卷引用:天津市武清区城关中学、杨村第四中学、黄花店中学2022-2023学年高二下学期第一次阶段考化学试题
8 . 嫦娥5号月球探测器带回的月壤样品的元素分析结果如图,下列有关含量前六位元素的说法正确的是
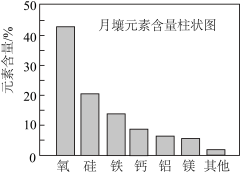
| A.原子半径:Al<Si | B.第一电离能:Mg<Ca |
| C.Fe位于元素周期表的p区 | D.这六种元素中,电负性最大的是O |
您最近一年使用:0次
2023-02-23更新
|
3965次组卷
|
17卷引用:天津市南开区2022-2023学年高二上学期阶段性质量监测化学试题
天津市南开区2022-2023学年高二上学期阶段性质量监测化学试题2022年天津市普通高中学业水平等级性考试化学试题2022年天津高考化学真题(已下线)2022年天津市普通高中学业水平等级性考试化学试题变式题(选择题1-4)天津市第二南开学校2022--2023学年高二下学期期中质量调查化学试题天津市北辰区2023-2024学年高三上学期11月期中考试化学试题(已下线)专题07 突破原子结构和元素周期表(律)(选择题)-2023年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)(已下线)第19讲元素周期律与元素周期表黑龙江省齐齐哈尔市恒昌中学校2022-2023学年高二下学期7月期末考试化学试题(已下线)专题08 物质结构与性质 元素推断-2023年高考化学真题题源解密(全国通用)(已下线)考点18 元素周期律与元素周期表(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)(已下线)选择题1-5(已下线)专题11 原子结构 原子结构与元素的性质-【好题汇编】备战2023-2024学年高二化学上学期期末真题分类汇编(人教版2019)湖南省长沙市明德中学2023-2024学年高二上学期12月月考化学试题浙江省宁波市奉化区2023-2024学年高二上学期期末检测化学试题(已下线)热点02 原子结构与元素的性质广东省肇庆市加美学校2023-2024学年高二下学期竞赛化学试题
名校
9 . 能源、材料与生产生活和社会发展密切相关。
I.光伏材料是指能将太阳能直接转换成电能的材料。光伏材料又称太阳能材料,只有半导体材料具有这种功能。可作太阳能电池材料的有单晶硅、多晶硅、非晶硅、GaAs、GaAlAs、InP、CdS、CdTe等。
(1)写出31号元素镓(Ga)的原子结构示意图:_______ 。
(2)P、S、Ga电负性从大到小的顺序为_______ 。
(3)As元素的第一电离能_______ (填“大于”“小于”或“等于”)Se元素的第一电离能。
(4)写出原子序数最小的第VIII族元素基态原子的核外电子排布式:_______ 。
(5)写出3p轨道上只有2个未成对电子的元素的符号:_______ 、_______ 。
II.从化学键的角度分析,化学反应的过程就是反应物的化学键断裂和生成物的化学键形成的过程。在化学反应过程中,断裂化学键需要消耗能量,形成化学键又会释放能量。
(6)已知:
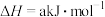 ,根据上表中所列键能数据可计算出a=
,根据上表中所列键能数据可计算出a=_______ 。
I.光伏材料是指能将太阳能直接转换成电能的材料。光伏材料又称太阳能材料,只有半导体材料具有这种功能。可作太阳能电池材料的有单晶硅、多晶硅、非晶硅、GaAs、GaAlAs、InP、CdS、CdTe等。
(1)写出31号元素镓(Ga)的原子结构示意图:
(2)P、S、Ga电负性从大到小的顺序为
(3)As元素的第一电离能
(4)写出原子序数最小的第VIII族元素基态原子的核外电子排布式:
(5)写出3p轨道上只有2个未成对电子的元素的符号:
II.从化学键的角度分析,化学反应的过程就是反应物的化学键断裂和生成物的化学键形成的过程。在化学反应过程中,断裂化学键需要消耗能量,形成化学键又会释放能量。
| 化学键 | H—H | N—H | N≡N |
| 键能/(kJ/mol) | 436 | 391 | 945 |

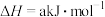 ,根据上表中所列键能数据可计算出a=
,根据上表中所列键能数据可计算出a=
您最近一年使用:0次
10 . N、P两种元素位于元素周期表第VA族。请回答下列问题:
(1)基态氮原子的电子排布式为________ ;基态氮原子的价层电子的轨道表示式为________ 。
(2)基态磷原子中,其占据的最高能层的符号是________ ;基态磷原子占据的最高能级共有________ 个原子轨道,其形状是________ 。
(3)电负性:N________ P(填>或<)。
(4)雷酸汞曾被用作起爆药,雷酸汞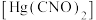 中C、N、O三种元素第一电离能从大到小的顺序为
中C、N、O三种元素第一电离能从大到小的顺序为________ >________ >________ (填元素符号)。
(1)基态氮原子的电子排布式为
(2)基态磷原子中,其占据的最高能层的符号是
(3)电负性:N
(4)雷酸汞曾被用作起爆药,雷酸汞
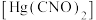 中C、N、O三种元素第一电离能从大到小的顺序为
中C、N、O三种元素第一电离能从大到小的顺序为
您最近一年使用:0次
2023-02-15更新
|
383次组卷
|
2卷引用:天津市朱唐庄中学2022-2023学年高二下学期3月阶段性检测化学试题



