名校
解题方法
1 . 很多含巯基(-SH)的有机化合物是重金属元素汞的解毒剂。例如,解毒剂化合物Ⅰ可与氧化汞生成化合物Ⅱ。
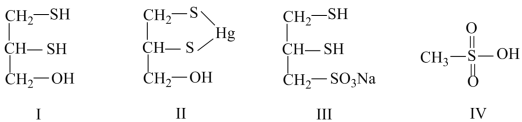
(1)1mol化合物Ⅰ含有_______ mol σ键。
(2)基态硫原子价层电子排布式为_______ 。
(3)H2S、CH4、H2O的沸点由高到低顺序为_______ 。
(4)汞的原子序数为80,位于元素周期表第_______ 周期第ⅡB族。
(5)化合物Ⅲ也是一种汞解毒剂。化合物Ⅳ是一种强酸。下列说法正确的有_______ 。
A.在Ⅰ中S原子采取sp3杂化
B.在Ⅱ中S元素的电负性最大
C.在Ⅲ中C-C-C键角是180°
D.在Ⅲ中存在离子键与共价键
E.在Ⅳ中硫氧键的键能均相等

(1)1mol化合物Ⅰ含有
(2)基态硫原子价层电子排布式为
(3)H2S、CH4、H2O的沸点由高到低顺序为
(4)汞的原子序数为80,位于元素周期表第
(5)化合物Ⅲ也是一种汞解毒剂。化合物Ⅳ是一种强酸。下列说法正确的有
A.在Ⅰ中S原子采取sp3杂化
B.在Ⅱ中S元素的电负性最大
C.在Ⅲ中C-C-C键角是180°
D.在Ⅲ中存在离子键与共价键
E.在Ⅳ中硫氧键的键能均相等
您最近一年使用:0次
名校
2 . 完成下列问题。
Ⅰ.短周期元素D、E、X、Y、Z原子序数逐渐增大,它们的最简单氢化物分子空间结构依次是正四面体形、三角锥形、正四面体形、V形、直线形。回答下列问题:
(1)HZO分子的中心原子价层电子对数的计算式为___________ ,该分子的空间结构为___________ 。
(2)Y的价层电子排布式为_________ ,Y的最高价氧化物的VSEPR模型为________ 。
(3)D、E的最简单氢化物的分子空间结构分别是正四面体形与三角锥形,这是因为_______ 。
a.两种分子的中心原子的价层电子对数不同
b.D、E的非金属性不同
c.E的氢化物分子中有一个孤电子对,而D的氢化物分子中没有
Ⅱ.有A、B、C、D、E、F六种主族元素,有关信息如下:
①短周期元素C原子的价电子排布式为ns2np2,E的单质可在空气中燃烧;
②如图是元素周期表中主族元素的一部分:
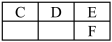
③A、B同周期,其电离能数据如下(单位:kJ·mol-1):
试回答下列问题:
(4)F原子的核外电子排布式为___________ 。
(5)C、D、E元素的电负性相对大小为___________ (用元素符号表示)。
(6)化合价是元素的一种性质,由A、B的电离能数据判断下列说法正确的是______ (填字母)。
a.A通常显+1价,B通常显+4价
b.B元素的第一电离能较小,其活泼性比A强
c.A、B的单质分别与盐酸反应放出等量氢气时,消耗单质的物质的量之比为3∶2
Ⅰ.短周期元素D、E、X、Y、Z原子序数逐渐增大,它们的最简单氢化物分子空间结构依次是正四面体形、三角锥形、正四面体形、V形、直线形。回答下列问题:
(1)HZO分子的中心原子价层电子对数的计算式为
(2)Y的价层电子排布式为
(3)D、E的最简单氢化物的分子空间结构分别是正四面体形与三角锥形,这是因为
a.两种分子的中心原子的价层电子对数不同
b.D、E的非金属性不同
c.E的氢化物分子中有一个孤电子对,而D的氢化物分子中没有
Ⅱ.有A、B、C、D、E、F六种主族元素,有关信息如下:
①短周期元素C原子的价电子排布式为ns2np2,E的单质可在空气中燃烧;
②如图是元素周期表中主族元素的一部分:

③A、B同周期,其电离能数据如下(单位:kJ·mol-1):
| I1 | I2 | I3 | I4 | |
| A | 738 | 1 451 | 7 733 | 10 540 |
| B | 578 | 1 817 | 2 745 | 11 575 |
(4)F原子的核外电子排布式为
(5)C、D、E元素的电负性相对大小为
(6)化合价是元素的一种性质,由A、B的电离能数据判断下列说法正确的是
a.A通常显+1价,B通常显+4价
b.B元素的第一电离能较小,其活泼性比A强
c.A、B的单质分别与盐酸反应放出等量氢气时,消耗单质的物质的量之比为3∶2
您最近一年使用:0次
名校
3 . W、X、Y、Z为原子序数依次增大的短周期主族元素,且原子核外L层的电子数分别为0、5、8、8,其最外层电子数之和为18,下列说法正确的是
| A.电负性:Y<Z |
| B.第一电离能:Y>X |
| C.化合物WZ难溶于水 |
| D.由Y与Z形成的化合物YZ3和YZ5均满足8电子稳定结构 |
您最近一年使用:0次
4 . 元素N、O、F的某些性质随核电荷数的变化趋势如图所示。下列图示不正确的是
A. | B. |
C. | D. |
您最近一年使用:0次
名校
5 . 碳、硫、氧、氮是中学常见元素,下列说法不正确的是
A. 、 、 、 、 都是直线形分子 都是直线形分子 |
B. 、 、 、 、 的键角依次减小 的键角依次减小 |
C. 、 、 分子的中心原子都是 分子的中心原子都是 化 化 |
| D.C、N、F元素的电负性依次增大 |
您最近一年使用:0次
2023-06-08更新
|
148次组卷
|
5卷引用:福建省三明市四地四校2021-2022学年高二下学期期中联考化学试题
解题方法
6 . 下列说法正确的是
| A.元素的第一电离能越大,其金属性一定越强 |
| B.元素的第一电离能越小,其金属性一定越强 |
| C.同主族元素的单质从上到下,熔点升高 |
| D.一般情况下,金属单质与酸反应越容易,其元素的电负性越小 |
您最近一年使用:0次
7 . 嫦娥5号月球探测器带回的月壤样品的元素分析结果如图,下列有关含量前六位元素的说法正确的是
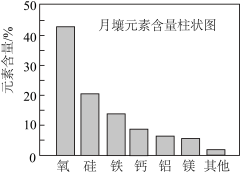
| A.原子半径:Al<Si | B.第一电离能:Mg<Ca |
| C.Fe位于元素周期表的p区 | D.这六种元素中,电负性最大的是O |
您最近一年使用:0次
2023-02-23更新
|
4000次组卷
|
17卷引用:2022年天津市普通高中学业水平等级性考试化学试题
2022年天津市普通高中学业水平等级性考试化学试题2022年天津高考化学真题(已下线)2022年天津市普通高中学业水平等级性考试化学试题变式题(选择题1-4)天津市南开区2022-2023学年高二上学期阶段性质量监测化学试题(已下线)专题07 突破原子结构和元素周期表(律)(选择题)-2023年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)天津市第二南开学校2022--2023学年高二下学期期中质量调查化学试题(已下线)第19讲元素周期律与元素周期表黑龙江省齐齐哈尔市恒昌中学校2022-2023学年高二下学期7月期末考试化学试题(已下线)专题08 物质结构与性质 元素推断-2023年高考化学真题题源解密(全国通用)(已下线)考点18 元素周期律与元素周期表(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)(已下线)选择题1-5天津市北辰区2023-2024学年高三上学期11月期中考试化学试题(已下线)专题11 原子结构 原子结构与元素的性质-【好题汇编】备战2023-2024学年高二化学上学期期末真题分类汇编(人教版2019)湖南省长沙市明德中学2023-2024学年高二上学期12月月考化学试题浙江省宁波市奉化区2023-2024学年高二上学期期末检测化学试题(已下线)热点02 原子结构与元素的性质广东省肇庆市加美学校2023-2024学年高二下学期竞赛化学试题
8 . 现有三种元素的基态原子的电子排布式如下:①1s22s22p63s23p4;②1s22s22p63s23p3;③1s22s22p63s23p5,下列排序正确的是
| A.含氧酸的酸性:③>①>② | B.原子半径:③>②>① |
| C.第一电离能:③>②>① | D.电负性:③>②>① |
您最近一年使用:0次
解题方法
9 . 立方氮化硼硬度高,耐磨性好,在机械加工行业有广泛应用。制备立方氮化硼的一种方法为BCl3(g)+NH3(g)=BN(s)+3HCl(g),下列说法错误的是
| A.反应混合物中所有化学键均为共价键 |
| B.元素电负性大小为N>B |
| C.BCl3和BN均为共价晶体 |
D.形成BCl3时B原子先激发后杂化,其激发态价电子轨道表示式为: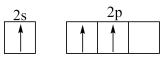 |
您最近一年使用:0次
22-23高三下·福建泉州·阶段练习
解题方法
10 . 点击化学(click chemistry)是一种能够让分子的构建模块快速、高效地结合在一起的化学反应。科学工作者可以利用基础模块搭建出变化无穷的造型,就如同玩乐高玩具一般。叠氨化物和块经合成抗真菌药物三唑是点击化学的重要应用,反应示例如下:
(1) 的核外电子排布式为
的核外电子排布式为_______ 。
(2)C、N、Cu的电负性由大到小的顺序为_______ 。
(3)分子乙中存在5中心6电子的大 键,其中,提供两个电子形成大
键,其中,提供两个电子形成大 键(
键( )的原子是
)的原子是_______ (填对应原子的序号)。
(4)分子中碳碳三键的活泼性:甲_______ 丙(填“>”“=”“<”),理由是_______ (从分子的结构角度分析)。
(5)丁形成的晶体中不存在的微粒间作用力有_______ 。
A.离子键 B.极性键 C.非极性键 D.氢键 E.范德华力
(6)CuCl的晶胞中, 的位置如图所示,
的位置如图所示, 填充于
填充于 构成的四面体空隙中。
构成的四面体空隙中。 的配位数为
的配位数为_______ 。
②由 构成的八面体空隙与有
构成的八面体空隙与有 填充的
填充的 构成的四面体空隙的数目之比为
构成的四面体空隙的数目之比为_______ 。
 +CH3CH2N3
+CH3CH2N3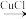

 +CH3CH2N3→
+CH3CH2N3→
(1)
 的核外电子排布式为
的核外电子排布式为(2)C、N、Cu的电负性由大到小的顺序为
(3)分子乙中存在5中心6电子的大
 键,其中,提供两个电子形成大
键,其中,提供两个电子形成大 键(
键( )的原子是
)的原子是(4)分子中碳碳三键的活泼性:甲
(5)丁形成的晶体中不存在的微粒间作用力有
A.离子键 B.极性键 C.非极性键 D.氢键 E.范德华力
(6)CuCl的晶胞中,
 的位置如图所示,
的位置如图所示, 填充于
填充于 构成的四面体空隙中。
构成的四面体空隙中。
 的配位数为
的配位数为②由
 构成的八面体空隙与有
构成的八面体空隙与有 填充的
填充的 构成的四面体空隙的数目之比为
构成的四面体空隙的数目之比为
您最近一年使用:0次



