9-10高二下·福建泉州·期末
名校
解题方法
1 . 观察下表模型并结合有关信息,判断下列说法中不正确的是
| B12结构单元 | SF6分子 | S8分子 | HCN | |
| 结构模型示意图 | 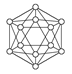 |  | 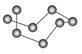 |  |
| 备注 | 熔点1873 K | — | 易溶于CS2 | — |
| A.单质硼属于原子晶体,每个B12结构单元中含有30个B—B键和20个正三角形 |
| B.SF6是由极性键构成的非极性分子 |
| C.固态硫S8属于原子晶体 |
| D.HCN的结构式为H—C≡N |
您最近一年使用:0次
2014-04-15更新
|
1162次组卷
|
10卷引用:2010年福建省南安一中高二下学期期末考试化学试卷
(已下线)2010年福建省南安一中高二下学期期末考试化学试卷(已下线)2014年高考化学苏教版总复习 12-2 微粒间作用力与物质性质练习卷河北省邢台市2019-2020学年高二下学期期末考试化学试题(鲁科版2019)选择性必修2 第3章 不同聚集状态的物质与性质 章末综合检测卷(人教版2019)选择性必修2 第三章 晶体结构与性质 章末综合检测卷(人教版2019)选择性必修2 第三章 晶体结构与性质 B 素养拓展区山西省怀仁市大地学校2020-2021学年高二下学期第三次月考化学试题吉林省通化市部分重点中学校2021-2022学年高二下学期期末联考化学试题安徽省滁州市定远县育才学校2021-2022学年高二下学期分层班第二次月考化学试题山东省济南市山东省实验中学2023-2024学年高二下学期4月月考化学试题
11-12高三上·上海松江·期中
名校
解题方法
2 . 已知丙氨酸的结构简式为: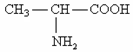 ,根据题意完成下面小题:
,根据题意完成下面小题:
(1)丙氨酸中涉及到四种元素,它们的原子半径由小到大的顺序为___________ 。
(2)丙氨酸分子属于___ (填“极性”或“非极性”)分子,一个丙氨酸分子中含有_____ 个非极性共价键。
(3)丙氨酸分子中的氮原子核外有_____ 个未成对电子,有_____ 种不同能量的电子。
(4)碳、氮、氧都可以形成氢化物,氧元素的氢化物除H2O外,还有H2O2,碳元素的氢化物除CH4外,还有C2H6等。与之相似的氮元素的氢化物的除NH3外,还有________ ,该氢化物与足量盐酸反应的化学方程式为________________ 。
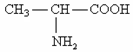 ,根据题意完成下面小题:
,根据题意完成下面小题:(1)丙氨酸中涉及到四种元素,它们的原子半径由小到大的顺序为
(2)丙氨酸分子属于
(3)丙氨酸分子中的氮原子核外有
(4)碳、氮、氧都可以形成氢化物,氧元素的氢化物除H2O外,还有H2O2,碳元素的氢化物除CH4外,还有C2H6等。与之相似的氮元素的氢化物的除NH3外,还有
您最近一年使用:0次
10-11高二下·江西南昌·期末
3 . 在①HF、②H2S、③BF3、④CS2、⑤CCl4、⑥N2、⑦SO2分子中:
(1)以非极性键结合的非极性分子是___________
(2)以极性键相结合,具有直线型结构的非极性分子是___________
(3)以极性键相结合,具有正四面体结构的非极性分子是___________
(4)以极性键相结合,而且分子极性最大的是___________
(1)以非极性键结合的非极性分子是
(2)以极性键相结合,具有直线型结构的非极性分子是
(3)以极性键相结合,具有正四面体结构的非极性分子是
(4)以极性键相结合,而且分子极性最大的是
您最近一年使用:0次
10-11高二下·湖北襄阳·期中
4 . 水是自然界中普遍存在的一种重要物质,根据下列信息回答问题:
(1)氧原子基态时价层电子的电子排布图为____________ 。
(2)已知2H2O H3O+ +OH-,H3O+的立体构型是
H3O+ +OH-,H3O+的立体构型是____________ ,中心原子的杂化类型是___________ 。
(3)下列关于水的说法正确的是__________ (选填序号)。
①在冰晶体中每一个水分子内含有两个氢键;
②水分子是由极性键构成的极性分子;
③水在化学反应中可以作氧化剂,也可以作还原剂;
④水分子中既含σ键,又含有π键;
⑤纯水呈中性,所以在任何条件下纯水的PH均为7;
⑥水分子中的氧原子的杂化类型是sp3杂化,价层电子对数是2。
(4)试比较同主族元素的氢化物H2O、H2S和H2Se的稳定性和沸点高低。
稳定性:___________________ 沸点:___________________
(1)氧原子基态时价层电子的电子排布图为
(2)已知2H2O
 H3O+ +OH-,H3O+的立体构型是
H3O+ +OH-,H3O+的立体构型是(3)下列关于水的说法正确的是
①在冰晶体中每一个水分子内含有两个氢键;
②水分子是由极性键构成的极性分子;
③水在化学反应中可以作氧化剂,也可以作还原剂;
④水分子中既含σ键,又含有π键;
⑤纯水呈中性,所以在任何条件下纯水的PH均为7;
⑥水分子中的氧原子的杂化类型是sp3杂化,价层电子对数是2。
(4)试比较同主族元素的氢化物H2O、H2S和H2Se的稳定性和沸点高低。
稳定性:
您最近一年使用:0次
10-11高二下·福建三明·阶段练习
5 . 在下列物质中(填序号)
A.Cl2 B. NaI C. H2S D.CO2 E. CaCl2 F. N2 G. CCl4 H.Na2O I. NH3 J. HBr
(1)含离子键的物质是____________ ;
(2)含有共价键化合物的是_____________________ ;
(3)由极性键形成的非极性分子是_______________ ;
(4)由非极性键形成的非极性分子是_______________ 。
A.Cl2 B. NaI C. H2S D.CO2 E. CaCl2 F. N2 G. CCl4 H.Na2O I. NH3 J. HBr
(1)含离子键的物质是
(2)含有共价键化合物的是
(3)由极性键形成的非极性分子是
(4)由非极性键形成的非极性分子是
您最近一年使用:0次
真题
6 . 四种元素X、Y、Z、W位于元素周期表的前四周期,已知它们的核电荷数
依次增加,且核电荷数之和为51;Y原子的L层p轨道中有2个电子;Z与Y原子的价层电子数相同;W原子的L层电子数与最外层电子数之比为4:1,其d轨道中的电子数与最外层电子数之比为5:1。
(1)Y、Z可分别与X形成只含一个中心原子的共价化合物a、b,它们的分子式分别是_____ 、_______ ; 杂化轨道分别是________ 、_________ ;a分子的立体结构是____________ 。
(2)Y的最高价氧化物和Z的最高价氧化物的晶体类型分别是_______ 晶体、_______ 晶体:
(3)X的氧化物与Y的氧化物中,分子极性较小的是(填分子式)__________ ;
(4)Y与Z比较,电负性较大的____________ , 其+2价离子的核外电子排布式是_________ 。
依次增加,且核电荷数之和为51;Y原子的L层p轨道中有2个电子;Z与Y原子的价层电子数相同;W原子的L层电子数与最外层电子数之比为4:1,其d轨道中的电子数与最外层电子数之比为5:1。
(1)Y、Z可分别与X形成只含一个中心原子的共价化合物a、b,它们的分子式分别是
(2)Y的最高价氧化物和Z的最高价氧化物的晶体类型分别是
(3)X的氧化物与Y的氧化物中,分子极性较小的是(填分子式)
(4)Y与Z比较,电负性较大的
您最近一年使用:0次



