名校
解题方法
1 . 碱式氧化镍是镍电池的正极活性材料。利用镍渣(主要含NiO,及少量 、CuO、CaO、
、CuO、CaO、 等杂质)制备碱式氧化镍的流程如下:
等杂质)制备碱式氧化镍的流程如下:
(2)浸渣的主要成分是_______ 。
(3)“沉铜”过程中生成单质S的离子方程式为______ 。
(4)“氧化”中的目的是将 氧化为
氧化为 ,试剂R可选用
,试剂R可选用_____ (填标号)。写出“氧化”时反应的离子方程式:_____ 。
A.氯水 B. 酸性溶液 C.
酸性溶液 C.
(5)碱式氧化镍(NiOOH)可用作镍氢电池的正极材料,电池的总反应为
 ,其工作时的正极电极反应式为
,其工作时的正极电极反应式为_______ 。
(6)若用2.0t废料(含NiO75%)制得NiOOH 0.92 t,则NiOOH的产率为_____ %。
 、CuO、CaO、
、CuO、CaO、 等杂质)制备碱式氧化镍的流程如下:
等杂质)制备碱式氧化镍的流程如下: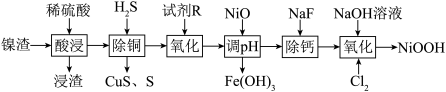
| A.研磨废料 | B.加入大量水 | C.搅拌 | D.适当升高温度 |
(2)浸渣的主要成分是
(3)“沉铜”过程中生成单质S的离子方程式为
(4)“氧化”中的目的是将
 氧化为
氧化为 ,试剂R可选用
,试剂R可选用A.氯水 B.
 酸性溶液 C.
酸性溶液 C.
(5)碱式氧化镍(NiOOH)可用作镍氢电池的正极材料,电池的总反应为

 ,其工作时的正极电极反应式为
,其工作时的正极电极反应式为(6)若用2.0t废料(含NiO75%)制得NiOOH 0.92 t,则NiOOH的产率为
您最近一年使用:0次
2024-05-03更新
|
278次组卷
|
2卷引用:广东省深圳市翠园中学、龙城高级中学2023-2024学年高一下学期第一次月考化学试题
名校
解题方法
2 . 已知:溴苯的沸点为 ,苯的沸点为
,苯的沸点为 。实验室用苯和液溴制取溴苯并验证反应类型的实验装置如图:
。实验室用苯和液溴制取溴苯并验证反应类型的实验装置如图:
(1)冷凝管的进水口为__________ (填“A”或“B”);冷凝管的作用:__________ 。
(2)d中盛放的试剂是__________ 。
(3)有同学认为苯与溴的反应为取代反应,请根据该实验装置特点和实验现象。叙述得出这一结论的实验现象:_____________ 。
(4)分离提纯:
①反应后a瓶中的溴苯中因溶有溴而显褐色,提纯溴苯的过程中,除去溴苯中的溴可加入__________ 溶液,振荡,再通过__________ (填分离方法)分离提纯;
②苯与溴还可能发生副反应生成对二溴苯(沸点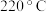 )和邻二溴苯(沸点
)和邻二溴苯(沸点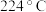 ),因此最后再经
),因此最后再经_______ (填分离方法)即可得到较纯净的溴苯,该过程中为了受热均匀和易于控制温度,可采用_______ (填“水浴”或“油浴”)加热
(5)检验鉴别:充分反应后,三颈烧瓶中的粗产品经水洗、分液后得到水洗液,为验证水洗液中是否存在 不能选用的试剂是__________(填字母)
不能选用的试剂是__________(填字母)
 ,苯的沸点为
,苯的沸点为 。实验室用苯和液溴制取溴苯并验证反应类型的实验装置如图:
。实验室用苯和液溴制取溴苯并验证反应类型的实验装置如图: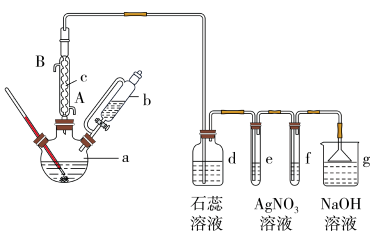
(1)冷凝管的进水口为
(2)d中盛放的试剂是
(3)有同学认为苯与溴的反应为取代反应,请根据该实验装置特点和实验现象。叙述得出这一结论的实验现象:
(4)分离提纯:
①反应后a瓶中的溴苯中因溶有溴而显褐色,提纯溴苯的过程中,除去溴苯中的溴可加入
②苯与溴还可能发生副反应生成对二溴苯(沸点
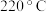 )和邻二溴苯(沸点
)和邻二溴苯(沸点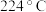 ),因此最后再经
),因此最后再经(5)检验鉴别:充分反应后,三颈烧瓶中的粗产品经水洗、分液后得到水洗液,为验证水洗液中是否存在
 不能选用的试剂是__________(填字母)
不能选用的试剂是__________(填字母)A. 溶液 溶液 | B. 溶液 溶液 | C. 溶液 溶液 | D.苯酚溶液 |
您最近一年使用:0次
3 . 黑木耳富含蛋白质、铁、具有还原性的维生素C等,每100 g黑木耳含铁量高达185 mg。
I.为了确定黑木耳中含有铁元素,甲同学设计实验方案如下。____________ 。
(2)步骤④检验Fe3+所用试剂是_____________ (填化学式)溶液。
(3)已知:3Fe2++2[Fe(CN)6]3-=Fe3[Fe(CN)6]2↓,则滤液A中大量含有的阳离子 的离子符号为____________ 。
II.紫色的KMnO4溶液在酸性条件下具有强氧化性,其还原产物是无色的Mn2+。本实验用KMnO4酸性溶液来测定黑木耳中铁元素的含量,乙同学设计实验方案如下。_______ (填序号)。
a.Na b.Cu c.Fe
(5)步骤⑥的离子方程式为_______________ 。
(6)若乙同学实验操作规范,但测得含铁量远远偏高,其可能的原因是_______________ 。
I.为了确定黑木耳中含有铁元素,甲同学设计实验方案如下。
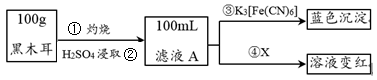
(2)步骤④检验Fe3+所用试剂是
(3)已知:3Fe2++2[Fe(CN)6]3-=Fe3[Fe(CN)6]2↓,则滤液A中大量含有的
II.紫色的KMnO4溶液在酸性条件下具有强氧化性,其还原产物是无色的Mn2+。本实验用KMnO4酸性溶液来测定黑木耳中铁元素的含量,乙同学设计实验方案如下。
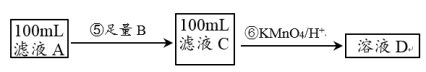
a.Na b.Cu c.Fe
(5)步骤⑥的离子方程式为
(6)若乙同学实验操作规范,但测得含铁量远远偏高,其可能的原因是
您最近一年使用:0次
解题方法
4 . 除杂和离子的检验是中学化学的重要内容。回答下列问题:
(1)欲除去粗盐水中的 设计如下工艺流程(所加试剂均过量)。
设计如下工艺流程(所加试剂均过量)。______________________ ;
②试剂a、试剂b、试剂c 依次为______________________ (填字母)。
A. Na2CO3溶液、 BaCl2溶液、 稀盐酸 B. BaCl2溶液、 Na2CO3溶液、 稀盐酸
C. Na2CO3溶液、 NaOH溶液、 稀盐酸 D. BaCl2溶液、 NaOH溶液、 稀盐酸
③实验室中进行操作x 需用到的玻璃仪器有烧杯、玻璃棒和______________________ 。
(2)某无色透明溶液可能存在大量 中的一种或几种,进行如下实验:
中的一种或几种,进行如下实验:
I.取少量原溶液,加入过量稀盐酸,有白色沉淀生成,再加入过量稀硝酸,沉淀不消失;
Ⅱ.取I的滤液加过量的NaOH 溶液,出现白色沉淀。
①由操作I确定原溶液中肯定存在的阳离子是______________________ ,操作I中产生白色沉淀的离子方 程式为______________________ 。
②通过以上信息可知肯定不存在的离子是______________________ 。
(1)欲除去粗盐水中的
 设计如下工艺流程(所加试剂均过量)。
设计如下工艺流程(所加试剂均过量)。
②试剂a、试剂b、试剂c 依次为
A. Na2CO3溶液、 BaCl2溶液、 稀盐酸 B. BaCl2溶液、 Na2CO3溶液、 稀盐酸
C. Na2CO3溶液、 NaOH溶液、 稀盐酸 D. BaCl2溶液、 NaOH溶液、 稀盐酸
③实验室中进行操作x 需用到的玻璃仪器有烧杯、玻璃棒和
(2)某无色透明溶液可能存在大量
 中的一种或几种,进行如下实验:
中的一种或几种,进行如下实验:I.取少量原溶液,加入过量稀盐酸,有白色沉淀生成,再加入过量稀硝酸,沉淀不消失;
Ⅱ.取I的滤液加过量的NaOH 溶液,出现白色沉淀。
①由操作I确定原溶液中肯定存在的阳离子是
②通过以上信息可知肯定不存在的离子是
您最近一年使用:0次
名校
解题方法
5 . 利用石灰乳和硝酸工业的尾气(含NO、 )反应,既能净化尾气,又能获得应用广泛的
)反应,既能净化尾气,又能获得应用广泛的 其部分工艺流程如图:
其部分工艺流程如图:___________ 。
(2)已知 受热会发生分解,最后从溶液中获得无水
受热会发生分解,最后从溶液中获得无水 的方法是
的方法是___________ 。
(3)下列说法不正确的是______。
 )反应,既能净化尾气,又能获得应用广泛的
)反应,既能净化尾气,又能获得应用广泛的 其部分工艺流程如图:
其部分工艺流程如图:
(2)已知
 受热会发生分解,最后从溶液中获得无水
受热会发生分解,最后从溶液中获得无水 的方法是
的方法是(3)下列说法不正确的是______。
| A.NO分子中只存在共价键 |
B. 晶体中既有离子键又有共价键 晶体中既有离子键又有共价键 |
C. 晶体溶于水时有离子键的断裂 晶体溶于水时有离子键的断裂 |
D. 分子中每个原子都达到了8电子稳定结构 分子中每个原子都达到了8电子稳定结构 |
您最近一年使用:0次
名校
6 . 四氧化三锰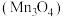 广泛应用于软磁材料、电池材料等高科技材料制备领域。一种以低品位锰矿(含
广泛应用于软磁材料、电池材料等高科技材料制备领域。一种以低品位锰矿(含 、
、 及少量
及少量 、
、 、
、 )为原料生产
)为原料生产 的工艺流程如下:
的工艺流程如下:
回答以下问题:
(1)元素Si在周期表的位置为___________ 。
(2)为提高反应和生产效率,“溶浸”时适宜采取的预处理措施是(回答一种措施)___________ 。不采取“升温”措施的原因是___________ 。
(3)“溶浸”时 发生反应的离子方程式为:
发生反应的离子方程式为:___________ 。此步骤的硫酸可用后续从“沉锰”滤液中获得的副产品 代替,但不能用盐酸代替,主要原因是:
代替,但不能用盐酸代替,主要原因是:___________ 。
(4)滤渣2主要成分的化学式为___________ 。
(5)“调pH=5”工艺中,以下的___________(填写序号)最适宜选作“物质A”来添加。
(6)写出“沉锰”工艺中反应的离子方程式___________ 。
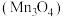 广泛应用于软磁材料、电池材料等高科技材料制备领域。一种以低品位锰矿(含
广泛应用于软磁材料、电池材料等高科技材料制备领域。一种以低品位锰矿(含 、
、 及少量
及少量 、
、 、
、 )为原料生产
)为原料生产 的工艺流程如下:
的工艺流程如下: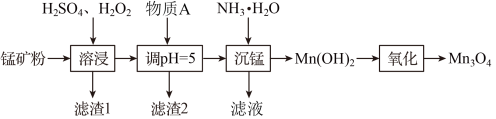
| 金属离子 |  |  |  |  |
| 开始沉淀的pH | 7.2 | 2.2 | 3.8 | 8.8 |
| 完全沉淀的pH | 9.5 | 3.2 | 5.0 | 10.4 |
(1)元素Si在周期表的位置为
(2)为提高反应和生产效率,“溶浸”时适宜采取的预处理措施是(回答一种措施)
(3)“溶浸”时
 发生反应的离子方程式为:
发生反应的离子方程式为: 代替,但不能用盐酸代替,主要原因是:
代替,但不能用盐酸代替,主要原因是:(4)滤渣2主要成分的化学式为
(5)“调pH=5”工艺中,以下的___________(填写序号)最适宜选作“物质A”来添加。
A. | B. | C. | D. |
(6)写出“沉锰”工艺中反应的离子方程式
您最近一年使用:0次
7 . 如图所示,某研究性学习小组欲探究氯气的制备和化学性质,设计的实验装置如图所示: 的升华。
的升华。
回答下列问题:
(1)仪器A的名称是___________ ,按图组装好装置后首先要进行的操作是___________ 。
(2)装置②中盛放的试剂是___________ (填名称),作用是___________ 。
(3)装置①中发生反应的化学方程式为___________ 。
(4)装置①和④两处都需要加热,在实验操作过程中应先点燃___________ (填序号)处的酒精灯,其目的是___________ 。
(5)实验中可观察到紫色石蕊溶液颜色的变化为___________ 。
(6)⑦中氢氧化钠溶液的作用是___________ 。
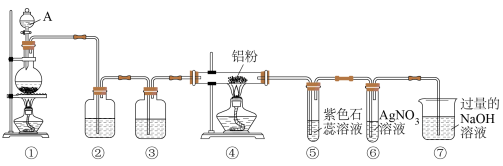
 的升华。
的升华。回答下列问题:
(1)仪器A的名称是
(2)装置②中盛放的试剂是
(3)装置①中发生反应的化学方程式为
(4)装置①和④两处都需要加热,在实验操作过程中应先点燃
(5)实验中可观察到紫色石蕊溶液颜色的变化为
(6)⑦中氢氧化钠溶液的作用是
您最近一年使用:0次
名校
8 . 工业上以钛铁矿(主要成分为 ,含有
,含有 、
、 、
、 、
、 杂质)为原料制备金属钛,并得到副产品
杂质)为原料制备金属钛,并得到副产品 ,其工艺流程如图:
,其工艺流程如图: 反应。回答下列问题:
反应。回答下列问题:
(1)矿渣的主要成分是__________ ;试剂A为__________ (填化学式)。
(2)“操作Ⅱ”为__________ 、__________ 、过滤、洗涤、干燥。
(3)沸腾氯化中,氯气与矿料逆流而行,目的是__________ ,充分反应后,混合气体中CO与 的分压之比为
的分压之比为 ,该温度下,
,该温度下, 与C、
与C、 反应的总化学方程式为
反应的总化学方程式为__________ 。
(4)高温下镁与 反应制备粗钛时需加保护气,下列可作为保护气的是
反应制备粗钛时需加保护气,下列可作为保护气的是__________ (填选项)。
a. b.
b. c.
c. d.Ar
d.Ar
 ,含有
,含有 、
、 、
、 、
、 杂质)为原料制备金属钛,并得到副产品
杂质)为原料制备金属钛,并得到副产品 ,其工艺流程如图:
,其工艺流程如图: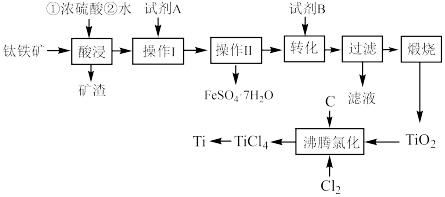
 反应。回答下列问题:
反应。回答下列问题:(1)矿渣的主要成分是
(2)“操作Ⅱ”为
(3)沸腾氯化中,氯气与矿料逆流而行,目的是
 的分压之比为
的分压之比为 ,该温度下,
,该温度下, 与C、
与C、 反应的总化学方程式为
反应的总化学方程式为(4)高温下镁与
 反应制备粗钛时需加保护气,下列可作为保护气的是
反应制备粗钛时需加保护气,下列可作为保护气的是a.
 b.
b. c.
c. d.Ar
d.Ar
您最近一年使用:0次
名校
9 . 非金属元素与人类的生产生活关系密切,根据常见非金属元素及其化合物的性质回答下列问题。
(1)硅酸盐材料是传统无机非金属材料,硅酸盐具有特殊的性质与应用。下列产品属于硅酸盐的是_______ (填序号)。
①玻璃②陶瓷③水晶④硅芯片⑤光导纤维⑥水泥⑦砖瓦
(2)①实验室盛放氢氧化钠溶液的试剂瓶采用橡胶塞的原因是:_______ (用化学方程式表示)。
②熔化烧碱应选用的坩埚为_______ (填字母)。
A.铁坩埚 B.玻璃坩埚 C.石英坩埚 D.瓷坩埚
(3)工业废气中往往含有 、
、 、NO、CO等气态非金属化合物,对环境影响很大。采用如下流程处理工业废气(主要含
、NO、CO等气态非金属化合物,对环境影响很大。采用如下流程处理工业废气(主要含 、
、 、NO、CO,不考虑其他成分),在减少污染的同时可充分利用资源:
、NO、CO,不考虑其他成分),在减少污染的同时可充分利用资源:_______ (填化学式)。
②工业废气中的 可以和具有臭鸡蛋气味的气体发生氧化还原反应,其中还原剂和氧化剂的物质的量之比为
可以和具有臭鸡蛋气味的气体发生氧化还原反应,其中还原剂和氧化剂的物质的量之比为_______ 。
③适量空气的作用是_______ 。
④吸收剂吸收的气体是_______ (填化学式),在汽车排气管安装催化转化装置,可使该气体和NO相互作用生成两种无污染气体,反应的化学方程式为_______ 。
(1)硅酸盐材料是传统无机非金属材料,硅酸盐具有特殊的性质与应用。下列产品属于硅酸盐的是
①玻璃②陶瓷③水晶④硅芯片⑤光导纤维⑥水泥⑦砖瓦
(2)①实验室盛放氢氧化钠溶液的试剂瓶采用橡胶塞的原因是:
②熔化烧碱应选用的坩埚为
A.铁坩埚 B.玻璃坩埚 C.石英坩埚 D.瓷坩埚
(3)工业废气中往往含有
 、
、 、NO、CO等气态非金属化合物,对环境影响很大。采用如下流程处理工业废气(主要含
、NO、CO等气态非金属化合物,对环境影响很大。采用如下流程处理工业废气(主要含 、
、 、NO、CO,不考虑其他成分),在减少污染的同时可充分利用资源:
、NO、CO,不考虑其他成分),在减少污染的同时可充分利用资源: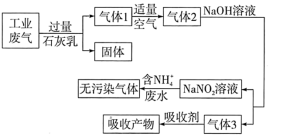
②工业废气中的
 可以和具有臭鸡蛋气味的气体发生氧化还原反应,其中还原剂和氧化剂的物质的量之比为
可以和具有臭鸡蛋气味的气体发生氧化还原反应,其中还原剂和氧化剂的物质的量之比为③适量空气的作用是
④吸收剂吸收的气体是
您最近一年使用:0次
名校
10 . 某同学设计如图实验方案,从海带中提取 。下列说法正确的是
。下列说法正确的是
 。下列说法正确的是
。下列说法正确的是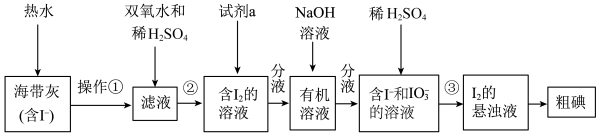
| A.操作①是萃取 |
| B.②中双氧水作还原剂 |
C.③的离子方程式是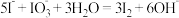 |
D.含 的溶液经3步转化为 的溶液经3步转化为 的悬浊液,其目的是富集,便于分离提纯 的悬浊液,其目的是富集,便于分离提纯 |
您最近一年使用:0次



