24. 碱式硫酸铁[Fe(OH)SO
4]是一种用于污水处理的新型高效絮凝剂。工业上利用废铁屑(含少量氧化铝、氧化铁等)生产碱式硫酸铁的工艺流程如图:
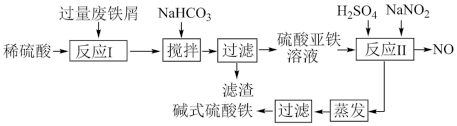
已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见表:
| 沉淀物 | Fe(OH)2 | Al(OH)3 |
| 开始沉淀 | 7.5 | 3.4 |
| 完全沉淀 | 9.7 | 4.4 |
回答下列问题:
(1)加入少量NaHCO
3调节pH在4.4~7.5内,得到的滤渣成分为
___________,写出滤渣中电解质的电离方程式
___________;实验室进行过滤操作时需用到的玻璃仪器有漏斗、烧杯和
___________ 。
(2)反应Ⅱ中加入NaNO
2的目的是氧化亚铁离子,写出亚铁离子是否完全被氧化的检验方法
___________,在实际生产中,反应Ⅱ常同时通入O
2以减少NaNO
2的用量,若参与反应的O
2有11.2L(标准状况),则相当于节约NaNO
2的物质的量为
___________ mol。
(3)碱式硫酸铁溶于水后生成的Fe(OH)
2+可部分水解生成Fe
2(OH)

聚合离子,该水解反应的离子方程式为
___________。
为测定含Fe
2+和Fe
3+溶液中铁元素的总含量,实验操作如下:
准确量取20.00 mL溶液于带塞锥形瓶中,加入足量H
2O
2,调节pH<2,加热除去过量H
2O
2;加入过量KI充分反应后,再用 0.1000 mol·L
-1 Na
2S
2O
3标准溶液滴定至终点,消耗标准溶液20.00 mL。
已知:2Fe
3++2I
- → 2Fe
2++I
2 2S
2O

+I
2 → 2I
-+S
4O

(4)则溶液中铁元素的总含量为
___________g·L
-1.若滴定前溶液中H
2O
2没有除尽,所测定的铁元素的含量将会
___________(填“偏高”“偏低”或“不变”)。