名校
1 . 下列实验操作能达到实验目的的是
| 实验操作 |
|
|
| 实验目的 | A.验证Cl2与FeCl2发生氧化还原反应 | B.NH4Cl和 制氨气 制氨气 |
| 实验操作 |
|
|
| 实验目的 | C.灼烧 失水制Fe2O3 失水制Fe2O3 | D.蒸馏分离苯(沸点:80℃)和硝基苯(沸点:210℃) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
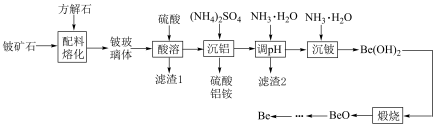
2 . Be是重要的战略性金属,其性质与铝相似。以铍矿石、方解石为原料制备铍的工艺流程如图所示: (氧化物形式为
(氧化物形式为 ),还含有Fe2O3(忽略其他元素对工艺流程的影响);方解石的主要成分为CaCO3;铍玻璃体的主要成分为CaAl2Si2O8、CaBe3SiO6,Fe2O3、SiO2;
),还含有Fe2O3(忽略其他元素对工艺流程的影响);方解石的主要成分为CaCO3;铍玻璃体的主要成分为CaAl2Si2O8、CaBe3SiO6,Fe2O3、SiO2;
②硫酸铝铵微溶于水;常温下,相关物质溶度积如下表所示:
回答下列问题:
(1)提高“配料熔化”时的反应速率及效率的措施为___________ (任写一条),该过程中主要反应的化学方程式为___________ 。
(2)“酸溶”时CaBe3SiO6发生反应的离子方程式为___________ 。
(3)常温下,“调pH”时所得滤液的pH为5,则“滤渣2”的成分为___________ (填化学式,下同)。该工业流程中可循环使用的物质为___________ 。
(4)常温时调节pH为7.5进行“沉铍”,通过计算判断 是否完全沉淀:
是否完全沉淀:___________ (溶液中离子浓度低于 时认为该离子完全沉淀);“沉铍”时不选用NaOH溶液的原因为
时认为该离子完全沉淀);“沉铍”时不选用NaOH溶液的原因为___________ (用离子方程式解释)。
(5)先将原料BeO与碳质还原剂压制成团块,再在高温下将其氯化为BeCl2,然后用镍坩埚为阴极,石墨棒为阳极,将等量的BeCl2与氯化钠混合熔融后进行电解,在___________ (填“阴”或“阳”)极上析出固态金属铍,该法的缺点为___________ 。
 (氧化物形式为
(氧化物形式为 ),还含有Fe2O3(忽略其他元素对工艺流程的影响);方解石的主要成分为CaCO3;铍玻璃体的主要成分为CaAl2Si2O8、CaBe3SiO6,Fe2O3、SiO2;
),还含有Fe2O3(忽略其他元素对工艺流程的影响);方解石的主要成分为CaCO3;铍玻璃体的主要成分为CaAl2Si2O8、CaBe3SiO6,Fe2O3、SiO2;②硫酸铝铵微溶于水;常温下,相关物质溶度积如下表所示:
| 难溶物 |  |  |  |
 | 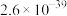 | 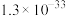 |  |
(1)提高“配料熔化”时的反应速率及效率的措施为
(2)“酸溶”时CaBe3SiO6发生反应的离子方程式为
(3)常温下,“调pH”时所得滤液的pH为5,则“滤渣2”的成分为
(4)常温时调节pH为7.5进行“沉铍”,通过计算判断
 是否完全沉淀:
是否完全沉淀: 时认为该离子完全沉淀);“沉铍”时不选用NaOH溶液的原因为
时认为该离子完全沉淀);“沉铍”时不选用NaOH溶液的原因为(5)先将原料BeO与碳质还原剂压制成团块,再在高温下将其氯化为BeCl2,然后用镍坩埚为阴极,石墨棒为阳极,将等量的BeCl2与氯化钠混合熔融后进行电解,在
您最近一年使用:0次
名校
3 . 已知由钛渣制取 (沸点:136℃)的反应为
(沸点:136℃)的反应为 。下列说法正确的是
。下列说法正确的是
 (沸点:136℃)的反应为
(沸点:136℃)的反应为 。下列说法正确的是
。下列说法正确的是A. 的电子式为: 的电子式为: | B. 、CO、 、CO、 均为非极性分子 均为非极性分子 |
C.反应中 是氧化剂、C和 是氧化剂、C和 是还原剂 是还原剂 | D. 是分子晶体 是分子晶体 |
您最近一年使用:0次
解题方法
4 . 某大学研究团队推出一种新型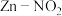 电池。该电池能有效地捕获
电池。该电池能有效地捕获 ,将其转化为
,将其转化为 ,再将产生的
,再将产生的 电解制氨,过程如图所示。下列说法正确的是
电解制氨,过程如图所示。下列说法正确的是
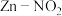 电池。该电池能有效地捕获
电池。该电池能有效地捕获 ,将其转化为
,将其转化为 ,再将产生的
,再将产生的 电解制氨,过程如图所示。下列说法正确的是
电解制氨,过程如图所示。下列说法正确的是
A. 电极的电势比 电极的电势比 电极的电势高 电极的电势高 |
B. 的空间结构为平面三角形 的空间结构为平面三角形 |
C. 极的电极反应为 极的电极反应为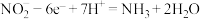 |
D.电路中转移0.2mol 时,理论上能得到1.12L 时,理论上能得到1.12L |
您最近一年使用:0次
解题方法
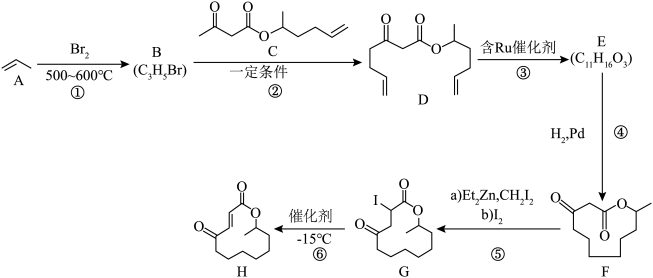
5 . 化合物H是某种药物的重要成分,其合成路线如图:
回答下列问题:
(1)有机物A的名称为___________ 。
(2)D中含氧官能团的名称为___________ 。
(3)④的反应类型为___________ 。
(4)已知②为取代反应,则B的结构简式为___________ 。
(5)写出反应③的化学方程式:___________ 。
(6)芳香族化合物K与E互为同分异构体,写出一种满足下列条件的K的结构简式:___________ 。
i.苯环上含有4个取代基,其中有3个取代基相同;
ii.能与 溶液发生显色反应;
溶液发生显色反应;
iii.核磁共振氢谱有5组峰且峰面积之比为9:2:2:2:1。
(7)上述流程中的E、F、G、H4种分子中,手性碳原子数最多的是___________ (填标号)。

回答下列问题:
(1)有机物A的名称为
(2)D中含氧官能团的名称为
(3)④的反应类型为
(4)已知②为取代反应,则B的结构简式为
(5)写出反应③的化学方程式:
(6)芳香族化合物K与E互为同分异构体,写出一种满足下列条件的K的结构简式:
i.苯环上含有4个取代基,其中有3个取代基相同;
ii.能与
 溶液发生显色反应;
溶液发生显色反应;iii.核磁共振氢谱有5组峰且峰面积之比为9:2:2:2:1。
(7)上述流程中的E、F、G、H4种分子中,手性碳原子数最多的是
您最近一年使用:0次
6 . 稀土元素是国家战略资源,目前我国稀土提炼技术处于世界领先地位。某课题组以含铈废渣(含较多的 、
、 、
、 及少量其他可溶于酸的物质)为原料,设计如图流程回收稀土元素铈,实现资源再利用。
及少量其他可溶于酸的物质)为原料,设计如图流程回收稀土元素铈,实现资源再利用。 不溶于稀硫酸,也不溶于
不溶于稀硫酸,也不溶于 溶液。
溶液。
回答下列问题:
(1)为提高“酸溶”的速率,实验室常用图示仪器进行固体物质的粉碎,该仪器的名称是___________ 。___________ ;“反应1”的离子方程式为___________ ,其中 的作用是
的作用是___________ 。
(3)“反应2”的离子方程式为___________ 。
(4)“滤液1”经一系列反应与操作可制得硫酸铁铵,硫酸铁铵可用作净水剂,其净水原理是___________ (用离子方程式表示)。
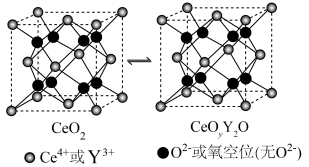
(5)氧化铈( )常用作玻璃工业添加剂,在其立方晶胞中掺杂
)常用作玻璃工业添加剂,在其立方晶胞中掺杂 ,
, 占据原来
占据原来 的位置,可以得到更稳定的结构,这种稳定的结构使得氧化铈具有许多独特的性质和应用,
的位置,可以得到更稳定的结构,这种稳定的结构使得氧化铈具有许多独特的性质和应用, 晶胞中
晶胞中 与最近
与最近 的核间距为
的核间距为 。已知:
。已知: 。
。 晶胞中与
晶胞中与 最近的
最近的 的个数为
的个数为___________ 。
②若掺杂 后得到:
后得到: 的晶体,则此晶体中
的晶体,则此晶体中 的空缺率为
的空缺率为___________ 。
③ 晶体的密度为
晶体的密度为___________ (列出表达式) 。
。
 、
、 、
、 及少量其他可溶于酸的物质)为原料,设计如图流程回收稀土元素铈,实现资源再利用。
及少量其他可溶于酸的物质)为原料,设计如图流程回收稀土元素铈,实现资源再利用。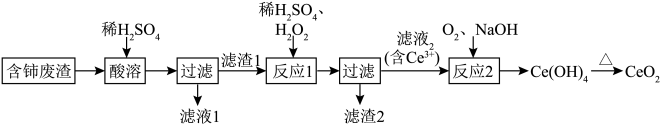
 不溶于稀硫酸,也不溶于
不溶于稀硫酸,也不溶于 溶液。
溶液。回答下列问题:
(1)为提高“酸溶”的速率,实验室常用图示仪器进行固体物质的粉碎,该仪器的名称是
 的作用是
的作用是(3)“反应2”的离子方程式为
(4)“滤液1”经一系列反应与操作可制得硫酸铁铵,硫酸铁铵可用作净水剂,其净水原理是
(5)氧化铈(
 )常用作玻璃工业添加剂,在其立方晶胞中掺杂
)常用作玻璃工业添加剂,在其立方晶胞中掺杂 ,
, 占据原来
占据原来 的位置,可以得到更稳定的结构,这种稳定的结构使得氧化铈具有许多独特的性质和应用,
的位置,可以得到更稳定的结构,这种稳定的结构使得氧化铈具有许多独特的性质和应用, 晶胞中
晶胞中 与最近
与最近 的核间距为
的核间距为 。已知:
。已知: 。
。
 晶胞中与
晶胞中与 最近的
最近的 的个数为
的个数为②若掺杂
 后得到:
后得到: 的晶体,则此晶体中
的晶体,则此晶体中 的空缺率为
的空缺率为③
 晶体的密度为
晶体的密度为 。
。
您最近一年使用:0次
7 . 橄榄石型 是一种潜在的锂离子电池正极材料,它可以通过
是一种潜在的锂离子电池正极材料,它可以通过 ,
, 与
与 溶液发生共沉淀反应制得,反应方程式为
溶液发生共沉淀反应制得,反应方程式为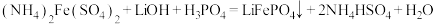 。下列说法正确的是
。下列说法正确的是
 是一种潜在的锂离子电池正极材料,它可以通过
是一种潜在的锂离子电池正极材料,它可以通过 ,
, 与
与 溶液发生共沉淀反应制得,反应方程式为
溶液发生共沉淀反应制得,反应方程式为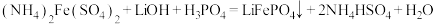 。下列说法正确的是
。下列说法正确的是A. 的空间填充模型: 的空间填充模型: |
B. 键角: 键角: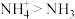 |
C.基态 原子的价层电子轨道表示式: 原子的价层电子轨道表示式: |
D.用电子式表示 的形成过程: 的形成过程: |
您最近一年使用:0次
8 . 某研究小组制备配合物顺式一二甘氨酸合铜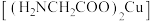 并测定所得产品中铜的含量。回答下列问题:
并测定所得产品中铜的含量。回答下列问题:
I.制备
如图所示,向装有 溶液的三颈烧瓶中滴加氨水,先出现蓝色沉淀,后蓝色沉淀消失,溶液变为深蓝色。再加入过量的
溶液的三颈烧瓶中滴加氨水,先出现蓝色沉淀,后蓝色沉淀消失,溶液变为深蓝色。再加入过量的 溶液,过滤,洗涤,干燥。
溶液,过滤,洗涤,干燥。 原子的价层电子排布式为
原子的价层电子排布式为___________ 。
(2)写出过量的氨水和硫酸铜溶液反应的离子方程式:___________ 。
Ⅱ.制备顺式一二甘氨酸合铜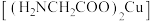
将制得的 固体置于烧杯中,加入甘氨酸,水浴加热至65~70℃,搅拌,充分反应后趁热过滤,往滤液中加入10mL95%的乙醇溶液,冷却结晶,过滤、洗涤、干燥,得产品。
固体置于烧杯中,加入甘氨酸,水浴加热至65~70℃,搅拌,充分反应后趁热过滤,往滤液中加入10mL95%的乙醇溶液,冷却结晶,过滤、洗涤、干燥,得产品。
(3)写出 与甘氨酸反应的化学方程式:
与甘氨酸反应的化学方程式:___________ 。
(4)下列说法中正确的是___________(填标号)。
a.实验I中不用 溶液直接与
溶液直接与 反应的原因可能是防止生成碱式硫酸铜沉淀
反应的原因可能是防止生成碱式硫酸铜沉淀
b.实验Ⅱ中,趁热过滤的目的是除去 的同时减少产物的析出
的同时减少产物的析出
c.加入95%的乙醇溶液能增大溶剂极性,促进顺式一二甘氨酸合铜析出
Ⅲ.产品中 元素含量的测定
元素含量的测定
实验流程如下:
A.用分析天平称量产品 ,配制成100mL样品溶液;
,配制成100mL样品溶液;
B.用移液管移取20.00mL溶液到碘量瓶中,加入过量 固体,在暗处静置5分钟,用标准
固体,在暗处静置5分钟,用标准 溶液滴定至溶液呈浅黄色,加入适量
溶液滴定至溶液呈浅黄色,加入适量 溶液,剧烈振荡碘量瓶,加入淀粉溶液,用标准
溶液,剧烈振荡碘量瓶,加入淀粉溶液,用标准 溶液滴定至终点;再取20.00mL溶液进行一次平行实验。
溶液滴定至终点;再取20.00mL溶液进行一次平行实验。
已知:i. ,
,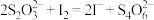 ;
;
ii. 固体能吸附溶液中的少量碘单质;
固体能吸附溶液中的少量碘单质;
iii. 。
。
(5)①溶解产品时,需加入硫酸,其作用是___________ 。
②滴定终点的现象是___________ 。
③若两次平行实验,平均消耗
 溶液20.00mL,则
溶液20.00mL,则 产品中含
产品中含 的质量为
的质量为___________ g。
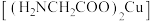 并测定所得产品中铜的含量。回答下列问题:
并测定所得产品中铜的含量。回答下列问题:I.制备

如图所示,向装有
 溶液的三颈烧瓶中滴加氨水,先出现蓝色沉淀,后蓝色沉淀消失,溶液变为深蓝色。再加入过量的
溶液的三颈烧瓶中滴加氨水,先出现蓝色沉淀,后蓝色沉淀消失,溶液变为深蓝色。再加入过量的 溶液,过滤,洗涤,干燥。
溶液,过滤,洗涤,干燥。
 原子的价层电子排布式为
原子的价层电子排布式为(2)写出过量的氨水和硫酸铜溶液反应的离子方程式:
Ⅱ.制备顺式一二甘氨酸合铜
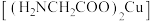
将制得的
 固体置于烧杯中,加入甘氨酸,水浴加热至65~70℃,搅拌,充分反应后趁热过滤,往滤液中加入10mL95%的乙醇溶液,冷却结晶,过滤、洗涤、干燥,得产品。
固体置于烧杯中,加入甘氨酸,水浴加热至65~70℃,搅拌,充分反应后趁热过滤,往滤液中加入10mL95%的乙醇溶液,冷却结晶,过滤、洗涤、干燥,得产品。(3)写出
 与甘氨酸反应的化学方程式:
与甘氨酸反应的化学方程式:(4)下列说法中正确的是___________(填标号)。
a.实验I中不用
 溶液直接与
溶液直接与 反应的原因可能是防止生成碱式硫酸铜沉淀
反应的原因可能是防止生成碱式硫酸铜沉淀b.实验Ⅱ中,趁热过滤的目的是除去
 的同时减少产物的析出
的同时减少产物的析出c.加入95%的乙醇溶液能增大溶剂极性,促进顺式一二甘氨酸合铜析出
Ⅲ.产品中
 元素含量的测定
元素含量的测定实验流程如下:
A.用分析天平称量产品
 ,配制成100mL样品溶液;
,配制成100mL样品溶液;B.用移液管移取20.00mL溶液到碘量瓶中,加入过量
 固体,在暗处静置5分钟,用标准
固体,在暗处静置5分钟,用标准 溶液滴定至溶液呈浅黄色,加入适量
溶液滴定至溶液呈浅黄色,加入适量 溶液,剧烈振荡碘量瓶,加入淀粉溶液,用标准
溶液,剧烈振荡碘量瓶,加入淀粉溶液,用标准 溶液滴定至终点;再取20.00mL溶液进行一次平行实验。
溶液滴定至终点;再取20.00mL溶液进行一次平行实验。已知:i.
 ,
,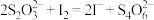 ;
;ii.
 固体能吸附溶液中的少量碘单质;
固体能吸附溶液中的少量碘单质;iii.
 。
。(5)①溶解产品时,需加入硫酸,其作用是
②滴定终点的现象是
③若两次平行实验,平均消耗

 溶液20.00mL,则
溶液20.00mL,则 产品中含
产品中含 的质量为
的质量为
您最近一年使用:0次
9 . 有机物M(结构如图所示)是制备酪氨酸酶过程中常见的副产物,下列说法错误的是

| A.有机物M含有三种含氧官能团 |
B.1molM可与5mol 发生反应 发生反应 |
| C.有机物M能发生取代、加成和氧化反应 |
D.该有机物既能与金属 反应生成气体,又能与 反应生成气体,又能与 反应生成气体 反应生成气体 |
您最近一年使用:0次
10 . 由实验操作和现象,能得出相应结论的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向等体积的水中分别通入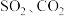 至饱和,再用 至饱和,再用 计测定两种溶液的 计测定两种溶液的 | 通 后所得溶液的 后所得溶液的 更小 更小 | 碳酸的酸性比亚硫酸弱 |
| B | 溴乙烷与 的乙醇溶液共热,将产生的气体直接通入酸性高锰酸钾溶液中 的乙醇溶液共热,将产生的气体直接通入酸性高锰酸钾溶液中 | 溶液紫红色褪去 | 反应有乙烯生成 |
| C | 向试管中加入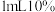 蔗糖溶液,再加入过量 蔗糖溶液,再加入过量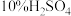 溶液后加热煮沸。经冷却后加入新制备的 溶液后加热煮沸。经冷却后加入新制备的 并加热 并加热 | 没有砖红色沉淀产生 | 蔗糖不属于还原糖 |
| D | 向盛有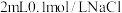 溶液的试管中滴加2滴 溶液的试管中滴加2滴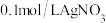 溶液、振荡后再向中滴加4滴 溶液、振荡后再向中滴加4滴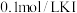 溶液 溶液 | 先出现白色沉淀,后出现黄色沉淀 | 相同温度下 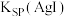 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次