解题方法
1 . 二甘氨酸合锌是常用的补锌药品,化学式为 ,针状白色晶体,可溶于水。制备过程如下:
,针状白色晶体,可溶于水。制备过程如下:
I.称取3.00 g 固体溶于25 mL水,滴加氨水产生大量白色沉淀,过滤,洗涤。
固体溶于25 mL水,滴加氨水产生大量白色沉淀,过滤,洗涤。
II.称取1.50 g甘氨酸,溶于40 mL水形成甘氨酸溶液,搅拌下用甘氨酸溶液溶解I中的白色沉淀。
III.过滤,转移液体于烧杯中。经一系列操作后,过滤、洗涤、干燥,得到针状白色晶体1.92 g。
请回答下列问题:
(1)①步骤I中所使用的玻璃仪器除烧杯、量筒外,还有___________ 。
②步骤I中若氨水过量较多、浓度较大,产率会明显降低,原因是___________ 。
③步骤I中洗涤除去的离子是___________ 。
(2)步骤II中发生的化学方程式为___________ 。
(3)步骤III中“一系列操作”是指___________ 、___________ 。
(4)产率为___________ 。
(5)直接法制备二甘氨酸合锌的方法是:用硫酸锌与甘氨酸直接反应,经实验步骤III得到晶体。本实验方法与直接法相比较,优点与缺点分别为___________ 、___________ 。
 ,针状白色晶体,可溶于水。制备过程如下:
,针状白色晶体,可溶于水。制备过程如下:I.称取3.00 g
 固体溶于25 mL水,滴加氨水产生大量白色沉淀,过滤,洗涤。
固体溶于25 mL水,滴加氨水产生大量白色沉淀,过滤,洗涤。II.称取1.50 g甘氨酸,溶于40 mL水形成甘氨酸溶液,搅拌下用甘氨酸溶液溶解I中的白色沉淀。
III.过滤,转移液体于烧杯中。经一系列操作后,过滤、洗涤、干燥,得到针状白色晶体1.92 g。
请回答下列问题:
(1)①步骤I中所使用的玻璃仪器除烧杯、量筒外,还有
②步骤I中若氨水过量较多、浓度较大,产率会明显降低,原因是
③步骤I中洗涤除去的离子是
(2)步骤II中发生的化学方程式为
(3)步骤III中“一系列操作”是指
(4)产率为
(5)直接法制备二甘氨酸合锌的方法是:用硫酸锌与甘氨酸直接反应,经实验步骤III得到晶体。本实验方法与直接法相比较,优点与缺点分别为
您最近一年使用:0次
解题方法
2 . 江西富含稀有金属铝,钼具有优异的物理化学性能,在冶金、农业、环保和航天等领域有着广泛应用。工业上以钼精矿(主要成分为 ,杂质有
,杂质有 、
、 、
、 和
和 等元素)制备四钼酸铵的流程如下:
等元素)制备四钼酸铵的流程如下:
(1)气体A化学式为___________ ,气体B的分子空间构型是___________ ,基态氧原子的最外层轨道表示式为___________ 。
(2)碱浸时把 转化成
转化成 ,其离子方程式为
,其离子方程式为___________ 。
(3)工业上探究了碱浸中钼浸出率与蒸发温度的关系,如下图所示:___________ 。
②80℃以后,蒸发温度上升,钼浸出率迅速下降,主要原因为___________ 。
(4)碱浸后的滤液中仍然有部分铜、锌和低价钼金属存在,净化时依次加入适量 、
、 溶液,其作用分别是
溶液,其作用分别是___________ 、___________ 。
(5)酸沉时主要发生的离子方程式为___________ 。
 ,杂质有
,杂质有 、
、 、
、 和
和 等元素)制备四钼酸铵的流程如下:
等元素)制备四钼酸铵的流程如下:
(1)气体A化学式为
(2)碱浸时把
 转化成
转化成 ,其离子方程式为
,其离子方程式为(3)工业上探究了碱浸中钼浸出率与蒸发温度的关系,如下图所示:

②80℃以后,蒸发温度上升,钼浸出率迅速下降,主要原因为
(4)碱浸后的滤液中仍然有部分铜、锌和低价钼金属存在,净化时依次加入适量
 、
、 溶液,其作用分别是
溶液,其作用分别是(5)酸沉时主要发生的离子方程式为
您最近一年使用:0次
3 . 水系锌离子可充电电池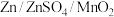 ,电解质中含有少量
,电解质中含有少量 。放电时总反应为:
。放电时总反应为: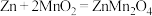 。下列说法正确的是
。下列说法正确的是
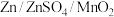 ,电解质中含有少量
,电解质中含有少量 。放电时总反应为:
。放电时总反应为: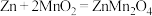 。下列说法正确的是
。下列说法正确的是| A.充、放电时锌离子浓度减小或增大 |
B. 可以抑制正极材料溶解 可以抑制正极材料溶解 |
C.放电时,正极反应: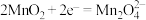 |
| D.充电时,锌离子移向电池的正极 |
您最近一年使用:0次
解题方法
4 . 离子液体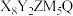 ,X、Y、Z、M、Q是原子序数依次增大且不同主族的短周期元素,其中Y、Z、M同周期。基态未成对电子有如下关系:
,X、Y、Z、M、Q是原子序数依次增大且不同主族的短周期元素,其中Y、Z、M同周期。基态未成对电子有如下关系: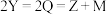 。下列说法正确的是
。下列说法正确的是
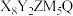 ,X、Y、Z、M、Q是原子序数依次增大且不同主族的短周期元素,其中Y、Z、M同周期。基态未成对电子有如下关系:
,X、Y、Z、M、Q是原子序数依次增大且不同主族的短周期元素,其中Y、Z、M同周期。基态未成对电子有如下关系: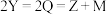 。下列说法正确的是
。下列说法正确的是| A.Y为元素 | B.Z为氨元素 |
| C.M为氧元素 | D.该离子液体正负离子均为二价离子 |
您最近一年使用:0次
5 . 液态硝基甲烷(化学式 )可溶于水,
)可溶于水,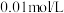 的硝基甲烷溶液
的硝基甲烷溶液 ,能使紫色石蕊试液显红色。在水中存在互变异构反应(
,能使紫色石蕊试液显红色。在水中存在互变异构反应( 很小):
很小):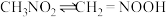 。下列说法错误的是
。下列说法错误的是
 )可溶于水,
)可溶于水,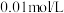 的硝基甲烷溶液
的硝基甲烷溶液 ,能使紫色石蕊试液显红色。在水中存在互变异构反应(
,能使紫色石蕊试液显红色。在水中存在互变异构反应( 很小):
很小):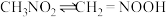 。下列说法错误的是
。下列说法错误的是A.硝基甲烷的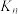 约为 约为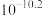 | B.滴入少量 溶液,互变异构反应不移动 溶液,互变异构反应不移动 |
| C.二硝基甲烷酸性强于硝基甲烷 | D.液态硝基甲烷可以作炸药 |
您最近一年使用:0次
解题方法
6 . 金雀花碱可以用于烟草置换治疗,其结构式为:

A.金雀花碱分子式为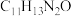 | B.金雀花碱具有芳香性 |
C.金雀花碱分子中碳原子均为 杂化 杂化 | D.金雀花碱能与盐酸反应生成盐 |
您最近一年使用:0次
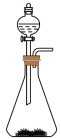
7 . 实验室使用下图装置作为气体发生装置,能达到实验目的的是
| 选项 | 气体发生装置 | 锥形瓶所盛物质 | 分液漏斗所盛物质 | 实验目的 |
| A |
| 亚硫酸钠 | 稀硝酸 | 制备 |
| B | 熟石灰 | 氯化铵固体 | 制备 | |
| C | 高锰酸钾固体 | 浓盐酸 | 制备 | |
| D | 碳酸钙 | 硫酸 | 制备 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
8 . 某实验室测定并计算了在136~180℃范围内下列反应的平衡常数 :
:
①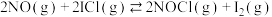

②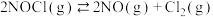
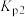
得到 和
和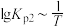 均为线性关系,如下图所示,有关下列说法错误的是
均为线性关系,如下图所示,有关下列说法错误的是
 :
:①
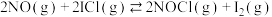

②
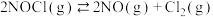
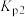
得到
 和
和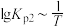 均为线性关系,如下图所示,有关下列说法错误的是
均为线性关系,如下图所示,有关下列说法错误的是
| A.反应②高温下可自发进行 |
B.反应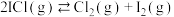 的 的 |
| C.升温,反应体系中分子总数会增大 |
| D.当混合气体颜色不变时,说明反应①和②已达平衡状态 |
您最近一年使用:0次
2024-06-03更新
|
243次组卷
|
3卷引用:江西省新八校2024届高三下学期第二次联考(二模)化学试题
名校
9 . 酸性条件下,砷酸具有较强氧化性,能被正四价硫、碘离子等还原为正三价砷。某工厂以废渣(主要含 )制备砷的流程如下:
)制备砷的流程如下:
(1)砷的原子结构示意图为_______ 。 的结构简式为
的结构简式为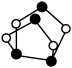 ,0.5mol
,0.5mol  所含有S-S键的物质的量为
所含有S-S键的物质的量为_______ mol。
(2)“碱浸”后溶液中含有 、
、 ,则该工序主反应的化学方程式为
,则该工序主反应的化学方程式为______________ 。
(3)“沉砷”时,加入试剂A的作用为_______ ;结合必要的化学用语说明为了提高 的产率,加石灰乳时控制温度45℃~85℃的目的是
的产率,加石灰乳时控制温度45℃~85℃的目的是_______ 。
(4)滤渣1含硫酸钙和沉淀a,实验室里,用_______ 试剂除去试管壁上的沉淀a。
(5)加热时“再还原”的化学方程式为_______ 。“还原”中,氧化产物与还原产物的物质的量之比为_______ 。
(6)该流程中可以循环使用的物质为_______ 。
(7)设计实验检验“还原”后的溶液中是否存在正五价砷元素_______ 。
 )制备砷的流程如下:
)制备砷的流程如下: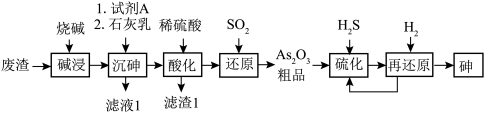
(1)砷的原子结构示意图为
 的结构简式为
的结构简式为 ,0.5mol
,0.5mol  所含有S-S键的物质的量为
所含有S-S键的物质的量为(2)“碱浸”后溶液中含有
 、
、 ,则该工序主反应的化学方程式为
,则该工序主反应的化学方程式为(3)“沉砷”时,加入试剂A的作用为
 的产率,加石灰乳时控制温度45℃~85℃的目的是
的产率,加石灰乳时控制温度45℃~85℃的目的是(4)滤渣1含硫酸钙和沉淀a,实验室里,用
(5)加热时“再还原”的化学方程式为
(6)该流程中可以循环使用的物质为
(7)设计实验检验“还原”后的溶液中是否存在正五价砷元素
您最近一年使用:0次
2024-06-03更新
|
92次组卷
|
2卷引用:2024年江西省宜春市第一中学高三下学期第三次模拟考试化学试卷
名校
10 . 常温下,向含有 和
和 的悬浊液中滴加弱酸HC,溶液中pM[
的悬浊液中滴加弱酸HC,溶液中pM[ ,M代表
,M代表 、
、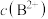 、
、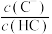 ]与pH的关系如下图所示,下列说法正确的是
]与pH的关系如下图所示,下列说法正确的是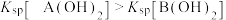
 和
和 的悬浊液中滴加弱酸HC,溶液中pM[
的悬浊液中滴加弱酸HC,溶液中pM[ ,M代表
,M代表 、
、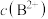 、
、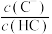 ]与pH的关系如下图所示,下列说法正确的是
]与pH的关系如下图所示,下列说法正确的是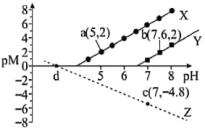
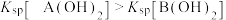
A.X、Y、Z分别表示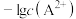 、 、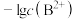 、 、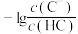 与pH的关系 与pH的关系 |
B. ;d点坐标为 ;d点坐标为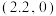 |
C. 和 和 均能完全溶解于足量的HC中 均能完全溶解于足量的HC中 |
D.向 悬浊液中加入足量的 悬浊液中加入足量的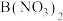 , , 可完全转化为 可完全转化为 |
您最近一年使用:0次
2024-06-03更新
|
129次组卷
|
2卷引用:2024年江西省宜春市第一中学高三下学期第三次模拟考试化学试卷