1 . 按要求回答下列问题:
(1)已知下列物质电离平衡常数
①次氯酸的电离方程式为___________ 。
②物质的量浓度相同的HF、CH3COOH、H2CO3、HClO中,酸性由小到大的顺序为___________ 。
③下列实验事实不能证明醋酸是弱酸的是___________ 。
A.相同pH的醋酸溶液和盐酸分别与同样颗粒大小的锌反应时,产生H2的起始速率相等
B.常温下,测得0.1mol·L-1醋酸溶液的pH=4
C.常温下,将pH=1的醋酸溶液稀释1000倍,测得pH<4
D.在相同条件下,同浓度醋酸溶液的导电性比盐酸的弱
(2)高温下H2O可以分解成分子或原子。
①若在相同温度下,1molH2O按下列两种途径转化成氢原子与氧原子。则△H1、△H2、△H3三者之间的关系是___________ 。
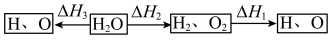
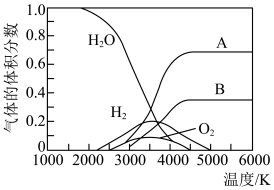
②高温下水分解体系中主要气体的体积分数与温度的关系如图所示。图中A表示的物质(或微粒)是___________ 。等物质的量的A、H2相比,化学能较低的物质是___________ 。
(1)已知下列物质电离平衡常数
| 化学式 | HF |  |  |  |
| 电离平衡常数 | 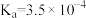 |  | 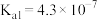  | 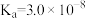 |
②物质的量浓度相同的HF、CH3COOH、H2CO3、HClO中,酸性由小到大的顺序为
③下列实验事实不能证明醋酸是弱酸的是
A.相同pH的醋酸溶液和盐酸分别与同样颗粒大小的锌反应时,产生H2的起始速率相等
B.常温下,测得0.1mol·L-1醋酸溶液的pH=4
C.常温下,将pH=1的醋酸溶液稀释1000倍,测得pH<4
D.在相同条件下,同浓度醋酸溶液的导电性比盐酸的弱
(2)高温下H2O可以分解成分子或原子。
①若在相同温度下,1molH2O按下列两种途径转化成氢原子与氧原子。则△H1、△H2、△H3三者之间的关系是
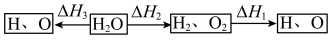
②高温下水分解体系中主要气体的体积分数与温度的关系如图所示。图中A表示的物质(或微粒)是

您最近一年使用:0次
2 . 回答下列问题:
(1)在298K、100Kpa时,已知:
2H2O(g)=2H2(g)+O2(g) △H1
Cl2(g)+H2(g)=2HCl(g) △H2
2Cl2(g)+2H2O(g)=4HCl(g)+O2(g) △H3=___________ (用△H1和△H2表示)。
(2)在一定体积的密闭容器中,进行如下化学反应: ,其化学平衡常数K和温度t的关系如表所示:
,其化学平衡常数K和温度t的关系如表所示:
①该反应的化学平衡常数表达式为K=___________ 。
②该反应为___________ (填“吸热”或“放热)反应。
③某温度下平衡浓度符合下式: ,试判断此时的温度为
,试判断此时的温度为______ ℃。
④在800℃时,发生上述反应,某一时刻测得容器内各物质的浓度分别为 ,
, ,
, ,
, ,则下一时刻,反应向
,则下一时刻,反应向___________ (填“正向”、“逆向”或“平衡”)进行。
(3)已知常温时红磷比白磷稳定,比较下列反应中 的大小:
的大小:
___________  (填“>”或“<”)。
(填“>”或“<”)。
①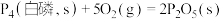

②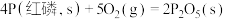

(1)在298K、100Kpa时,已知:
2H2O(g)=2H2(g)+O2(g) △H1
Cl2(g)+H2(g)=2HCl(g) △H2
2Cl2(g)+2H2O(g)=4HCl(g)+O2(g) △H3=
(2)在一定体积的密闭容器中,进行如下化学反应:
 ,其化学平衡常数K和温度t的关系如表所示:
,其化学平衡常数K和温度t的关系如表所示:| t/℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
②该反应为
③某温度下平衡浓度符合下式:
 ,试判断此时的温度为
,试判断此时的温度为④在800℃时,发生上述反应,某一时刻测得容器内各物质的浓度分别为
 ,
, ,
, ,
, ,则下一时刻,反应向
,则下一时刻,反应向(3)已知常温时红磷比白磷稳定,比较下列反应中
 的大小:
的大小:
 (填“>”或“<”)。
(填“>”或“<”)。①
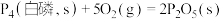

②
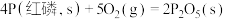

您最近一年使用:0次
名校
3 . 化学有自己独特的语言。下列化学用语表达正确的是
A.水溶液中, 的电离方程式: 的电离方程式: |
B.水溶液中, 的电离方程式: 的电离方程式: |
C.用单线桥表示电子转移过程: |
D.钠的原子结构示意图: |
您最近一年使用:0次
2023-12-08更新
|
185次组卷
|
2卷引用:新疆伊犁州霍城县江苏中学2023-2024学年高一上学期12月 化学试题
名校
解题方法
4 . 下列实验操作、现象和结论都正确的是
| 选项 | 操作 | 现象 | 结论 |
| A | 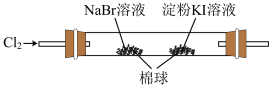 | 左边棉球变为橙色,右边棉球变为蓝色 | 氧化性: |
| B | 向 溶液中加入一小块钠 溶液中加入一小块钠 | 产生无色气泡,溶液底部有蓝色沉淀生成 | 水溶液中 不能置换铜 不能置换铜 |
| C | 向某溶液中加入盐酸产生无色气体,将该气体通入澄清石灰水 | 澄清石灰水变浑浊 | 该溶液中一定含有 或 或 |
| D | 干燥的氯气依次通过干燥有色布条、湿润有色布条 | 干燥有色布条不褪色、湿润有色布条褪色 | 证明 具有漂白性 具有漂白性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-12-04更新
|
193次组卷
|
3卷引用:新疆伊犁州霍城县江苏中学2023-2024学年高一上学期12月 化学试题
5 . 电化学是化学研究重要分支,在生产生活中发挥着非常重要的作用。请回答下列问题:
铅酸蓄电池是最常见的二次电池,电压稳定,安全可靠,价格低廉,应用广泛。电池总反应为 。
。
(1)放电时,正极的电极反应式:______ ,电解质溶液中硫酸的浓度______ (填“增大”“减小”或“不变”),当外电路通过1mol 时,理论上负极板的质量增加
时,理论上负极板的质量增加______ g。
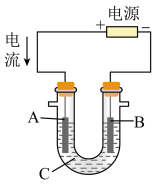
(2)用该蓄电池作电源,进行粗铜(含Ag、Pt、Au等杂质)的电解精炼。
如下图所示,电解液c选用______ 溶液,A电极的材料是______ ,B电极反应式是______ 。
铅酸蓄电池是最常见的二次电池,电压稳定,安全可靠,价格低廉,应用广泛。电池总反应为
 。
。(1)放电时,正极的电极反应式:
 时,理论上负极板的质量增加
时,理论上负极板的质量增加(2)用该蓄电池作电源,进行粗铜(含Ag、Pt、Au等杂质)的电解精炼。
如下图所示,电解液c选用

您最近一年使用:0次
2023-12-04更新
|
72次组卷
|
2卷引用:新疆伊犁州霍城县江苏中学2023-2024学年高二上学期12月月考化学试题
名校
解题方法
6 . 填空题
Ⅰ.在室温下,下列五种溶液:
①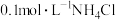 溶液 ②pH=a的
溶液 ②pH=a的 溶液 ③
溶液 ③ 溶液
溶液
请根据要求填写下列空白:
(1)比较溶液①、③中 的大小关系是①
的大小关系是①___________ ③(填“>”“<”或“=”)。
(2)溶液②稀释100倍后所得溶液pH___________ a+2(填“>”或“<”或“=”)。
(3)用离子方程式表示①溶液显酸性的原因___________ 。
Ⅱ.在水的电离平衡中, 和
和 的关系如图所示:
的关系如图所示:
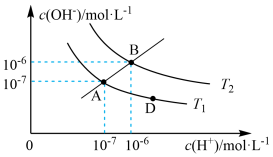
(4)下列说法正确的是___________ (填字母)。
a.图中A、B、D三点处 的大小关系:B>A=D
的大小关系:B>A=D
b.在 温度下,向水中加入少量的NaOH可实现由A点向D点移动
温度下,向水中加入少量的NaOH可实现由A点向D点移动
c.AB线上任意点的溶液均呈中性
d.图中温度
(5)在 温度下,浓度为的
温度下,浓度为的 的
的 溶液中由水电离的
溶液中由水电离的
___________ mol/L。
(6)保持 温度不变,将pH=2的
温度不变,将pH=2的 溶液
溶液 与pH=11的KOH溶液
与pH=11的KOH溶液 混合后溶液pH=6(忽略混合时溶液体积变化),则
混合后溶液pH=6(忽略混合时溶液体积变化),则
___________ 。
Ⅰ.在室温下,下列五种溶液:
①
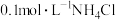 溶液 ②pH=a的
溶液 ②pH=a的 溶液 ③
溶液 ③ 溶液
溶液请根据要求填写下列空白:
(1)比较溶液①、③中
 的大小关系是①
的大小关系是①(2)溶液②稀释100倍后所得溶液pH
(3)用离子方程式表示①溶液显酸性的原因
Ⅱ.在水的电离平衡中,
 和
和 的关系如图所示:
的关系如图所示:
(4)下列说法正确的是
a.图中A、B、D三点处
 的大小关系:B>A=D
的大小关系:B>A=Db.在
 温度下,向水中加入少量的NaOH可实现由A点向D点移动
温度下,向水中加入少量的NaOH可实现由A点向D点移动c.AB线上任意点的溶液均呈中性
d.图中温度

(5)在
 温度下,浓度为的
温度下,浓度为的 的
的 溶液中由水电离的
溶液中由水电离的
(6)保持
 温度不变,将pH=2的
温度不变,将pH=2的 溶液
溶液 与pH=11的KOH溶液
与pH=11的KOH溶液 混合后溶液pH=6(忽略混合时溶液体积变化),则
混合后溶液pH=6(忽略混合时溶液体积变化),则
您最近一年使用:0次
2023-12-03更新
|
113次组卷
|
2卷引用:新疆伊犁州霍城县江苏中学2023-2024学年高二上学期12月月考化学试题
名校
7 . 以CH3OH燃料电池为电源电解法制取ClO2,二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂。
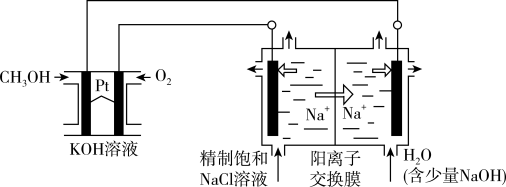
(1)CH3OH燃料电池放电过程中,通入O2的电极附近溶液的pH___________ (填“增大减小”或“不变”),负极反应式为。________________ 。
(2)图中电解池用石墨作电极,在一定条件下电解饱和食盐水制取ClO2,阳极产生ClO2的反应式为_______________ 。
(3)电解一段时间,从阴极处收集到的气体比阳极处收集到的气体多6.72L时(标准状况,忽略生成的气体溶解),停止电解,通过阳离子交换膜的阳离子为___________ mol。

(1)CH3OH燃料电池放电过程中,通入O2的电极附近溶液的pH
(2)图中电解池用石墨作电极,在一定条件下电解饱和食盐水制取ClO2,阳极产生ClO2的反应式为
(3)电解一段时间,从阴极处收集到的气体比阳极处收集到的气体多6.72L时(标准状况,忽略生成的气体溶解),停止电解,通过阳离子交换膜的阳离子为
您最近一年使用:0次
2023-12-02更新
|
98次组卷
|
2卷引用:新疆伊犁州霍城县江苏中学2023-2024学年高二上学期12月月考化学试题
10-11高二上·江西新余·期中
名校
解题方法
8 . 常温下,pH=13的强碱溶液与pH=2的强酸溶液混合,所得混合液的pH=11,则强碱与强酸的体积比是
| A.1:9 | B.9:1 | C.1:11 | D.11:1 |
您最近一年使用:0次
2023-12-02更新
|
231次组卷
|
90卷引用:新疆新源县第二中学2019-2020学年高二上学期期末考试化学试题
新疆新源县第二中学2019-2020学年高二上学期期末考试化学试题(已下线)2010年江西省新余一中高二上学期期中考试化学卷(已下线)2010年河南省周口市高二上学期期中考试化学卷(已下线)2011年河南省卫辉市第一中学高二1月月考化学试卷(已下线)2010—2011学年浙江省杭州学军中学高二下学期期中考试化学试卷(已下线)2010-2011学年云南省昆明一中高二下学期期中考试化学试卷(已下线)2011-2012年山西省太原五中高二上学期期中考试化学(理)试卷(已下线)2011-2012学年内蒙古巴彦淖尔市中学高二期中考试化学试卷(已下线)2011-2012学年黑龙江龙东地区高二第一学期高中教学联合体期末考试化学试卷(已下线)2011-2012学年陕西省宝鸡中学高二下学期期中考试化学试题(已下线)2011-2012学年天津市蓟县一中高二第三次月考化学试卷(已下线)2012-2013学年黑龙江省哈三中高二上学期期中考试化学试卷(已下线)2012年鲁科版高中化学选修4 3.1水溶液卷练习卷(已下线)2012年苏教版高中化学选修4 3.2溶液的酸碱性练习卷(已下线)2012-2013学年云南省昆明三中、滇池中学高二下学期期末考试化学卷(已下线)2013-2014学年福建省福州市八县高二上学期期末考试化学试卷(已下线)2013-2014学年安徽省宿州市高二上学期期末考试化学试卷2014-2015学年湖北省长阳县第一高级中学高二上学期期中化学试卷2014-2015学年重庆复旦中学高二上学期期中化学试卷2014-2015甘肃省兰州一中高二上学期期末化学试卷2014-2015四川省重点中学高二下学期期中考试化学试卷2014-2015学年北京市房山区周口店中学高二下期中考试化学试卷2015-2016学年河北省冀州中学高二上第二次月考化学试卷2015-2016学年广东省揭阳一中高二上第二次段考化学试卷2015-2016学年福建晨曦、冷曦、正曦、岐滨四校高二上联考化学卷2015-2016学年内蒙古巴彦淖尔一中高二上期中化学试卷2015-2016学年西藏日喀则高级中学高二上期末化学试卷2015-2016学年四川省彭州中学高二下2月月考化学试卷2015-2016学年吉林省延边二中高二上期末化学试卷2015-2016学年内蒙古巴彦淖尔一中高二普通班上期中化学试卷2015-2016学年青海省平安一中高二下期末化学试卷2016-2017学年辽宁省沈阳铁路中学高二上第一次月考化学试卷2016-2017学年河北省秦皇岛北戴河中学高二上月考化学试卷2016-2017学年河北省涿鹿县涿鹿中学高二上调研三化学卷黑龙江省牡丹江市第一高级中学2017-2018学年高二10月月考(理)化学试题黑龙江省大庆实验中学2017-2018学年高二10月月考化学试题河南省商丘市九校2017-2018学年高二上学期期中联考化学试题山西省吕梁市临县第一中学2017-2018学年高二上学期期中考试化学试题湖北省武汉2017-2018学年高二化学上学期期末考试题吉林省辽源市田家炳高级中学等五校2017-2018学年高二上学期期末联考化学试题黑龙江省哈尔滨市第六中学2017-2018学年高二3月月考化学试题山东省济南市历城第二中学2017-2018学年高二下学期开学考试化学试题四川省棠湖中学2017-2018学年高二下学期第一次月考理综化学试题辽宁省实验中学2017-2018学年高二上学期期中考试化学试题河南省鹤壁市淇县第一中学2018-2019学年高二上学期第一次月考化学试题【全国百强校】黑龙江省哈尔滨市第六中学2018-2019学年高二上学期10月月考化学试题安徽省阜阳三中2018-2019学年高二第一学期第一次调研考试化学试题湖南省邵东县第十中学2018-2019学年高二上学期期中考试理科班化学试题高二人教版选修4 第三章 第二节 水的电离和溶液的酸碱性吉林省汪清县第六中学2019-2020学年高二上学期期中考试化学试题陕西省咸阳百灵中学2019-2020学年高二上学期第二次月考化学(理)试题甘肃省张掖市山丹县第一中学2017—2018学年高二上学期期末质量检测化学试题辽宁省实验中学东戴河分校2019-2020学年高二12月月考化学试题甘肃省古浪县第二中学2019-2020学年高二12月基础知识竞赛化学试题河北省沧州市沧县风化店中学2019-2020学年高二上学期期末考试化学试题新疆博尔塔拉蒙古自治州第五师高级中学2019-2020学年高二上学期第二次月考化学试题重庆市凤鸣山中学2018-2019学年高二上学期期中考试化学试题河北省沧州市河间市第四中学2019-2020学年高二下学期期末模拟考试化学试卷宁夏银川市宁夏大学附属中学2019-2020学年高二下期第二次月考化学试题重庆市万州第二高级中学2020-2021学年高二上学期10月月考化学试题江苏省南通市2020-2021学年高二上学期期中考试化学试题鲁科版(2019)高二选择性必修第一册第3章 物质在水溶液中的行为 第1节 水与水溶液 课时2 溶液的酸碱性与pH湖南省临澧县第一中学2020-2021学年高二上学期期中考试化学试题(选考)山西省长治市第二中学校2020-2021学年高二上学期期中考试化学试题重庆市万州第三中学2020-2021学年高二上学期期中考试化学试题安徽省六安市裕安区新安中学2020-2021学年高二上学期期中考试化学试题吉林省白山市抚松县第五中学2020-2021学年高二上学期期中考试化学试题四川省广安市北京师范大学广安实验学校2020-2021学年高二上学期12月考试化学试题北京东城区2019-2020学年高二下学期期中考试化学试题北京市首都师范大学附属中学2021-2022学年高二上学期期中考试化学试题(已下线)第2讲 水的电离及溶液PH-【微专题·大素养】备战2022年高考化学核心突破(水溶液中的离子反应与平衡)吉林省汪清县第六中学2021-2022学年高二上学期期中考试化学试题天津市外国语大学附属外国语学校2021-2022学年高二上学期期中阶段性检测化学试题宁夏青铜峡市高级中学2021-2022学年高二上学期期中考试化学试题黑龙江省哈尔滨市第九中学校2021-2022学年高二上学期期中学业阶段性评价考试化学(理)试题湖南省长沙市南雅中学2018-2019学年高二上学期期中考试化学试题宁夏青铜峡市高级中学2021-2022学年高二上学期11月测试化学试题黑龙江省哈尔滨市宾县第二中学2021-2022学年高二上学期期末考试化学试题黑龙江省哈尔滨市阿城区第一中学2022-2023学年高二上学期第一次月考化学试题辽宁省重点高中沈阳市郊联体2022-2023学年高二上学期期中考试化学试题辽宁省沈阳市辽中区第二高级中学2022-2023学年高二上学期期中考试化学试题山西省晋中市平遥县第二中学校2021-2022学年高二上学期期中考试化学试题广东省连平县忠信中学2020-2021学年高二下学期第二次段考化学试题宁夏贺兰县景博中学2022-2023学年高二上学期第二次月考化学试题重庆市为明学校2022-2023学年高二上学期期末检测化学试题北京首都师范大学附属中学2023-2024学年高二上学期10月月考化学试题云南省昆明市第一中学2023-2024学年高二上学期期中化学试题陕西省/渭南市蒲城县尧山中学2023-2024学年高二上学期第三次月考化学试题上海市进才中学2023-2024学年高一下学期期中考试化学试卷(等级)安徽省马鞍山市第二中学2023-2024学年高二上学期期末检测化学试题
名校
9 . 若将浓盐酸滴入烧瓶中进行如图(a、c、d均为浸有相应试液的棉花)所示的探究实验,下列分析正确的是


| A.装置A中的KMnO4可用MnO2代替 |
| B.b处红色鲜花瓣褪色,说明Cl2具有漂白性 |
| C.d处淀粉—KI溶液与Cl2反应的离子方程式为:2I- + Cl2 = I2 + 2Cl- |
| D.含有0.001molCl2的尾气进入C装置时,最多消耗0.001molNaOH |
您最近一年使用:0次
2023-11-26更新
|
132次组卷
|
2卷引用:新疆伊犁州霍城县江苏中学2023-2024学年高一上学期12月 化学试题
24-25高一上·全国·假期作业
名校
解题方法
10 . 据报道,某核潜艇上的核反应堆内使用了液体铝钠合金(单质钠和单质铝熔合而成)作载热介质。下列有关说法中不正确的是
| A.铝钠合金是混合物 |
B.若将适量铝钠合金投入一定量水中得到无色澄清溶液,则合金中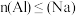 |
C.若将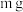 组成不同的铝钠合金分别投入足量盐酸中,放出 组成不同的铝钠合金分别投入足量盐酸中,放出 越多,则合金中铝的质量分数越小 越多,则合金中铝的质量分数越小 |
| D.将铝钠合金投入足量氯化铜溶液中,一定有氢氧化铜沉淀析出,可能有铜析出 |
您最近一年使用:0次
2023-11-25更新
|
149次组卷
|
4卷引用:新疆伊犁州霍城县江苏中学2023-2024学年高一上学期12月 化学试题



