名校
1 . 下列实验装置或操作能达到实验目的的是
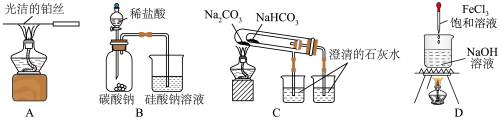
| A.用图A装置观察KCl的焰色试验现象 |
| B.用图B装置证明非金属性强弱:Cl>C>Si |
C.用图C装置比较 和 和 的热稳定性 的热稳定性 |
| D.用图D装置制备氢氧化铁胶体 |
您最近一年使用:0次
名校
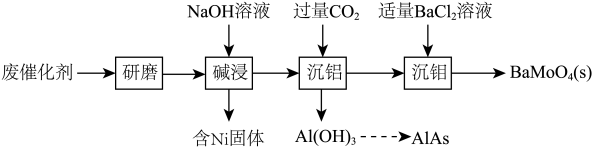
2 . 一种回收利用某废催化剂[主要含铝(Al)、钼(Mo)、镍(Ni)等元素的氧化物]中Al、Mo的工艺流程如下:
(1)“研磨”的目的是_______ 。
(2)“碱浸”中,有 生成,其中Mo元素的化合价为
生成,其中Mo元素的化合价为_______ 。
(3)“沉铝”中,发生反应的离子方程式为_______ 。“沉钼”中,发生反应的离子方程式为_______ 。
(4)“沉钼”后所得滤液中主要存在的钠盐有NaCl和Y,Y受热分解可制得纯碱,Y为______ 。
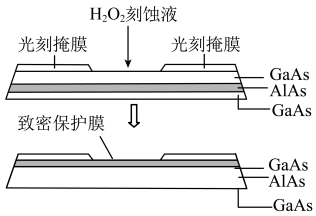
(5)高纯AIAs(砷化铝)可用于芯片制造。芯片制造中的一种刻蚀过程如图所示。 与上层GaAs的反应中,As元素的化合价变为+5价,则该反应的氧化剂与还原剂物质的量之比为
与上层GaAs的反应中,As元素的化合价变为+5价,则该反应的氧化剂与还原剂物质的量之比为_______ 。
②图中所示致密保护膜为一种氧化物,可阻止 刻蚀液与下层GaAs反应,该氧化物为
刻蚀液与下层GaAs反应,该氧化物为_____ 。
(1)“研磨”的目的是
(2)“碱浸”中,有
 生成,其中Mo元素的化合价为
生成,其中Mo元素的化合价为(3)“沉铝”中,发生反应的离子方程式为
(4)“沉钼”后所得滤液中主要存在的钠盐有NaCl和Y,Y受热分解可制得纯碱,Y为
(5)高纯AIAs(砷化铝)可用于芯片制造。芯片制造中的一种刻蚀过程如图所示。
 与上层GaAs的反应中,As元素的化合价变为+5价,则该反应的氧化剂与还原剂物质的量之比为
与上层GaAs的反应中,As元素的化合价变为+5价,则该反应的氧化剂与还原剂物质的量之比为②图中所示致密保护膜为一种氧化物,可阻止
 刻蚀液与下层GaAs反应,该氧化物为
刻蚀液与下层GaAs反应,该氧化物为
您最近一年使用:0次
名校
解题方法
3 . 水处理:水是身体的重要组成部分,具有重要的生理功能。河流湖泊水是人类用水的主要来源,但使用前需要经过净化处理。
(1)常见的水处理剂包括氯气、臭氧、漂白粉、活性炭等,游泳场馆常用臭氧、活性炭对游泳池进行消毒和净化。下列说法错误的是_______。
(2)明矾溶于水可以得到 胶体,明矾能用于净水的原因是胶体具有
胶体,明矾能用于净水的原因是胶体具有_______ 。现将此法制得的 胶体装入半透膜内,将此半透膜袋浸入盛蒸馏水的烧杯中,设计实验证明
胶体装入半透膜内,将此半透膜袋浸入盛蒸馏水的烧杯中,设计实验证明 能够透过半透膜:
能够透过半透膜:_______ 。
(3)亚氯酸钠( )是一种高效的漂白剂和消毒剂,它在酸性条件下生成NaCl并放出
)是一种高效的漂白剂和消毒剂,它在酸性条件下生成NaCl并放出 ,
, 有类似
有类似 的性质。某兴趣小组探究亚氯酸钠的制备。
的性质。某兴趣小组探究亚氯酸钠的制备。
①关闭止水夹②,打开止水夹①,从进气口通入足量 ,充分反应。仪器a的名称为
,充分反应。仪器a的名称为_______ ,仪器b的作用是_______ 。
②装置A中生成 的化学方程式为
的化学方程式为_______ ,B中的现象为_______ 。
③若从装置A反应后的溶液中获得 晶体,则主要操作有:减压蒸发浓缩、
晶体,则主要操作有:减压蒸发浓缩、_______ 、过滤、洗涤、干燥等。
(1)常见的水处理剂包括氯气、臭氧、漂白粉、活性炭等,游泳场馆常用臭氧、活性炭对游泳池进行消毒和净化。下列说法错误的是_______。
| A.臭氧、活性炭处理水的原理不同 |
| B.用氯气消毒后的水,可用于配制各种化学试剂 |
| C.用漂白粉漂白时,向其中滴入浓盐酸或通入二氧化碳可以增强漂白效果 |
| D.漂白粉长期露置在空气中会失效 |
(2)明矾溶于水可以得到
 胶体,明矾能用于净水的原因是胶体具有
胶体,明矾能用于净水的原因是胶体具有 胶体装入半透膜内,将此半透膜袋浸入盛蒸馏水的烧杯中,设计实验证明
胶体装入半透膜内,将此半透膜袋浸入盛蒸馏水的烧杯中,设计实验证明 能够透过半透膜:
能够透过半透膜:(3)亚氯酸钠(
 )是一种高效的漂白剂和消毒剂,它在酸性条件下生成NaCl并放出
)是一种高效的漂白剂和消毒剂,它在酸性条件下生成NaCl并放出 ,
, 有类似
有类似 的性质。某兴趣小组探究亚氯酸钠的制备。
的性质。某兴趣小组探究亚氯酸钠的制备。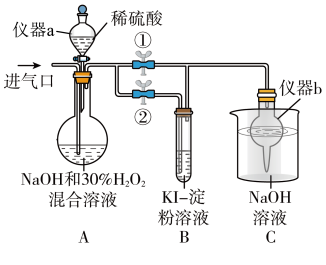
①关闭止水夹②,打开止水夹①,从进气口通入足量
 ,充分反应。仪器a的名称为
,充分反应。仪器a的名称为②装置A中生成
 的化学方程式为
的化学方程式为③若从装置A反应后的溶液中获得
 晶体,则主要操作有:减压蒸发浓缩、
晶体,则主要操作有:减压蒸发浓缩、
您最近一年使用:0次
解题方法
4 . 以 为原料制备甲烷、氢气等能源物质具有较好的发展前景。
为原料制备甲烷、氢气等能源物质具有较好的发展前景。
(1) 和
和 联合催化重整能减少温室气体的排放。其主要反应如下:
联合催化重整能减少温室气体的排放。其主要反应如下:
Ⅰ.

Ⅱ.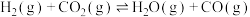
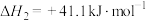
Ⅲ.

①
___________ 。
②其他条件相同,投料比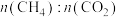 为1∶1.3时,不同温度下
为1∶1.3时,不同温度下 和
和 的转化率及
的转化率及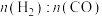 变化如图1。
变化如图1。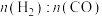 始终低于1.0的原因是
始终低于1.0的原因是___________________ 。 分解形成C的反应历程如图2所示。该历程分
分解形成C的反应历程如图2所示。该历程分________ 步进行,其中第__________ 步的正反应活化能最大。 和12mol
和12mol  ,在催化剂表面发生
,在催化剂表面发生 催化重整制
催化重整制 的主反应
的主反应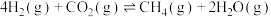 ,同时有副反应
,同时有副反应
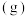 发生。初始压强为p,20min时反应都达到平衡状态,测得
发生。初始压强为p,20min时反应都达到平衡状态,测得 ,体系压强为
,体系压强为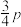 。
。
①0~20min内
_______  ,平衡时
,平衡时 选择性=
选择性=___________ (保留三位有效数字)。( 选择性
选择性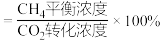 )
)
②副反应的平衡常数
__________ 。(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
③催化剂上的反应过程如图3所示。其他条件不变时, 的转化率和
的转化率和 的选择性随温度变化如图4所示。
的选择性随温度变化如图4所示。 催化加氢制
催化加氢制 的最适合温度为
的最适合温度为_________ ,除提高反应速率外,该催化剂的最大优点是____________ 。
 为原料制备甲烷、氢气等能源物质具有较好的发展前景。
为原料制备甲烷、氢气等能源物质具有较好的发展前景。(1)
 和
和 联合催化重整能减少温室气体的排放。其主要反应如下:
联合催化重整能减少温室气体的排放。其主要反应如下:Ⅰ.


Ⅱ.
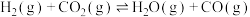
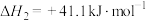
Ⅲ.


①

②其他条件相同,投料比
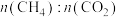 为1∶1.3时,不同温度下
为1∶1.3时,不同温度下 和
和 的转化率及
的转化率及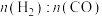 变化如图1。
变化如图1。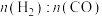 始终低于1.0的原因是
始终低于1.0的原因是
 分解形成C的反应历程如图2所示。该历程分
分解形成C的反应历程如图2所示。该历程分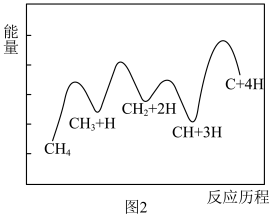
 和12mol
和12mol  ,在催化剂表面发生
,在催化剂表面发生 催化重整制
催化重整制 的主反应
的主反应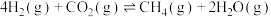 ,同时有副反应
,同时有副反应
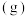 发生。初始压强为p,20min时反应都达到平衡状态,测得
发生。初始压强为p,20min时反应都达到平衡状态,测得 ,体系压强为
,体系压强为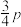 。
。①0~20min内

 ,平衡时
,平衡时 选择性=
选择性= 选择性
选择性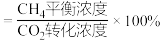 )
)②副反应的平衡常数

③催化剂上的反应过程如图3所示。其他条件不变时,
 的转化率和
的转化率和 的选择性随温度变化如图4所示。
的选择性随温度变化如图4所示。 催化加氢制
催化加氢制 的最适合温度为
的最适合温度为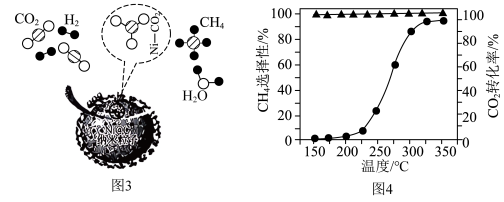
您最近一年使用:0次
5 . 某品牌净水器净水原理如图所示,当接通电源打开开关时,发现装自来水的烧杯中一电极附近迅速出现大量气泡,同时有绿色和红褐色浑浊物产生,而装纯净水的烧杯中没有任何变化。已知:常温下三种水样的电导率数据如表。
下列说法中正确的是

水样 | 自来水 | 蒸馏水 | 纯净水 |
电导率( | 639 | 44 | 2.2 |
| A.两烧杯中Al片作阳极,Fe片作阴极 |
| B.纯净水中加入食盐不会出现同样的产生浑浊和气泡的现象 |
C.自来水中出现的浑浊物可能含有 |
| D.如果水质电解器的电极都换成石墨电极,一定会出现同样的现象 |
您最近一年使用:0次
6 . 萤石的主要成分为 ,常用于冶金、化工和建材三大行业。
,常用于冶金、化工和建材三大行业。 的立方晶胞及坐标如图所示,其晶胞参数为
的立方晶胞及坐标如图所示,其晶胞参数为 ,用
,用 表示阿伏加德罗常数的值,下列说法正确的是
表示阿伏加德罗常数的值,下列说法正确的是
 ,常用于冶金、化工和建材三大行业。
,常用于冶金、化工和建材三大行业。 的立方晶胞及坐标如图所示,其晶胞参数为
的立方晶胞及坐标如图所示,其晶胞参数为 ,用
,用 表示阿伏加德罗常数的值,下列说法正确的是
表示阿伏加德罗常数的值,下列说法正确的是
| A.基态钙原子的核外电子共有20种空间运动状态 |
B. 晶体中 晶体中 的配位数为4 的配位数为4 |
C.B点F-的原子分数坐标为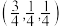 |
D. 晶体的密度为 晶体的密度为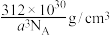 |
您最近一年使用:0次
名校
解题方法
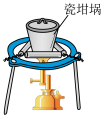
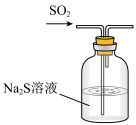
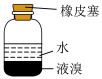
7 . 下列装置能达到实验目的的是
|
|
|
|
| A.熔化Na2CO3 | B.验证SO2氧化性 | C.实验室制CO2 | D.实验室保存液溴 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-06-05更新
|
387次组卷
|
4卷引用:广西壮族自治区贵港市2024届高三下学期收网考化学试题
广西壮族自治区贵港市2024届高三下学期收网考化学试题2024届浙江省金华市义乌市高三下学期三模化学试题(已下线)湖南师大附中2024届高三下学期第三次模拟考试化学试题黑龙江省大庆市实验中学实验二部2023-2024学年高三下学期阶段考试(二)化学试题
8 . 制备 (S呈+2价)的化学方程式为
(S呈+2价)的化学方程式为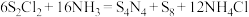 。下列说法正确的是
。下列说法正确的是
 (S呈+2价)的化学方程式为
(S呈+2价)的化学方程式为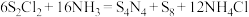 。下列说法正确的是
。下列说法正确的是A.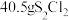 参与反应,转移电子的数目为 参与反应,转移电子的数目为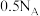 |
B.25℃、101kPa条件下,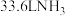 的分子数为 的分子数为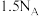 |
C.由 ( (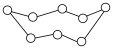 )与 )与 ( ( )组成的混合物中所含共价键的数目为 )组成的混合物中所含共价键的数目为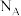 |
D.常温下,1LpH为5的 溶液中,由水电离出的 溶液中,由水电离出的 数目为 数目为 |
您最近一年使用:0次
2024-06-04更新
|
213次组卷
|
3卷引用:广西壮族自治区贵港市2024届高三下学期收网考化学试题
名校
解题方法
9 . 中国旅美教授JingjieWu及其学生利用石墨烯量子点为催化剂,将CO2转化为燃料甲烷,空间站基于该反应将宇航员呼出的CO2转化为火箭燃料。将5molCO2和20molH2通入某密闭容器中,发生如下反应:
 .
.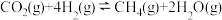
 H=-165kJ·mol-1 (主反应)
H=-165kJ·mol-1 (主反应)
 .
.
 H=+41kJ·mol-1 (副反应)
H=+41kJ·mol-1 (副反应)
平衡时容器中含碳元素物质的物质的量[n(X)]随温度(T)的变化如图甲、乙、丙曲线所示。
 .
.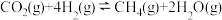
 H=-165kJ·mol-1 (主反应)
H=-165kJ·mol-1 (主反应) .
.
 H=+41kJ·mol-1 (副反应)
H=+41kJ·mol-1 (副反应)平衡时容器中含碳元素物质的物质的量[n(X)]随温度(T)的变化如图甲、乙、丙曲线所示。

| A.空间站中使CO2转化为CH4的反应不宜采用高温 |
| B.曲线甲、乙、丙分别表示CO2、CH4、CO |
| C.高于1050K时,曲线丙逐渐下降的原因是以反应Ⅱ为主 |
| D.800K时,反应达到平衡时水的物质的量为7.8mol |
您最近一年使用:0次
名校
10 . 研究碳、氮、硫元素化合物的性质及其相互转化对建设生态文明、美丽中国具有重要意义。请回答下列问题:
(1)已知I-可以催化二氧化硫在水溶液中发生歧化反应:3SO2(g) +2H2O(l)=2H2SO4(aq) +S(s) H<0。催化原理分为两步:
H<0。催化原理分为两步:
第一步:SO2+4I- +4H+ =2H2O+ S↓ +2I2 H>0 慢反应
H>0 慢反应
第二步:2H2O + I2 + ___________=___________+___________+ 2I- H<0 快反应
H<0 快反应
①请完整写出第二步反应的离子方程式___________ 。
②能正确表示I-催化SO2歧化反应原理的能量变化示意图为___________ 。
反应i:CO2(g)+3H2(g) CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)  H1= - 49.1kJ•mol-1
H1= - 49.1kJ•mol-1
反应ii:CO2(g)+H2(g) CO(g)+H2O(g)
CO(g)+H2O(g)  H2= + 41.1kJ•mol-1
H2= + 41.1kJ•mol-1
①往恒容密闭容器中按n(CO2)∶n(H2)=1∶3充入4mol反应物,在合适催化剂作用下,CO2的平衡转化率和甲醇的选择性[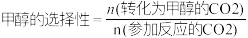 ]如图所示。在513K达平衡时,甲醇的物质的量为
]如图所示。在513K达平衡时,甲醇的物质的量为___________ mol。随着温度的升高,ABC所在曲线逐减升高的原因是___________ 。___________ MPa-2(分压=总压×物质的量分数,列出计算式即可)。
(3)一种电解氧化法吸收NO的原理如图所示:从A口中出来的物质是较浓的硫酸和___________ ;写出电解池阴极的电极反应式___________ 。
(1)已知I-可以催化二氧化硫在水溶液中发生歧化反应:3SO2(g) +2H2O(l)=2H2SO4(aq) +S(s)
 H<0。催化原理分为两步:
H<0。催化原理分为两步:第一步:SO2+4I- +4H+ =2H2O+ S↓ +2I2
 H>0 慢反应
H>0 慢反应第二步:2H2O + I2 + ___________=___________+___________+ 2I-
 H<0 快反应
H<0 快反应①请完整写出第二步反应的离子方程式
②能正确表示I-催化SO2歧化反应原理的能量变化示意图为

反应i:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)  H1= - 49.1kJ•mol-1
H1= - 49.1kJ•mol-1反应ii:CO2(g)+H2(g)
 CO(g)+H2O(g)
CO(g)+H2O(g)  H2= + 41.1kJ•mol-1
H2= + 41.1kJ•mol-1①往恒容密闭容器中按n(CO2)∶n(H2)=1∶3充入4mol反应物,在合适催化剂作用下,CO2的平衡转化率和甲醇的选择性[
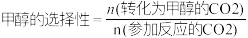 ]如图所示。在513K达平衡时,甲醇的物质的量为
]如图所示。在513K达平衡时,甲醇的物质的量为
(3)一种电解氧化法吸收NO的原理如图所示:从A口中出来的物质是较浓的硫酸和

您最近一年使用:0次

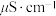 )
)