解题方法
1 . 下列说法错误的是
| A.福尔马林可用于食品保鲜 | B.臭氧可用于自来水消毒 |
| C.明矾可用于净水 | D.高纯硅可用于制芯片 |
您最近一年使用:0次
2 . 高温结构陶瓷氮化硅由石英与焦炭在高温的氮气流中通过以下反应制备: ,下列说法正确的是(
,下列说法正确的是( 为阿伏加德罗常数的值)
为阿伏加德罗常数的值)
 ,下列说法正确的是(
,下列说法正确的是( 为阿伏加德罗常数的值)
为阿伏加德罗常数的值)A.常温常压下, 中氧原子数目为 中氧原子数目为 | B.每消耗 转移的电子数目为 转移的电子数目为 |
C.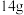 氮化硅中含有 氮化硅中含有 分子数目为 分子数目为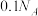 | D. 中含有 中含有 键数目为 键数目为 |
您最近一年使用:0次
名校
解题方法
3 . 某化学兴趣小组用甲、乙两套装置(如图所示)进行丙烯酸( )与乙醇(
)与乙醇( )酯化反应的实验。已知:乙醇的沸点为78.5℃,丙烯酸的沸点为141℃,丙烯酸乙酯的沸点为99.8℃、回答下列问题:
)酯化反应的实验。已知:乙醇的沸点为78.5℃,丙烯酸的沸点为141℃,丙烯酸乙酯的沸点为99.8℃、回答下列问题:_______ ,仪器A、B中的溶液均为_______ 。
(2)甲、乙两套装置中效果比较好的装置是_______ ,原因是_______ 。
(3)乙装置中冷凝水应该从_______ (填“a”或“b”)口进入。
(4)按甲图安装好仪器后,在反应管中加入配制的体积比为3∶2的乙醇和丙烯酸,加热至沸腾,很久也没有果香味液体生成,原因是_______ 。
(5)乙醇需要过量一些的原因是_______ 。
(6)某同学选用了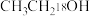 、
、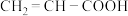 两个反应物,对酯化反应的原理进行探究。请写出该反应的化学方程式:
两个反应物,对酯化反应的原理进行探究。请写出该反应的化学方程式:_______ 。
(7)下列有关有机知识表述正确的是_______ (填字母)。
A.乙烯可以通过加成反应制得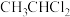
B.等物质的量的甲烷和乙酸完全燃烧时所需 的质量相同
的质量相同
C.乙酸乙酯中含有乙酸杂质,可加入一定量的乙醇和浓硫酸通过酯化反应除去
 )与乙醇(
)与乙醇( )酯化反应的实验。已知:乙醇的沸点为78.5℃,丙烯酸的沸点为141℃,丙烯酸乙酯的沸点为99.8℃、回答下列问题:
)酯化反应的实验。已知:乙醇的沸点为78.5℃,丙烯酸的沸点为141℃,丙烯酸乙酯的沸点为99.8℃、回答下列问题:
(2)甲、乙两套装置中效果比较好的装置是
(3)乙装置中冷凝水应该从
(4)按甲图安装好仪器后,在反应管中加入配制的体积比为3∶2的乙醇和丙烯酸,加热至沸腾,很久也没有果香味液体生成,原因是
(5)乙醇需要过量一些的原因是
(6)某同学选用了
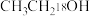 、
、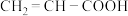 两个反应物,对酯化反应的原理进行探究。请写出该反应的化学方程式:
两个反应物,对酯化反应的原理进行探究。请写出该反应的化学方程式:(7)下列有关有机知识表述正确的是
A.乙烯可以通过加成反应制得
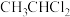
B.等物质的量的甲烷和乙酸完全燃烧时所需
 的质量相同
的质量相同C.乙酸乙酯中含有乙酸杂质,可加入一定量的乙醇和浓硫酸通过酯化反应除去
您最近一年使用:0次
4 . 苯甲酸是一种弱酸,用于制备防腐剂苯甲酸钠,下列说法错误的是
| A.升高温度,苯甲酸钠的水解平衡常数增大 |
B.加少量水稀释苯甲酸钠溶液,溶液的 减小 减小 |
C.常温下, 的苯甲酸溶液中,水电离的 的苯甲酸溶液中,水电离的 为1.0×10-4mol/L 为1.0×10-4mol/L |
D.用 溶液滴定苯甲酸溶液测浓度时,用酚酞作指示剂 溶液滴定苯甲酸溶液测浓度时,用酚酞作指示剂 |
您最近一年使用:0次
5 . 结构决定性质是化学学科的重要观念。下列叙述错误的是
| A.沸点:CH3COOH>HCOOCH3,主要与CH3COOH是极性分子有关 |
| B.MgO的熔点高于NaCl的熔点 |
| C.冠醚识别碱金属离子,与微粒直径有关 |
D.配位能力NH3大于H2O,向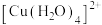 中加过量氨水可生成 中加过量氨水可生成 |
您最近一年使用:0次
解题方法
6 . W、X、Y、Z为短周期主族元素,原子序数依次增大,最外层电子数之和为17.其中,W、Z位于同一主族,X为同周期半径最大的主族元素,Y元素基态原子最高能层中s轨道和p轨道电子数相同。下列说法不正确的是
| A.第一电离能:Z>Y |
| B.Z元素的最高价氧化物的水化物为二元强酸 |
| C.W、Z对应的简单氢化物沸点:W>Z |
| D.W与X形成的化合物均属于离子晶体且化学键类型相同 |
您最近一年使用:0次
解题方法
7 . 以软锰矿(主要成分是MnO2,还含有Fe2O3、SiO2、CuO、CaO等少量杂质)为主要原料制备硫酸锰晶体的工艺流程如图所示,回答下列问题: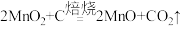 ;
;
② 在酸性条件下比较稳定,pH高于5.5时易被
在酸性条件下比较稳定,pH高于5.5时易被 氧化;
氧化;
③ ,
, ;离子浓度
;离子浓度 时,可认为完全沉淀。
时,可认为完全沉淀。
④ 溶于1份冷水、0.6份沸水,不溶于乙醇;
溶于1份冷水、0.6份沸水,不溶于乙醇;
(1)基态Mn原子的价电子排布式为___________ ,“过滤Ⅰ”得到的滤渣主要成分除了C、Cu、SiC,还有___________ (填化学式)。
(2)“氧化”时发生反应的离子方程式为___________ 。
(3)“调pH”时溶液中 的浓度约为
的浓度约为 ,常温下,调节pH的合理范围是
,常温下,调节pH的合理范围是___________ 。
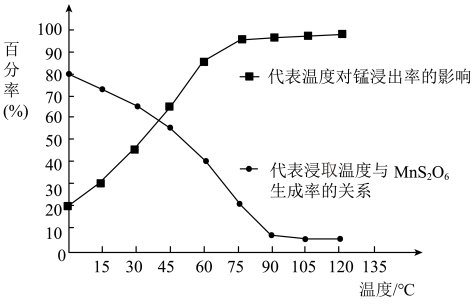
(4)“浸取”时,反应中往往有副产物MnS2O6生成,温度对浸取反应的影响如图所示,为减少MnS2O6的生成,“浸取”的适宜温度是___________ ;向过滤Ⅱ所得的“滤液”中加入NH4HCO3溶液时温度不宜太高的原因是___________ 。___________ 。
(6)获得MnSO4·H2O后常用乙醇洗涤,主要目的是___________ 。
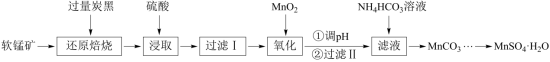
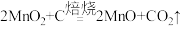 ;
;②
 在酸性条件下比较稳定,pH高于5.5时易被
在酸性条件下比较稳定,pH高于5.5时易被 氧化;
氧化;③
 ,
, ;离子浓度
;离子浓度 时,可认为完全沉淀。
时,可认为完全沉淀。④
 溶于1份冷水、0.6份沸水,不溶于乙醇;
溶于1份冷水、0.6份沸水,不溶于乙醇;(1)基态Mn原子的价电子排布式为
(2)“氧化”时发生反应的离子方程式为
(3)“调pH”时溶液中
 的浓度约为
的浓度约为 ,常温下,调节pH的合理范围是
,常温下,调节pH的合理范围是(4)“浸取”时,反应中往往有副产物MnS2O6生成,温度对浸取反应的影响如图所示,为减少MnS2O6的生成,“浸取”的适宜温度是
(6)获得MnSO4·H2O后常用乙醇洗涤,主要目的是
您最近一年使用:0次
8 . NA为阿伏加德罗常数的值。关于实验室制乙炔反应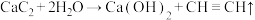 ,下列说法不正确的是
,下列说法不正确的是
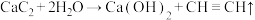 ,下列说法不正确的是
,下列说法不正确的是A. 与OH-所含电子数均为10NA 与OH-所含电子数均为10NA |
| B.26g乙炔分子中含有的π键数目为2NA |
C.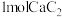 和 和 中含有的阴离子数目均为2NA 中含有的阴离子数目均为2NA |
D.标准状况下,3.36 L  所含氢原子数为0.3NA 所含氢原子数为0.3NA |
您最近一年使用:0次
解题方法
9 .  是重要的供氧剂。图所示装置(省略夹持部件)用于验证
是重要的供氧剂。图所示装置(省略夹持部件)用于验证 和
和 的反应,所需
的反应,所需 由
由 固体与稀盐酸反应制备。回答下列问题:
固体与稀盐酸反应制备。回答下列问题:______ 。
(2)验证装置的气密性时,需用F替换装置中的E。若装置气密性良好,应观察到F中的导管口会有______ 的现象。
(3)装置中的B与C用于除去 气体中的杂质。饱和
气体中的杂质。饱和 溶液的作用是吸收
溶液的作用是吸收______ (填化学式)气体;为了干燥 气体,C中盛放的试剂是足量的
气体,C中盛放的试剂是足量的______ 。
(4)实验过程中,D中部分 固体由淡黄色变为
固体由淡黄色变为______ 色。在E的瓶口放置一条带火星的木条,若木条复燃,则说明生成的气体是______ (填化学式),并且E中的气体______ (填“已集满”或“未集满”)。收集气体时,E的瓶口朝上的主要原因是______ 。
(5)完成上述实验后,除去玻璃纤维,回收D中的所有固体药品共22.76g。使该固体与过量的水充分反应,假定该反应生成的气体共224mL(标准状况)。据此计算,实验中与 反应的
反应的 的物质的量为
的物质的量为______ mol。
 是重要的供氧剂。图所示装置(省略夹持部件)用于验证
是重要的供氧剂。图所示装置(省略夹持部件)用于验证 和
和 的反应,所需
的反应,所需 由
由 固体与稀盐酸反应制备。回答下列问题:
固体与稀盐酸反应制备。回答下列问题:
(2)验证装置的气密性时,需用F替换装置中的E。若装置气密性良好,应观察到F中的导管口会有
(3)装置中的B与C用于除去
 气体中的杂质。饱和
气体中的杂质。饱和 溶液的作用是吸收
溶液的作用是吸收 气体,C中盛放的试剂是足量的
气体,C中盛放的试剂是足量的(4)实验过程中,D中部分
 固体由淡黄色变为
固体由淡黄色变为(5)完成上述实验后,除去玻璃纤维,回收D中的所有固体药品共22.76g。使该固体与过量的水充分反应,假定该反应生成的气体共224mL(标准状况)。据此计算,实验中与
 反应的
反应的 的物质的量为
的物质的量为
您最近一年使用:0次
10 . 下列关于硫及其化合物叙述正确的是
A.空气中排放过量 会形成酸雨,且酸雨的pH会随时间增长而增大 会形成酸雨,且酸雨的pH会随时间增长而增大 |
| B.浓硫酸放置在空气中浓度减小,是因为浓硫酸容易挥发 |
| C.常温下,浓硫酸与铁、铝不反应,所以可用铁、铝质容器盛放浓硫酸 |
| D.将浓硫酸加入滴有几滴水的蔗糖中,蔗糖逐渐变黑形成“黑面包”,产生有刺激性气体,体现浓硫酸的脱水性和强氧化性 |
您最近一年使用:0次



