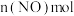名校
1 . 工业上用 处理氨氮水的原理如图所示。
处理氨氮水的原理如图所示。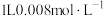 的氨水分别和不同量的
的氨水分别和不同量的 混合,测得溶液中氨去除率、总氮(
混合,测得溶液中氨去除率、总氮( 和
和 的总和)残余率与
的总和)残余率与 投入量(用x表示)的关系如图所示。下列说法错误的是
投入量(用x表示)的关系如图所示。下列说法错误的是
 处理氨氮水的原理如图所示。
处理氨氮水的原理如图所示。
 的氨水分别和不同量的
的氨水分别和不同量的 混合,测得溶液中氨去除率、总氮(
混合,测得溶液中氨去除率、总氮( 和
和 的总和)残余率与
的总和)残余率与 投入量(用x表示)的关系如图所示。下列说法错误的是
投入量(用x表示)的关系如图所示。下列说法错误的是
A.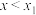 时, 时, 主要被氧化为 主要被氧化为 |
B.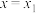 时,生成的 时,生成的 的物质的量为 的物质的量为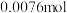 |
C.生成硝氮的离子方程式: |
D. 时,分批加入 时,分批加入 可以降低总氮残余率 可以降低总氮残余率 |
您最近一年使用:0次
名校
解题方法
2 . 用磷铁渣(含Fe、FeP、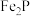 及少量杂质)制备磷酸铁晶体(
及少量杂质)制备磷酸铁晶体( )的工艺流程如下:
)的工艺流程如下:___________ 。
(2)“浸取”时,硝酸浓度过高会较多分解,化学方程式是___________ 。
(3)废气中含有 、NO,直接排放产生的危害主要有
、NO,直接排放产生的危害主要有___________ (写出两项),加入活性炭的目的是吸附氮氧化物;若用NaOH溶液吸收,物质的量比为 的
的 、NO被完全吸收转化生成的是一种盐,盐中Na、N质量比为
、NO被完全吸收转化生成的是一种盐,盐中Na、N质量比为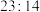 ,其化学式是
,其化学式是___________ 。
(4)若HNO₃的还原产物为NO,与1molFe2P完全反应而生成的NO有___________ mol。
(5)实验室完成操作X中用到的玻璃仪器有:烧杯、___________ 。
(6)“调pH”时,碱性过高产物中含铁量会增大,其原因有可能为___________ 。
(7)最终产品应洗涤,检验是否洗净的试剂是___________ 。
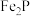 及少量杂质)制备磷酸铁晶体(
及少量杂质)制备磷酸铁晶体( )的工艺流程如下:
)的工艺流程如下:
(2)“浸取”时,硝酸浓度过高会较多分解,化学方程式是
(3)废气中含有
 、NO,直接排放产生的危害主要有
、NO,直接排放产生的危害主要有 的
的 、NO被完全吸收转化生成的是一种盐,盐中Na、N质量比为
、NO被完全吸收转化生成的是一种盐,盐中Na、N质量比为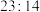 ,其化学式是
,其化学式是(4)若HNO₃的还原产物为NO,与1molFe2P完全反应而生成的NO有
(5)实验室完成操作X中用到的玻璃仪器有:烧杯、
(6)“调pH”时,碱性过高产物中含铁量会增大,其原因有可能为
(7)最终产品应洗涤,检验是否洗净的试剂是
您最近一年使用:0次
名校
3 . 硼、氮、铁、钴、镍等元素可形成结构、性质各异的物质,在生产、科研中发挥着重要用途。回答下列问题:
(1)下列不同状态的硼中,失去一个电子需要吸收能量最多的是______(填标号)。
(2)硼酸( )为片层状白色晶体,层内
)为片层状白色晶体,层内 分子间通过氢键相连,如图所示。
分子间通过氢键相连,如图所示。 水溶液中存在
水溶液中存在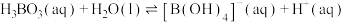 的平衡,回答下列问题。
的平衡,回答下列问题。__________ 。
②下列关于硼酸的说法正确的是__________ (填序号)。
a. 是一元酸 b.硼酸水溶液中水的电离平衡受到抑制
是一元酸 b.硼酸水溶液中水的电离平衡受到抑制
c.硼酸分子的稳定性与氢键有关 d.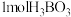 晶体中有
晶体中有 氢键
氢键
(3)叠氮化合物在化工上有重要应用, 为叠氮离子,写出与
为叠氮离子,写出与 互为等电子体的微粒的化学式
互为等电子体的微粒的化学式__________ (写出一种即可),其立体构型为__________ 。
(4) 的结构如图所示,
的结构如图所示, 中
中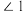 、
、 、
、 由大到小的顺序是
由大到小的顺序是____________________ 。 )晶胞沿
)晶胞沿 、
、 或
或 轴任意一个方向的投影如下图所示。晶胞中
轴任意一个方向的投影如下图所示。晶胞中 处于各顶角位置,则O处于
处于各顶角位置,则O处于__________ 位置。
①从该晶胞中能分割出来的结构图有_______ (填标号)。 ,
, 为阿伏加德罗常数的值。该晶胞中镍离子周围与其等距离且最近的镍离子有
为阿伏加德罗常数的值。该晶胞中镍离子周围与其等距离且最近的镍离子有__________ 个,该距离为__________ pm(仅列式不计算)。
(1)下列不同状态的硼中,失去一个电子需要吸收能量最多的是______(填标号)。
A.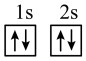 | B. |
C.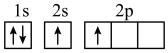 | D.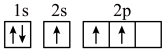 |
(2)硼酸(
 )为片层状白色晶体,层内
)为片层状白色晶体,层内 分子间通过氢键相连,如图所示。
分子间通过氢键相连,如图所示。 水溶液中存在
水溶液中存在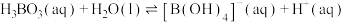 的平衡,回答下列问题。
的平衡,回答下列问题。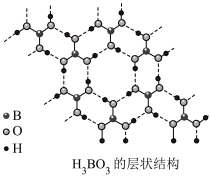
②下列关于硼酸的说法正确的是
a.
 是一元酸 b.硼酸水溶液中水的电离平衡受到抑制
是一元酸 b.硼酸水溶液中水的电离平衡受到抑制c.硼酸分子的稳定性与氢键有关 d.
 晶体中有
晶体中有 氢键
氢键(3)叠氮化合物在化工上有重要应用,
 为叠氮离子,写出与
为叠氮离子,写出与 互为等电子体的微粒的化学式
互为等电子体的微粒的化学式(4)
 的结构如图所示,
的结构如图所示, 中
中 、
、 、
、 由大到小的顺序是
由大到小的顺序是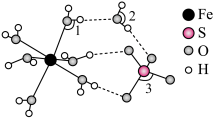
 )晶胞沿
)晶胞沿 、
、 或
或 轴任意一个方向的投影如下图所示。晶胞中
轴任意一个方向的投影如下图所示。晶胞中 处于各顶角位置,则O处于
处于各顶角位置,则O处于
①从该晶胞中能分割出来的结构图有
a.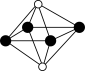 b.
b.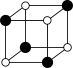 c.
c.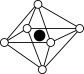 d.
d. e.
e.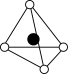
 ,
, 为阿伏加德罗常数的值。该晶胞中镍离子周围与其等距离且最近的镍离子有
为阿伏加德罗常数的值。该晶胞中镍离子周围与其等距离且最近的镍离子有
您最近一年使用:0次
名校
解题方法
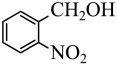
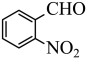
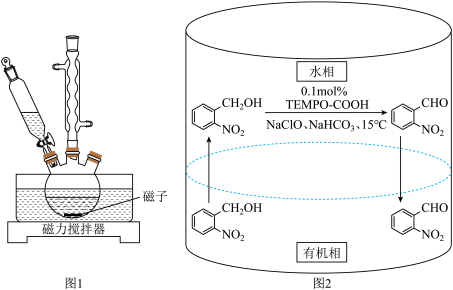
4 . 实验室以邻硝基苄醇为原料,通过图1装置(夹持仪器已略去)利用两相反应体系(图2)在TEMPO-COOH水溶液做催化剂下实现选择性氧化合成邻硝基苯甲醛。部分物质的性质如下表所示。
Ⅱ.反应完全后,将反应液倒入分液漏斗,分出有机层后,水相用10.0mL二氯甲烷萃取,合并有机相,经无水硫酸钠干燥、过滤后,除去并回收滤液中的二氯甲烷,得到粗品。
Ⅲ.将粗品溶解在20.0mL二氯甲烷中,加入10.0mL饱和NaHSO3溶液,充分作用后,分离得到水层,水层在冰浴中用5%氢氧化钠溶液调节pH到10,浅黄色固体析出完全。抽滤、干燥至恒重,得1.30g产品。
(1)控制反应温度为15℃的方法是___________ ;滴加NaC1O溶液时,需要先将漏斗上端玻璃塞打开,目的是___________ 。
(2)合成产品的化学方程式为___________ 。
(3)配制饱和NaHCO3溶液时,必须使用的仪器是(填写仪器名称)___________ 。____________ ,该副产物主要成分是___________ 。
(5)步骤Ⅱ中除去并回收二氯甲烷的实验方法是___________ 。
(6)本实验产率为___________ (计算结果保留3位有效数字)。
| 物质 |
|
| TEMPO-COOH |
| 溶解性 | 微溶于水,易溶于CH2Cl2 | 难溶于水,易溶于CH2Cl2 | 易溶于水,难溶于CH2Cl2 |
| 熔点/℃ | 70 | 43 | —— |
| 沸点/℃ | 270 | 153 | —— |
已知: 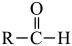 +NaHSO3
+NaHSO3
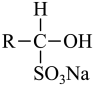 (易溶于水);
(易溶于水);
Ⅱ.反应完全后,将反应液倒入分液漏斗,分出有机层后,水相用10.0mL二氯甲烷萃取,合并有机相,经无水硫酸钠干燥、过滤后,除去并回收滤液中的二氯甲烷,得到粗品。
Ⅲ.将粗品溶解在20.0mL二氯甲烷中,加入10.0mL饱和NaHSO3溶液,充分作用后,分离得到水层,水层在冰浴中用5%氢氧化钠溶液调节pH到10,浅黄色固体析出完全。抽滤、干燥至恒重,得1.30g产品。
(1)控制反应温度为15℃的方法是
(2)合成产品的化学方程式为
(3)配制饱和NaHCO3溶液时,必须使用的仪器是(填写仪器名称)
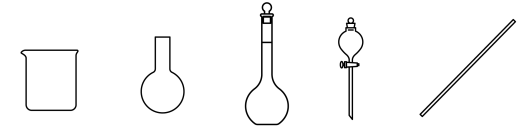
(5)步骤Ⅱ中除去并回收二氯甲烷的实验方法是
(6)本实验产率为
您最近一年使用:0次
名校
解题方法
5 . 道路千万条,安全第一条。当汽车在高速行驶中受到猛烈撞击时,会产生大量气体充满气囊,从而保护驾驶员和乘客的安全。
Ⅰ.安全气囊内叠氮化钠爆炸过程中的能量变化如图甲所示:______ (填“吸热”或“放热”)反应。
(2)若爆炸过程中有24mol非极性键生成(计算时将一对共用电子对作为一个化学键计量),则反应吸收(或释放)的能量为______ kJ(用含a、b的代数式表示)。
Ⅱ.汽车尾气中的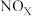 是常见的一种大气污染物,在2L密闭容器内,800℃时反应
是常见的一种大气污染物,在2L密闭容器内,800℃时反应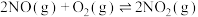 体系中,
体系中, 随时间的变化如表:
随时间的变化如表:
(3)下图表示 的变化的曲线是
的变化的曲线是______ ______ (选填序号,下同)。
a.容器内气体的颜色不再变化 b.
c. d.消耗
d.消耗 的同时生成
的同时生成
(5)为使该反应的反应速率增大,下列措施正确的是______ 。
a.增大 的浓度 b.适当升高温度 c.及时分离出
的浓度 b.适当升高温度 c.及时分离出 气体
气体
Ⅲ.化学能与其他能量间的转换在生活中处处可见,以反应 为原理设计成利用率高的燃料电池,装置如图所示:
为原理设计成利用率高的燃料电池,装置如图所示:______ 极(填写“正”或“负”),M处电极反应式是______ ;
(7)该电池产生11.2L(标况下) ,则外电路中转移的电子数目为
,则外电路中转移的电子数目为______ 。
Ⅰ.安全气囊内叠氮化钠爆炸过程中的能量变化如图甲所示:
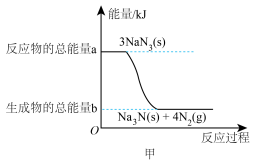
(2)若爆炸过程中有24mol非极性键生成(计算时将一对共用电子对作为一个化学键计量),则反应吸收(或释放)的能量为
Ⅱ.汽车尾气中的
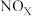 是常见的一种大气污染物,在2L密闭容器内,800℃时反应
是常见的一种大气污染物,在2L密闭容器内,800℃时反应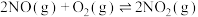 体系中,
体系中, 随时间的变化如表:
随时间的变化如表:时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(3)下图表示
 的变化的曲线是
的变化的曲线是 
a.容器内气体的颜色不再变化 b.

c.
 d.消耗
d.消耗 的同时生成
的同时生成
(5)为使该反应的反应速率增大,下列措施正确的是
a.增大
 的浓度 b.适当升高温度 c.及时分离出
的浓度 b.适当升高温度 c.及时分离出 气体
气体Ⅲ.化学能与其他能量间的转换在生活中处处可见,以反应
 为原理设计成利用率高的燃料电池,装置如图所示:
为原理设计成利用率高的燃料电池,装置如图所示: 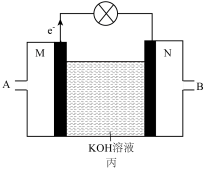
(7)该电池产生11.2L(标况下)
 ,则外电路中转移的电子数目为
,则外电路中转移的电子数目为
您最近一年使用:0次
名校
6 . 化学是以实验为基础的学科。
(1)某化学兴趣小组在实验室配制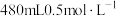 硫酸溶液。
硫酸溶液。
①在配制溶液时除了用到烧杯、玻璃棒、量筒、胶头滴管,还需要用到的玻璃仪器是_______ 。
②在配制过程中,以下操作会导致所配溶液浓度偏高的是_______ (填字母)。
A.量取浓硫酸时,仰视刻度线
B.转移前,容量瓶中含有少量蒸馏水
C.转移时,有少量液体溅出
D.未等溶液恢复至室温就转移到容量瓶中
(2)该小组同学取配制好的 的硫酸溶液
的硫酸溶液 与
与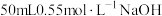 溶液进行中和反应,经过测定并计算得到该反应过程中放出热量为
溶液进行中和反应,经过测定并计算得到该反应过程中放出热量为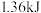 ,则该同学得到的中和热
,则该同学得到的中和热
____ 。
(3)该小组欲准确测定某市售双氧水中 的含量:取双氧水
的含量:取双氧水 至锥形瓶中,加入配制好的稀硫酸酸化,用蒸馏水稀释。用一定浓度的高锰酸钾标准液滴定。
至锥形瓶中,加入配制好的稀硫酸酸化,用蒸馏水稀释。用一定浓度的高锰酸钾标准液滴定。
①滴定反应的离子方程式为_______ 。
②滴定时,将高锰酸钾标准溶液注入_______ (填“酸”或“碱”)式滴定管中、滴定终点的判断是_______ 。
③根据实验测得,消耗 溶液,那么
溶液,那么 的浓度为
的浓度为_______ 。若滴定过程按以下操作会造成测定结果偏低的是_______ 。
A.滴定管未用 标准溶液润洗
标准溶液润洗
B.量取双氧水时,滴定前尖嘴有气泡,滴定后气泡消失
C.盛装标准溶液的滴定管,滴定前仰视凹液面最低处,滴定后平视读数
D.锥形瓶未用待测液润洗
(1)某化学兴趣小组在实验室配制
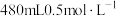 硫酸溶液。
硫酸溶液。①在配制溶液时除了用到烧杯、玻璃棒、量筒、胶头滴管,还需要用到的玻璃仪器是
②在配制过程中,以下操作会导致所配溶液浓度偏高的是
A.量取浓硫酸时,仰视刻度线
B.转移前,容量瓶中含有少量蒸馏水
C.转移时,有少量液体溅出
D.未等溶液恢复至室温就转移到容量瓶中
(2)该小组同学取配制好的
 的硫酸溶液
的硫酸溶液 与
与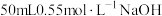 溶液进行中和反应,经过测定并计算得到该反应过程中放出热量为
溶液进行中和反应,经过测定并计算得到该反应过程中放出热量为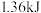 ,则该同学得到的中和热
,则该同学得到的中和热
(3)该小组欲准确测定某市售双氧水中
 的含量:取双氧水
的含量:取双氧水 至锥形瓶中,加入配制好的稀硫酸酸化,用蒸馏水稀释。用一定浓度的高锰酸钾标准液滴定。
至锥形瓶中,加入配制好的稀硫酸酸化,用蒸馏水稀释。用一定浓度的高锰酸钾标准液滴定。①滴定反应的离子方程式为
②滴定时,将高锰酸钾标准溶液注入
③根据实验测得,消耗
 溶液,那么
溶液,那么 的浓度为
的浓度为A.滴定管未用
 标准溶液润洗
标准溶液润洗B.量取双氧水时,滴定前尖嘴有气泡,滴定后气泡消失
C.盛装标准溶液的滴定管,滴定前仰视凹液面最低处,滴定后平视读数
D.锥形瓶未用待测液润洗
您最近一年使用:0次
名校
7 . Ⅰ. 和
和 在工农业、科研等方面应用广泛。
在工农业、科研等方面应用广泛。
(1) (氨硼烷)是具有广泛应用前景的储氢材料。
(氨硼烷)是具有广泛应用前景的储氢材料。
① 中存在配位键,提供空轨道的原子是
中存在配位键,提供空轨道的原子是_______ 。
② 的沸点高于
的沸点高于 的可能原因是
的可能原因是_______ 。
(2)工业合成 时用到含铁催化剂。
时用到含铁催化剂。
① 元素在周期表第
元素在周期表第_______ 族,基态 原子电子的空间运动状态有
原子电子的空间运动状态有_______ 种。
②从结构的角度分析 容易被氧化成
容易被氧化成 的原因是
的原因是_______ 。
(3)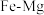 合金是储氢密度很高的材料之一,其晶胞结构如图所示。若该晶体储氢时,
合金是储氢密度很高的材料之一,其晶胞结构如图所示。若该晶体储氢时, 分子在晶胞的体心和棱的中心位置。
分子在晶胞的体心和棱的中心位置。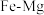 合金中,每个
合金中,每个 原子周围与它最近且相等距离的
原子周围与它最近且相等距离的 原子有
原子有_______ 个。
②要储存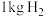 ,至少需要
,至少需要_______ 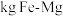 合金。
合金。
Ⅱ.钛及其化合物具有优异的物理、化学性能,相关的研究备受关注。具有双钙钛矿型结构的晶体通过掺杂改性可用作固体电解质材料。双钙钛矿型晶体的一种典型结构单元如图所示:_______ 个 原子。
原子。
②该晶胞的化学式为_______ 。
 和
和 在工农业、科研等方面应用广泛。
在工农业、科研等方面应用广泛。(1)
 (氨硼烷)是具有广泛应用前景的储氢材料。
(氨硼烷)是具有广泛应用前景的储氢材料。①
 中存在配位键,提供空轨道的原子是
中存在配位键,提供空轨道的原子是②
 的沸点高于
的沸点高于 的可能原因是
的可能原因是(2)工业合成
 时用到含铁催化剂。
时用到含铁催化剂。①
 元素在周期表第
元素在周期表第 原子电子的空间运动状态有
原子电子的空间运动状态有②从结构的角度分析
 容易被氧化成
容易被氧化成 的原因是
的原因是(3)
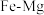 合金是储氢密度很高的材料之一,其晶胞结构如图所示。若该晶体储氢时,
合金是储氢密度很高的材料之一,其晶胞结构如图所示。若该晶体储氢时, 分子在晶胞的体心和棱的中心位置。
分子在晶胞的体心和棱的中心位置。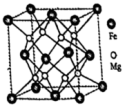
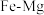 合金中,每个
合金中,每个 原子周围与它最近且相等距离的
原子周围与它最近且相等距离的 原子有
原子有②要储存
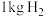 ,至少需要
,至少需要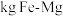 合金。
合金。Ⅱ.钛及其化合物具有优异的物理、化学性能,相关的研究备受关注。具有双钙钛矿型结构的晶体通过掺杂改性可用作固体电解质材料。双钙钛矿型晶体的一种典型结构单元如图所示:

 原子。
原子。②该晶胞的化学式为
您最近一年使用:0次
名校
解题方法
8 . 下列说法错误的是
| A.在现代化学中,常利用原子光谱上的特征谱线鉴定元素 |
| B.霓虹灯的发光原理是电子由基态向激发态跃迁时,以光的形式释放能量 |
| C.DNA形成螺旋结构是因为氢键的作用 |
| D.超分子内部分子之间通过非共价键相结合 |
您最近一年使用:0次
名校
9 . 钙及其化合物在生产生活中有着重要的作用。
(1)Ca与Fe属于同一周期元素,且核外最外层电子构型相闰,但Ca的熔、沸点都比Fe低,原因是:________ 。
(2) 与水反应生成的
与水反应生成的 分子中,碳原子杂化轨道类型是
分子中,碳原子杂化轨道类型是________ ,且 中
中 与
与 互为等电子体,
互为等电子体, 中含有的
中含有的 键数目为
键数目为________ 。
(3) 的结构如图甲所示,其中B离子表示
的结构如图甲所示,其中B离子表示________ ,晶体中与 最近且等距离的
最近且等距离的 数目为
数目为________ 。 中燃烧时,得到一种氧化物晶体,其结构如图乙所示,由此可判断该氧化物中阴、阳离子数目之比为
中燃烧时,得到一种氧化物晶体,其结构如图乙所示,由此可判断该氧化物中阴、阳离子数目之比为________ ,已知该氧化物的密度是 ,则晶胞内最近的两个
,则晶胞内最近的两个 间的距离为
间的距离为________ cm(写出计算式即可)。
(1)Ca与Fe属于同一周期元素,且核外最外层电子构型相闰,但Ca的熔、沸点都比Fe低,原因是:
(2)
 与水反应生成的
与水反应生成的 分子中,碳原子杂化轨道类型是
分子中,碳原子杂化轨道类型是 中
中 与
与 互为等电子体,
互为等电子体, 中含有的
中含有的 键数目为
键数目为(3)
 的结构如图甲所示,其中B离子表示
的结构如图甲所示,其中B离子表示 最近且等距离的
最近且等距离的 数目为
数目为
 中燃烧时,得到一种氧化物晶体,其结构如图乙所示,由此可判断该氧化物中阴、阳离子数目之比为
中燃烧时,得到一种氧化物晶体,其结构如图乙所示,由此可判断该氧化物中阴、阳离子数目之比为 ,则晶胞内最近的两个
,则晶胞内最近的两个 间的距离为
间的距离为
您最近一年使用:0次
10 . 乙二胺四乙酸(EDTA)是一种重要的络合剂,其能与绝大多数的金属离子形成稳定的配合物,简易机理如图所示。下列叙述错误的是

| A.EDTA的核磁共振氢谱上有3组峰 | B.EDTA中含有两种官能团 |
| C.螯合物中含有4个sp2-pπ键 | D.螯合物中有5个五元螯合环 |
您最近一年使用:0次