1 . 将质量为m的氧化铜粉末加入到100g14%的稀硫酸中,微热至氧化铜全部溶解,再向该蓝色溶液中加入10g铁粉,充分反应后过滤,得滤液和5.2g滤渣。求:
(1)氧化铜的质量m的值为___________ 。
(2)最后得到的滤液中溶质的质量分数为___________ (最后结果精确到0.1%)。
(1)氧化铜的质量m的值为
(2)最后得到的滤液中溶质的质量分数为
您最近一年使用:0次
名校
2 . 完成下列问题
(1)现有 、
、 和
和 组成的混合物,某研究性学习小组为了探究其组成情况,加入
组成的混合物,某研究性学习小组为了探究其组成情况,加入 溶液恰好使混合物完全溶解,同时收集到
溶液恰好使混合物完全溶解,同时收集到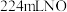 气体(标况)。则产物中硝酸铜的物质的量为
气体(标况)。则产物中硝酸铜的物质的量为___________ 。如原混合物中有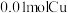 ,则其中
,则其中 与
与 的质量之比为
的质量之比为___________ 。
(2)将一定质量的铜粉加入到 某浓度的稀硝酸中,充分反应后,容器中剩有
某浓度的稀硝酸中,充分反应后,容器中剩有 铜粉,此时共收集到
铜粉,此时共收集到 气体
气体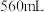 (标准状况)。然后向上述混合物中加入足量稀硫酸至不再反应为止,容器仍剩有铜粉
(标准状况)。然后向上述混合物中加入足量稀硫酸至不再反应为止,容器仍剩有铜粉 ,则
,则 为
为___________ 。
(3)将铁粉和铜粉的均匀混合物平均分成四等份,分别加入同浓度的稀硝酸,充分反应,在标准状况下生成 的体积和剩余金属的质量如下表(设硝酸的还原产物只有
的体积和剩余金属的质量如下表(设硝酸的还原产物只有 )。
)。
①稀硝酸的物质的量的浓度为___________  。
。
②V=___________ 。
(1)现有
 、
、 和
和 组成的混合物,某研究性学习小组为了探究其组成情况,加入
组成的混合物,某研究性学习小组为了探究其组成情况,加入 溶液恰好使混合物完全溶解,同时收集到
溶液恰好使混合物完全溶解,同时收集到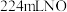 气体(标况)。则产物中硝酸铜的物质的量为
气体(标况)。则产物中硝酸铜的物质的量为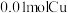 ,则其中
,则其中 与
与 的质量之比为
的质量之比为(2)将一定质量的铜粉加入到
 某浓度的稀硝酸中,充分反应后,容器中剩有
某浓度的稀硝酸中,充分反应后,容器中剩有 铜粉,此时共收集到
铜粉,此时共收集到 气体
气体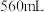 (标准状况)。然后向上述混合物中加入足量稀硫酸至不再反应为止,容器仍剩有铜粉
(标准状况)。然后向上述混合物中加入足量稀硫酸至不再反应为止,容器仍剩有铜粉 ,则
,则 为
为(3)将铁粉和铜粉的均匀混合物平均分成四等份,分别加入同浓度的稀硝酸,充分反应,在标准状况下生成
 的体积和剩余金属的质量如下表(设硝酸的还原产物只有
的体积和剩余金属的质量如下表(设硝酸的还原产物只有 )。
)。| 编号 | ① | ② | ③ | ④ |
硝酸体积 | 100 | 200 | 300 | 400 |
剩余金属 | 18.0 |  | 0 | 0 |
 体积 体积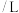 | 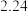 |  | 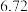 | V |
 。
。②V=
您最近一年使用:0次
23-24高二下·全国·课前预习
3 . 某种含C、H、O三种元素的未知物A,经燃烧分析实验测得其中碳的质量分数为52.16%,氢的质量分数为13.14%。则:
(1)氧的质量分数为___________ 。
(2)C、H、O的原子个数比N(C)∶N(H)∶N(O)≈___________ 。
(3)该未知物A的实验式为___________ 。
(1)氧的质量分数为
(2)C、H、O的原子个数比N(C)∶N(H)∶N(O)≈
(3)该未知物A的实验式为
您最近一年使用:0次
4 . 取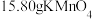 ,加热分解后剩余固体
,加热分解后剩余固体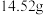 ,该剩余固体与足量的浓盐酸在加热条件下充分反应,生成单质气体A,产物中锰元素以
,该剩余固体与足量的浓盐酸在加热条件下充分反应,生成单质气体A,产物中锰元素以 存在,请计算:
存在,请计算:
(1)写出 受热分解的化学方程式
受热分解的化学方程式__________ 。
(2) 的分解率
的分解率__________ 。
(3)气体A的物质的量_________ 。
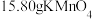 ,加热分解后剩余固体
,加热分解后剩余固体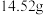 ,该剩余固体与足量的浓盐酸在加热条件下充分反应,生成单质气体A,产物中锰元素以
,该剩余固体与足量的浓盐酸在加热条件下充分反应,生成单质气体A,产物中锰元素以 存在,请计算:
存在,请计算:(1)写出
 受热分解的化学方程式
受热分解的化学方程式(2)
 的分解率
的分解率(3)气体A的物质的量
您最近一年使用:0次
解题方法
5 . 常温下,将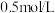 盐酸溶液和未知浓度的
盐酸溶液和未知浓度的 溶液以
溶液以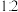 的体积比混合(忽略溶液体积变化),所得溶液的
的体积比混合(忽略溶液体积变化),所得溶液的 。用上述
。用上述 溶液与
溶液与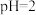 的某一元弱酸溶液
的某一元弱酸溶液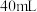 恰好完全反应,消耗了
恰好完全反应,消耗了 溶液
溶液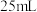 ,试求:
,试求:
(1) 溶液的物质的量浓度为
溶液的物质的量浓度为______  。
。
(2)该一元弱酸的物质的量浓度为______  。
。
(3)此条件下该一元弱酸的电离度为______ 。
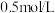 盐酸溶液和未知浓度的
盐酸溶液和未知浓度的 溶液以
溶液以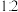 的体积比混合(忽略溶液体积变化),所得溶液的
的体积比混合(忽略溶液体积变化),所得溶液的 。用上述
。用上述 溶液与
溶液与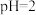 的某一元弱酸溶液
的某一元弱酸溶液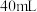 恰好完全反应,消耗了
恰好完全反应,消耗了 溶液
溶液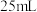 ,试求:
,试求:(1)
 溶液的物质的量浓度为
溶液的物质的量浓度为 。
。(2)该一元弱酸的物质的量浓度为
 。
。(3)此条件下该一元弱酸的电离度为
您最近一年使用:0次
6 . 回答下列问题
(1)在等体积的 三种溶液中,分别加入等量的
三种溶液中,分别加入等量的 溶液,恰好都完全反应,则以上三种溶液的物质的量浓度之比为
溶液,恰好都完全反应,则以上三种溶液的物质的量浓度之比为___________ 。
(2)Fe和 的混合物,加入
的混合物,加入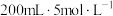 的盐酸,恰好完全溶解,再向其中加入KSCN溶液,未见血红色,则所得溶液中
的盐酸,恰好完全溶解,再向其中加入KSCN溶液,未见血红色,则所得溶液中 的物质的量浓度为
的物质的量浓度为___________  (假设反应后溶液体积仍为200mL)。
(假设反应后溶液体积仍为200mL)。
(3)把过量铁屑加入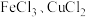 的混合溶液中,反应结束后,称得剩余固体的质量与所加铁屑的质量相等。则原溶液中
的混合溶液中,反应结束后,称得剩余固体的质量与所加铁屑的质量相等。则原溶液中 与
与 的物质的量之比是
的物质的量之比是___________ 。
(1)在等体积的
 三种溶液中,分别加入等量的
三种溶液中,分别加入等量的 溶液,恰好都完全反应,则以上三种溶液的物质的量浓度之比为
溶液,恰好都完全反应,则以上三种溶液的物质的量浓度之比为(2)Fe和
 的混合物,加入
的混合物,加入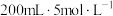 的盐酸,恰好完全溶解,再向其中加入KSCN溶液,未见血红色,则所得溶液中
的盐酸,恰好完全溶解,再向其中加入KSCN溶液,未见血红色,则所得溶液中 的物质的量浓度为
的物质的量浓度为 (假设反应后溶液体积仍为200mL)。
(假设反应后溶液体积仍为200mL)。(3)把过量铁屑加入
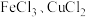 的混合溶液中,反应结束后,称得剩余固体的质量与所加铁屑的质量相等。则原溶液中
的混合溶液中,反应结束后,称得剩余固体的质量与所加铁屑的质量相等。则原溶液中 与
与 的物质的量之比是
的物质的量之比是
您最近一年使用:0次
7 . 已知锌与浓硫酸反应生成SO2,与稀硫酸反应生成H2。
I.39g的锌与50mL18.4mol/L的浓硫酸完分反应,锌完全溶解,同时收集到标准状况下气体VL,将反应后的溶液稀释到500mL,测得溶液中氢离子的浓度为0.08mol/L。
(1)反应过程中消耗H2SO4的物质的量是___________ 。
(2)气体的成分是___________ ,V=___________ 。
II.已知:SO2+I2+2H2O= +2I-+4H+。
+2I-+4H+。
(3)现将101.6mgI2固体溶于水配成400mL溶液,(为了便于观察,可以加几滴淀粉)用于吸收空气管道中的SO2,若管道中空气流量为40L/min,经过5min溶液恰好褪色,请计算:空气样品中SO2的含量为___________ mg/L。
I.39g的锌与50mL18.4mol/L的浓硫酸完分反应,锌完全溶解,同时收集到标准状况下气体VL,将反应后的溶液稀释到500mL,测得溶液中氢离子的浓度为0.08mol/L。
(1)反应过程中消耗H2SO4的物质的量是
(2)气体的成分是
II.已知:SO2+I2+2H2O=
 +2I-+4H+。
+2I-+4H+。(3)现将101.6mgI2固体溶于水配成400mL溶液,(为了便于观察,可以加几滴淀粉)用于吸收空气管道中的SO2,若管道中空气流量为40L/min,经过5min溶液恰好褪色,请计算:空气样品中SO2的含量为
您最近一年使用:0次
名校
解题方法
8 . 将Na2CO3和NaHCO3的混合物充分加热,生成的气体(假设无损耗)全部通入足量的石灰水中,得到20.0g白色沉淀,加热后的残留物加入200mL盐酸恰好完全反应,生成5.60LCO2气体(标准状况下)。试回答下列问题:
(1)所加盐酸的物质的量浓度为_______ mol/L。
(2)原混合物中碳酸钠的质量是_______ g。
(1)所加盐酸的物质的量浓度为
(2)原混合物中碳酸钠的质量是
您最近一年使用:0次
9 . 某研究性学习小组,进行甲、乙、丙三组实验:各取 同浓度的盐酸,加入不同质量的同种铝合金颗粒,充分反应,产生气体。有关数据记录如下:
同浓度的盐酸,加入不同质量的同种铝合金颗粒,充分反应,产生气体。有关数据记录如下:
请回答以下问题:
(1)计算丙中产生气体的物质的量为___________ mol;
(2)实验中所用合金粉末中镁、铝的物质的量之比为___________ ;
(3)实验乙结束后的混合体系中加入一定量的NOH溶液,充分反应,得到固体M。如果固体M的质量不再减少,消耗NaOH的质量至少为___________ g。
 同浓度的盐酸,加入不同质量的同种铝合金颗粒,充分反应,产生气体。有关数据记录如下:
同浓度的盐酸,加入不同质量的同种铝合金颗粒,充分反应,产生气体。有关数据记录如下:| 实验序号 | 甲 | 乙 | 丙 |
| 合金质量(g) | 1.008 | 1.260 | 1.512 |
| 生成气体体积(mL)(标况) | 1075.2 | 1344 | 1344 |
(1)计算丙中产生气体的物质的量为
(2)实验中所用合金粉末中镁、铝的物质的量之比为
(3)实验乙结束后的混合体系中加入一定量的NOH溶液,充分反应,得到固体M。如果固体M的质量不再减少,消耗NaOH的质量至少为
您最近一年使用:0次
10 . 32.5g的锌与50mL18.4mol/L浓硫酸充分反应,锌完全溶解,同时收集到标准状况下的混合气体VL。将反应后的溶液稀释到500mL,测得溶液中H+的浓度为0.08mol/L。
(1)反应过程中消耗的H2SO4的物质的量是_______ 。
(2)混合气体中的成分及它们体积之比为_______ 。
(1)反应过程中消耗的H2SO4的物质的量是
(2)混合气体中的成分及它们体积之比为
您最近一年使用:0次



