2024高三下·全国·专题练习
解题方法
1 . 对于基元反应,如aA+bB cC+dD,反应速率v正=k正·ca(A)·cb(B),v逆=k逆·cc(C)·cd(D),其中k正、k逆是取决于温度的速率常数。已知:
cC+dD,反应速率v正=k正·ca(A)·cb(B),v逆=k逆·cc(C)·cd(D),其中k正、k逆是取决于温度的速率常数。已知:
反应Ⅰ:4NH3(g)+5O2(g) 4NO(g)+6H2O(g)ΔH1=-902kJ·mol-1
4NO(g)+6H2O(g)ΔH1=-902kJ·mol-1
反应Ⅱ:8NH3(g)+6NO2(g) 7N2(g)+12H2O(g)ΔH2=-2740kJ·mol-1
7N2(g)+12H2O(g)ΔH2=-2740kJ·mol-1
反应Ⅲ:N2(g)+O2(g)=2NO(g)ΔH3=+182.6kJ·mol-1
对于基元反应Ⅳ:2NO(g)+O2(g) 2NO2(g)ΔH4,在653K时,速率常数k正=2.6×103L2·mol-2·s-1,k逆=4.1×103L·mol-1·s-1
2NO2(g)ΔH4,在653K时,速率常数k正=2.6×103L2·mol-2·s-1,k逆=4.1×103L·mol-1·s-1
(1)ΔH4=______ kJ·mol-1
(2)计算653K时的平衡常数K=______ 。
(3)653K时,若NO的浓度为0.006mol·L-1,O2的浓度为0.290mol·L-1,则正反应速率为______ mol·L-1·s-1
 cC+dD,反应速率v正=k正·ca(A)·cb(B),v逆=k逆·cc(C)·cd(D),其中k正、k逆是取决于温度的速率常数。已知:
cC+dD,反应速率v正=k正·ca(A)·cb(B),v逆=k逆·cc(C)·cd(D),其中k正、k逆是取决于温度的速率常数。已知:反应Ⅰ:4NH3(g)+5O2(g)
 4NO(g)+6H2O(g)ΔH1=-902kJ·mol-1
4NO(g)+6H2O(g)ΔH1=-902kJ·mol-1反应Ⅱ:8NH3(g)+6NO2(g)
 7N2(g)+12H2O(g)ΔH2=-2740kJ·mol-1
7N2(g)+12H2O(g)ΔH2=-2740kJ·mol-1反应Ⅲ:N2(g)+O2(g)=2NO(g)ΔH3=+182.6kJ·mol-1
对于基元反应Ⅳ:2NO(g)+O2(g)
 2NO2(g)ΔH4,在653K时,速率常数k正=2.6×103L2·mol-2·s-1,k逆=4.1×103L·mol-1·s-1
2NO2(g)ΔH4,在653K时,速率常数k正=2.6×103L2·mol-2·s-1,k逆=4.1×103L·mol-1·s-1(1)ΔH4=
(2)计算653K时的平衡常数K=
(3)653K时,若NO的浓度为0.006mol·L-1,O2的浓度为0.290mol·L-1,则正反应速率为
您最近一年使用:0次
2024高三下·全国·专题练习
解题方法
2 . 硫脲[CS(NH2)2]的分离及产品含量的测定。
装置C反应后的液体过滤后,将滤液减压蒸发浓缩,之后冷却结晶,离心分离,烘干即可得到产品。称取mg产品,加水溶解配成500mL溶液,量取25mL于锥形瓶中,滴加一定量的稀硫酸使溶液显酸性,用cmol·L-1 KMnO4标准溶液滴定,滴定至终点时消耗KMnO4标准溶液VmL。
(1)硫脲[CS(NH2)2]易溶于水,除硫脲和水都是极性分子外,其原因还有___________ 。
(2)滴定时,硫脲转化为CO2、N2、SO ,则
,则
___________ 。
(3)样品中硫脲的质量分数为___________ %(用含“m、c、V”的式子表示)。
装置C反应后的液体过滤后,将滤液减压蒸发浓缩,之后冷却结晶,离心分离,烘干即可得到产品。称取mg产品,加水溶解配成500mL溶液,量取25mL于锥形瓶中,滴加一定量的稀硫酸使溶液显酸性,用cmol·L-1 KMnO4标准溶液滴定,滴定至终点时消耗KMnO4标准溶液VmL。
(1)硫脲[CS(NH2)2]易溶于水,除硫脲和水都是极性分子外,其原因还有
(2)滴定时,硫脲转化为CO2、N2、SO
 ,则
,则
(3)样品中硫脲的质量分数为
您最近一年使用:0次
2024高三下·全国·专题练习
3 . 烟道气中的NOx是主要的大气污染物之一,为了监测其含量,选用如下检测方法:将v L气样通入适量酸化的H2O2溶液中,使NOx完全被氧化为NO ,加水稀释至100.00 mL;量取20.00 mL该溶液,加入v1 mL c1 mol·L−1 FeSO4标准溶液(过量),充分反应后,用c2 mol·L−1 K2Cr2O7标准溶液滴定剩余的Fe2+,终点时消耗v2 mL。
,加水稀释至100.00 mL;量取20.00 mL该溶液,加入v1 mL c1 mol·L−1 FeSO4标准溶液(过量),充分反应后,用c2 mol·L−1 K2Cr2O7标准溶液滴定剩余的Fe2+,终点时消耗v2 mL。
(1)NO被H2O2氧化为NO 的离子方程式是
的离子方程式是___________ 。
(2)滴定操作使用的玻璃仪器主要有___________ 。
(3)滴定过程中发生下列反应:3Fe2++NO +4H+=NO↑+3Fe3++2H2O
+4H+=NO↑+3Fe3++2H2O
Cr2O + 6Fe2+ +14H+ =2Cr3+ +6Fe3++7H2O,则气样中NOx折合成NO2的含量为
+ 6Fe2+ +14H+ =2Cr3+ +6Fe3++7H2O,则气样中NOx折合成NO2的含量为___________ mg·m−3.
(4)若FeSO4标准溶液部分变质,会使NOx含量测定结果___________ (填“偏高” 、“偏低”或“无影响 ”)。
 ,加水稀释至100.00 mL;量取20.00 mL该溶液,加入v1 mL c1 mol·L−1 FeSO4标准溶液(过量),充分反应后,用c2 mol·L−1 K2Cr2O7标准溶液滴定剩余的Fe2+,终点时消耗v2 mL。
,加水稀释至100.00 mL;量取20.00 mL该溶液,加入v1 mL c1 mol·L−1 FeSO4标准溶液(过量),充分反应后,用c2 mol·L−1 K2Cr2O7标准溶液滴定剩余的Fe2+,终点时消耗v2 mL。(1)NO被H2O2氧化为NO
 的离子方程式是
的离子方程式是(2)滴定操作使用的玻璃仪器主要有
(3)滴定过程中发生下列反应:3Fe2++NO
 +4H+=NO↑+3Fe3++2H2O
+4H+=NO↑+3Fe3++2H2OCr2O
 + 6Fe2+ +14H+ =2Cr3+ +6Fe3++7H2O,则气样中NOx折合成NO2的含量为
+ 6Fe2+ +14H+ =2Cr3+ +6Fe3++7H2O,则气样中NOx折合成NO2的含量为(4)若FeSO4标准溶液部分变质,会使NOx含量测定结果
您最近一年使用:0次
2024高三下·全国·专题练习
4 . 利用K2Cr2O7标准溶液定量测定硫代硫酸钠(Na2S2O3•5H2O)的纯度。测定步骤如下:
①溶液配制:称取1.2000g某硫代硫酸钠晶体样品,用新煮沸并冷却的蒸馏水配制成100 mL溶液。
②滴定:取0.00950mol•L-1的K2Cr2O7标准溶液20.00mL,硫酸酸化后加入过量KI,发生反应:Cr2O +6I-+14H+═3I2+2Cr3++7H2O,然后用硫代硫酸钠样品溶液滴定至淡黄绿色,发生反应:I2+2S2O
+6I-+14H+═3I2+2Cr3++7H2O,然后用硫代硫酸钠样品溶液滴定至淡黄绿色,发生反应:I2+2S2O ═S4O
═S4O +2I—,加入淀粉溶液作为指示剂,继续滴定,当滴入最后半滴Na2S2O3溶液,溶液
+2I—,加入淀粉溶液作为指示剂,继续滴定,当滴入最后半滴Na2S2O3溶液,溶液___________ ,即为终点,平行滴定3次,样品溶液的平均用量为24.80 mL,则样品纯度为___________ %(保留1位小数)。
①溶液配制:称取1.2000g某硫代硫酸钠晶体样品,用新煮沸并冷却的蒸馏水配制成100 mL溶液。
②滴定:取0.00950mol•L-1的K2Cr2O7标准溶液20.00mL,硫酸酸化后加入过量KI,发生反应:Cr2O
 +6I-+14H+═3I2+2Cr3++7H2O,然后用硫代硫酸钠样品溶液滴定至淡黄绿色,发生反应:I2+2S2O
+6I-+14H+═3I2+2Cr3++7H2O,然后用硫代硫酸钠样品溶液滴定至淡黄绿色,发生反应:I2+2S2O ═S4O
═S4O +2I—,加入淀粉溶液作为指示剂,继续滴定,当滴入最后半滴Na2S2O3溶液,溶液
+2I—,加入淀粉溶液作为指示剂,继续滴定,当滴入最后半滴Na2S2O3溶液,溶液
您最近一年使用:0次
5 . 利用某冶锌工厂的工业废料[除ZnO和少量Fe2O3外,还含有铋(Bi)、锗(Ge)的氧化物]制取几种金属化合物的工业流程如图:
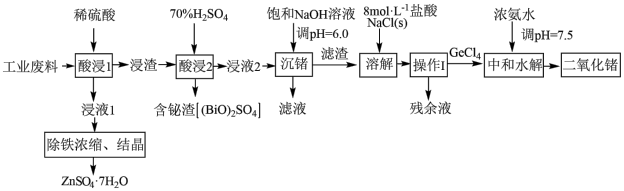
已知:该工艺条件下,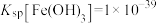 ,
,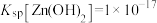 。
。
“浸液1”中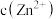 约为1.0mol/L,则除
约为1.0mol/L,则除 时应控制pH的范围为
时应控制pH的范围为___________ (已知:当溶液中某离子浓度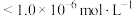 时,可认为该离子沉淀完全)。
时,可认为该离子沉淀完全)。

已知:该工艺条件下,
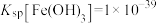 ,
,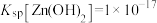 。
。“浸液1”中
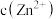 约为1.0mol/L,则除
约为1.0mol/L,则除 时应控制pH的范围为
时应控制pH的范围为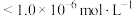 时,可认为该离子沉淀完全)。
时,可认为该离子沉淀完全)。
您最近一年使用:0次
6 . 当离子浓度小于或等于1×10-5 mol·L-1时可认为沉淀完全,若要使Cr3+完全沉淀则要保持c(OH-)≥___________ 。已知:Ksp[Cr(OH)3]=6.3×10-31,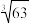 ≈4.0。
≈4.0。
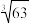 ≈4.0。
≈4.0。
您最近一年使用:0次
7 . K2Cr2O7在实验室中常用作基准试剂,在工业上大量用于颜料及电镀行业。回答下列问题:
利用含K2Cr2O7的工业废水制备Cr2O3的过程如下:废水经硫酸酸化后,利用NaHSO3将Cr2O 还原为Cr3+,向反应后的溶液中加入石灰乳,过滤得到的清液达到排放标准外排,得到的沉淀物经干化、煅烧制得Cr2O3。{已知:常温下Ksp[Cr(OH)3=6.3×10-31]},常温下,若清液中c(Cr3+)≤1.5 mg·L-1,则达到国家排放标准。试判断当清液的pH=5时,是否符合排放标准:
还原为Cr3+,向反应后的溶液中加入石灰乳,过滤得到的清液达到排放标准外排,得到的沉淀物经干化、煅烧制得Cr2O3。{已知:常温下Ksp[Cr(OH)3=6.3×10-31]},常温下,若清液中c(Cr3+)≤1.5 mg·L-1,则达到国家排放标准。试判断当清液的pH=5时,是否符合排放标准:___________ (要有计算过程和必要的文字叙述)。
利用含K2Cr2O7的工业废水制备Cr2O3的过程如下:废水经硫酸酸化后,利用NaHSO3将Cr2O
 还原为Cr3+,向反应后的溶液中加入石灰乳,过滤得到的清液达到排放标准外排,得到的沉淀物经干化、煅烧制得Cr2O3。{已知:常温下Ksp[Cr(OH)3=6.3×10-31]},常温下,若清液中c(Cr3+)≤1.5 mg·L-1,则达到国家排放标准。试判断当清液的pH=5时,是否符合排放标准:
还原为Cr3+,向反应后的溶液中加入石灰乳,过滤得到的清液达到排放标准外排,得到的沉淀物经干化、煅烧制得Cr2O3。{已知:常温下Ksp[Cr(OH)3=6.3×10-31]},常温下,若清液中c(Cr3+)≤1.5 mg·L-1,则达到国家排放标准。试判断当清液的pH=5时,是否符合排放标准:
您最近一年使用:0次
2024高三下·全国·专题练习
解题方法
8 . 已知C40Hx中的碳氢键和碳碳键的键能分别为431.0kJ·mol-1和298.0kJ·mol-1,H-H键能为436.0kJ·mol-1.估算C40H20(g) C40H18(g)+H2(g)的ΔH=
C40H18(g)+H2(g)的ΔH=_____ kJ·mol-1。
 C40H18(g)+H2(g)的ΔH=
C40H18(g)+H2(g)的ΔH=
您最近一年使用:0次
9 . 已知下列反应的热化学方程式:
①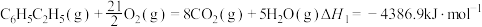
②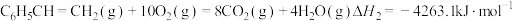
③
计算反应④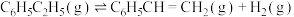 的
的
_____  ;
;
①
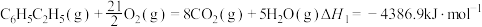
②
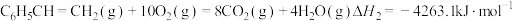
③

计算反应④
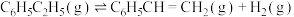 的
的
 ;
;
您最近一年使用:0次
2024高三·全国·专题练习
解题方法
10 . 工业上,可以采用 催化还原制备
催化还原制备 、
、 。发生反应如下:
。发生反应如下:
① (主反应);
(主反应);
② (主反应);
(主反应);
③ (副反应)。
(副反应)。
一定温度下,向总压强恒定为100kPa的反应器中充入 和
和 ,发生(4)中反应①②③,达到平衡时
,发生(4)中反应①②③,达到平衡时 转化率为50%,甲醇选择性为
转化率为50%,甲醇选择性为 ,生成
,生成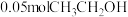 ,则反应①的平衡常数
,则反应①的平衡常数 为
为___________ 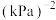 (写出数字表达式即可)[用分压计算的平衡常数为压强平衡常数
(写出数字表达式即可)[用分压计算的平衡常数为压强平衡常数 ,分压=总压×物质的量分数;甲醇选择性:
,分压=总压×物质的量分数;甲醇选择性: ]。
]。
 催化还原制备
催化还原制备 、
、 。发生反应如下:
。发生反应如下:①
 (主反应);
(主反应);②
 (主反应);
(主反应);③
 (副反应)。
(副反应)。一定温度下,向总压强恒定为100kPa的反应器中充入
 和
和 ,发生(4)中反应①②③,达到平衡时
,发生(4)中反应①②③,达到平衡时 转化率为50%,甲醇选择性为
转化率为50%,甲醇选择性为 ,生成
,生成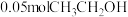 ,则反应①的平衡常数
,则反应①的平衡常数 为
为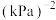 (写出数字表达式即可)[用分压计算的平衡常数为压强平衡常数
(写出数字表达式即可)[用分压计算的平衡常数为压强平衡常数 ,分压=总压×物质的量分数;甲醇选择性:
,分压=总压×物质的量分数;甲醇选择性: ]。
]。
您最近一年使用:0次



