名校
解题方法
1 . 某100 mL的CuCl2溶液中,已知溶液中的Cl-的浓度为0.2 mol·L-1。现将一定量的铁粉投入到该溶液中,若反应后溶液体积不变,回答下列问题:
(1)原溶液中Cu2+的浓度为___________ ;
(2)反应后测得Cl-的浓度为___________ ;
(3)反应中氧化剂是___________ ,反应后测得溶液中Fe2+的浓度为0.05 mol/L,则反应生成铜单质的质量为___________ g,转移电子___________ 个;
(4)剩余的Cu2+的物质的量浓度为___________ 。
(1)原溶液中Cu2+的浓度为
(2)反应后测得Cl-的浓度为
(3)反应中氧化剂是
(4)剩余的Cu2+的物质的量浓度为
您最近一年使用:0次
2024高三下·全国·专题练习
2 . 研究CO2 加氢制CH4 对资源综合利用有重要意义。相关的主要化学反应如下:
Ⅰ.CO2(g)+4H2(g) CH4(g)+2H2O(g) ΔH1<0
CH4(g)+2H2O(g) ΔH1<0
Ⅱ.CO2(g)+H2(g) CO(g)+H2O(g) ΔH2
CO(g)+H2O(g) ΔH2
Ⅲ.2CO(g)+2H2(g) CO2(g)+CH4(g) ΔH3=-247.1kJ· mol-1
CO2(g)+CH4(g) ΔH3=-247.1kJ· mol-1
在一定条件下,向体积为V L的恒容密闭容器中通入1 mol CO2和4 mol H2发生上述反应,20 min时,容器内反应达到平衡,容器中CH4(g)为a mol,CO为b mol,以H2表示的0~20 min内平均反应速率v(H2)=________ mol·L-1·min-1(用含a、b、V的代数式表示,下同),此时H2O(g) 的浓度为________ mol·L-1,反应Ⅱ的平衡常数为________ (列出计算式)。
Ⅰ.CO2(g)+4H2(g)
 CH4(g)+2H2O(g) ΔH1<0
CH4(g)+2H2O(g) ΔH1<0Ⅱ.CO2(g)+H2(g)
 CO(g)+H2O(g) ΔH2
CO(g)+H2O(g) ΔH2Ⅲ.2CO(g)+2H2(g)
 CO2(g)+CH4(g) ΔH3=-247.1kJ· mol-1
CO2(g)+CH4(g) ΔH3=-247.1kJ· mol-1在一定条件下,向体积为V L的恒容密闭容器中通入1 mol CO2和4 mol H2发生上述反应,20 min时,容器内反应达到平衡,容器中CH4(g)为a mol,CO为b mol,以H2表示的0~20 min内平均反应速率v(H2)=
您最近一年使用:0次
2024高三下·全国·专题练习
3 . 一定条件下,CO2与H2反应可合成CH2=CH2,2CO2(g)+6H2(g) CH2=CH2(g)+4H2O(g),该反应分两步进行:
CH2=CH2(g)+4H2O(g),该反应分两步进行:
i.CO2(g)+H2(g) CO(g)+H2O(g) ΔH1
CO(g)+H2O(g) ΔH1
ii.2CO(g)+4H2(g) CH2=CH2(g)+2H2O(g) ΔH2
CH2=CH2(g)+2H2O(g) ΔH2
T℃,压强恒定为100kPa时,将n(CO2):n(H2)=1:3的混合气体和催化剂投入反应器中,达平衡时,部分组分的物质的量分数如表所示:
CO2的平衡转化率为________ ,反应i的平衡常数Kp=________ (Kp是以分压表示的平衡常数,分压=总压×物质的量分数)
 CH2=CH2(g)+4H2O(g),该反应分两步进行:
CH2=CH2(g)+4H2O(g),该反应分两步进行:i.CO2(g)+H2(g)
 CO(g)+H2O(g) ΔH1
CO(g)+H2O(g) ΔH1ii.2CO(g)+4H2(g)
 CH2=CH2(g)+2H2O(g) ΔH2
CH2=CH2(g)+2H2O(g) ΔH2T℃,压强恒定为100kPa时,将n(CO2):n(H2)=1:3的混合气体和催化剂投入反应器中,达平衡时,部分组分的物质的量分数如表所示:
| 组分 | H2 | CO | CH2=CH2 |
| 物质的量分数(%) | 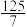 |  | 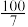 |
您最近一年使用:0次
2024高三下·全国·专题练习
解题方法
4 . 一定条件下,反应:CH3CH2CH3(g)  CH2=CHCH3(g)+H2(g) △H1=+123.8kJ/mol;丙烷平衡转化率x与平衡常数Kp的关系可表示为:
CH2=CHCH3(g)+H2(g) △H1=+123.8kJ/mol;丙烷平衡转化率x与平衡常数Kp的关系可表示为: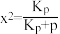 ,式中p为系统总压。p分别为0.10MPa和0.010MPa时,丙烷平衡转化率与温度的关系如图所示,其中表示0.10MPa下的关系曲线是
,式中p为系统总压。p分别为0.10MPa和0.010MPa时,丙烷平衡转化率与温度的关系如图所示,其中表示0.10MPa下的关系曲线是_______ (填“Ⅰ”或“Ⅱ”)。570℃时,KP=_______ MPa (保留2位有效数字)。

 CH2=CHCH3(g)+H2(g) △H1=+123.8kJ/mol;丙烷平衡转化率x与平衡常数Kp的关系可表示为:
CH2=CHCH3(g)+H2(g) △H1=+123.8kJ/mol;丙烷平衡转化率x与平衡常数Kp的关系可表示为: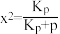 ,式中p为系统总压。p分别为0.10MPa和0.010MPa时,丙烷平衡转化率与温度的关系如图所示,其中表示0.10MPa下的关系曲线是
,式中p为系统总压。p分别为0.10MPa和0.010MPa时,丙烷平衡转化率与温度的关系如图所示,其中表示0.10MPa下的关系曲线是
您最近一年使用:0次
2024高三下·全国·专题练习
5 . 氮是自然界重要元素之一,研究氮及其化合物的性质以及氮的循环利用对解决环境和能源问题都具有重要意义。已知:1mol物质中的化学键断裂时所需能量如下表。
回答下列问题:
恒温下,将1mol空气(N2和O2的体积分数分别为0.78和0.21,其余为惰性组分)置于容积为VL的恒容密闭容器中,假设体系中只存在如下两个反应:
i.N2(g)+O2(g) 2NO(g) K1 △H1
2NO(g) K1 △H1
ii.2NO(g)+O2(g) 2NO2(g) K2 △H2=-114kJ∙mol-1
2NO2(g) K2 △H2=-114kJ∙mol-1
(1)△H1=_______ kJ∙mol-1。
(2)以下操作可以降低上述平衡体系中NO浓度的有_______(填标号)。
(3)若上述平衡体系中c(NO2)=amol·L-1,c(NO)=bmol·L-1,则c(O2)=_______ mol·L-1,K1=_______ (写出含a、b、V的计算式)。
| 物质 | N2(g) | O2(g) | NO(g) |
| 能量/kJ | 945 | 498 | 631 |
恒温下,将1mol空气(N2和O2的体积分数分别为0.78和0.21,其余为惰性组分)置于容积为VL的恒容密闭容器中,假设体系中只存在如下两个反应:
i.N2(g)+O2(g)
 2NO(g) K1 △H1
2NO(g) K1 △H1ii.2NO(g)+O2(g)
 2NO2(g) K2 △H2=-114kJ∙mol-1
2NO2(g) K2 △H2=-114kJ∙mol-1(1)△H1=
(2)以下操作可以降低上述平衡体系中NO浓度的有_______(填标号)。
| A.缩小体积 | B.升高温度 | C.移除NO2 | D.降低N2浓度 |
您最近一年使用:0次
2024高三下·全国·专题练习
解题方法
6 . 乙酸是基本的有机化工原料,乙酸制氢具有重要意义,制氢过程发生如下反应:
热裂解反应Ⅰ: CH3COOH(g) 2CO (g)+ 2H2(g) ΔH1
2CO (g)+ 2H2(g) ΔH1
脱羧基反应Ⅱ:CH3COOH(g) CO2 (g)+CH4(g) ΔH2
CO2 (g)+CH4(g) ΔH2
若利用合适的催化剂发生热裂解反应Ⅰ和脱羧基反应Ⅱ,温度为TK时达到平衡,总压强为p kPa,乙酸体积分数为20%,其中热裂解反应Ⅰ消耗的乙酸占投入量的20%,脱羧基反应Ⅱ的平衡常数Kp为_____ kPa (Kp为以分压表示的平衡常数)。
热裂解反应Ⅰ: CH3COOH(g)
 2CO (g)+ 2H2(g) ΔH1
2CO (g)+ 2H2(g) ΔH1脱羧基反应Ⅱ:CH3COOH(g)
 CO2 (g)+CH4(g) ΔH2
CO2 (g)+CH4(g) ΔH2若利用合适的催化剂发生热裂解反应Ⅰ和脱羧基反应Ⅱ,温度为TK时达到平衡,总压强为p kPa,乙酸体积分数为20%,其中热裂解反应Ⅰ消耗的乙酸占投入量的20%,脱羧基反应Ⅱ的平衡常数Kp为
您最近一年使用:0次
2024高三下·全国·专题练习
解题方法
7 . 1200K时,假定体系内只有反应C40H12 (g) C40H10(g) + H2(g)发生,反应过程中压强恒定为p0(即C40H12的初始压强),平衡转化率为α,该反应的平衡常数Kp为
C40H10(g) + H2(g)发生,反应过程中压强恒定为p0(即C40H12的初始压强),平衡转化率为α,该反应的平衡常数Kp为_______ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
 C40H10(g) + H2(g)发生,反应过程中压强恒定为p0(即C40H12的初始压强),平衡转化率为α,该反应的平衡常数Kp为
C40H10(g) + H2(g)发生,反应过程中压强恒定为p0(即C40H12的初始压强),平衡转化率为α,该反应的平衡常数Kp为
您最近一年使用:0次
2024高三下·全国·专题练习
8 . R的衍生物L可用于分离稀土。溶液中某稀土离子(用M表示)与L存在平衡:
M+L ML K1
ML K1
ML+L ML2 K2
ML2 K2
研究组用吸收光谱法研究了上述反应中M与L反应体系。当c0(L)=1.0×10-5mol·L-1时,测得平衡时各物种c平/c0(L)随c0(M)/c0(L)的变化曲线如图。c0(M)/c0(L)=0.51时,计算M的平衡转化率______ (写出计算过程,结果保留两位有效数字)。

M+L
 ML K1
ML K1ML+L
 ML2 K2
ML2 K2研究组用吸收光谱法研究了上述反应中M与L反应体系。当c0(L)=1.0×10-5mol·L-1时,测得平衡时各物种c平/c0(L)随c0(M)/c0(L)的变化曲线如图。c0(M)/c0(L)=0.51时,计算M的平衡转化率

您最近一年使用:0次
2024高三下·全国·专题练习
解题方法
9 . H2S与CO2在高温下发生反应:H2S(g)+CO2(g) COS(g)+H2O(g) ΔH>0.在610K时,将0.1molH2S与0.3molCO2充入2.5L的空钢瓶中,经过10min反应达到平衡,平衡时H2O(g)的物质的量分数为0.125,用H2O(g)的浓度变化表示的反应速率v(H2O)=
COS(g)+H2O(g) ΔH>0.在610K时,将0.1molH2S与0.3molCO2充入2.5L的空钢瓶中,经过10min反应达到平衡,平衡时H2O(g)的物质的量分数为0.125,用H2O(g)的浓度变化表示的反应速率v(H2O)=______ 。H2S的平衡转化率
______ %。
 COS(g)+H2O(g) ΔH>0.在610K时,将0.1molH2S与0.3molCO2充入2.5L的空钢瓶中,经过10min反应达到平衡,平衡时H2O(g)的物质的量分数为0.125,用H2O(g)的浓度变化表示的反应速率v(H2O)=
COS(g)+H2O(g) ΔH>0.在610K时,将0.1molH2S与0.3molCO2充入2.5L的空钢瓶中,经过10min反应达到平衡,平衡时H2O(g)的物质的量分数为0.125,用H2O(g)的浓度变化表示的反应速率v(H2O)=
您最近一年使用:0次
2024高三下·全国·专题练习
解题方法
10 . 空气中CO2含量的控制和CO2资源利用具有重要意义。
(1)已知25℃、101 下,在合成塔中,可通过二氧化碳和氢气合成甲醇,后续可制备甲酸。某反应体系中发生反应如下:
下,在合成塔中,可通过二氧化碳和氢气合成甲醇,后续可制备甲酸。某反应体系中发生反应如下:
Ⅰ:CO2(g)+H2(g) CO(g)+H2O(g)ΔH1=+41.2kJ·mol-1
CO(g)+H2O(g)ΔH1=+41.2kJ·mol-1
该反应的速率方程为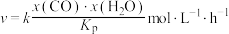 ,其中x表示相应气体的物质的量分数,
,其中x表示相应气体的物质的量分数, 为平衡常数(用平衡分压代替平衡浓度计算),k为反应的速率常数。已知平衡后
为平衡常数(用平衡分压代替平衡浓度计算),k为反应的速率常数。已知平衡后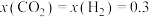 ,此时反应Ⅰ的速率
,此时反应Ⅰ的速率
______  (用含k的代数式表示)。
(用含k的代数式表示)。
(1)已知25℃、101
 下,在合成塔中,可通过二氧化碳和氢气合成甲醇,后续可制备甲酸。某反应体系中发生反应如下:
下,在合成塔中,可通过二氧化碳和氢气合成甲醇,后续可制备甲酸。某反应体系中发生反应如下:Ⅰ:CO2(g)+H2(g)
 CO(g)+H2O(g)ΔH1=+41.2kJ·mol-1
CO(g)+H2O(g)ΔH1=+41.2kJ·mol-1该反应的速率方程为
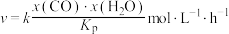 ,其中x表示相应气体的物质的量分数,
,其中x表示相应气体的物质的量分数, 为平衡常数(用平衡分压代替平衡浓度计算),k为反应的速率常数。已知平衡后
为平衡常数(用平衡分压代替平衡浓度计算),k为反应的速率常数。已知平衡后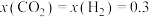 ,此时反应Ⅰ的速率
,此时反应Ⅰ的速率
 (用含k的代数式表示)。
(用含k的代数式表示)。
您最近一年使用:0次



