解题方法
1 . 下列离子方程式书写正确的是
A.氢氧化钡溶液与硫酸铜溶液混合: |
B.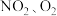 混合通入 混合通入 溶液中: 溶液中: |
C. 溶液中通入 溶液中通入 ,证明非金属性 ,证明非金属性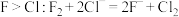 |
D.漂白粉溶液中通入少量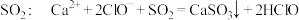 |
您最近一年使用:0次
解题方法
2 . 下列表示物质结构的化学用语正确的是
A.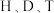 表示不同的核素 表示不同的核素 | B.甲烷的分子结构模型: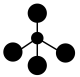 |
C. 的电子式: 的电子式: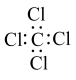 | D.钾原子的结构示意图: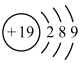 |
您最近一年使用:0次
名校
解题方法
3 . 常温下,二氧化氯(ClO2)是一种黄绿色气体,具有强氧化性,其中心原子Cl为sp2杂化已被联合国卫生组织(WTO)列为Al级高效安全消毒剂,其中心原子Cl为sp2杂化。已知,工业上制备二氧化氯的方法之一是用甲醇在酸性条件下与氯酸钠反应,其反应的化学方程式:CH3OH+6NaClO3+3H2SO4=CO2↑+6ClO2↑+3Na2SO4+5H2O,则下列说法错误的是
| A.CO2是非极性分子 | B.键角: < < |
| C.CH3OH在反应中发生氧化反应 | D.ClO2分子空间构型为V形 |
您最近一年使用:0次
名校
解题方法
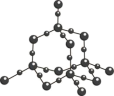
4 . 观察下列模型并结合信息,判断有关说法错误的是
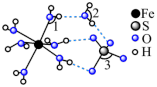
| 石英 | FeSO4·7H2O | |
| 结构模型示意图 |
|
|
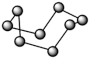
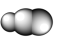
| 结构模型示意图 | S8分子 | HCN |
|
|
| A.石英属于共价晶体,且两原子个数比为2:1 |
| B.FeSO4·7H2O结构中键角1、2、3由大到小的顺序:3>1>2 |
| C.固态硫S8中S原子为sp2杂化 |
D.HCN的结构式为 |
您最近一年使用:0次
名校
解题方法
5 . 下列有关化学用语表示正确的是
A.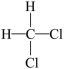 和 和 为同种物质 为同种物质 |
B.乙烷的结构式: |
C. 的电子式: 的电子式: |
D.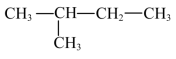 与 与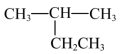 互为同分异构体 互为同分异构体 |
您最近一年使用:0次
名校
解题方法
6 . 回答下列问题:
Ⅰ.自然界中硫元素的存在如图1,硫元素的常见化合价与部分物质类别的对应关系如图2,回答下列问题:______________ 。
(2)X与Z反应中氧化剂与还原剂的物质的量之比为___________ 。
(3)Na2SO3溶液易被氧化成Na2SO4,检验Na2SO3溶液是否变质的试剂为_____________ 。
(4)铜和M的浓溶液反应生成Z的化学方程式为________________ 。
Ⅱ.氮氧化物(NOx)是大气污染物之一,处理NOx对于环境保护具有重要的意义。
在一定条件下NH3可将NO2还原。甲同学在实验室对该反应进行了探究。实验设计如图(部分夹持装置省略)。______________ 。
(6)在装置M中NH3和NO2充分反应,生成两种对环境友好的物质,则该反应的化学方程式__________________ 。
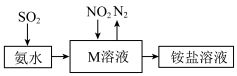
(7)工业生产中利用氨水吸收少量SO2和NO2,原理如图所示。NO2被吸收过程的离子方程式是_________________ 。
Ⅰ.自然界中硫元素的存在如图1,硫元素的常见化合价与部分物质类别的对应关系如图2,回答下列问题:
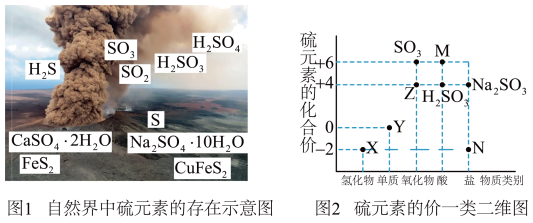
(2)X与Z反应中氧化剂与还原剂的物质的量之比为
(3)Na2SO3溶液易被氧化成Na2SO4,检验Na2SO3溶液是否变质的试剂为
(4)铜和M的浓溶液反应生成Z的化学方程式为
Ⅱ.氮氧化物(NOx)是大气污染物之一,处理NOx对于环境保护具有重要的意义。
在一定条件下NH3可将NO2还原。甲同学在实验室对该反应进行了探究。实验设计如图(部分夹持装置省略)。
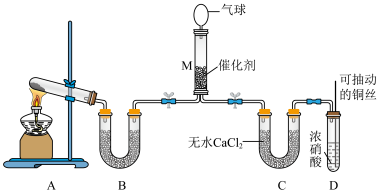
(6)在装置M中NH3和NO2充分反应,生成两种对环境友好的物质,则该反应的化学方程式
(7)工业生产中利用氨水吸收少量SO2和NO2,原理如图所示。NO2被吸收过程的离子方程式是
您最近一年使用:0次
7 . NA为阿伏加徳罗常数的值。下列说法正确的是
| A.50 mL、18.4 mol/L浓硫酸与足量铜加热反应,生成SO2分子的数目为0.46NA |
| B.1molFe和足量S充分反应转移电子数为2NA |
| C.常温下,将2.7 g铝片投入足量的浓硝酸中,铝失去的电子数为0.3NA |
| D.标准状况下,22.4 LSO2与足量O2的反应,生成的SO3分子数为NA |
您最近一年使用:0次
名校
8 . 下列有关化学用语的表示正确的是
A.中子数为20的氯原子: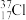 |
| B.CO2的空间结构为V形 |
C.过氧化氢的电子式: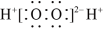 |
| D.HClO的结构式H-Cl-O |
您最近一年使用:0次
名校
解题方法
9 . 下列化学用语表示不正确的是
A.HClO的电子式: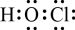 |
B.氯离子的结构示意图: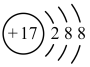 |
C.四氯化碳分子的空间填充模型: |
D.I、Ⅱ互为对映异构体: |
您最近一年使用:0次
名校
10 . 我国成功利用大功率运载火箭发射“天宫二号”空间实验室。火箭推进器中装有还原剂肼(N2H4)(液态)和强氧化剂过氧化氢(H2O2),请回答下列问题:
(1)肼又名联氨,其结构式为_____ 。
(2)液态肼与过氧化氢的反应属于_____ (填“吸热”或“放热”)反应。
(3)写出该火箭推进器中相关反应的化学方程式:_____ 。
(4)在一定温度下,向0.5L密闭容器中充入2molN2H4和2molO2发生如下反应:N2H4(g)+O2(g)⇌N2(g)+2H2O(g),其中有关物质的物质的量随时间变化的曲线如图所示,请回答下列问题:_____
②下列能说明该反应达到平衡状态的是_____ 。
A.υ正(N2)=2υ逆(H2O)
B.c(N2H4):c(O2):c(N2)=1:1:1
C.体系的压强不再发生变化
D.混合气体的密度不再发生变化
E.每断开1molO=O键,同时断开4molH-O键
③该反应达到平衡时,O2的体积百分数为_____ (结果保留一位小数)
④下列措施能够增大正反应的化学反应速率的有( )
A.升高反应温度 B.加入适当的催化剂C.向容器中加入氧气 D.向容器中加入氖气
(5)广泛应用的肼(N2H4)燃料电池属于环境友好型电池,该电池以空气中的氧气作氧化剂,氢氧化钠溶液作电解质,其负极的电极方程式:_____
(1)肼又名联氨,其结构式为
(2)液态肼与过氧化氢的反应属于
(3)写出该火箭推进器中相关反应的化学方程式:
(4)在一定温度下,向0.5L密闭容器中充入2molN2H4和2molO2发生如下反应:N2H4(g)+O2(g)⇌N2(g)+2H2O(g),其中有关物质的物质的量随时间变化的曲线如图所示,请回答下列问题:
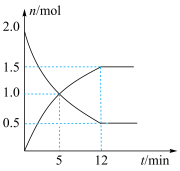
②下列能说明该反应达到平衡状态的是
A.υ正(N2)=2υ逆(H2O)
B.c(N2H4):c(O2):c(N2)=1:1:1
C.体系的压强不再发生变化
D.混合气体的密度不再发生变化
E.每断开1molO=O键,同时断开4molH-O键
③该反应达到平衡时,O2的体积百分数为
④下列措施能够增大正反应的化学反应速率的有
A.升高反应温度 B.加入适当的催化剂C.向容器中加入氧气 D.向容器中加入氖气
(5)广泛应用的肼(N2H4)燃料电池属于环境友好型电池,该电池以空气中的氧气作氧化剂,氢氧化钠溶液作电解质,其负极的电极方程式:
您最近一年使用:0次