1 . 工业废气中的NO可用来生产NH4NO3,工艺流程如图所示: ):n(
):n( )=1:1,下列说法错误的是
)=1:1,下列说法错误的是

 ):n(
):n( )=1:1,下列说法错误的是
)=1:1,下列说法错误的是A.装置Ⅰ中反应的离子方程式为2NO+4Ce4++3H2O=4Ce3++ + + +6H+ +6H+ |
| B.装置Ⅰ中若有5.6 L(标况)NO参与反应,则转移0.625 mol电子 |
| C.装置Ⅱ中的操作是电解,则阳极反应式为Ce3+-e-=Ce4+ |
| D.装置Ⅲ中反应的氧化剂是O2 |
您最近一年使用:0次
名校
2 . 高铁酸钾(K2FeO4)是一种新型多功能净水剂,强碱性条件下制取,干燥环境下冷藏。制备过程如图:
漂白粉与苏打 溶液1
溶液1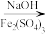 溶液2
溶液2 K2FeO4固体
K2FeO4固体
下列说法不正确 的是
漂白粉与苏打
 溶液1
溶液1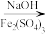 溶液2
溶液2 K2FeO4固体
K2FeO4固体下列说法
| A.高铁酸钾既能杀菌消毒、又有净水作用,净水作用与胶体的性质有关 |
B.溶液1→溶液2的离子方程式为:2Fe3++3ClO-+10OH-=2FeO +3Cl-+5H2O +3Cl-+5H2O |
| C.溶液2中加入KOH析出了K2FeO4固体,说明K2FeO4难溶于水 |
| D.高铁酸钾受热分解可放出氧气 |
您最近一年使用:0次
2021-06-30更新
|
852次组卷
|
4卷引用:山西省太原市第五十六中学2021-2022学年高三上学期第一次月考化学试题
山西省太原市第五十六中学2021-2022学年高三上学期第一次月考化学试题浙江省北斗星盟2021届高三下学期5月适应性联考化学试题黑龙江省双鸭山市第一中学2022届高三上学期开学考试化学试题(已下线)微专题14 氢氧化亚铁、高铁酸盐的制备实验探究-备战2023年高考化学一轮复习考点微专题
3 . 对废催化剂进行回收可有效利用金属资源。某废催化剂主要含铝( )、钼(
)、钼( )、镍(
)、镍( )等元素的氧化物,一种回收利用工艺的部分流程如下:
)等元素的氧化物,一种回收利用工艺的部分流程如下: 的
的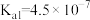 ,
, ;
;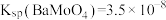 ;
;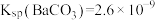 ;该工艺中,
;该工艺中,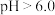 时,溶液中
时,溶液中 元素以
元素以 的形态存在。
的形态存在。
(1)“焙烧”中,有 生成,其中
生成,其中 元素的化合价为
元素的化合价为_______ 。
(2)“沉铝”中,生成的沉淀 为
为_______ 。
(3)“沉钼”中, 为7.0。
为7.0。
①生成 的离子方程式为
的离子方程式为_______ 。
②若条件控制不当, 也会沉淀。为避免
也会沉淀。为避免 中混入
中混入 沉淀,溶液中
沉淀,溶液中
_______ (列出算式)时,应停止加入 溶液。
溶液。
(4)①滤液Ⅲ中,主要存在的钠盐有 和
和 ,
, 为
为_______ 。
②往滤液Ⅲ中添加适量 固体后,通入足量
固体后,通入足量_______ (填化学式)气体,再通入足量 ,可析出
,可析出 。
。
(5)高纯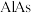 (砷化铝)可用于芯片制造。芯片制造中的一种刻蚀过程如图所示,图中所示致密保护膜为一种氧化物,可阻止
(砷化铝)可用于芯片制造。芯片制造中的一种刻蚀过程如图所示,图中所示致密保护膜为一种氧化物,可阻止 刻蚀液与下层
刻蚀液与下层 (砷化镓)反应。
(砷化镓)反应。_______ 。
②已知: 和
和 同族,
同族, 和
和 同族。在
同族。在 与上层
与上层 的反应中,
的反应中, 元素的化合价变为+5价,则该反应的氧化剂与还原剂物质的量之比为
元素的化合价变为+5价,则该反应的氧化剂与还原剂物质的量之比为_______ 。
 )、钼(
)、钼( )、镍(
)、镍( )等元素的氧化物,一种回收利用工艺的部分流程如下:
)等元素的氧化物,一种回收利用工艺的部分流程如下:
 的
的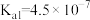 ,
, ;
;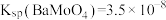 ;
;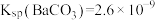 ;该工艺中,
;该工艺中,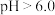 时,溶液中
时,溶液中 元素以
元素以 的形态存在。
的形态存在。(1)“焙烧”中,有
 生成,其中
生成,其中 元素的化合价为
元素的化合价为(2)“沉铝”中,生成的沉淀
 为
为(3)“沉钼”中,
 为7.0。
为7.0。①生成
 的离子方程式为
的离子方程式为②若条件控制不当,
 也会沉淀。为避免
也会沉淀。为避免 中混入
中混入 沉淀,溶液中
沉淀,溶液中
 溶液。
溶液。(4)①滤液Ⅲ中,主要存在的钠盐有
 和
和 ,
, 为
为②往滤液Ⅲ中添加适量
 固体后,通入足量
固体后,通入足量 ,可析出
,可析出 。
。(5)高纯
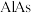 (砷化铝)可用于芯片制造。芯片制造中的一种刻蚀过程如图所示,图中所示致密保护膜为一种氧化物,可阻止
(砷化铝)可用于芯片制造。芯片制造中的一种刻蚀过程如图所示,图中所示致密保护膜为一种氧化物,可阻止 刻蚀液与下层
刻蚀液与下层 (砷化镓)反应。
(砷化镓)反应。
②已知:
 和
和 同族,
同族, 和
和 同族。在
同族。在 与上层
与上层 的反应中,
的反应中, 元素的化合价变为+5价,则该反应的氧化剂与还原剂物质的量之比为
元素的化合价变为+5价,则该反应的氧化剂与还原剂物质的量之比为
您最近一年使用:0次
2021-06-11更新
|
14337次组卷
|
27卷引用:山西省晋中市祁县中学2022-2023学年高三上学期10月月考化学试题
山西省晋中市祁县中学2022-2023学年高三上学期10月月考化学试题2021年新高考广东化学高考真题(已下线)微专题31 化学工艺流程题——原料的预处理-备战2022年高考化学考点微专题(已下线)考点14 铝及其化合物-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点14 铝及其化合物-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)考向09 工艺流程初探-备战2022年高考化学一轮复习考点微专题重庆市缙云教育联盟2021-2022学年高三9月月度质量检测化学试题2021年广东省高考化学试卷变式题11-21(已下线)解密06 金属及其化合物(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)解密06 金属及其化合物(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)专题15 工艺流程综合题-2022年高考化学二轮复习重点专题常考点突破练(已下线)专题11 无机工艺流程题—2022年高考化学二轮复习讲练测(全国版)-练习(已下线)押新高考卷14题 工艺流程综合题-备战2022年高考化学临考题号押题(新高考通版)(已下线)回归教材重难点08 化学工艺流程分析-【查漏补缺】2022年高考化学三轮冲刺过关(新高考专用)(已下线)微专题16 热点金属及其化合物制备流程(Li、Sr、Pb、Zn、Ti、Mo)-备战2023年高考化学一轮复习考点微专题(已下线)考点15 铝及其化合物-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)微专题25 化学工艺流程题-----原料的预处理-备战2023年高考化学一轮复习考点微专题(已下线)微专题26 化学工艺流程题-----核心反应与条件控制-备战2023年高考化学一轮复习考点微专题内蒙古呼伦贝尔市海拉尔第二中学2022届高三第四次模拟考试理科综合化学试题山东省临沂市兰陵县第四中学2021-2022学年高三12月月考化学试题(已下线)易错点08 金属材料-备战2023年高考化学考试易错题(已下线)专题18 工艺流程题(已下线)专题18 工艺流程题(已下线)专题13 工艺流程综合题-2023年高考化学真题题源解密(新高考专用)(已下线)考点47 无机工艺流程(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)微专题 无机化工流程题的解题策略2024届黑龙江省齐齐哈尔市高三下学期联合考试模拟预测化学试题
4 .  常用作食盐中的补碘剂,可用“氯酸钾氧化法”制备,该方法的第一步反应为
常用作食盐中的补碘剂,可用“氯酸钾氧化法”制备,该方法的第一步反应为 。下列说法错误的是
。下列说法错误的是
 常用作食盐中的补碘剂,可用“氯酸钾氧化法”制备,该方法的第一步反应为
常用作食盐中的补碘剂,可用“氯酸钾氧化法”制备,该方法的第一步反应为 。下列说法错误的是
。下列说法错误的是A.产生22.4L(标准状况) 时,反应中转移 时,反应中转移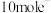 |
| B.反应中氧化剂和还原剂的物质的量之比为11:6 |
C.可用石灰乳吸收反应产生的 制备漂白粉 制备漂白粉 |
D.可用酸化的淀粉碘化钾溶液检验食盐中 的存在 的存在 |
您最近一年使用:0次
2021-06-09更新
|
15633次组卷
|
75卷引用:山西省运城市2021-2022学年高三上学期期中考试化学试题
山西省运城市2021-2022学年高三上学期期中考试化学试题2021年新高考湖南化学高考真题河北省辛集中学 2020-2021学年高二下学期期末考试化学试题(已下线)课时09 氧化还原反应概念及应用-2022年高考化学一轮复习小题多维练(全国通用)(已下线)考向05 氧化还原反应-备战2022年高考化学一轮复习考点微专题(已下线)考点05 氧化还原反应-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点05 氧化还原反应-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)专题11 富集在海水中的元素——氯 (热点讲义)-2022年高三毕业班化学常考点归纳与变式演练(已下线)第5讲 氧化还原反应(讲)— 2022年高考化学一轮复习讲练测(新教材新高考)山东省济宁市实验中学2022届高三上学期开学考试化学试题湖南省邵阳邵东市第一中学2022届高三上学期第一次月考化学试题安徽省合肥市第九中学2022届高三第一次阶段测验化学试卷江西省赣州市第十四中学2022届高三上学期第二次月考化学试题北京市第二十中学2021-2022学年高一上学期期中考试化学试题(已下线)考点04 氧化还原反应-备战2022年高考化学学霸纠错(全国通用)吉林省东北师范大学附属中学2021-2022学年高三上学期一模考试化学试题甘肃省天水市第一中学2021-2022高三上学期第三次考试化学试题天津市第一中学2021-2022学年高三上学期第二次月考化学试题2021年湖南省高考化学试卷变式题1-10(已下线)解密03 氧化还原反应(分层训练)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)解密03 氧化还原反应(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)湖南省湘潭凤凰中学2021-2022学年高一上学期12月月考化学试题(已下线)解密03 氧化还原反应(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)河南省名校联盟2021-2022学年高三上学期第三次诊断考试化学试题辽宁省凌源市2021-2022学年高三下学期高三开学考试化学试题河南省顶尖名校联盟2021-2022学年高二下学期联赛考试化学试题(已下线)卷06 氧化还原-【小题小卷】冲刺2022年高考化学小题限时集训(全国卷专用)(已下线)查补易混易错点05 氧化还原反应-【查漏补缺】2022年高考化学三轮冲刺过关(新高考专用)(已下线)查补易混易错点05 氧化还原反应-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)(已下线)押新高考卷10题 氧化还原反应-备战2022年高考化学临考题号押题(新高考通版)(已下线)专题04 氧化还原反应-三年(2020-2022)高考真题分项汇编(已下线)微专题10 “守恒法”在氧化还原反应计算中的应用-备战2023年高考化学一轮复习考点微专题(已下线)考点05 氧化还原反应-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第03讲 氧化还原反应(讲)-2023年高考化学一轮复习讲练测(新教材新高考)河南省濮阳市第一高级中学2023届高三第一次质量检测化学试题陕西省西安市长安区第一中学2021-2022学年高二下学期期末考试化学试题(已下线)第03练 氧化还原反应-2023年高考化学一轮复习小题多维练(全国通用)(已下线)微专题30 非金属及其化合物制备流程与实验探究(S、Se、Te、Cl、Br、I)-备战2023年高考化学一轮复习考点微专题第二章 海水中的重要元素——钠和氯 ★综合拔高练江苏省南通市通州区金沙中学2021-2022学年高一上学期1月学业水平调研化学试题四川省广元市树人中学2021-2022学年高三上学期第二次段考化学试题江西省瑞金市第二中学2022-2023学年高三上学期开学考试化学试题江西省赣州市赣县第三中学2022-2023学年高三上学期(奥赛班)强化训练化学试题湖南省常德市桃源县第一中学2022-2023学年高三上学期9月月考化学试题河北省石家庄市第四中学2022-2023学年高三上学期十月月考化学试题安徽省六安市新安中学2022-2023学年高三上学期第二次月考化学试题(已下线)易错点09 氯元素及其化合物-备战2023年高考化学考试易错题湖南省郴州市汝城县第一中学2022-2023学年高一上学期期中考试化学试题湖南省长沙市同升湖实验学校2022-2023学年高三上学期第三次月考化学试题安徽省宿城第一中学2022-2023学年高一上学期阶段检测化学试题(已下线)专题04 氧化还原反应及其应用(讲)-2023年高考化学二轮复习讲练测(新高考专用)广西钟山县钟山中学2021-2022学年高二上学期第一次(9月)月考化学(文科)试题湖南省株洲市九方中学2022-2023学年高一上学期第三次月考化学试题(已下线)专题07 氧化还原反应分析-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)专题卷07 氧化还原反应的概念、规律及应用-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)(已下线)专题09 氧化还原反应(已下线)专题09 氧化还原反应(已下线)第5讲 氧化还原反应方程式的配平与计算(已下线)第05练 氧化还原反应的综合考查-2023年【暑假分层作业】高二化学(2024届一轮复习通用)(已下线)【知识图鉴】单元讲练测必修第一册第一单元03巩固练(已下线)考点04 氧化还原反应的基本概念和规律(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)(已下线)考点09 氯及其化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)考点05 氧化还原反应(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)专题04 氧化还原反应-2023年高考化学真题题源解密(全国通用)(已下线)专题05 氧化还原反应及其计算-2023年高考化学真题题源解密(新高考专用)云南省开远市第一中学校2022-2023学年高二下学期5月月考化学试题广东省台山市第一中学2023-2024学年高三上学期第一次月考化学试题广东省东莞市光正实验学校2023-2024学年高三上学期第一次月考化学试题吉林省长春外国语学校2023-2024学年高三上学期9月月考化学试题北京工业大学附属中学2022-2023学年高三上学期开学测试化学试题辽宁省沈阳市新民市高级中学2023-2024学年高三上学期10月月考化学试题广东省惠州市博罗县博师高级中学2023-2024学年高三上学期9月月考化学试题福建省厦门第六中学2023-2024学年高一上学期1月月考化学试题甘肃省天水市甘谷县第三中学2023-2024学年高一上学期12月第三次月考化学试卷(已下线)第05讲 氧化还原反应方程式的配平、书写及计算(讲义)-【上好课】2025年高考化学一轮复习讲练测(新教材新高考)
解题方法
5 . K2Cr2O7中学化学重要氧化剂。从废料(含Cr3+、Al3+、Fe2+、Fe3+和Cu2+等)提取重铬酸钾的流程如下:

已知:Cr(OH)3是两性氢氧化物。
回答下列问题:
(1)“氧化1”中加入水、双氧水和稀硫酸调节pH=1,双氧水的作用是_______ ,为了提高反应速率,适当加热,但是温度不宜过高,其原因是_______ 。
(2)“除杂1”加入过量NaOH溶液,过滤,得到滤渣成分是_______ (填化学式)。将滤渣溶于过量氨水、_______ (填实验步骤)得到铁红。
(3)“氧化2”中通入氯气,写出离子方程式:_______ 。
(4)“除杂2”中向含AlO ,CrO
,CrO 的溶液通入过量CO2,CO2的作用是
的溶液通入过量CO2,CO2的作用是_______ 。不能用稀硫酸替代CO2,原因是_______ 。
(5)“结晶”析出Na2Cr2O7,在饱和Na2Cr2O7溶液中加入KCl粉末,Na2Cr2O7转化成K2Cr2O7晶体(两种氯化物留在母液中),预测:Ksp(K2Cr2O7)_______ Ksp(Na2Cr2O7)(填“>”“<”或“=”)。
(6)100kg废料(含铬质量分数为5.2%铬元素)经上述转化制得8.82kgK2Cr2O7,铬元素转化率为_______ 。

已知:Cr(OH)3是两性氢氧化物。
回答下列问题:
(1)“氧化1”中加入水、双氧水和稀硫酸调节pH=1,双氧水的作用是
(2)“除杂1”加入过量NaOH溶液,过滤,得到滤渣成分是
(3)“氧化2”中通入氯气,写出离子方程式:
(4)“除杂2”中向含AlO
 ,CrO
,CrO 的溶液通入过量CO2,CO2的作用是
的溶液通入过量CO2,CO2的作用是(5)“结晶”析出Na2Cr2O7,在饱和Na2Cr2O7溶液中加入KCl粉末,Na2Cr2O7转化成K2Cr2O7晶体(两种氯化物留在母液中),预测:Ksp(K2Cr2O7)
(6)100kg废料(含铬质量分数为5.2%铬元素)经上述转化制得8.82kgK2Cr2O7,铬元素转化率为
您最近一年使用:0次
6 . 皮蛋,又称松花蛋,因其独特的口味,是不少市民心爱的食物。传统皮蛋的主要原料有生石灰、纯碱、食盐、红茶、植物灰等。央视曝光了某皮蛋生产企业使用工业硫酸铜“炮制”皮蛋,工业硫酸铜中含有大量重金属。

硫酸铜是重要的工业原料。对下列有关硫酸铜的制备方法进行讨论。
查阅资料可知:铜在低温下不能和O2发生反应,也不能和稀硫酸共热发生反应。
(1)工业上是将废铜屑倒入热的稀硫酸中并不断地通入空气来制取CuSO4溶液的。写出铜屑在此状态下发生的一系列反应的化学方程式:___________ 。
(2)利用铜和浓硫酸在加热条件下反应也能制备CuSO4溶液,在该反应中硫酸表现出___________ ,氧化剂与还原剂的物质的量之比是___________ 。写出反应的化学方程式:___________ 。
(3)试分析以上两种方法哪种好,说明原因:___________ 。

硫酸铜是重要的工业原料。对下列有关硫酸铜的制备方法进行讨论。
查阅资料可知:铜在低温下不能和O2发生反应,也不能和稀硫酸共热发生反应。
(1)工业上是将废铜屑倒入热的稀硫酸中并不断地通入空气来制取CuSO4溶液的。写出铜屑在此状态下发生的一系列反应的化学方程式:
(2)利用铜和浓硫酸在加热条件下反应也能制备CuSO4溶液,在该反应中硫酸表现出
(3)试分析以上两种方法哪种好,说明原因:
您最近一年使用:0次
20-21高一下·浙江·阶段练习
7 . 已知反应S+K2SO3=K2S2O3(硫代硫酸钾),下列说法的不正确的是
| A.K2S2O3在氧气中加热的产物为K2SO4和SO3 |
B.K2S2O3与氯水反应的离子方程式:5H2O+4Cl2+ =10H++8C1-+2 =10H++8C1-+2 |
| C.向碳酸钾和硫化钾混合溶液中通入一定量的二氧化硫也可以制得硫代硫酸钾 |
| D.K2S2O3与稀硫酸反应生成硫,二氧化硫、硫酸钾和水 |
您最近一年使用:0次
8 . 下列说法正确的是
A. 可与 可与 完全反应生成 完全反应生成 |
B. 即可作氧化剂又可作还原剂 即可作氧化剂又可作还原剂 |
| C.二氧化硫具有漂白性,能使品红溶液和紫色石蕊试液褪色 |
| D.陶瓷餐具、混凝土桥墩、水晶镜片都使用了硅酸盐材料 |
您最近一年使用:0次
2021-05-21更新
|
118次组卷
|
2卷引用:山西省怀仁市2020-2021学年高一下学期期中化学试题
名校
9 . 全钒液流氧化还原电池被认为是最具有应用前景的绿色储能电池。通常钒电池主要采用硫酸氧钒(VOSO4)溶液作为电池的电解质溶液,用V2O5制备硫酸氧钒的方法如下:

已知在溶液中钒以VO 、VO2+等形式存在。下列相关说法不正确的是
、VO2+等形式存在。下列相关说法不正确的是

已知在溶液中钒以VO
 、VO2+等形式存在。下列相关说法不正确的是
、VO2+等形式存在。下列相关说法不正确的是| A.加入硫酸过程并加热的目的是加快V2O5溶解速率 |
| B.用FeSO4代替草酸不会对产品造成影响 |
C.加入草酸发生反应的离子方程式为 |
| D.操作1的名称为加热浓缩、冷却结晶 |
您最近一年使用:0次
2021-05-04更新
|
480次组卷
|
3卷引用:山西省怀仁市第一中学2021-2022学年高三上学期第二次月考理科综合化学试题
山西省怀仁市第一中学2021-2022学年高三上学期第二次月考理科综合化学试题山东省菏泽市2021届4月高三联考(二模)化学试题(已下线)专题12 工艺流程选择题-备战2022年高考化学真题及地市好题专项集训【山东专用】
10 . 将硫粉和铁粉均匀混合,放在石棉网上堆成条状,用灼热的玻璃棒触及混合粉末的一端,当混合物呈红热状态时,移开玻璃棒。下列有关叙述错误的是


| A.反应生成Fe2S3 |
| B.该反应为放热反应 |
| C.该反应中的氧化剂是S |
| D.1molS参加该反应转移2mol电子 |
您最近一年使用:0次



