解题方法
1 .  用于制三价铬盐及三氧化二铬,也用于油漆颜料及羊毛处理等。下图是制备
用于制三价铬盐及三氧化二铬,也用于油漆颜料及羊毛处理等。下图是制备 的一种路径,已知焙烧后
的一种路径,已知焙烧后 元素以+6价形式存在。下列说法正确的是
元素以+6价形式存在。下列说法正确的是
 用于制三价铬盐及三氧化二铬,也用于油漆颜料及羊毛处理等。下图是制备
用于制三价铬盐及三氧化二铬,也用于油漆颜料及羊毛处理等。下图是制备 的一种路径,已知焙烧后
的一种路径,已知焙烧后 元素以+6价形式存在。下列说法正确的是
元素以+6价形式存在。下列说法正确的是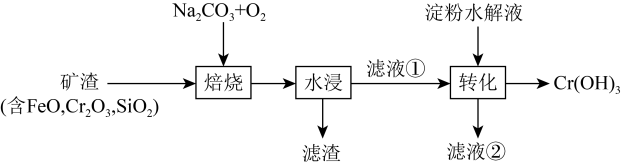
| A.若在实验室中进行“焙烧”,可选择陶瓷坩埚作反应容器 |
B.“焙烧”时 参与的转化反应可能是 参与的转化反应可能是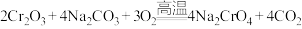 |
C.滤渣的主要成分为 |
| D.“转化”时,淀粉水解液中的葡萄糖做氧化剂 |
您最近一年使用:0次
2 . 镍、钴均是一种重要的战略资源,广泛应用于飞机发动机、锂离子电池等领域。以红土镍矿常压盐酸浸液(含 、
、 、
、 、
、 、
、 和
和 )为原料提取Ni、Co。工艺流程如下:
)为原料提取Ni、Co。工艺流程如下:
回答下列问题:
(1)滤渣1的成分是 、
、___________ 。
(2)“调 ”时,发生反应的主要化学方程式为
”时,发生反应的主要化学方程式为___________ 。
(3)“碱性氧化”时,由 转化为
转化为 的离子方程式为
的离子方程式为___________ ,常温下,若pH控制为9,则溶液中 浓度最多为
浓度最多为___________ mol·L 。
。
(4)“析晶”时,通入的酸性气体A为___________ (化学式)。
(5)①“电解”时Ni在___________ (“阴”或“阳”)极析出。
②Ni可以进一步制备超导体 ,其立方晶胞如图。C与Ni最小间距小于Ni与Mg最小间距,x为整数,则Ni在晶胞中的位置为
,其立方晶胞如图。C与Ni最小间距小于Ni与Mg最小间距,x为整数,则Ni在晶胞中的位置为___________ (“顶点”“面心”或“体心”),晶体中一个C周围与其最近的Ni的个数为___________ 。
 、
、 、
、 、
、 、
、 和
和 )为原料提取Ni、Co。工艺流程如下:
)为原料提取Ni、Co。工艺流程如下: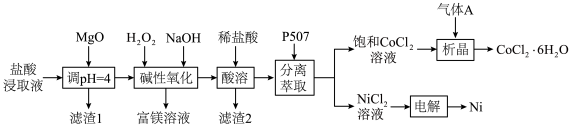
| 物质 |  |  |  |  |  |  |
 |  | 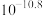 | 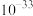 | 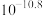 |  |  |
(1)滤渣1的成分是
 、
、(2)“调
 ”时,发生反应的主要化学方程式为
”时,发生反应的主要化学方程式为(3)“碱性氧化”时,由
 转化为
转化为 的离子方程式为
的离子方程式为 浓度最多为
浓度最多为 。
。(4)“析晶”时,通入的酸性气体A为
(5)①“电解”时Ni在
②Ni可以进一步制备超导体
 ,其立方晶胞如图。C与Ni最小间距小于Ni与Mg最小间距,x为整数,则Ni在晶胞中的位置为
,其立方晶胞如图。C与Ni最小间距小于Ni与Mg最小间距,x为整数,则Ni在晶胞中的位置为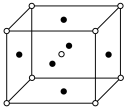
您最近一年使用:0次
3 . 四氧化三铁俗称磁性氧化铁,常用于制造录音磁带和电讯器材,也可作颜料和抛光剂。某工厂以硫铁矿烧渣(主要含有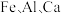 等元素的氧化物及
等元素的氧化物及 )为原料,制备
)为原料,制备 的工艺流程如图所示。
的工艺流程如图所示。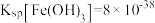 、
、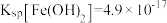 、
、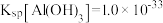 。
。
回答下列问题:
(1)“酸溶”硫铁矿烧渣时,为了加快酸溶速率可采取的措施有___________ (任写两条)。
(2)料渣1的主要成分有___________ (填化学式)。
(3)常温下,已知溶液中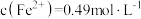 ,要使
,要使 沉淀完全,则“调
沉淀完全,则“调 ”的范围是
”的范围是___________ (保留2位有效数字,一般离子浓度 认为沉淀完全)。
认为沉淀完全)。
(4)加入 “沉铁”时,发生反应的离子方程式为
“沉铁”时,发生反应的离子方程式为___________ 。
(5)①“煅烧1”的目的是将 转化为
转化为 ,若“煅烧2”阶段发生反应时
,若“煅烧2”阶段发生反应时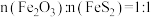 ,则该反应的化学方程式为
,则该反应的化学方程式为___________ 。
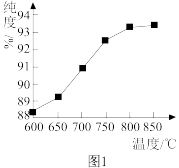
②“煅烧2”时温度对 的纯度有很大影响。已知温度对
的纯度有很大影响。已知温度对 纯度的影响如图1所示,则“煅烧2”时,温度最好控制在
纯度的影响如图1所示,则“煅烧2”时,温度最好控制在___________  。
。 )的晶胞如图2所示。已知:该晶胞底边边长为
)的晶胞如图2所示。已知:该晶胞底边边长为 ,高为
,高为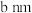 ,l号原子的高为
,l号原子的高为 。
。 为阿伏加德罗常数的值。
为阿伏加德罗常数的值。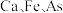 原子的个数之比为
原子的个数之比为___________ ;距2号原子最近的铁有___________ 个。
②该晶体的密度为___________  ,1号原子的坐标为
,1号原子的坐标为___________ 。
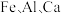 等元素的氧化物及
等元素的氧化物及 )为原料,制备
)为原料,制备 的工艺流程如图所示。
的工艺流程如图所示。
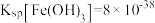 、
、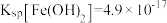 、
、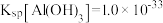 。
。回答下列问题:
(1)“酸溶”硫铁矿烧渣时,为了加快酸溶速率可采取的措施有
(2)料渣1的主要成分有
(3)常温下,已知溶液中
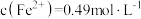 ,要使
,要使 沉淀完全,则“调
沉淀完全,则“调 ”的范围是
”的范围是 认为沉淀完全)。
认为沉淀完全)。(4)加入
 “沉铁”时,发生反应的离子方程式为
“沉铁”时,发生反应的离子方程式为(5)①“煅烧1”的目的是将
 转化为
转化为 ,若“煅烧2”阶段发生反应时
,若“煅烧2”阶段发生反应时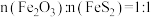 ,则该反应的化学方程式为
,则该反应的化学方程式为②“煅烧2”时温度对
 的纯度有很大影响。已知温度对
的纯度有很大影响。已知温度对 纯度的影响如图1所示,则“煅烧2”时,温度最好控制在
纯度的影响如图1所示,则“煅烧2”时,温度最好控制在 。
。
 )的晶胞如图2所示。已知:该晶胞底边边长为
)的晶胞如图2所示。已知:该晶胞底边边长为 ,高为
,高为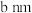 ,l号原子的高为
,l号原子的高为 。
。 为阿伏加德罗常数的值。
为阿伏加德罗常数的值。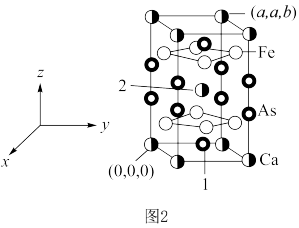
 原子的个数之比为
原子的个数之比为②该晶体的密度为
 ,1号原子的坐标为
,1号原子的坐标为
您最近一年使用:0次
解题方法
4 . 一种从含银废催化剂[其主要成分为银和铼( ),还含有
),还含有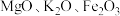 和
和 ]中回收银和铼的工艺流程如图所示。下列说法错误的是
]中回收银和铼的工艺流程如图所示。下列说法错误的是
 ),还含有
),还含有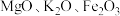 和
和 ]中回收银和铼的工艺流程如图所示。下列说法错误的是
]中回收银和铼的工艺流程如图所示。下列说法错误的是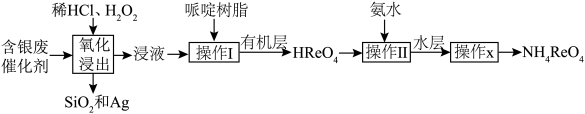
A.“氧化浸出”过程中铼被氧化,该反应中氧化剂与还原剂物质的量之比为 |
B.实验室中完成“操作 ”和“操作 ”和“操作 ”所需要的玻璃仪器主要有烧杯和分液漏斗 ”所需要的玻璃仪器主要有烧杯和分液漏斗 |
| C.“操作x”为结晶过程,该过程不可选用蒸发结晶,应选用降温结晶 |
D.“操作 ”过程中为加快反应速率,可在高温条件下进行 ”过程中为加快反应速率,可在高温条件下进行 |
您最近一年使用:0次
名校
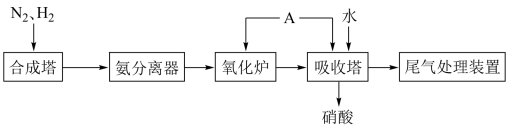
5 . 硝酸是重要的化工原料。工业制硝酸的原理示意图可简略表示如下(反应条件和部分生成物已略去):___________ 。
(2)物质A是___________ 。向吸收塔中通入A的作用是___________ 。
(3)硝酸能溶解铜,请写出铜和稀硝酸反应的离子方程式:___________ ,在该反应中硝酸体现了___________ 性。
(4)用绿色氧化剂(10%H2O2和20%稀硝酸的混合液)溶解铜,基本无氮氧化物排放,写出Cu与绿色氧化剂反应的离子反应方程式___________ 。
(5)硝酸工业尾气中的 会造成光化学烟雾和酸雨,污染环境,可用碱性溶液吸收。已知
会造成光化学烟雾和酸雨,污染环境,可用碱性溶液吸收。已知 用碳酸钠溶液吸收时会生成CO2、
用碳酸钠溶液吸收时会生成CO2、 和另一种化合物,写出反应的离子方程式
和另一种化合物,写出反应的离子方程式___________ 。
(2)物质A是
(3)硝酸能溶解铜,请写出铜和稀硝酸反应的离子方程式:
(4)用绿色氧化剂(10%H2O2和20%稀硝酸的混合液)溶解铜,基本无氮氧化物排放,写出Cu与绿色氧化剂反应的离子反应方程式
(5)硝酸工业尾气中的
 会造成光化学烟雾和酸雨,污染环境,可用碱性溶液吸收。已知
会造成光化学烟雾和酸雨,污染环境,可用碱性溶液吸收。已知 用碳酸钠溶液吸收时会生成CO2、
用碳酸钠溶液吸收时会生成CO2、 和另一种化合物,写出反应的离子方程式
和另一种化合物,写出反应的离子方程式
您最近一年使用:0次
名校
解题方法
6 . 以废旧锌锰干电池的炭包(含炭粉、 、
、 和少量
和少量 、
、 等物质)为原料,从中回收
等物质)为原料,从中回收 的工艺流程如下:
的工艺流程如下:
(1)“酸浸”时需将结块的炭包粉碎,目的是_______ 。
(2)“酸浸”过程中, 与稀硝酸反应的离子方程式为
与稀硝酸反应的离子方程式为_______ ,该反应中氧化剂和还原剂的物质的量之比为_______ 。
(3)“溶解”时加入 的作用是
的作用是_______ , 的实际消耗量比理论值高的原因
的实际消耗量比理论值高的原因_______ 。
(4)写出“焙烧”过程的化学反应方程式为_______ 。
(5)碱性锌锰干电池是一种使用广泛的便携式电源,结构如图所示。其电池总反应为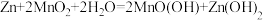 。
。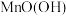 中
中 的化合价为
的化合价为_______ 。
②该电池工作时,负极的反应式为_______ 。
 、
、 和少量
和少量 、
、 等物质)为原料,从中回收
等物质)为原料,从中回收 的工艺流程如下:
的工艺流程如下: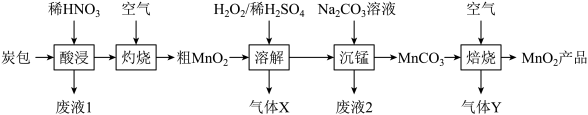
(1)“酸浸”时需将结块的炭包粉碎,目的是
(2)“酸浸”过程中,
 与稀硝酸反应的离子方程式为
与稀硝酸反应的离子方程式为(3)“溶解”时加入
 的作用是
的作用是 的实际消耗量比理论值高的原因
的实际消耗量比理论值高的原因(4)写出“焙烧”过程的化学反应方程式为
(5)碱性锌锰干电池是一种使用广泛的便携式电源,结构如图所示。其电池总反应为
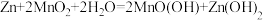 。
。
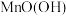 中
中 的化合价为
的化合价为②该电池工作时,负极的反应式为
您最近一年使用:0次
名校
解题方法
7 . 零价铝是一种应用于环境修复的极有潜力的两性金属材料。构建微观腐蚀原电池体系(如图),实现了零价铝在近中性溶液中处理硝酸盐。下列叙述正确的是
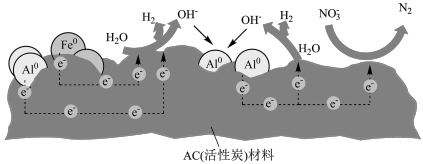
A. 在 在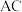 电极上发生氧化反应 电极上发生氧化反应 |
B.生成 的电极反应式: 的电极反应式: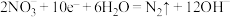 |
C.若 表面生成了致密的 表面生成了致密的 ,能提高去除率 ,能提高去除率 |
D.生成等物质的量的 和 和 ,转移的电子数之比为1∶5 ,转移的电子数之比为1∶5 |
您最近一年使用:0次
2024-04-16更新
|
565次组卷
|
4卷引用:贵州省安顺市部分学校2024届高三下学期二模考试化学试题
贵州省安顺市部分学校2024届高三下学期二模考试化学试题辽宁省锦州市渤海大学附属高级中学2023-2024学年高三下学期3月摸底考试化学试题河北省邢台市五岳联盟2024届高三下学期模拟预测化学试题(已下线)通关练01 化学基本概念再回归-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)
名校
8 . 已知:① ,②
,②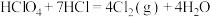 。
。 为阿伏加德罗常数的值。下列叙述正确的是
为阿伏加德罗常数的值。下列叙述正确的是
 ,②
,②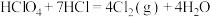 。
。 为阿伏加德罗常数的值。下列叙述正确的是
为阿伏加德罗常数的值。下列叙述正确的是A.反应①中物质的氧化性: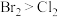 |
B.标准状况下,11.2L 参与反应时转移的电子数为5NA 参与反应时转移的电子数为5NA |
C.1L0.5  溶液含有的 溶液含有的 分子数为0.5 分子数为0.5 |
D.反应②生成28.4g 时,还原产物分子数为0.05 时,还原产物分子数为0.05 |
您最近一年使用:0次
2024-04-16更新
|
639次组卷
|
4卷引用:贵州省安顺市部分学校2024届高三下学期二模考试化学试题
贵州省安顺市部分学校2024届高三下学期二模考试化学试题辽宁省锦州市渤海大学附属高级中学2023-2024学年高三下学期3月摸底考试化学试题河北省邢台市五岳联盟2024届高三下学期模拟预测化学试题(已下线)通关练01 化学基本概念再回归-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)
解题方法
9 . 偏磷酸钡Ba(PO3)2具有耐高温、透光性良好等性能,是制备磷酸盐光学玻璃的基础物质。利用湿法磷酸(主要成分为H3PO4,含有少量Mg2+、Fe3+、 、
、 等杂质)制备偏磷酸钡的一种工艺的主要流程如图所示:
等杂质)制备偏磷酸钡的一种工艺的主要流程如图所示: 时:①
时:①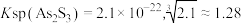 ;
;
②将NH3通入H3PO4溶液中,当pH=3.8~4.5时生成NH4H2PO4,pH=8.0~8.2时生成(NH4)2HPO4。
回答下列问题:
(1)“滤渣1”中含硫化合物的化学式为___________ 。
(2)“滤渣2”的主要成分有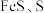 及
及 ,其中生成
,其中生成 的离子方程式为
的离子方程式为___________ ; 下,当
下,当 沉淀完全时,
沉淀完全时, 至少为
至少为___________  [当
[当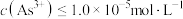 时认为沉淀完全]。
时认为沉淀完全]。
(3)“氨化”的目的之一是通入NH3调节溶液的pH,当溶液pH为4.3时H3PO4转化为___________ (填化学式)。
(4)“脱镁”的目的是生成MgF2沉淀除去Mg2+。若将流程中“氨化”与“脱镁”交换,Mg2+沉淀不完全,原因是___________ 。
(5)“结晶”后得到 晶体,“煅烧”时生成
晶体,“煅烧”时生成 和
和 等物质,其反应的化学方程式为
等物质,其反应的化学方程式为___________ ;比较 键角:
键角: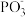
_________  (选填“
(选填“ ”“
”“ ”或“
”或“ ”),其原因是
”),其原因是___________ 。
 、
、 等杂质)制备偏磷酸钡的一种工艺的主要流程如图所示:
等杂质)制备偏磷酸钡的一种工艺的主要流程如图所示:
 时:①
时:①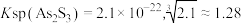 ;
;②将NH3通入H3PO4溶液中,当pH=3.8~4.5时生成NH4H2PO4,pH=8.0~8.2时生成(NH4)2HPO4。
回答下列问题:
(1)“滤渣1”中含硫化合物的化学式为
(2)“滤渣2”的主要成分有
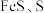 及
及 ,其中生成
,其中生成 的离子方程式为
的离子方程式为 下,当
下,当 沉淀完全时,
沉淀完全时, 至少为
至少为 [当
[当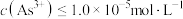 时认为沉淀完全]。
时认为沉淀完全]。(3)“氨化”的目的之一是通入NH3调节溶液的pH,当溶液pH为4.3时H3PO4转化为
(4)“脱镁”的目的是生成MgF2沉淀除去Mg2+。若将流程中“氨化”与“脱镁”交换,Mg2+沉淀不完全,原因是
(5)“结晶”后得到
 晶体,“煅烧”时生成
晶体,“煅烧”时生成 和
和 等物质,其反应的化学方程式为
等物质,其反应的化学方程式为 键角:
键角: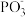
 (选填“
(选填“ ”“
”“ ”或“
”或“ ”),其原因是
”),其原因是
您最近一年使用:0次
2024-04-15更新
|
199次组卷
|
2卷引用:2024届贵州省高三下学期二模化学试题
10 . 工业上可用反应 制备
制备 粗品,进而制取高纯硅。下列说法正确的是
粗品,进而制取高纯硅。下列说法正确的是 为阿伏加德罗常数的值)
为阿伏加德罗常数的值)
 制备
制备 粗品,进而制取高纯硅。下列说法正确的是
粗品,进而制取高纯硅。下列说法正确的是 为阿伏加德罗常数的值)
为阿伏加德罗常数的值)| A.晶体硅属于分子晶体 |
B.用原子轨道描述氢原子形成氢分子的过程示意图: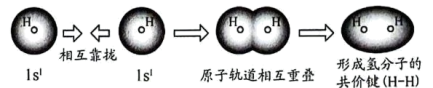 |
C.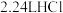 中含有分子的数目为 中含有分子的数目为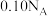 |
D.每生成 转移电子数目为 转移电子数目为 |
您最近一年使用:0次
2024-04-15更新
|
123次组卷
|
2卷引用:2024届贵州省高三下学期二模化学试题



