解题方法
1 . 以菱锰矿(主要成分为MnCO3,还含有铁、镍的碳酸盐以及SiO2杂质)为原料生产次锰酸钠(Na3MnO4)的工艺流程如图:
(1)次锰酸钠中Mn的化合价为___________ ;滤渣1的主要成分为MnO2和___________ (填化学式)。
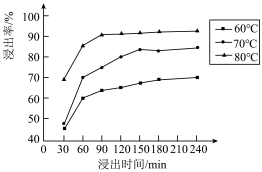
(2)锰的浸出率结果如图所示。由图可知,所采用的最佳实验条件为___________ 。___________ 。
(4)“除镍”步骤发生的反应为:MnS(s)+Ni2+(aq)=NiS(s)+Mn2+(aq)。反应的平衡常数K=___________ 。
(5)“母液1”中主要溶质的用途___________ 。
(6)煅烧产物MnO2在“共熔”过程中,反应得到Na2MnO4及一种单质气体,则该反应的化学方程式为___________ 。
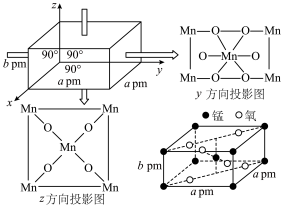
(7)某MnxO,四方晶胞结构及其投影如图所示,该晶胞由O2-和Mn3+构成。___________ ,Mn与Mn之间最近(顶点和体心)距离为___________ pm。(用含a、b的代数式表示)

| 物质 | MnS | NiS |
| Ksp | 2.0×10-13 | 1.0×10-21 |
(1)次锰酸钠中Mn的化合价为
(2)锰的浸出率结果如图所示。由图可知,所采用的最佳实验条件为
(4)“除镍”步骤发生的反应为:MnS(s)+Ni2+(aq)=NiS(s)+Mn2+(aq)。反应的平衡常数K=
(5)“母液1”中主要溶质的用途
(6)煅烧产物MnO2在“共熔”过程中,反应得到Na2MnO4及一种单质气体,则该反应的化学方程式为
(7)某MnxO,四方晶胞结构及其投影如图所示,该晶胞由O2-和Mn3+构成。
您最近一年使用:0次
名校
2 . 学以致用是学习化学的动力和源泉,掌握化学知识有助于我们更好地认识世界。回答下列问题:
(1)云、雾属于胶体,鉴别胶体和溶液的方法是______ ,胶体和溶液的本质区别是_______ 。
(2)生铁是______ (填“混合物”或“化合物”)。通常合金的熔点_____ (填“高于”或“低于”)其组成单质的熔点。
(3)ClO2是一种新型含氯消毒剂,已经用于自来水消毒。实验室可通过以下反应制得: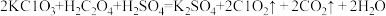 。产生1molC1O2时,转移电子的物质的量为
。产生1molC1O2时,转移电子的物质的量为______ mol;该反应中的还原剂是______ (填化学式)。
(4)在标准状况下,由CO2和CO组成的混合气体的密度是H2的19倍,则两者体积比V(CO2):V(CO)=____ 。
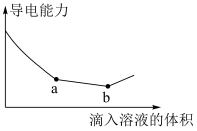
(5)Ba(OH)2溶液中滴入浓度相等的NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如图所示。从开始到a点总的离子方程式是______ ,从a点到b点反应的离子方程式是______ ,解释b点之后导电能力上升的原因:______ 。
(1)云、雾属于胶体,鉴别胶体和溶液的方法是
(2)生铁是
(3)ClO2是一种新型含氯消毒剂,已经用于自来水消毒。实验室可通过以下反应制得:
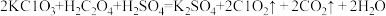 。产生1molC1O2时,转移电子的物质的量为
。产生1molC1O2时,转移电子的物质的量为(4)在标准状况下,由CO2和CO组成的混合气体的密度是H2的19倍,则两者体积比V(CO2):V(CO)=
(5)Ba(OH)2溶液中滴入浓度相等的NaHSO4溶液,其导电能力随滴入溶液体积变化的曲线如图所示。从开始到a点总的离子方程式是
您最近一年使用:0次
2024-01-28更新
|
103次组卷
|
4卷引用:新疆生产建设兵团第三师图木舒克市第二中学2023-2024学年高一下学期开学考试化学试题
名校
解题方法
3 . 合成氨技术对全球农业、工业和医药等领域都产生了重大影响。一种以N2和H2为原料光催化合成氨气的部分原理如图,其中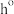 表示失去电子后带正电的空穴,
表示失去电子后带正电的空穴,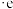 表示电子。下列说法错误的是
表示电子。下列说法错误的是
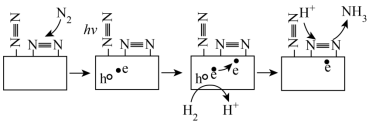
 表示失去电子后带正电的空穴,
表示失去电子后带正电的空穴, 表示电子。下列说法错误的是
表示电子。下列说法错误的是
| A.反应过程中,N2得电子 |
| B.图示反应过程中有极性键和非极性键的断裂与形成 |
| C.每生成17gNH3,转移3mol电子 |
| D.标准状况下,相同体积的N2和NH3的物质的量相同 |
您最近一年使用:0次
2024-01-25更新
|
114次组卷
|
2卷引用:新疆维吾尔自治区乌鲁木齐市第101中学2023-2024学年高一上学期1月期末化学试题
名校
4 . 按要求填空。
(1)同温同压下,同体积的氨气( )和硫化氢(
)和硫化氢( )气体的物质的量之比为
)气体的物质的量之比为_______ ;质量比为_______ ,其中含有的氢原子数目比为_______ 。
(2)40.5g某金属氯化物MCl2中含有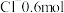 ,则M的相对原子质量为
,则M的相对原子质量为_______ 。
(3)在钢铁厂的生产中,炽热的铁水或钢水注入模具之前必须进行充分的干燥处理,不得留有水,请用化学方程式解释_______ 。
(4)已知在酸性条件下NaClO2可发生反应生成NaCl并释放出ClO2,该反应的离子方程式为_______ 。
(5) 中氧元素的化合价为-1价,处于中间价态,既有氧化性又有还原性。过氧化钠能使酸性高锰酸钾溶液褪色(已知高锰酸钾用硫酸酸化,还原产物为二价锰离子),请写出化学方程式为:
中氧元素的化合价为-1价,处于中间价态,既有氧化性又有还原性。过氧化钠能使酸性高锰酸钾溶液褪色(已知高锰酸钾用硫酸酸化,还原产物为二价锰离子),请写出化学方程式为:_______ 。
(1)同温同压下,同体积的氨气(
 )和硫化氢(
)和硫化氢( )气体的物质的量之比为
)气体的物质的量之比为(2)40.5g某金属氯化物MCl2中含有
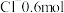 ,则M的相对原子质量为
,则M的相对原子质量为(3)在钢铁厂的生产中,炽热的铁水或钢水注入模具之前必须进行充分的干燥处理,不得留有水,请用化学方程式解释
(4)已知在酸性条件下NaClO2可发生反应生成NaCl并释放出ClO2,该反应的离子方程式为
(5)
 中氧元素的化合价为-1价,处于中间价态,既有氧化性又有还原性。过氧化钠能使酸性高锰酸钾溶液褪色(已知高锰酸钾用硫酸酸化,还原产物为二价锰离子),请写出化学方程式为:
中氧元素的化合价为-1价,处于中间价态,既有氧化性又有还原性。过氧化钠能使酸性高锰酸钾溶液褪色(已知高锰酸钾用硫酸酸化,还原产物为二价锰离子),请写出化学方程式为:
您最近一年使用:0次
名校
5 . 氮、磷元素的单质和它们的化合物用途广泛,与生产、生活有密切关系。请回答下列问题。
(1)下列属于氮的固定的是________ 。
a. 工业上N2和H2合成NH3 b. NH3催化氧化生成NO
c. N2和O2放电条件下生成NO d. NH3与灼热的氧化铜反应生成N2
(2)N2H4(联氨)可用作喷气式发动机推进剂、火箭燃料,可由次氯酸钠与氨反应制取,其化学反应方程式为_____________ 。
(3)三氟化氮( )是一种无色、无味的气体,是微电子工业技术的关键原料之一,
)是一种无色、无味的气体,是微电子工业技术的关键原料之一, 在潮湿的空气中与水蒸气能发生氧化还原反应,该反应的产物有:HF、NO和
在潮湿的空气中与水蒸气能发生氧化还原反应,该反应的产物有:HF、NO和 。
。
①写出该反应的化学方程式:___________ ,反应中生成0.2 mol  ,转移的电子数目为
,转移的电子数目为___________ ( 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。
② 无色、无臭,可一旦在空气中泄漏,却易于发现,判断该气体泄漏的现象是
无色、无臭,可一旦在空气中泄漏,却易于发现,判断该气体泄漏的现象是___________ 。
(4)Si3N4是一种性能优异的无机非金属材料,它的熔点高硬度大,电绝缘性好,化学性质稳定,但生产成本较高。根据以上描述推测Si3N4可能有哪些用途______ 。
a. 制作坩埚 b. 用作建筑陶瓷 c. 制作耐高温轴承 d. 制作切削刀具
(5)磷元素可以形成多种含氧酸。
①已知4.0g NaOH最多可中和100 mL 1mol·L−1 H3PO2溶液,则NaH2PO2是_________________ (填“正盐”或“酸式盐”)。
②已知常温下酸性:H3PO3 > CH3COOH > H2PO3-,则H3PO3与足量CH3COONa溶液混合的离子反应方程式为_____________ 。
(1)下列属于氮的固定的是
a. 工业上N2和H2合成NH3 b. NH3催化氧化生成NO
c. N2和O2放电条件下生成NO d. NH3与灼热的氧化铜反应生成N2
(2)N2H4(联氨)可用作喷气式发动机推进剂、火箭燃料,可由次氯酸钠与氨反应制取,其化学反应方程式为
(3)三氟化氮(
 )是一种无色、无味的气体,是微电子工业技术的关键原料之一,
)是一种无色、无味的气体,是微电子工业技术的关键原料之一, 在潮湿的空气中与水蒸气能发生氧化还原反应,该反应的产物有:HF、NO和
在潮湿的空气中与水蒸气能发生氧化还原反应,该反应的产物有:HF、NO和 。
。①写出该反应的化学方程式:
 ,转移的电子数目为
,转移的电子数目为 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。②
 无色、无臭,可一旦在空气中泄漏,却易于发现,判断该气体泄漏的现象是
无色、无臭,可一旦在空气中泄漏,却易于发现,判断该气体泄漏的现象是(4)Si3N4是一种性能优异的无机非金属材料,它的熔点高硬度大,电绝缘性好,化学性质稳定,但生产成本较高。根据以上描述推测Si3N4可能有哪些用途
a. 制作坩埚 b. 用作建筑陶瓷 c. 制作耐高温轴承 d. 制作切削刀具
(5)磷元素可以形成多种含氧酸。
①已知4.0g NaOH最多可中和100 mL 1mol·L−1 H3PO2溶液,则NaH2PO2是
②已知常温下酸性:H3PO3 > CH3COOH > H2PO3-,则H3PO3与足量CH3COONa溶液混合的离子反应方程式为
您最近一年使用:0次
名校
6 . 二氧化氯(ClO2)常温下是一种黄绿色或橘红色的气体,是国际上公认的安全、无毒的绿色消毒剂。其熔点为﹣59.5℃,沸点为11.0℃,温度过高可能引起爆炸;其能与碱溶液发生类似于氯气与碱溶液的反应:遇水则生成次氯酸、氯气和氧气。工业制取方法之一:用潮湿的KClO3和草酸(H2C2O4)在60℃时发生反应。某同学在实验室中设计了如下制取装置。
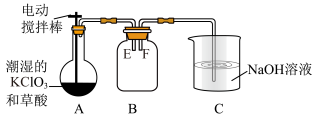
回答下列问题:
(1)装置A除酒精灯外,还必须添加________ 装置,目的是_______ 。为收集ClO2,B瓶中________ (填“E”或“F”)端应改为长导管。
(2)装置A中发生反应会产生K2CO3、ClO2和CO2等物质,请写出该反应的化学方程式______ 。
(3)若将二氧化氯通入品红试液中,能看到的现象是_______ ,你判断的理由是________ 。
(4)C装置的作用是________ ,写出C中发生反应的离子方程式,并用双线桥法标出电子转移情况________ 。

回答下列问题:
(1)装置A除酒精灯外,还必须添加
(2)装置A中发生反应会产生K2CO3、ClO2和CO2等物质,请写出该反应的化学方程式
(3)若将二氧化氯通入品红试液中,能看到的现象是
(4)C装置的作用是
您最近一年使用:0次
名校
解题方法
7 . 高铁酸钾 具有强氧化性,且在中性环境中可水解生成具有吸附性的氢氧化铁,因此可用于净水。下列有关铁及其化合物的性质与用途具有对应关系的是
具有强氧化性,且在中性环境中可水解生成具有吸附性的氢氧化铁,因此可用于净水。下列有关铁及其化合物的性质与用途具有对应关系的是
 具有强氧化性,且在中性环境中可水解生成具有吸附性的氢氧化铁,因此可用于净水。下列有关铁及其化合物的性质与用途具有对应关系的是
具有强氧化性,且在中性环境中可水解生成具有吸附性的氢氧化铁,因此可用于净水。下列有关铁及其化合物的性质与用途具有对应关系的是| A.氢氧化铁胶体具有碱性,可用于净水 |
B. 具有氧化性,可作为特定环境中的抗氧化剂 具有氧化性,可作为特定环境中的抗氧化剂 |
| C.高铁酸钾能溶于水,水溶液呈紫色,可作氧化剂 |
| D.氧化铁呈红棕色且遮盖效果好,可用作红色颜料 |
您最近一年使用:0次
2023-12-31更新
|
243次组卷
|
2卷引用:新疆乌鲁木齐市第十二中学2023-2024学年高三下学期2月月考化学试题
名校
解题方法
8 . 实验室以含锌废液(主要成分为 ,还含有少量的
,还含有少量的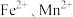 )为原料制备
)为原料制备 的实验流程如下:
的实验流程如下:
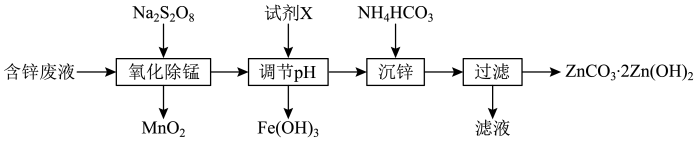
(1)写出基态 原子的电子排布式:
原子的电子排布式:___________ , 中
中 元素的化合价为
元素的化合价为___________ 。
(2)写出“氧化除锰”时反应的离子方程式:___________ 。
(3)常温下“调节 ”时,试剂
”时,试剂 可选用
可选用___________ ;已知溶液中 物质的量浓度为
物质的量浓度为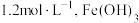 的
的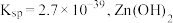 的
的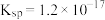 ,则
,则 的调节范围为
的调节范围为___________ 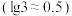 。已知:当溶液中离子浓度小于或等于
。已知:当溶液中离子浓度小于或等于 ,认为该离子已除尽。
,认为该离子已除尽。
(4)写出“沉锌”时反应的离子方程式:___________ 。
(5)“滤液”中的主要成分的用途:___________ 。
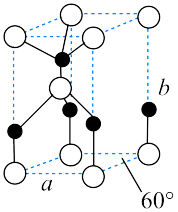
(6) 经焙解得到的活性
经焙解得到的活性 晶胞结构如图所示。该晶胞中
晶胞结构如图所示。该晶胞中 原子的配位数为
原子的配位数为___________ ;已知晶胞参数为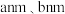 ,则该晶胞的密度为
,则该晶胞的密度为___________  。(写出计算表达式即可)
。(写出计算表达式即可)
 ,还含有少量的
,还含有少量的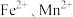 )为原料制备
)为原料制备 的实验流程如下:
的实验流程如下:
(1)写出基态
 原子的电子排布式:
原子的电子排布式: 中
中 元素的化合价为
元素的化合价为(2)写出“氧化除锰”时反应的离子方程式:
(3)常温下“调节
 ”时,试剂
”时,试剂 可选用
可选用 物质的量浓度为
物质的量浓度为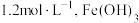 的
的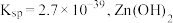 的
的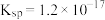 ,则
,则 的调节范围为
的调节范围为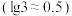 。已知:当溶液中离子浓度小于或等于
。已知:当溶液中离子浓度小于或等于 ,认为该离子已除尽。
,认为该离子已除尽。(4)写出“沉锌”时反应的离子方程式:
(5)“滤液”中的主要成分的用途:
(6)
 经焙解得到的活性
经焙解得到的活性 晶胞结构如图所示。该晶胞中
晶胞结构如图所示。该晶胞中 原子的配位数为
原子的配位数为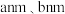 ,则该晶胞的密度为
,则该晶胞的密度为 。(写出计算表达式即可)
。(写出计算表达式即可)
您最近一年使用:0次
2023-12-18更新
|
188次组卷
|
2卷引用:新疆生产建设兵团第二中学2023-2024学年高三上学期12月月考化学题
名校
解题方法
9 . 下列方案设计、现象和结论都正确的是
| 目的 | 方案设计 | 现象和结论 | |
| A | 探究钠在氧气中燃烧所得固体成分 | 取少量加热后的固体粉末,加入少量蒸馏水 | 若有气泡产生,则证明燃烧后的固体粉末为Na2O2 |
| B | 比较KMnO4、Cl2 和Fe3+的氧化性 | 向酸性 KMnO4 溶液中滴入 FeCl2溶液,紫红色溶液变浅并伴有黄绿色气体产生 | 氧化性强弱:KMnO4>Cl2>Fe3+ |
| C | 制备 Fe(OH)3胶体 | 向沸水中滴加5~6滴FeCl3饱和溶液,继续煮沸至液体呈红褐色,停止加热。用红色激光笔照射液体 | 若产生一条光亮的“通路”,则得到Fe(OH)3 胶体 |
| D | 检验某溶液中是否存在K+ | 用玻璃棒蘸取待测液放在酒精灯外焰上灼烧,观察火焰的颜色 | 若看到火焰为黄色,则一定不存在 K+ |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-11-27更新
|
209次组卷
|
2卷引用:新疆乌鲁木齐八一中学2023-2024学年高一上学期1月月考化学试卷
名校
10 . 工业上氮氧化物( :NO和
:NO和 混合气)废气吸收利用的某流程如下:
混合气)废气吸收利用的某流程如下:
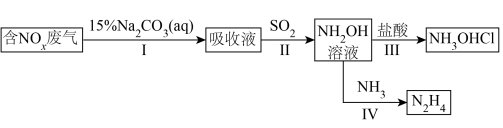
已知:氧化度 ;吸收液含有的产物有
;吸收液含有的产物有 和
和 ;
; 在碱性条件下受热分解产物之一为
在碱性条件下受热分解产物之一为 。
。
请回答:
(1)过程Ⅳ以“肼合成酶”催化 与
与 转化为肼(
转化为肼(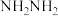 )的反应历程如下所示:
)的反应历程如下所示:
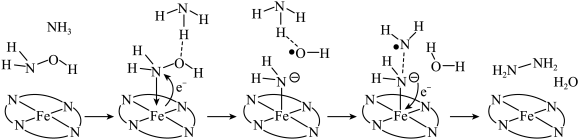
该反应历程中Fe元素的化合价___________ (填“变化”或“不变”)。若将 替换为
替换为 ,反应制得的肼的结构简式为
,反应制得的肼的结构简式为___________ 。
(2)写出过程Ⅰ中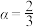 时反应的离子方程式
时反应的离子方程式___________ 。
(3)下列说法正确的是___________。
(4) 是一种理想还原剂,氧化产物对环境友好,写出
是一种理想还原剂,氧化产物对环境友好,写出 还原
还原 的化学方程式
的化学方程式___________ 。
(5)设计实验证明 中存在N元素
中存在N元素___________ 。
 :NO和
:NO和 混合气)废气吸收利用的某流程如下:
混合气)废气吸收利用的某流程如下:
已知:氧化度
 ;吸收液含有的产物有
;吸收液含有的产物有 和
和 ;
; 在碱性条件下受热分解产物之一为
在碱性条件下受热分解产物之一为 。
。请回答:
(1)过程Ⅳ以“肼合成酶”催化
 与
与 转化为肼(
转化为肼(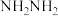 )的反应历程如下所示:
)的反应历程如下所示:
该反应历程中Fe元素的化合价
 替换为
替换为 ,反应制得的肼的结构简式为
,反应制得的肼的结构简式为(2)写出过程Ⅰ中
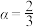 时反应的离子方程式
时反应的离子方程式(3)下列说法正确的是___________。
A.过程Ⅰ采用气、液逆流的方式可提高 的吸收效率 的吸收效率 |
B. 的键角小于 的键角小于 |
C. 可作为配体,与 可作为配体,与 等金属离子形成配合物 等金属离子形成配合物 |
D. 的水溶液显弱碱性,且 的水溶液显弱碱性,且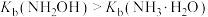 |
(4)
 是一种理想还原剂,氧化产物对环境友好,写出
是一种理想还原剂,氧化产物对环境友好,写出 还原
还原 的化学方程式
的化学方程式(5)设计实验证明
 中存在N元素
中存在N元素
您最近一年使用:0次
2023-11-15更新
|
405次组卷
|
3卷引用:新疆乌鲁木齐市第六十八中学2023-2024学年高三上学期1月月考化学试题
新疆乌鲁木齐市第六十八中学2023-2024学年高三上学期1月月考化学试题浙江省宁波市2023-2024学年高三上学期选考模拟考试化学试题(已下线)专题08 工艺流程综合题(浙江专用)-【好题汇编】2024年高考化学一模试题分类汇编(浙江专用)



