2022·新疆·三模
解题方法
1 . 2021年9月,中国科学家首次实现了利用二氧化碳人工合成淀粉,合成途径由11个核心反应组成。这一突破对于粮食安全、外星探索、气候变化都有着巨大意义。下列说法错误的是
| A.人工合成的淀粉与植物合成的淀粉均为混合物 |
| B.淀粉与葡萄糖都属于糖类,二者互为同系物 |
C.该合成法中第一步将 转化为甲醇, 转化为甲醇, 发生了还原反应 发生了还原反应 |
| D.该成果既可有利于碳中和又可助力太空探索 |
您最近一年使用:0次
2022高三·全国·专题练习
2 . 用尿素水解生成的 催化还原
催化还原 ,是柴油机车辆尾气净化的主要方法。反应为
,是柴油机车辆尾气净化的主要方法。反应为 ,下列说法正确的是
,下列说法正确的是
 催化还原
催化还原 ,是柴油机车辆尾气净化的主要方法。反应为
,是柴油机车辆尾气净化的主要方法。反应为 ,下列说法正确的是
,下列说法正确的是A.上述反应 |
B.上述反应平衡常数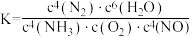 |
C.上述反应中消耗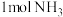 ,转移电子的数目为 ,转移电子的数目为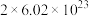 |
| D.实际应用中,加入尿素的量越多,柴油机车辆排放的尾气对空气污染程度越小 |
您最近一年使用:0次
2022-07-21更新
|
8905次组卷
|
23卷引用:新疆乌鲁木齐八一中学2023-2024学年高二上学期第一次月考化学试题
新疆乌鲁木齐八一中学2023-2024学年高二上学期第一次月考化学试题(已下线)专题09 化学反应速率、化学平衡-2022年高考真题模拟题分项汇编江苏省2022年普通高中学业水平选择性考试(已下线)2022年江苏卷高考真题变式题1-13(已下线)第20讲 化学平衡常数及转化率的计算(讲)-2023年高考化学一轮复习讲练测(新教材新高考)江苏省马坝高级中学2022-2023学年高三上学期9月份质量检测化学试题(已下线)易错点22 化学反应平衡和移动-备战2023年高考化学考试易错题广东省深圳市红岭中学2022-2023学年高二上学期期中考试化学试题(已下线)专题09 化学反应速率与化学平衡(讲)-2023年高考化学二轮复习讲练测(新高考专用)(已下线)江苏省2022年普通高中学业水平选择性考试变式题(选择题6-10)(已下线)专题卷11 化学反应速率与化学平衡归因分析-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)四川省广元中学2022-2023学年高二下学期4月月考化学试题(已下线)题型24 单反应体系中的化学平衡四川省乐山市沫若中学2021-2022学年高二下学期第二次月考化学试题(已下线)专题15 化学反应速率和化学平衡(已下线)专题15 化学反应速率和化学平衡(已下线)专题08 反应速率与化学平衡-2023年高考化学真题题源解密(新高考专用)(已下线)专题11 化学反应速率与化学平衡-2023年高考化学真题题源解密(全国通用)(已下线)考点23 化学平衡常数(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)第28讲化化学平衡的移动及反应进行的方向(已下线)考点3 化学平衡常数及转化率的计算(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)(已下线)题型13 化学平衡常数的计算及应用-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)(已下线)第05讲 氧化还原反应方程式的配平、书写及计算(练习)-【上好课】2025年高考化学一轮复习讲练测(新教材新高考)
名校
3 . 以下是对重要金属和非金属及其化合物的讨论,根据要求回答问题:
(1)氯碱工业是以电解饱和食盐水为基础的基本化学工业。电解饱和食盐水的产物中一种是所有气体中密度最小的气体、一种是黄绿色气体和一种易溶、易电离的碱,则电解食盐水的化学方程式_______ 。工业上制取漂白粉的反应化学方程式为_______ 。
(2)浓 常用作气体干燥剂,是因为它具有
常用作气体干燥剂,是因为它具有_______ ;将适量的蔗糖放入烧杯中,滴入几滴水,搅拌均匀。然后加入适量浓硫酸,迅速搅拌,放出大量的热,同时观察到蔗糖逐渐变黑,体积膨胀,并放出有刺激性气味的气体。请回答:
①产生刺激性气味气体的化学方程式为_______ 。
②根据上述实验现象,表明浓硫酸具有_______ (填字母)。
A.酸性 B.吸水性 C.脱水性 D.强氧化性
(3)铜和浓硝酸反应的离子方程式是_______ 。若参加反应的Cu质量为3.2g,生成 气体
气体_______ L(标准状况下),则转移电子物质的量为_______  。
。
(4)同学们已经学习了几种典型的有机化学反应类型,如取代反应、加成反应,请写出下列反应的化学反应方程式,并判断其反应类型。
①乙烯使溴的四氯化碳溶液褪色的反应:_______ ,属于_______ 反应;
②由乙烯制聚乙烯:_______ ,属于_______ 反应;
(1)氯碱工业是以电解饱和食盐水为基础的基本化学工业。电解饱和食盐水的产物中一种是所有气体中密度最小的气体、一种是黄绿色气体和一种易溶、易电离的碱,则电解食盐水的化学方程式
(2)浓
 常用作气体干燥剂,是因为它具有
常用作气体干燥剂,是因为它具有①产生刺激性气味气体的化学方程式为
②根据上述实验现象,表明浓硫酸具有
A.酸性 B.吸水性 C.脱水性 D.强氧化性
(3)铜和浓硝酸反应的离子方程式是
 气体
气体 。
。(4)同学们已经学习了几种典型的有机化学反应类型,如取代反应、加成反应,请写出下列反应的化学反应方程式,并判断其反应类型。
①乙烯使溴的四氯化碳溶液褪色的反应:
②由乙烯制聚乙烯:
您最近一年使用:0次
名校
4 . 下列各物质均含有同一种元素,其中只有A和H为单质,A是目前用量最大、用途最广的合金的主要成分,H为黄绿色气体;C和F所含元素种类相同;将D的悬浊液露置在空气中,可观察到白色絮状沉淀迅速变为灰绿色,最后变为红褐色沉淀E,各物质间的转化关系如下图(部分反应物、生成物及反应条件已略去)
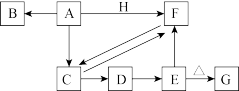
回答下列问题:
(1)A是_______ ,C是_______ (填化学式)。
(2)G的俗名为_______ 。
(3)若要除去F溶液中混有的C,应采取的实验操作为_______ ;若要除去C溶液中混有的F,涉及的化学反应的离子方程式为_______ 。
(4)写出D转化为E的化学反应方程式_______ 。
(5)人体正常的血红蛋白中含有D的阳离子,若误食亚硝酸盐,会导致血红蛋白中此阳离子被氧化而使人中毒。服用维生素C可以解毒,在此过程中体现了维生素C的_______ 性。

回答下列问题:
(1)A是
(2)G的俗名为
(3)若要除去F溶液中混有的C,应采取的实验操作为
(4)写出D转化为E的化学反应方程式
(5)人体正常的血红蛋白中含有D的阳离子,若误食亚硝酸盐,会导致血红蛋白中此阳离子被氧化而使人中毒。服用维生素C可以解毒,在此过程中体现了维生素C的
您最近一年使用:0次
2022-07-10更新
|
166次组卷
|
3卷引用:新疆石河子第一中学2023-2024学年高一上学期11月月考化学试题
5 . 阳离子只有氧化性,阴离子只有还原性。(______)
您最近一年使用:0次
2022-07-08更新
|
550次组卷
|
8卷引用:新疆维吾尔自治区且末县第二中学2018-2019学年高一上学期期末考试化学试题
新疆维吾尔自治区且末县第二中学2018-2019学年高一上学期期末考试化学试题(已下线)考点05 氧化还原反应-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点05 氧化还原反应-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)考点05 氧化还原反应-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第06讲 氧化剂和还原剂 (讲义)-【帮课堂】2022-2023学年高一化学同步精品讲义(人教2019必修第一册 )(已下线)第06讲 氧化剂和还原剂 (讲义)-【帮课堂】2022-2023学年高一化学同步精品讲义(人教2019必修第一册 )(已下线)第4讲 氧化还原反应的基本概念与规律(已下线)考点05 氧化还原反应(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)
名校
解题方法
6 . “龙芯一号”的问世填补了我国电脑芯片制造史上的一项空白。用硝酸与氢氟酸的混合液作制作芯片的刻蚀液,发生的反应为 。下列有关叙述正确的是
。下列有关叙述正确的是
 。下列有关叙述正确的是
。下列有关叙述正确的是A.电脑芯片的主要成分为 , , 具有良好的光学性能 具有良好的光学性能 |
| B.实验室中,可用玻璃仪器密封保存氢氟酸 |
C.在该反应中, 作还原剂,被氧化为 作还原剂,被氧化为 |
D.该反应转移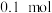 电子时,生成 电子时,生成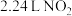 |
您最近一年使用:0次
2022-07-07更新
|
761次组卷
|
15卷引用:新疆乌鲁木齐市第八中学2022-2023学年高一下学期期中考试化学试题
新疆乌鲁木齐市第八中学2022-2023学年高一下学期期中考试化学试题湖南省衡阳市部分校2021-2022学年高一下学期期末考试化学试题河南省豫东名校2021-2022学年高一下学期高中教学质量检测(期末)化学试题云南省楚雄州2021-2022学年高一下学期期末考试化学试题辽宁省沈阳实验中学2022-2023学年高二上学期开学考试化学试题(已下线)化学(人教版2019A卷)-学易金卷:2022-2023学年高一下学期期中考前必刷卷河北省邢台市第二中学2022-2023学年高一下学期第二次月考化学试题河北省邢台市南宫中学2022-2023学年高一下学期第二次月考化学试题江西省赣州市南康区第三中学2022-2023学年高一下学期期中考试化学试题吉林省长春外国语学校2022-2023学年高一下学期5月期中考试化学试题江西省赣州市石城中学2022-2023学年高一下学期第一次月考化学试题(已下线)第03练 无机非金属材料-2023年【暑假分层作业】高一化学(人教版2019必修第二册)河南省焦作市博爱县第一中学2022-2023学年高一下学期6月期末考试化学试题重庆市涪陵第五中学校2023-2024学年高一下学期5月月考化学试题河南省信阳高级中学2023-2024学年高一下学期月考(四)化学试题
名校
解题方法
7 . 工业上以黄铁矿(主要成分为FeS2)为原料来制备硫酸,过程如下:
i.4FeS2+11O2 _______+8SO2
_______+8SO2
ii.2SO2+O2 2SO3
2SO3
iii.SO3+H2O=H2SO4
(1)补全过程i的方程式_______ 。
(2)硫酸工厂的烟气中含有SO2,工业上用NaOH溶液作吸收剂脱除烟气中的SO2。

①过程Ⅰ的化学方程式是_______ 。
②过程Ⅱ参加反应的物质A有_______ 。
③NaOH吸收SO2过程中常伴有少量SO42-,证明吸收液中含SO42-的方法是:取少量上层清液,_______ (填操作和现象)。
(3)测定烟气中SO2的含量。将V1 L烟气缓慢通过1L水(假设SO2完全被吸收,且溶液体积变化忽略不计),取20.00mL溶液,滴加2~3滴淀粉溶液,用c mol•L-1的碘水滴定,消耗碘水V2 mL。该烟气中SO2的含量为_______ mg•L-1。(已知:滴定反应为SO2+I2+2H2O=H2SO4+2HI)
i.4FeS2+11O2
 _______+8SO2
_______+8SO2ii.2SO2+O2
 2SO3
2SO3iii.SO3+H2O=H2SO4
(1)补全过程i的方程式
(2)硫酸工厂的烟气中含有SO2,工业上用NaOH溶液作吸收剂脱除烟气中的SO2。

①过程Ⅰ的化学方程式是
②过程Ⅱ参加反应的物质A有
③NaOH吸收SO2过程中常伴有少量SO42-,证明吸收液中含SO42-的方法是:取少量上层清液,
(3)测定烟气中SO2的含量。将V1 L烟气缓慢通过1L水(假设SO2完全被吸收,且溶液体积变化忽略不计),取20.00mL溶液,滴加2~3滴淀粉溶液,用c mol•L-1的碘水滴定,消耗碘水V2 mL。该烟气中SO2的含量为
您最近一年使用:0次
2022-07-07更新
|
192次组卷
|
4卷引用:新疆维吾尔自治区喀什地区喀什市第六中学2022-2023学年高二上学期10月期中考试化学试题
新疆维吾尔自治区喀什地区喀什市第六中学2022-2023学年高二上学期10月期中考试化学试题北京市朝阳区2020-2021学年高一下学期期末化学试题北京市回民学校2022-2023学年高一下学期期中考试化学试题(已下线)重难点04 硫和氮综合题-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(北京专用)
名校
解题方法
8 . 一氧化二氯(Cl2O)是一种工业上常用的氯化剂和氧化剂,还可用作灭菌和漂白。常压下,Cl2O的熔点为-120.6°C,沸点为3.5°C,遇水会发生反应。某化学实验小组用纯碱和氯气利用下图中装置制备Cl2O(夹持装置、装置C中的冷却装置或加热装置均略去)。

回答下列问题:
(1)分液漏斗使用前必须进行的操作为_______ ,欲使分液漏斗内的浓盐酸顺利滴下,可将分液漏斗上部的玻璃塞打开或_______ 。
(2)装置的正确连接顺序是_______ (按气流方向,用小写字母表示)。
(3)装置C中发生Cl2O的制备反应中的固体产物为NaHCO3和NaCl,写出该反应的化学方程式_______ 。反应一段时间后,装置B中观察到的实验现象为_______ 。
(4)研究表明,装置B中Cl2O的收率与装置C的温度和纯碱的含水量的关系如下表所示:
本实验中适宜选用的温度范围和纯碱的含水量分别为_______ 、_______ 。
(5)装置F中盛放碱石灰的仪器名称为_______ ,碱石灰的作用为_______ 。
(6)若将少量Cl2O气体通入用稀硫酸酸化的KI-淀粉溶液中,溶液会变蓝色,溶液变蓝色的原因为_______ (用离子方程式表示)。

回答下列问题:
(1)分液漏斗使用前必须进行的操作为
(2)装置的正确连接顺序是
(3)装置C中发生Cl2O的制备反应中的固体产物为NaHCO3和NaCl,写出该反应的化学方程式
(4)研究表明,装置B中Cl2O的收率与装置C的温度和纯碱的含水量的关系如下表所示:
| 温度/°C | 纯碱中含水量/% | Cl2O的收率/% |
| 0~10 | 5.44 | 67.85 |
| 0~10 | 7.88 | 89.26 |
| 10~20 | 8.00 | 64.24 |
| 30~40 | 10.25 | 52.63 |
| 30~40 | 12.50 | 30.38 |
(5)装置F中盛放碱石灰的仪器名称为
(6)若将少量Cl2O气体通入用稀硫酸酸化的KI-淀粉溶液中,溶液会变蓝色,溶液变蓝色的原因为
您最近一年使用:0次
2022-06-27更新
|
293次组卷
|
2卷引用:新疆莎车县第一中学2022-2023学年高三上学期11月月考化学试题
名校
9 . O2在一定条件下能有效去除烟气中的SO2、NO,其可能的反应机理如下图所示,下列说法不正确 的是(HO•表示羟基自由基,•表示未成对电子)

A.O2转化为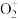 时失去电子 时失去电子 |
| B.HO•中氧元素的化合价为-1 |
| C.净化器内SO2被还原 |
| D.净化器内NO发生的反应为3HO• + NO = HNO3 + H2O |
您最近一年使用:0次
2022-06-26更新
|
1194次组卷
|
15卷引用:新疆克孜勒苏柯尔克孜自治州第二中学2022-2023学年高一下学期期末考试化学试题
新疆克孜勒苏柯尔克孜自治州第二中学2022-2023学年高一下学期期末考试化学试题江苏省扬州市2021-2022学年高一下学期期末调研化学试题(已下线)第05讲 氧化还原反应(讲义)-【帮课堂】2022-2023学年高一化学同步精品讲义(人教2019必修第一册 )(已下线)第05讲 氧化还原反应(讲义)-【帮课堂】2022-2023学年高一化学同步精品讲义(人教2019必修第一册 )(已下线)第06讲 氧化剂和还原剂 (讲义)-【帮课堂】2022-2023学年高一化学同步精品讲义(人教2019必修第一册 )(已下线)第06讲 氧化剂和还原剂 (讲义)-【帮课堂】2022-2023学年高一化学同步精品讲义(人教2019必修第一册 )安徽省淮北市第一中学2022-2023学年高一下学期第二次月考化学试题天津市静海区第一中学2022-2023学年高一下学期3月学业能力调研化学试题江苏省南通市通州区2022-2023学年高一下学期第一次月考化学试题江苏省南京师范大学附属扬子中学、江浦高级中学两校2022-2023学年高一下学期联合调研化学试题广东省东莞市东华高级中学2022-2023学年高一下学期3月月考化学试题河南省濮阳市第一高级中学2022-2023学年高一下学期6月月考化学试题江苏省前黄高级中学2022-2023学年高二上学期期初检测化学试题江苏省扬州大学附属中学东部分校2023-2024学年高一下学期3月月考化学试题(已下线)重难点02 化学反应与能量-【好题汇编】备战2023-2024学年高一化学下学期期末真题分类汇编(江苏专用)
解题方法
10 . 合理使用化学品是每一位生产者和消费者的责任。下列说法正确的是
| A.为减少对生态环境的危害,农业生产中应禁止使用农药 |
| B.抗坏血酸(Vc)能抗氧化,可做食品添加剂 |
| C.天然有机物都是绿色健康的,人工合成有机物均有潜在的危害性 |
| D.将阿司匹林制成缓释剂,用药安全性提高,可以大量口服使用 |
您最近一年使用:0次
2022-06-21更新
|
428次组卷
|
5卷引用:新疆乌鲁木齐市六校联考2022-2023学年高一下学期6月期末考试化学试题
新疆乌鲁木齐市六校联考2022-2023学年高一下学期6月期末考试化学试题浙江省杭州市2021-2022学年高二下学期教学质量期末检测化学试题甘肃省张掖市2021-2022学年高一下学期期末考试化学试题(已下线)专题11 化学与可持续发展(专题过关)-2022-2023学年高一化学下学期期中期末考点大串讲(人教版2019必修第二册)(已下线)猜想08 化学与可持续发展(考题猜想)-2023-2024学年高一化学下学期期末考点大串讲(人教版2019必修第二册)



