解题方法
1 . 根据要求和所给条件,书写反应方程式(系数为最简整数比)。
(1)碳化铝(Al4C3)与水反应_____ 。
(2)乙酸酐与Mn(NO3)2•6H2O反应制备无水盐Mn(CH3COO)3_____ 。
(3)在真空和900℃下于钼舟中用TiO2与CaH2反应制备金属Ti_____ 。
(4)在约200℃下NaNH2与笑气反应制备叠氮化物_____ 。
(5)SeCl4与无水液氨作用转化为爆炸性很强的化合物Se4N4_____ 。
(1)碳化铝(Al4C3)与水反应
(2)乙酸酐与Mn(NO3)2•6H2O反应制备无水盐Mn(CH3COO)3
(3)在真空和900℃下于钼舟中用TiO2与CaH2反应制备金属Ti
(4)在约200℃下NaNH2与笑气反应制备叠氮化物
(5)SeCl4与无水液氨作用转化为爆炸性很强的化合物Se4N4
您最近一年使用:0次
2 . 高锰酸钾是锰的重要化合物和常用的氧化剂。下列是工业上用软锰矿(主要成分为 )制备高锰酸钾的流程图。请回答下列问题:
)制备高锰酸钾的流程图。请回答下列问题:
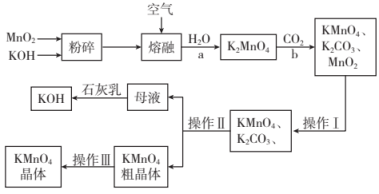
(1)软锰矿和 的混合物在空气中加热熔融反应生成
的混合物在空气中加热熔融反应生成 的化学方程式为
的化学方程式为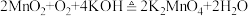 。
。
① 中
中 元素的化合价为
元素的化合价为_______ 价,由流程中的信息分析, 具有
具有_______ 性。
②该反应中氧化剂和还原剂的物质的量之比为_______ 。
(2)操作Ⅰ的名称为_______ 。
(3)母液中加入石灰乳后发生反应的离子方程式为_______ 。该反应所属的反应类型为_______ 。
(4)将 加入浓盐酸中可以制备氯气,写出该反应的化学方程式:
加入浓盐酸中可以制备氯气,写出该反应的化学方程式:_______ 。该反应中作还原剂的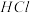 占总反应的
占总反应的_______ 。当消耗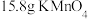 时,产生标准状况下
时,产生标准状况下_______ 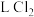 。
。
 )制备高锰酸钾的流程图。请回答下列问题:
)制备高锰酸钾的流程图。请回答下列问题:
(1)软锰矿和
 的混合物在空气中加热熔融反应生成
的混合物在空气中加热熔融反应生成 的化学方程式为
的化学方程式为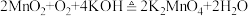 。
。①
 中
中 元素的化合价为
元素的化合价为 具有
具有②该反应中氧化剂和还原剂的物质的量之比为
(2)操作Ⅰ的名称为
(3)母液中加入石灰乳后发生反应的离子方程式为
(4)将
 加入浓盐酸中可以制备氯气,写出该反应的化学方程式:
加入浓盐酸中可以制备氯气,写出该反应的化学方程式: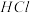 占总反应的
占总反应的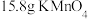 时,产生标准状况下
时,产生标准状况下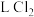 。
。
您最近一年使用:0次
3 .  是大气污染的主要元凶之一,工业上常用碱液吸收法来处理
是大气污染的主要元凶之一,工业上常用碱液吸收法来处理 ,
,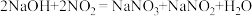 ,使废气得以净化,下列有关说法正确的是
,使废气得以净化,下列有关说法正确的是
 是大气污染的主要元凶之一,工业上常用碱液吸收法来处理
是大气污染的主要元凶之一,工业上常用碱液吸收法来处理 ,
,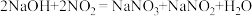 ,使废气得以净化,下列有关说法正确的是
,使废气得以净化,下列有关说法正确的是A. 在该反应中作氧化剂 在该反应中作氧化剂 | B. 在反应过程中仅失去电子 在反应过程中仅失去电子 |
C. 是酸性氧化物 是酸性氧化物 | D.上述反应中还原剂与氧化剂的质量之比为1∶1 |
您最近一年使用:0次
4 . 某反应涉及7种粒子:PbO2、PbSO4、 、Mn2+、H2O、H+、
、Mn2+、H2O、H+、 ,其中PbSO4是产物,其对应的化学计量数为5,下列说法正确的是
,其中PbSO4是产物,其对应的化学计量数为5,下列说法正确的是
 、Mn2+、H2O、H+、
、Mn2+、H2O、H+、 ,其中PbSO4是产物,其对应的化学计量数为5,下列说法正确的是
,其中PbSO4是产物,其对应的化学计量数为5,下列说法正确的是A.氧化剂为 | B.失去电子的元素是Pb |
| C.随着反应进行,溶液的pH减小 | D.氧化剂与还原剂的化学计量数之比为5:2 |
您最近一年使用:0次
2022-10-10更新
|
427次组卷
|
3卷引用:新疆维吾尔自治区和田地区策勒县2022-2023学年高三上学期11月期中考试化学试题
5 . I.回答下列问题:
(1)人体缺乏某种微量元素将导致血液输送氧气能力下降,人体就无法获得充足的氧气,生理机能就会下降,该微量元素是_____ (填字母)。
a.碘 b.锌 c.铁
(2)抗生素是抑制某些微生物生长或杀灭某些微生物的一类物质,下列属于抗生素的是_____ (填字母)。
a.阿莫西林 b.胃舒平 c.阿司匹林
II.表中是我国部分城市空气质量周报,回答下列问题:(TSP—空气中的飘尘)
(3)最容易出现酸雨的城市是____ 。
(4)NaOH溶液可吸收废气中的氮氧化物,反应方程式:2NO2+2NaOH=NaNO2+NaNO3+H2O。反应时消耗了10L0.1mol•L-1NaOH溶液,则反应中转移电子的数目为:____ 。
III.湘江流域工厂较多,如果污水处理不当,容易造成工业污染。我国工业废水中几种污染物的最高允许排放浓度如表:
(5)现有某工厂每日排放的污水中汞的质量分数为(1×10-6)%,镉的质量分数为(2×10-5)%,铅的质量分数为(5×10-5)%(设该污水的密度为1g/cm3)。根据计算该厂三项污染物中____ 超标。
(1)人体缺乏某种微量元素将导致血液输送氧气能力下降,人体就无法获得充足的氧气,生理机能就会下降,该微量元素是
a.碘 b.锌 c.铁
(2)抗生素是抑制某些微生物生长或杀灭某些微生物的一类物质,下列属于抗生素的是
a.阿莫西林 b.胃舒平 c.阿司匹林
II.表中是我国部分城市空气质量周报,回答下列问题:(TSP—空气中的飘尘)
| 城市 | 污染指数 | 首要污染物 | 空气质量级别 | 城市 | 污染指数 | 首要污染物 | 空气质量级别 |
| 天津 | 82 | TSP | II | 武汉 | 83 | NOx | II |
| 哈尔滨 | 96 | TSP | II | 重庆 | 98 | SOx | II |
(4)NaOH溶液可吸收废气中的氮氧化物,反应方程式:2NO2+2NaOH=NaNO2+NaNO3+H2O。反应时消耗了10L0.1mol•L-1NaOH溶液,则反应中转移电子的数目为:
III.湘江流域工厂较多,如果污水处理不当,容易造成工业污染。我国工业废水中几种污染物的最高允许排放浓度如表:
| 污染物 | 汞 | 镉 | 铅 |
| 主要存在形式 | Hg2+ | Cd2+ | Pb2+ |
| 最高允许排放浓度/(mg•dm-3) | 0.05 | 0.1 | 1.0 |
您最近一年使用:0次
6 . 计算题
(1)氮原子的摩尔质量是_______ ;0.5molN2的质量是_______
(2)1molO2含有电子数是_______ 。
 分子中所含质子数
分子中所含质子数_______
(3)2L0.1mol/LNa2SO4溶液中Na+的物质的量浓度为_______ mol/L
(4)0.2molFe2(SO4)3溶液中含SO 的物质的量为
的物质的量为_______
(5)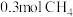 中氢原子的数目
中氢原子的数目_______ ,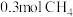 在标准状况下的体积为
在标准状况下的体积为_______ L
(6)2Na2O2+2CO2=2Na2CO3+O2中O元素的化合价发生改变,属于氧化还原反应,该反应中氧化剂和还原剂物质的量之比_______ ,生成1molO2转移的电子数目为_______ 。
(1)氮原子的摩尔质量是
(2)1molO2含有电子数是

 分子中所含质子数
分子中所含质子数(3)2L0.1mol/LNa2SO4溶液中Na+的物质的量浓度为
(4)0.2molFe2(SO4)3溶液中含SO
 的物质的量为
的物质的量为(5)
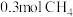 中氢原子的数目
中氢原子的数目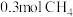 在标准状况下的体积为
在标准状况下的体积为(6)2Na2O2+2CO2=2Na2CO3+O2中O元素的化合价发生改变,属于氧化还原反应,该反应中氧化剂和还原剂物质的量之比
您最近一年使用:0次
7 . 回答下列问题
(1)火药是中国的“四大发明”之一、黑火药在发生爆炸时,发生如下反应: ,其中被氧化的元素是
,其中被氧化的元素是_______ (填元素名称)。
(2)人体内的铁元素是以 和
和 的形式存在。
的形式存在。 易被人体吸收,服用维生素C,可使
易被人体吸收,服用维生素C,可使 转化成
转化成 ,有利于人体吸收,说明维生素C具有
,有利于人体吸收,说明维生素C具有_______ (填“氧化性”或“还原性”)。
(3)现有以下物质:①NaCl晶体 ②液态HCl③CaCO3固体 ④熔融KCl ⑤蔗糖 ⑥铜 ⑦CO2 ⑧H2SO4 ⑨KOH固体
以上物质中属于电解质的是_______ ,属于非电解质的是_______ 。
(4)一定条件下,酸性KMnO4溶液还可以氧化其他还原性物质。________
_______MnO +_______C2O
+_______C2O +_______=_______Mn2++_______CO2↑+_______(注:C2O
+_______=_______Mn2++_______CO2↑+_______(注:C2O 中的C的化合价为+3价)
中的C的化合价为+3价)
(1)火药是中国的“四大发明”之一、黑火药在发生爆炸时,发生如下反应:
 ,其中被氧化的元素是
,其中被氧化的元素是(2)人体内的铁元素是以
 和
和 的形式存在。
的形式存在。 易被人体吸收,服用维生素C,可使
易被人体吸收,服用维生素C,可使 转化成
转化成 ,有利于人体吸收,说明维生素C具有
,有利于人体吸收,说明维生素C具有(3)现有以下物质:①NaCl晶体 ②液态HCl③CaCO3固体 ④熔融KCl ⑤蔗糖 ⑥铜 ⑦CO2 ⑧H2SO4 ⑨KOH固体
以上物质中属于电解质的是
(4)一定条件下,酸性KMnO4溶液还可以氧化其他还原性物质。
_______MnO
 +_______C2O
+_______C2O +_______=_______Mn2++_______CO2↑+_______(注:C2O
+_______=_______Mn2++_______CO2↑+_______(注:C2O 中的C的化合价为+3价)
中的C的化合价为+3价)
您最近一年使用:0次
名校
8 . 下图是氯元素的“价-类”二维图,据此下列分析正确的是


| A.由“价-类”二维图推测ClONO2具有强氧化性,可与水反应生成两种强酸 |
| B.可用pH试纸分别测定等浓度的HClO2和HClO溶液的pH,比较酸性强弱 |
C.工业上常用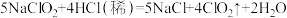 制备ClO2,该反应氧化产物与还原产物之比为4:1 制备ClO2,该反应氧化产物与还原产物之比为4:1 |
| D.常用于炸药、火箭推进剂的某种强氧化剂在“价-类”二维图中的位置为(盐,-1) |
您最近一年使用:0次
2022-09-21更新
|
367次组卷
|
4卷引用:新疆乌鲁木齐市第八中学2022-2023学年高一上学期期中考试化学试题
9 . 氯及其化合物在工业生产生活中有很重要的作用。图中为实验室通常制取氯气及性质验证的装置图:
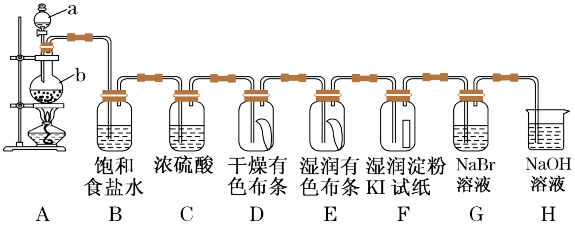
(1)H装置的作用____ ,写出发生的离子反应方程式____ 。
(2)在装置E中可观察到的现象是____ ,通过D、E中的现象说明什么结论____ 。
(3)装置G中发生的离子方程式____ 。
(4)可用KMnO4与浓盐酸快速制氯气,发生如下反应(未配平):KMnO4+HCl(浓)—KCl+Cl2↑+H2O+MnCl2。
写出配平的该反应的离子方程式_____ 。该反应中氧化剂与还原剂的物质的量之比为____ 。标况下反应生成11.2L的Cl2,则该反应转移的电子的数目为____ ;被氧化的HCl的物质的量为____ 。
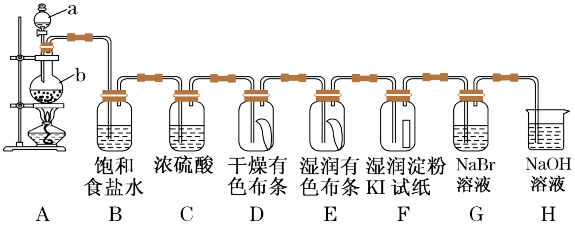
(1)H装置的作用
(2)在装置E中可观察到的现象是
(3)装置G中发生的离子方程式
(4)可用KMnO4与浓盐酸快速制氯气,发生如下反应(未配平):KMnO4+HCl(浓)—KCl+Cl2↑+H2O+MnCl2。
写出配平的该反应的离子方程式
您最近一年使用:0次
名校
10 . 已知酸性 ,下列有关叙述中正确的是
,下列有关叙述中正确的是
①向 溶液中通入少量二氧化碳的离子反应方程式为
溶液中通入少量二氧化碳的离子反应方程式为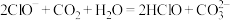
②向 和
和 混合溶液中加入足量
混合溶液中加入足量 溶液,用
溶液,用 萃取后,取上层中的液体少许并加入
萃取后,取上层中的液体少许并加入 溶液,有淡黄色沉淀生成
溶液,有淡黄色沉淀生成
③向 溶液中滴加少量氯水,反应的离子方程式为
溶液中滴加少量氯水,反应的离子方程式为
④“84”消毒液(有效成分 )和“洁厕灵”(主要成分盐酸)混合使用时放出氯气,其离子方程式为
)和“洁厕灵”(主要成分盐酸)混合使用时放出氯气,其离子方程式为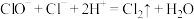
⑤在海带灰的浸出液(含有 )中滴加
)中滴加 得到
得到 ,其离子方程式为
,其离子方程式为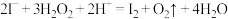
 ,下列有关叙述中正确的是
,下列有关叙述中正确的是①向
 溶液中通入少量二氧化碳的离子反应方程式为
溶液中通入少量二氧化碳的离子反应方程式为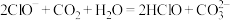
②向
 和
和 混合溶液中加入足量
混合溶液中加入足量 溶液,用
溶液,用 萃取后,取上层中的液体少许并加入
萃取后,取上层中的液体少许并加入 溶液,有淡黄色沉淀生成
溶液,有淡黄色沉淀生成③向
 溶液中滴加少量氯水,反应的离子方程式为
溶液中滴加少量氯水,反应的离子方程式为
④“84”消毒液(有效成分
 )和“洁厕灵”(主要成分盐酸)混合使用时放出氯气,其离子方程式为
)和“洁厕灵”(主要成分盐酸)混合使用时放出氯气,其离子方程式为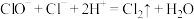
⑤在海带灰的浸出液(含有
 )中滴加
)中滴加 得到
得到 ,其离子方程式为
,其离子方程式为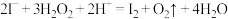
| A.②④ | B.①③⑤ | C.②③ | D.①④⑤ |
您最近一年使用:0次
2022-09-05更新
|
450次组卷
|
2卷引用:新疆石河子第一中学2023-2024学年高三上学期第三次月考化学试题



