解题方法
1 . 三氯氧钒( )是一种重要的无机试剂,主要用作溶剂、烯烃聚合的催化剂,还可用于钒有机化合物的合成。某兴趣小组利用如图所示装置以氯气、
)是一种重要的无机试剂,主要用作溶剂、烯烃聚合的催化剂,还可用于钒有机化合物的合成。某兴趣小组利用如图所示装置以氯气、 和碳粉为原料制备三氯氧钒。
和碳粉为原料制备三氯氧钒。 ;熔点为-77℃,沸点为126℃;
;熔点为-77℃,沸点为126℃;
②三氯氧钒遇水会迅速水解生成HCl和一种氧化物。
回答下列问题:
(1)仪器X的名称为___________ ,仪器Y为球形冷凝管,冷却水应从___________ 口(填“M”或“N”)进入。仪器X可以换为如图装置,其优点是___________ 。 ,正确的连接顺序为
,正确的连接顺序为___________ →d→e→h(按气流方向,用小写字母表示,装置可重复使用)。
(3)装置C的作用是为了防止___________ 反应发生(写化学方程式)。
(4)管式炉中发生反应生成CO的化学方程式为___________ 。
(5)已知: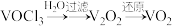 ,
, 的立方晶胞结构如图所示,晶胞参数为a pm。
的立方晶胞结构如图所示,晶胞参数为a pm。___________ 。
②晶体的密度为___________  (列出计算式,阿伏加德罗常数的值为
(列出计算式,阿伏加德罗常数的值为 )。
)。
(6)取装置B烧瓶中的液体少许,先溶于水再过滤,在滤渣中加入稀硫酸溶解后,向其中加入0.2000
 溶液25mL,再用0.1000
溶液25mL,再用0.1000
 溶液滴定过量的草酸溶液至终点,消耗
溶液滴定过量的草酸溶液至终点,消耗 溶液的体积为4mL,则所取液体中
溶液的体积为4mL,则所取液体中 的质量为
的质量为___________ g(保留1位小数)。已知: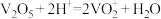 ,
,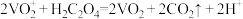 。
。
 )是一种重要的无机试剂,主要用作溶剂、烯烃聚合的催化剂,还可用于钒有机化合物的合成。某兴趣小组利用如图所示装置以氯气、
)是一种重要的无机试剂,主要用作溶剂、烯烃聚合的催化剂,还可用于钒有机化合物的合成。某兴趣小组利用如图所示装置以氯气、 和碳粉为原料制备三氯氧钒。
和碳粉为原料制备三氯氧钒。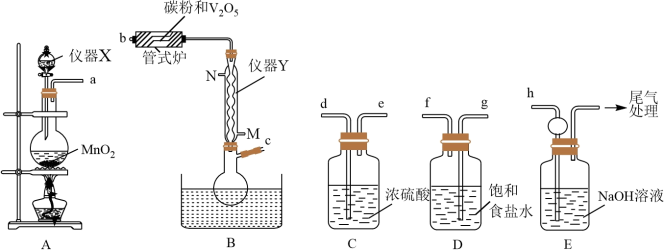
 ;熔点为-77℃,沸点为126℃;
;熔点为-77℃,沸点为126℃;②三氯氧钒遇水会迅速水解生成HCl和一种氧化物。
回答下列问题:
(1)仪器X的名称为

 ,正确的连接顺序为
,正确的连接顺序为(3)装置C的作用是为了防止
(4)管式炉中发生反应生成CO的化学方程式为
(5)已知:
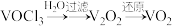 ,
, 的立方晶胞结构如图所示,晶胞参数为a pm。
的立方晶胞结构如图所示,晶胞参数为a pm。
②晶体的密度为
 (列出计算式,阿伏加德罗常数的值为
(列出计算式,阿伏加德罗常数的值为 )。
)。(6)取装置B烧瓶中的液体少许,先溶于水再过滤,在滤渣中加入稀硫酸溶解后,向其中加入0.2000

 溶液25mL,再用0.1000
溶液25mL,再用0.1000
 溶液滴定过量的草酸溶液至终点,消耗
溶液滴定过量的草酸溶液至终点,消耗 溶液的体积为4mL,则所取液体中
溶液的体积为4mL,则所取液体中 的质量为
的质量为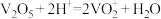 ,
,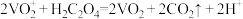 。
。
您最近一年使用:0次
2 . 宋代《千里江山图》中大量使用两种含铜的矿物颜料。对于如图所示转化关系,下列说法正确的是

| A.反应①②③均为氧化还原反应 |
| B.孔雀石颜料和蓝铜矿颜料受热都可能变为黑色 |
| C.保存古画需控制温度和湿度,目的是防止孔雀石颜料等被氧化 |
| D.孔雀石颜料、蓝铜矿颜料耐酸碱腐蚀 |
您最近一年使用:0次
3 . 二氧化铈(CeO2)作为一种脱硝催化剂,能在Ce4+和Ce3+之间改变氧化状态,将NO氧化为NO2,并引起氧空位的形成,得到新的铈氧化物[Cex(Ⅲ)Cey(Ⅳ)Oz]。当二氧化铈晶胞发生如下图变化时,有关说法错误的是
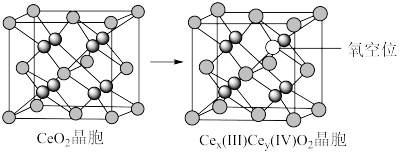
| A.铈位于氧原子形成的八面体空隙中 |
| B.生成新的铈氧化物中x、y、z的最简整数比为2:2:7,当1 mol CeO2发生变化时,可吸收标况下NO的体积为5.6 L |
C.晶胞的俯视图为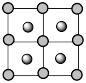 |
D.若晶胞边长为a pm,则CeO2晶体的密度为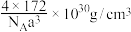 (NA表示阿伏加德罗常数的值) (NA表示阿伏加德罗常数的值) |
您最近一年使用:0次
解题方法
4 . 铁酸锌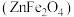 是一种性能优良的软磁材料,可作烯类有机化合物氧化脱氢的催化剂。实验室制备铁酸锌可采用如下步骤:
是一种性能优良的软磁材料,可作烯类有机化合物氧化脱氢的催化剂。实验室制备铁酸锌可采用如下步骤:
Ⅰ.制备前驱物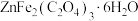
①分别配制 溶液和
溶液和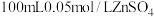 溶液,并将二者混合备用。
溶液,并将二者混合备用。
②另外称取 溶于
溶于 蒸馏水中。
蒸馏水中。
③将①和②所得溶液混合加热到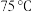 ,并在
,并在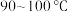 加热搅拌
加热搅拌 ;待溶液冷却后进行减压过滤、洗涤,干燥,得到前驱物。
;待溶液冷却后进行减压过滤、洗涤,干燥,得到前驱物。
Ⅱ.制备铁酸锌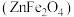
将步骤Ⅰ所得前驱物在 灼烧
灼烧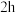 ,冷却后称量质量为
,冷却后称量质量为 ,计算产率。
,计算产率。
回答下列问题:
(1)步骤Ⅰ中配制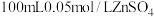 溶液需要的玻璃仪器有烧杯、量筒、胶头滴管、
溶液需要的玻璃仪器有烧杯、量筒、胶头滴管、 容量瓶和
容量瓶和___________ 。下列关于容量瓶的操作,正确的是___________ (填标号)。 晶体,加水溶解,滴加
晶体,加水溶解,滴加___________ (填写试剂名称),无明显现象,由此可知样品___________ (填“已”或“未”)变质。
(3)步骤Ⅰ中检验沉淀是否洗涤干净的操作是___________ 。
(4)步骤Ⅱ中“灼烧”发生的反应属于分解反应,其化学方程式为___________ 。
(5)该实验的总产率为___________ 。
(6) 晶体的一种晶胞结构如图所示,晶胞可看成由A、B单元按C方式交替排布构成,“○”表示
晶体的一种晶胞结构如图所示,晶胞可看成由A、B单元按C方式交替排布构成,“○”表示 。则“●”表示的微粒是
。则“●”表示的微粒是___________ (填符号), 晶体的密度为
晶体的密度为___________  (已知晶胞参数为
(已知晶胞参数为 ,列出计算式)。
,列出计算式)。
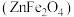 是一种性能优良的软磁材料,可作烯类有机化合物氧化脱氢的催化剂。实验室制备铁酸锌可采用如下步骤:
是一种性能优良的软磁材料,可作烯类有机化合物氧化脱氢的催化剂。实验室制备铁酸锌可采用如下步骤:Ⅰ.制备前驱物
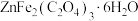
①分别配制
 溶液和
溶液和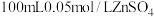 溶液,并将二者混合备用。
溶液,并将二者混合备用。②另外称取
 溶于
溶于 蒸馏水中。
蒸馏水中。③将①和②所得溶液混合加热到
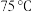 ,并在
,并在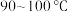 加热搅拌
加热搅拌 ;待溶液冷却后进行减压过滤、洗涤,干燥,得到前驱物。
;待溶液冷却后进行减压过滤、洗涤,干燥,得到前驱物。Ⅱ.制备铁酸锌
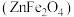
将步骤Ⅰ所得前驱物在
 灼烧
灼烧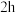 ,冷却后称量质量为
,冷却后称量质量为 ,计算产率。
,计算产率。回答下列问题:
(1)步骤Ⅰ中配制
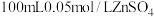 溶液需要的玻璃仪器有烧杯、量筒、胶头滴管、
溶液需要的玻璃仪器有烧杯、量筒、胶头滴管、 容量瓶和
容量瓶和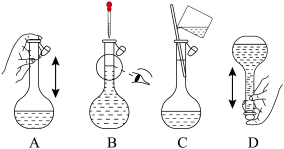
 晶体,加水溶解,滴加
晶体,加水溶解,滴加(3)步骤Ⅰ中检验沉淀是否洗涤干净的操作是
(4)步骤Ⅱ中“灼烧”发生的反应属于分解反应,其化学方程式为
(5)该实验的总产率为
(6)
 晶体的一种晶胞结构如图所示,晶胞可看成由A、B单元按C方式交替排布构成,“○”表示
晶体的一种晶胞结构如图所示,晶胞可看成由A、B单元按C方式交替排布构成,“○”表示 。则“●”表示的微粒是
。则“●”表示的微粒是 晶体的密度为
晶体的密度为 (已知晶胞参数为
(已知晶胞参数为 ,列出计算式)。
,列出计算式)。
您最近一年使用:0次
解题方法
5 . 下列解释事实的离子方程式或化学方程式书写错误的是
A.铜在存在 的环境中被氧气腐蚀: 的环境中被氧气腐蚀: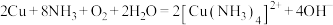 |
B.锌锰碱性电池放电时正极反应式: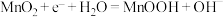 |
C.向冷的石灰乳中通入 制漂白粉: 制漂白粉: |
D.一定条件下,由乳酸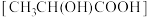 合成聚乳酸的化学方程式: 合成聚乳酸的化学方程式: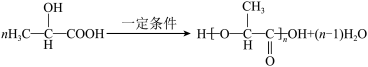 |
您最近一年使用:0次
6 . 亚硝酸钠 是工业用盐,具有着色、增色、抑菌、防腐等作用。实验室将一定量已知的高锰酸钾标准液放入锥形瓶中再加入硫酸,用亚硝酸钠滴定高锰酸钾标准液,进行样品中亚硝酸钠的含量分析。下列有关说法错误的是
是工业用盐,具有着色、增色、抑菌、防腐等作用。实验室将一定量已知的高锰酸钾标准液放入锥形瓶中再加入硫酸,用亚硝酸钠滴定高锰酸钾标准液,进行样品中亚硝酸钠的含量分析。下列有关说法错误的是
 是工业用盐,具有着色、增色、抑菌、防腐等作用。实验室将一定量已知的高锰酸钾标准液放入锥形瓶中再加入硫酸,用亚硝酸钠滴定高锰酸钾标准液,进行样品中亚硝酸钠的含量分析。下列有关说法错误的是
是工业用盐,具有着色、增色、抑菌、防腐等作用。实验室将一定量已知的高锰酸钾标准液放入锥形瓶中再加入硫酸,用亚硝酸钠滴定高锰酸钾标准液,进行样品中亚硝酸钠的含量分析。下列有关说法错误的是A.滴定前滴定管尖嘴处有气泡,滴定后无气泡会使测得的 含量偏高 含量偏高 |
B.亚硝酸根( )空间结构为V形 )空间结构为V形 |
| C.酸性高锰酸钾溶液可以鉴别食盐和亚硝酸钠 |
D.滴定过程离子反应为: |
您最近一年使用:0次
7 . 已知:
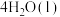
 ,设NA为阿伏伽德罗常数的数值。下列说法正确的是
,设NA为阿伏伽德罗常数的数值。下列说法正确的是

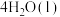
 ,设NA为阿伏伽德罗常数的数值。下列说法正确的是
,设NA为阿伏伽德罗常数的数值。下列说法正确的是A.0.1  溶液中含有NA个K+ 溶液中含有NA个K+ |
B.1mol  参与反应断裂的π键数目为NA 参与反应断裂的π键数目为NA |
C.反应每放出m kJ的热量,生成NA个 分子 分子 |
| D.每转移10NA个电子,产生CO2的体积标况下约为44.8L |
您最近一年使用:0次
8 . 焦锑酸钠 可用于制作电视机显像管玻壳、纺织品阻燃剂和搪瓷乳白剂。以某含锑净渣(主要成分是SbOCl,还含有少量Cu、As等元素)为原料制备焦锑酸钠的工艺流程如下图所示。
可用于制作电视机显像管玻壳、纺织品阻燃剂和搪瓷乳白剂。以某含锑净渣(主要成分是SbOCl,还含有少量Cu、As等元素)为原料制备焦锑酸钠的工艺流程如下图所示。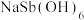 难溶于水。
难溶于水。
②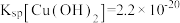 ,
, 。
。
回答下列问题:
(1)含锑净渣需进行粉碎研磨,其目的是_______ ,“浸渣”的主要成分是_______ (填“ ”或“CuS”)。
”或“CuS”)。
(2)“碱溶”时SbOCl转化为Na3SbS3,转化的化学方程式为_______ 。
(3)“氧化”时,溶液中的 转化为易溶于水的Na3AsO4与锑分离,同时生成S,写出该反应的离子方程式
转化为易溶于水的Na3AsO4与锑分离,同时生成S,写出该反应的离子方程式_______ 。
(4)“滤液”的主要成分是_______ 。
(5)产品纯度测定:称取1.30gNaSb(OH)6样品,酸溶后加入适量硫酸肼固体配成250mL溶液,取25.00mL溶液于锥形瓶中,用0.0500mol·L-1Ce(SO4)2标准液滴定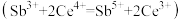 ,平均消耗标准液20.00mL。
,平均消耗标准液20.00mL。
①硫酸肼的作用是_______ 。
②产品的纯度为_______ [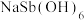 的摩尔质量为247g·mol-1]。
的摩尔质量为247g·mol-1]。
 可用于制作电视机显像管玻壳、纺织品阻燃剂和搪瓷乳白剂。以某含锑净渣(主要成分是SbOCl,还含有少量Cu、As等元素)为原料制备焦锑酸钠的工艺流程如下图所示。
可用于制作电视机显像管玻壳、纺织品阻燃剂和搪瓷乳白剂。以某含锑净渣(主要成分是SbOCl,还含有少量Cu、As等元素)为原料制备焦锑酸钠的工艺流程如下图所示。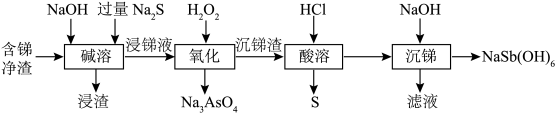
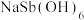 难溶于水。
难溶于水。②
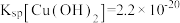 ,
, 。
。回答下列问题:
(1)含锑净渣需进行粉碎研磨,其目的是
 ”或“CuS”)。
”或“CuS”)。(2)“碱溶”时SbOCl转化为Na3SbS3,转化的化学方程式为
(3)“氧化”时,溶液中的
 转化为易溶于水的Na3AsO4与锑分离,同时生成S,写出该反应的离子方程式
转化为易溶于水的Na3AsO4与锑分离,同时生成S,写出该反应的离子方程式(4)“滤液”的主要成分是
(5)产品纯度测定:称取1.30gNaSb(OH)6样品,酸溶后加入适量硫酸肼固体配成250mL溶液,取25.00mL溶液于锥形瓶中,用0.0500mol·L-1Ce(SO4)2标准液滴定
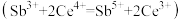 ,平均消耗标准液20.00mL。
,平均消耗标准液20.00mL。①硫酸肼的作用是
②产品的纯度为
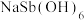 的摩尔质量为247g·mol-1]。
的摩尔质量为247g·mol-1]。
您最近一年使用:0次
解题方法
9 . 近日,清华大学某课题组报道了一种在碳纳米管上负载金属钴酞菁的分子催化剂(CoPc/CNT),实现了一步电化学乙烯( )制备乙二醇(EG),其可能反应机理如图所示:
)制备乙二醇(EG),其可能反应机理如图所示:
 )制备乙二醇(EG),其可能反应机理如图所示:
)制备乙二醇(EG),其可能反应机理如图所示: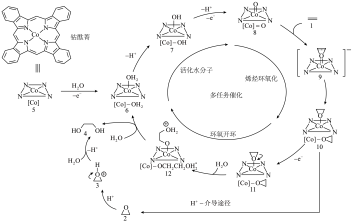
已知: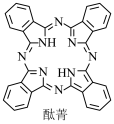 为平面形分子。
为平面形分子。
A.酞菁分子中氮原子的杂化类型为 、 、 |
| B.步骤“5→6”中钴元素被还原 |
| C.上述反应过程中没有极性键的形成 |
D.步骤“2→3→4”的总反应为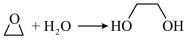 |
您最近一年使用:0次
名校
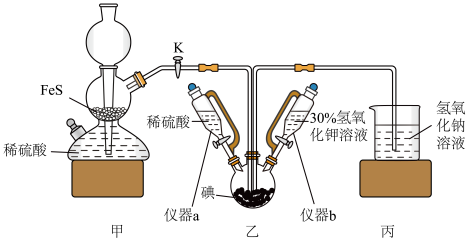
10 . 碘化钾用作制有机化合物及制药原料,医疗上用于防治甲状腺肿和甲状腺机能亢进的手术前准备,也可用作祛痰药。某实验室通过碘酸钾和硫化氢反应制备碘化钾。实验装置如图所示(夹持及加热装置已省略)回答下列问题:___________ ,实验中先关闭K,打开仪器___________ (填“a”、“b”或“ab”)制备碘酸钾,其反应的离子方程式为___________ 。某同学认为可以将甲装置中的 更换为粉末状
更换为粉末状 固体,你认为是否合理?
固体,你认为是否合理?___________ (填“合理”、“不合理”或“无法判断”)。
(2)乙装置中加入稀 的主要作用是
的主要作用是___________ 。
(3)如果乙装置最终生成 黄色沉淀,理论上可制得碘化钾的质量为
黄色沉淀,理论上可制得碘化钾的质量为___________ g。
(4)本实验尾气中的硫化氢可以用 溶液吸收,也可以用
溶液吸收,也可以用 溶液吸收。向
溶液吸收。向 溶液中通尾气直至饱和(
溶液中通尾气直至饱和( )时,溶液中刚好有
)时,溶液中刚好有 沉淀生成,此时溶液中
沉淀生成,此时溶液中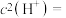
___________  (结果保留四位有效数字)。(已知
(结果保留四位有效数字)。(已知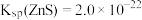 ,
, 的
的 ,
,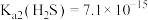 。)
。)
 更换为粉末状
更换为粉末状 固体,你认为是否合理?
固体,你认为是否合理?(2)乙装置中加入稀
 的主要作用是
的主要作用是(3)如果乙装置最终生成
 黄色沉淀,理论上可制得碘化钾的质量为
黄色沉淀,理论上可制得碘化钾的质量为(4)本实验尾气中的硫化氢可以用
 溶液吸收,也可以用
溶液吸收,也可以用 溶液吸收。向
溶液吸收。向 溶液中通尾气直至饱和(
溶液中通尾气直至饱和( )时,溶液中刚好有
)时,溶液中刚好有 沉淀生成,此时溶液中
沉淀生成,此时溶液中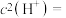
 (结果保留四位有效数字)。(已知
(结果保留四位有效数字)。(已知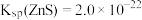 ,
, 的
的 ,
,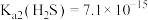 。)
。)
您最近一年使用:0次
2024-05-12更新
|
104次组卷
|
2卷引用:安徽师范大学附属中学2024届高三下学期5月测试化学试卷



