名校
解题方法
1 . 钼( )及其化合物广泛地应用于医疗卫生、国防等领域。某镍钼矿中的镍和钼以
)及其化合物广泛地应用于医疗卫生、国防等领域。某镍钼矿中的镍和钼以 和
和 形式存在,从镍钼矿中分离钼,并得到
形式存在,从镍钼矿中分离钼,并得到 的一种工艺流程如下:
的一种工艺流程如下:
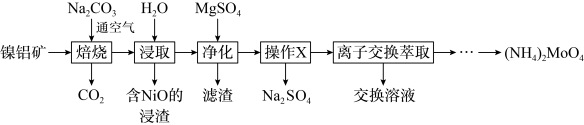
回答下列问题:
(1) 位于元素周期表第
位于元素周期表第_______ 周期第_______ 族。 中钼元素的化合价为
中钼元素的化合价为_______ 。
(2)“焙烧”中生成 的化学方程式为
的化学方程式为_______ 。
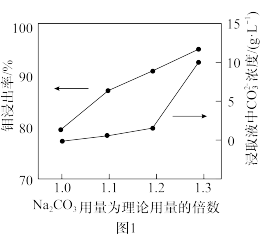
(3) 用量对钼浸出率和浸取液中
用量对钼浸出率和浸取液中 浓度的影响如图1所示,分析实际生产中选择
浓度的影响如图1所示,分析实际生产中选择 用量为理论用量1.2倍的原因:
用量为理论用量1.2倍的原因:_______ 。
(4) 的溶解度曲线如图2所示,为充分分离
的溶解度曲线如图2所示,为充分分离 ,工艺流程中的“操作
,工艺流程中的“操作 ”应为_______(填标号)。
”应为_______(填标号)。

(5)为充分利用资源,“离子交换萃取”步骤产生的交换溶液应返回“_______ ”步骤。
(6) 分解可得
分解可得 。高温下,用铝粉还原
。高温下,用铝粉还原 得到金属钼的化学方程式为
得到金属钼的化学方程式为_______ 。
 )及其化合物广泛地应用于医疗卫生、国防等领域。某镍钼矿中的镍和钼以
)及其化合物广泛地应用于医疗卫生、国防等领域。某镍钼矿中的镍和钼以 和
和 形式存在,从镍钼矿中分离钼,并得到
形式存在,从镍钼矿中分离钼,并得到 的一种工艺流程如下:
的一种工艺流程如下:
回答下列问题:
(1)
 位于元素周期表第
位于元素周期表第 中钼元素的化合价为
中钼元素的化合价为(2)“焙烧”中生成
 的化学方程式为
的化学方程式为(3)
 用量对钼浸出率和浸取液中
用量对钼浸出率和浸取液中 浓度的影响如图1所示,分析实际生产中选择
浓度的影响如图1所示,分析实际生产中选择 用量为理论用量1.2倍的原因:
用量为理论用量1.2倍的原因:
(4)
 的溶解度曲线如图2所示,为充分分离
的溶解度曲线如图2所示,为充分分离 ,工艺流程中的“操作
,工艺流程中的“操作 ”应为_______(填标号)。
”应为_______(填标号)。
| A.蒸发结晶 | B.低温结晶 | C.蒸馏 | D.萃取 |
(5)为充分利用资源,“离子交换萃取”步骤产生的交换溶液应返回“
(6)
 分解可得
分解可得 。高温下,用铝粉还原
。高温下,用铝粉还原 得到金属钼的化学方程式为
得到金属钼的化学方程式为
您最近一年使用:0次
2024-01-22更新
|
1131次组卷
|
7卷引用:2024年1月安徽普通高等学校招生考试适应性测试化学试题
2024年1月安徽普通高等学校招生考试适应性测试化学试题(已下线)T16-工业流程题(已下线)2024年1月“九省联考”安徽真题完全解读与考后提升(已下线)热点23 化学工艺流程综合题(已下线)专题08 工艺流程综合题-【好题汇编】2024年高考化学一模试题分类汇编(新高考七省专用)黑龙江省大庆市大庆中学2023-2024学年高三下学期开学化学试题江西省宜春市丰城市第九中学2023-2024学年高三(复读班)上学期期末考试化学试题
名校
解题方法
2 . 完成下列问题。
(1)向氢氧化铁胶体中逐滴滴入氢碘酸至过量,实验现象________ ,原因是___________ (并写出相关的离子方程式)。
(2)向溴化亚铁和碘化亚铁溶液中通入氯气,依据图像写出相应的离子方程式:
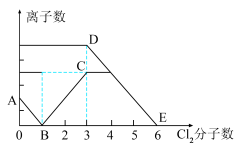
①AB段:___________ 。
②BC段:___________ 。
③DE段:___________ 。
④溶液中I-:Br-:Fe2+粒子数目之比为______ 。
(1)向氢氧化铁胶体中逐滴滴入氢碘酸至过量,实验现象
(2)向溴化亚铁和碘化亚铁溶液中通入氯气,依据图像写出相应的离子方程式:

①AB段:
②BC段:
③DE段:
④溶液中I-:Br-:Fe2+粒子数目之比为
您最近一年使用:0次
3 . 铼(Re)是一种熔点高、耐磨、耐腐蚀的金属,广泛用于航天航空等领域。
某实验室制备铼的原理如下:
Ⅰ.①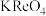 先与
先与 反应生成
反应生成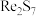 。
。
②滴入足量的含 的氨水溶液,生成
的氨水溶液,生成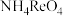 ,同时有
,同时有 生成,装置如图1所示。
生成,装置如图1所示。
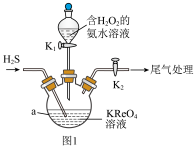
(1)仪器a的名称是___________ 。
(2)金属铼比同周期的Ba熔点高,从结构的角度解释原因是___________ 。
(3)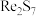 生成
生成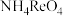 的化学方程式是
的化学方程式是___________ 。
Ⅱ.用氢气还原Ⅰ中生成的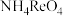 得到Re。实验装置如图2所示。
得到Re。实验装置如图2所示。
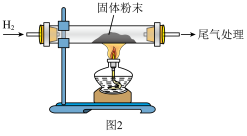
(4)在加热实验装置前,先通入一段时间的氢气,再___________ ,最后点燃酒精灯;停止实验时,先关闭酒精灯,再持续通一段时间 。制备Re反应的化学方程式为
。制备Re反应的化学方程式为___________ 。
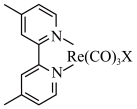
(5)铼可形成多种配位化合物,下图是它的一种配位化合物的结构(X表示卤素原子),其中碳原子的杂化方式为___________ ,Re的配位数为___________ 。
某实验室制备铼的原理如下:
Ⅰ.①
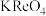 先与
先与 反应生成
反应生成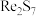 。
。②滴入足量的含
 的氨水溶液,生成
的氨水溶液,生成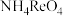 ,同时有
,同时有 生成,装置如图1所示。
生成,装置如图1所示。
(1)仪器a的名称是
(2)金属铼比同周期的Ba熔点高,从结构的角度解释原因是
(3)
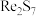 生成
生成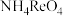 的化学方程式是
的化学方程式是Ⅱ.用氢气还原Ⅰ中生成的
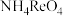 得到Re。实验装置如图2所示。
得到Re。实验装置如图2所示。
(4)在加热实验装置前,先通入一段时间的氢气,再
 。制备Re反应的化学方程式为
。制备Re反应的化学方程式为(5)铼可形成多种配位化合物,下图是它的一种配位化合物的结构(X表示卤素原子),其中碳原子的杂化方式为

您最近一年使用:0次
4 . 1868年狄肯和洪特发明了用氯化铜作催化剂,加热空气来氧化氯化氢制取氯气。该反应的能量变化关系如图所示,下列叙述错误的是


| A.反应物总能量高于生成物的总能量 |
B.若a、b曲线均使用了催化剂,则催化效果: |
C.反应放出28.9kJ热量时有 电子发生转移 电子发生转移 |
D.若反应生成 液态水,放出的热量低于115.6kJ 液态水,放出的热量低于115.6kJ |
您最近一年使用:0次
名校
5 . 氧化还原反应在人类的生产、生活中有着重要的应用。回答下列问题:
(1)我国古代四大发明之一的黑火药是由硫黄粉、硝酸钾和木炭按一定比例混合而成的,爆炸时发生的反应为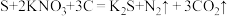 。该反应中,被还原的元素是
。该反应中,被还原的元素是________ (填元素符号),消耗的还原剂和氧化剂质量比为_________ 。
(2)实验室制备Cl2有三种常用方法:
a.
b.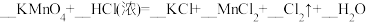
c.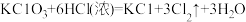
①配平反应b的方程式:___________ 。
②当三个反应中参与反应的HCl的质量相同时,得到Cl2的质量最多的是反应_____ (填“a”“b”或“c”)。
(3)以MnO2为原料在加热熔融条件下可以制取K2MnO4,该反应中包含的所有物质为MnO2、K2 MnO4、KCl、KOH、KClO3、H2O。写出该反应的化学方程式:___________ 。
(4)油画创作通常需要用到多种无机颜料。研究发现,在不同的空气湿度和光照条件下,颜料雌黄(As2S3,As为+3价,S为-2价)褪色的主要原因是发生了以下两种化学反应:
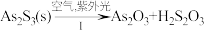 ,
,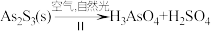 。则反应I和Ⅱ中氧化相同量的As2S3,消耗O2与H2O的化学计量数之比:I
。则反应I和Ⅱ中氧化相同量的As2S3,消耗O2与H2O的化学计量数之比:I______ Ⅱ(填“>”“<”或“=”),转移的电子数之比为_______ 。
(1)我国古代四大发明之一的黑火药是由硫黄粉、硝酸钾和木炭按一定比例混合而成的,爆炸时发生的反应为
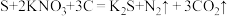 。该反应中,被还原的元素是
。该反应中,被还原的元素是(2)实验室制备Cl2有三种常用方法:
a.

b.
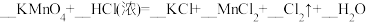
c.
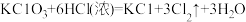
①配平反应b的方程式:
②当三个反应中参与反应的HCl的质量相同时,得到Cl2的质量最多的是反应
(3)以MnO2为原料在加热熔融条件下可以制取K2MnO4,该反应中包含的所有物质为MnO2、K2 MnO4、KCl、KOH、KClO3、H2O。写出该反应的化学方程式:
(4)油画创作通常需要用到多种无机颜料。研究发现,在不同的空气湿度和光照条件下,颜料雌黄(As2S3,As为+3价,S为-2价)褪色的主要原因是发生了以下两种化学反应:
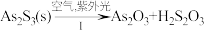 ,
,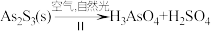 。则反应I和Ⅱ中氧化相同量的As2S3,消耗O2与H2O的化学计量数之比:I
。则反应I和Ⅱ中氧化相同量的As2S3,消耗O2与H2O的化学计量数之比:I
您最近一年使用:0次
解题方法
6 . 化学源于生活,下列物质为生活中常见的日用品,括号内为对应物品的主要成分或有效成分。
①食盐(NaCl) ②食醋(醋酸) ③碱面( ) ④双氧水(
) ④双氧水( ) ⑤高锰酸钾消毒液(
) ⑤高锰酸钾消毒液( ) ⑥洁厕灵(HCl) ⑦84消毒液(NaClO) ⑧管道疏通剂(NaOH和铝粉)
) ⑥洁厕灵(HCl) ⑦84消毒液(NaClO) ⑧管道疏通剂(NaOH和铝粉)
回答下列问题:
(1)以上物质的主要成分或有效成分属于盐的是__________ (填序号)。
(2)若要鉴别某白色固体是食盐还是碱面,可以用____________ (填序号)来鉴别,若白色固体是碱面,观察到的现象是___________________________ 。
(3)酸性 和
和 会发生如下反应:
会发生如下反应:
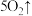 ,该反应的氧化产物为
,该反应的氧化产物为_________ ,若反应过程中转移2mol  ,参与反应的
,参与反应的 的物质的量为
的物质的量为____________ 。
(4)在清洗卫生间时,84消毒液和洁厕灵不能混合使用,用离子方程式表示其原因:____________________ ;84消毒液能与 反应生成具有漂白作用的HClO,该反应的化学方程式为
反应生成具有漂白作用的HClO,该反应的化学方程式为____________________ 。
(5)家庭厨卫管道内常因毛发、菜渣、纸棉纤维等而造成堵塞,请用化学方程式表示管道疏通剂的疏通原理:___________________________________________ 。
①食盐(NaCl) ②食醋(醋酸) ③碱面(
 ) ④双氧水(
) ④双氧水( ) ⑤高锰酸钾消毒液(
) ⑤高锰酸钾消毒液( ) ⑥洁厕灵(HCl) ⑦84消毒液(NaClO) ⑧管道疏通剂(NaOH和铝粉)
) ⑥洁厕灵(HCl) ⑦84消毒液(NaClO) ⑧管道疏通剂(NaOH和铝粉)回答下列问题:
(1)以上物质的主要成分或有效成分属于盐的是
(2)若要鉴别某白色固体是食盐还是碱面,可以用
(3)酸性
 和
和 会发生如下反应:
会发生如下反应:
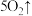 ,该反应的氧化产物为
,该反应的氧化产物为 ,参与反应的
,参与反应的 的物质的量为
的物质的量为(4)在清洗卫生间时,84消毒液和洁厕灵不能混合使用,用离子方程式表示其原因:
 反应生成具有漂白作用的HClO,该反应的化学方程式为
反应生成具有漂白作用的HClO,该反应的化学方程式为(5)家庭厨卫管道内常因毛发、菜渣、纸棉纤维等而造成堵塞,请用化学方程式表示管道疏通剂的疏通原理:
您最近一年使用:0次
名校
7 . 下图为氯及其化合物的“价-类”二维图,请按要求填空。
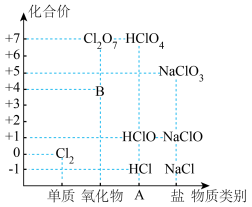
(1)填写二维图中缺失的类别A为___________ ,B的化学式为___________ 。
(2)某同学利用以下试剂研究 的性质,进行以下预测:
的性质,进行以下预测:
从物质类别上看, 属于
属于___________ (填“强”或“弱”)酸,所以可与___________ (填序号)反应,写出其离子反应方程式:___________ 。
a. 溶液 b.
溶液 b. 溶液 c.
溶液 c. 溶液
溶液
(3)①用 配成的
配成的 溶液,与
溶液,与 恰好完全反应(忽略溶液体积变化),
恰好完全反应(忽略溶液体积变化), 与
与 溶液反应可生成
溶液反应可生成 和
和 ,则反应后溶液中
,则反应后溶液中 为
为___________  。
。
②我国从2000年起逐步用 替代氯气进行消毒,工业上常利用反应
替代氯气进行消毒,工业上常利用反应 制备
制备 ,其中氧化产物是
,其中氧化产物是___________ (填化学式)。 的消毒效率是
的消毒效率是 的
的___________ 倍(保留小数点后一位)(还原产物都为 ,消毒效率以单位质量的物质得到的电子数表示)。
,消毒效率以单位质量的物质得到的电子数表示)。

(1)填写二维图中缺失的类别A为
(2)某同学利用以下试剂研究
 的性质,进行以下预测:
的性质,进行以下预测:从物质类别上看,
 属于
属于a.
 溶液 b.
溶液 b. 溶液 c.
溶液 c. 溶液
溶液(3)①用
 配成的
配成的 溶液,与
溶液,与 恰好完全反应(忽略溶液体积变化),
恰好完全反应(忽略溶液体积变化), 与
与 溶液反应可生成
溶液反应可生成 和
和 ,则反应后溶液中
,则反应后溶液中 为
为 。
。②我国从2000年起逐步用
 替代氯气进行消毒,工业上常利用反应
替代氯气进行消毒,工业上常利用反应 制备
制备 ,其中氧化产物是
,其中氧化产物是 的消毒效率是
的消毒效率是 的
的 ,消毒效率以单位质量的物质得到的电子数表示)。
,消毒效率以单位质量的物质得到的电子数表示)。
您最近一年使用:0次
名校
8 .  与
与 在不同条件下会发生不同的反应(F在化合物中呈现
在不同条件下会发生不同的反应(F在化合物中呈现 价)。常温条件下,
价)。常温条件下, 与水发生反应①:
与水发生反应①: ;
;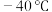 条件下,
条件下, 与冰发生反应②:
与冰发生反应②: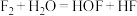 。下列有关上述反应叙述错误的是
。下列有关上述反应叙述错误的是
 与
与 在不同条件下会发生不同的反应(F在化合物中呈现
在不同条件下会发生不同的反应(F在化合物中呈现 价)。常温条件下,
价)。常温条件下, 与水发生反应①:
与水发生反应①: ;
;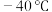 条件下,
条件下, 与冰发生反应②:
与冰发生反应②: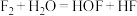 。下列有关上述反应叙述错误的是
。下列有关上述反应叙述错误的是A.反应①和②中 均作氧化剂 均作氧化剂 |
B.反应②中氧化产物是 ,还原产物是 ,还原产物是 |
C.在不同条件下,等量的 与 与 反应转移电子数相同 反应转移电子数相同 |
D.反应①中生成标准状况下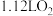 ,转移电子数为 ,转移电子数为 |
您最近一年使用:0次
名校
9 . 草酸( )为无色晶体,是一种二元弱酸,在实验研究和化学工业上有着广泛的应用。某化学实验小组设计实验探究
)为无色晶体,是一种二元弱酸,在实验研究和化学工业上有着广泛的应用。某化学实验小组设计实验探究 ,的制备及有关性质实验。
,的制备及有关性质实验。
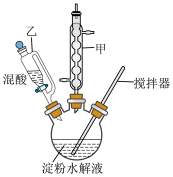
回答下列问题:
I.制备
查阅资料,利用淀粉的水解液,在浓硫酸催化作用下用硝酸氧化可得 (装置如图,加热及夹持仪器已省略)。
(装置如图,加热及夹持仪器已省略)。
(1)实验时___________ (填“必需”或“无需”)打开仪器乙的玻璃塞,仪器甲冷凝水必须从下口通入,原因是_________________________________ 。
(2)反应温度控制不超过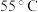 ,可采用的方法是
,可采用的方法是_________________________________ 。
(3)下列可以证明 是弱电解质的是___________(填字母)。
是弱电解质的是___________(填字母)。
Ⅱ.有关性质实验
小组同学拟用溶液与 溶液的反应(用作指示剂)来探究“外界条件对化学反应速率的影响”,实验记录如下:
溶液的反应(用作指示剂)来探究“外界条件对化学反应速率的影响”,实验记录如下:
(4) 溶液与
溶液与 反应,溶液立即呈紫红色,写出该反应的离子方程式:
反应,溶液立即呈紫红色,写出该反应的离子方程式:____________________ 。
(5)表格中a、b的数值分别为___________ 、___________ , 、
、 、
、 数值最大的是
数值最大的是___________ 。
(6)实验编号①④的目的是探究___________ 对化学反应速率的影响。
 )为无色晶体,是一种二元弱酸,在实验研究和化学工业上有着广泛的应用。某化学实验小组设计实验探究
)为无色晶体,是一种二元弱酸,在实验研究和化学工业上有着广泛的应用。某化学实验小组设计实验探究 ,的制备及有关性质实验。
,的制备及有关性质实验。
回答下列问题:
I.制备

查阅资料,利用淀粉的水解液,在浓硫酸催化作用下用硝酸氧化可得
 (装置如图,加热及夹持仪器已省略)。
(装置如图,加热及夹持仪器已省略)。(1)实验时
(2)反应温度控制不超过
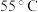 ,可采用的方法是
,可采用的方法是(3)下列可以证明
 是弱电解质的是___________(填字母)。
是弱电解质的是___________(填字母)。| A.向草酸溶液中滴加石蕊,溶液呈红色 |
B.室温下,测得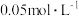 的 的 溶液的 溶液的 约为3 约为3 |
C.室温下,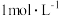 的 的 溶液的 溶液的 |
D.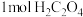 完全反应消耗 完全反应消耗 |
Ⅱ.有关性质实验
小组同学拟用溶液与
 溶液的反应(用作指示剂)来探究“外界条件对化学反应速率的影响”,实验记录如下:
溶液的反应(用作指示剂)来探究“外界条件对化学反应速率的影响”,实验记录如下:编号 |
| V( | V( | V(蒸馏水)/ | 变色时间/s |
① | 25 | 2.0 | 8.0 | 0 |
|
② | 25 | 2.0 | 5.0 | a |
|
③ | 25 | 2.0 | b | 2 |
|
④ | 30 | 2.0 | 8.0 | 0 |
|
(4)
 溶液与
溶液与 反应,溶液立即呈紫红色,写出该反应的离子方程式:
反应,溶液立即呈紫红色,写出该反应的离子方程式:(5)表格中a、b的数值分别为
 、
、 、
、 数值最大的是
数值最大的是(6)实验编号①④的目的是探究
您最近一年使用:0次
名校
解题方法
10 . 廉价的“84消毒液”能有效杀灭病毒。有效氯含量是衡量含氯消毒液的消毒能力的物理量,有效氯含量指一定量消毒剂的氧化能力相当于多少Cl2氧化能力。
(1)某同学欲用NaClO固体配制有效氯含量为35.5g·L-184消毒液960mL,用托盘天平称量NaClO的质量为___________ 。
(2)配制该消毒液的几个关键操作步骤中有错误的操作是___________
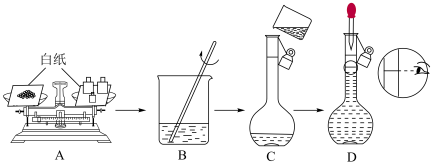
(3)若定容操作时仰视观察,配制溶液的浓度将___________ (填“偏大”“偏小”“无影响”);若有误差将如何处理完成实验?___________ 。
(4)①在适当的条件下NaClO溶液可以除去生活污水中的氨氮(以NH3计算)生成无污染性气体,该反应的离子方程式为___________ 。
②实验发现废水中的氨氮去除率与溶液pH、温度及次氯酸钠投入量等因素有关。
其他条件一定时,氨氮去除率与温度的关系如下图所示(已知NaClO+H2O NaOH+HClO)。
NaOH+HClO)。
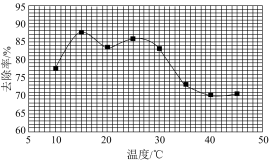
实验现象可知用NaClO消除生活污水中的氨氮选择的合适温度为___________ ;当温度高于30℃时,温度越高,氨氮去除率减小的原因可能是___________ 。
(1)某同学欲用NaClO固体配制有效氯含量为35.5g·L-184消毒液960mL,用托盘天平称量NaClO的质量为
(2)配制该消毒液的几个关键操作步骤中有错误的操作是

(3)若定容操作时仰视观察,配制溶液的浓度将
(4)①在适当的条件下NaClO溶液可以除去生活污水中的氨氮(以NH3计算)生成无污染性气体,该反应的离子方程式为
②实验发现废水中的氨氮去除率与溶液pH、温度及次氯酸钠投入量等因素有关。
其他条件一定时,氨氮去除率与温度的关系如下图所示(已知NaClO+H2O
 NaOH+HClO)。
NaOH+HClO)。
实验现象可知用NaClO消除生活污水中的氨氮选择的合适温度为
您最近一年使用:0次

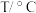
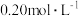 的
的
 的
的


