1 . 铼常用作催化剂。工业上,常从冶炼铜的富铼渣(含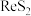 )中提取铼,工艺流程如下:
)中提取铼,工艺流程如下:
①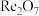 是酸性氧化物,高铼酸(
是酸性氧化物,高铼酸(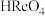 )是一元强酸。
)是一元强酸。
②高铼酸铵( )微溶于冷水,易溶于热水。
)微溶于冷水,易溶于热水。
下列说法正确的是
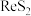 )中提取铼,工艺流程如下:
)中提取铼,工艺流程如下: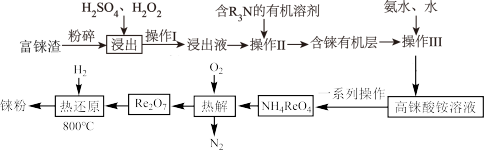
①
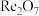 是酸性氧化物,高铼酸(
是酸性氧化物,高铼酸(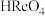 )是一元强酸。
)是一元强酸。②高铼酸铵(
 )微溶于冷水,易溶于热水。
)微溶于冷水,易溶于热水。下列说法正确的是
A.高铼酸在含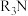 的有机溶剂中的溶解度小于在水中的溶解度 的有机溶剂中的溶解度小于在水中的溶解度 |
B.高铼酸铵溶液加热蒸发结晶得到 |
| C.“热解”时,氧化剂与还原剂的物质的量之比为4∶3 |
D.测得“浸出液”含 ,浸出时的离子方程式为 ,浸出时的离子方程式为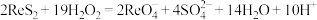 |
您最近一年使用:0次
解题方法
2 . 铁盐的氧化性
(1)取3 mLFeCl3稀溶液加入试管中,加入几小块铜片,振荡,过一会儿,观察到的现象是铜片_______ ,溶液_______ ,化学方程式:_______ 。
(2)在一支盛有3 mL水的试管中滴加几滴FeCl3稀溶液,再滴加3滴KI溶液,观察到的现象是溶液_______ ,然后向溶液中滴加2滴淀粉溶液,溶液_______ ,离子方程式:_______ 。
(1)取3 mLFeCl3稀溶液加入试管中,加入几小块铜片,振荡,过一会儿,观察到的现象是铜片
(2)在一支盛有3 mL水的试管中滴加几滴FeCl3稀溶液,再滴加3滴KI溶液,观察到的现象是溶液
您最近一年使用:0次
3 .  是重要的化工原料,软锰矿制备
是重要的化工原料,软锰矿制备 的一种工艺流程如图:
的一种工艺流程如图:
软锰矿
资料:①软锰矿的主要成分为 ,主要杂质有
,主要杂质有 和
和 ;
;
②金属离于沉淀的 。
。
③该工艺条件下, 与
与 反应。
反应。
(1)溶出
①溶出前,软锰矿需研磨。目的是_____ 。
②溶出时, 的氧化过程及得到
的氧化过程及得到 的主要途径如图所示:
的主要途径如图所示: 的主要反应,反应的离子方程式是
的主要反应,反应的离子方程式是_____ 。
ii.若 全部来源于反应
全部来源于反应 ,完全溶出
,完全溶出 所需
所需 与
与 的物质的量比值为2.而实际比值
的物质的量比值为2.而实际比值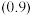 小于2,原因是
小于2,原因是_____ 。
(2)纯化。已知: 的氧化性与溶液
的氧化性与溶液 有关。纯化时先加入
有关。纯化时先加入 ,目的是
,目的是_____ ,后加入 ,调节溶液
,调节溶液 的区间是:
的区间是:_____ 。
(3)电解 纯化液经电解得
纯化液经电解得 。生成
。生成 的电极反应式是
的电极反应式是_____ 。
(4)写出铁原子 的电子排布式:
的电子排布式:_____ 。
 是重要的化工原料,软锰矿制备
是重要的化工原料,软锰矿制备 的一种工艺流程如图:
的一种工艺流程如图:软锰矿

资料:①软锰矿的主要成分为
 ,主要杂质有
,主要杂质有 和
和 ;
;②金属离于沉淀的
 。
。 |  |  |  | |
| 开始沉淀时 | 1.5 | 3.4 | 5.8 | 6.3 |
| 完全沉淀时 | 2.8 | 4.7 | 7.8 | 8.3 |
 与
与 反应。
反应。(1)溶出
①溶出前,软锰矿需研磨。目的是
②溶出时,
 的氧化过程及得到
的氧化过程及得到 的主要途径如图所示:
的主要途径如图所示: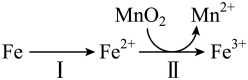
 的主要反应,反应的离子方程式是
的主要反应,反应的离子方程式是ii.若
 全部来源于反应
全部来源于反应 ,完全溶出
,完全溶出 所需
所需 与
与 的物质的量比值为2.而实际比值
的物质的量比值为2.而实际比值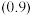 小于2,原因是
小于2,原因是(2)纯化。已知:
 的氧化性与溶液
的氧化性与溶液 有关。纯化时先加入
有关。纯化时先加入 ,目的是
,目的是 ,调节溶液
,调节溶液 的区间是:
的区间是:(3)电解
 纯化液经电解得
纯化液经电解得 。生成
。生成 的电极反应式是
的电极反应式是(4)写出铁原子
 的电子排布式:
的电子排布式:
您最近一年使用:0次
解题方法
4 . 利用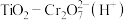 可快速测定水体化学需氧量,以
可快速测定水体化学需氧量,以 表示水体中的有机物,已知
表示水体中的有机物,已知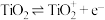 ,部分反应机理如图所示。下列叙述错误的是
,部分反应机理如图所示。下列叙述错误的是
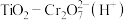 可快速测定水体化学需氧量,以
可快速测定水体化学需氧量,以 表示水体中的有机物,已知
表示水体中的有机物,已知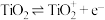 ,部分反应机理如图所示。下列叙述错误的是
,部分反应机理如图所示。下列叙述错误的是
A.该过程中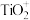 和 和 均表现出还原性 均表现出还原性 |
B.该过程中 是催化剂 是催化剂 |
C. 可以防止 可以防止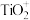 和 和 重新结合 重新结合 |
D.该过程的离子方程式可以表示为 |
您最近一年使用:0次
5 . 某兴趣小组为研究几种常见气体的性质,设计如下实验装置。已知实验室常用 与
与 反应制取
反应制取 气体。实验中N装置出现的现象记录如下表,其对应的反应离子方程式错误的是。
气体。实验中N装置出现的现象记录如下表,其对应的反应离子方程式错误的是。
 与
与 反应制取
反应制取 气体。实验中N装置出现的现象记录如下表,其对应的反应离子方程式错误的是。
气体。实验中N装置出现的现象记录如下表,其对应的反应离子方程式错误的是。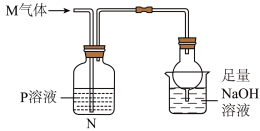
| 选项 | M | P | N中的实验现象 | N中的反应离子方程式 |
| A |  | 淀粉碘化钾溶液 | 溶液变蓝 |  |
| B |  | 氯化铁溶液 | 溶液黄色变浅,出现淡黄色沉淀 | 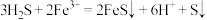 |
| C |  | 酸性高锰酸钾溶液 | 紫红色变浅 | 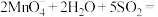 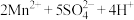 |
| C |  | 氢氧化钡溶液 | 白色沉淀 |  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
6 . 铜陵素有“中国古铜都,当代铜基地”之称,铜是人类祖先最早应用的金属。目前工业上生产铜以黄铜矿为原料(主要成分为 )火法冶炼铜,部分工业流程如下,其中熔炼反应为:
)火法冶炼铜,部分工业流程如下,其中熔炼反应为: 。
。 表示阿伏加德罗常数的值,下列说法错误的是。
表示阿伏加德罗常数的值,下列说法错误的是。
 )火法冶炼铜,部分工业流程如下,其中熔炼反应为:
)火法冶炼铜,部分工业流程如下,其中熔炼反应为: 。
。 表示阿伏加德罗常数的值,下列说法错误的是。
表示阿伏加德罗常数的值,下列说法错误的是。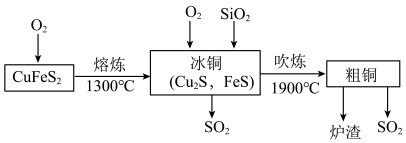
| A.青铜器表面易产生铜绿,文物修复专家常用稀硝酸浸泡 |
B.在熔炼反应中, 既是氧化剂也是还原剂 既是氧化剂也是还原剂 |
C. 尾气如直接排放可能会引起酸雨,可以回收用于生产硫酸 尾气如直接排放可能会引起酸雨,可以回收用于生产硫酸 |
D.生成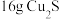 时,转移的电子数为 时,转移的电子数为 |
您最近一年使用:0次
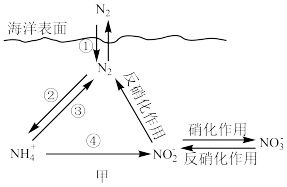
7 . 氮元素在海洋中的循环,是整个海洋生态系统的基础和关键,海洋中无机氮的循环过程可用图甲表示。回答下列问题:___________ (填图甲中编号)。
(2)有氧时,在硝化细菌的作用下, 可实现过程④的转化,若消耗
可实现过程④的转化,若消耗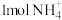 ,至少需
,至少需_______ mol氧气。
(3)已知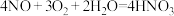 ,甲同学利用排空气法收集到一烧瓶的
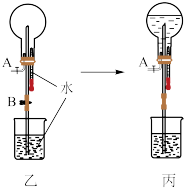
,甲同学利用排空气法收集到一烧瓶的 气体并搭建如图乙装置。关闭止水夹A和B后,挤压胶头滴管,一段时间后打开止水夹B,当烧瓶内液面不再变化后,烧瓶中仍然存在一定量气体(如图丙),对于残留气体的成分及原因,甲同学提出如下假设:
气体并搭建如图乙装置。关闭止水夹A和B后,挤压胶头滴管,一段时间后打开止水夹B,当烧瓶内液面不再变化后,烧瓶中仍然存在一定量气体(如图丙),对于残留气体的成分及原因,甲同学提出如下假设:
假设一:由于 与水反应产生NO,剩余气体可能主要是NO;
与水反应产生NO,剩余气体可能主要是NO;
假设二:排空气法收集的气体不纯,剩余气体可能主要是 。
。
乙同学打开止水夹A,缓慢通入少量 ,观察到烧瓶内液面继续升高,由此推断
,观察到烧瓶内液面继续升高,由此推断___________ (填“假设一”或“假设二”)成立。
(4)实验室制备 的方法有很多,以下为甲同学提出的方案,你认为合理的是
的方法有很多,以下为甲同学提出的方案,你认为合理的是___________ 。
A.加热 和
和 固体混合物
固体混合物
B. 、
、 混合气体在高温高压催化剂条件下反应
混合气体在高温高压催化剂条件下反应
C.将氨水缓慢滴入 固体中
固体中
D.将浓氨水缓慢滴入碱石灰中
E.加热 固体
固体
乙同学查阅资料发现 与
与 可结合为
可结合为 ,设计利用镁条在氮气中燃烧后的白色固体与水反应制取氨气,该方案如能实现请写出反应方程式:
,设计利用镁条在氮气中燃烧后的白色固体与水反应制取氨气,该方案如能实现请写出反应方程式:___________ 。
(5)已知有氧条件下, 可在催化剂作用下将NO还原为
可在催化剂作用下将NO还原为 ,某研究机构利用钒基催化剂
,某研究机构利用钒基催化剂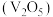 发生脱硝反应处理NO有害气体,机理如图所示。
发生脱硝反应处理NO有害气体,机理如图所示。 和NO物质的量之比为
和NO物质的量之比为 ,总反应的化学方程式为:
,总反应的化学方程式为:___________ 。
______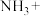 ______NO+______
______NO+______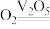 _______
_______ ______
______
(6) 也是一种有毒气体,已知
也是一种有毒气体,已知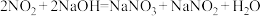 ,
,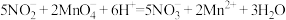 。某化工厂每天约产生2000立方米废气,其中
。某化工厂每天约产生2000立方米废气,其中 为主要有毒气体(不考虑
为主要有毒气体(不考虑 ),在洗气塔中利用
),在洗气塔中利用 溶液吸收废气中的
溶液吸收废气中的 ,每天约产生
,每天约产生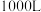 吸收液。某兴趣小组为了检测废气中
吸收液。某兴趣小组为了检测废气中 的含量,取
的含量,取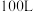 该吸收液,逐滴加入
该吸收液,逐滴加入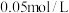 酸性高锰酸钾溶液,当滴入
酸性高锰酸钾溶液,当滴入 时恰好完全反应。则该厂废气中
时恰好完全反应。则该厂废气中 含量为
含量为___________ 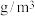 (提示:本题除
(提示:本题除 外,不考虑其它可能与酸性高锰酸钾反应的物质)。
外,不考虑其它可能与酸性高锰酸钾反应的物质)。
(2)有氧时,在硝化细菌的作用下,
 可实现过程④的转化,若消耗
可实现过程④的转化,若消耗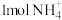 ,至少需
,至少需(3)已知
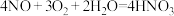 ,甲同学利用排空气法收集到一烧瓶的
,甲同学利用排空气法收集到一烧瓶的 气体并搭建如图乙装置。关闭止水夹A和B后,挤压胶头滴管,一段时间后打开止水夹B,当烧瓶内液面不再变化后,烧瓶中仍然存在一定量气体(如图丙),对于残留气体的成分及原因,甲同学提出如下假设:
气体并搭建如图乙装置。关闭止水夹A和B后,挤压胶头滴管,一段时间后打开止水夹B,当烧瓶内液面不再变化后,烧瓶中仍然存在一定量气体(如图丙),对于残留气体的成分及原因,甲同学提出如下假设:假设一:由于
 与水反应产生NO,剩余气体可能主要是NO;
与水反应产生NO,剩余气体可能主要是NO;假设二:排空气法收集的气体不纯,剩余气体可能主要是
 。
。乙同学打开止水夹A,缓慢通入少量
 ,观察到烧瓶内液面继续升高,由此推断
,观察到烧瓶内液面继续升高,由此推断(4)实验室制备
 的方法有很多,以下为甲同学提出的方案,你认为合理的是
的方法有很多,以下为甲同学提出的方案,你认为合理的是A.加热
 和
和 固体混合物
固体混合物B.
 、
、 混合气体在高温高压催化剂条件下反应
混合气体在高温高压催化剂条件下反应C.将氨水缓慢滴入
 固体中
固体中D.将浓氨水缓慢滴入碱石灰中
E.加热
 固体
固体乙同学查阅资料发现
 与
与 可结合为
可结合为 ,设计利用镁条在氮气中燃烧后的白色固体与水反应制取氨气,该方案如能实现请写出反应方程式:
,设计利用镁条在氮气中燃烧后的白色固体与水反应制取氨气,该方案如能实现请写出反应方程式:(5)已知有氧条件下,
 可在催化剂作用下将NO还原为
可在催化剂作用下将NO还原为 ,某研究机构利用钒基催化剂
,某研究机构利用钒基催化剂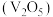 发生脱硝反应处理NO有害气体,机理如图所示。
发生脱硝反应处理NO有害气体,机理如图所示。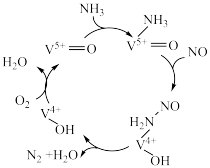
 和NO物质的量之比为
和NO物质的量之比为 ,总反应的化学方程式为:
,总反应的化学方程式为:______
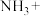 ______NO+______
______NO+______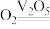 _______
_______ ______
______
(6)
 也是一种有毒气体,已知
也是一种有毒气体,已知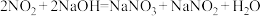 ,
,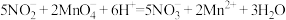 。某化工厂每天约产生2000立方米废气,其中
。某化工厂每天约产生2000立方米废气,其中 为主要有毒气体(不考虑
为主要有毒气体(不考虑 ),在洗气塔中利用
),在洗气塔中利用 溶液吸收废气中的
溶液吸收废气中的 ,每天约产生
,每天约产生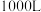 吸收液。某兴趣小组为了检测废气中
吸收液。某兴趣小组为了检测废气中 的含量,取
的含量,取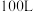 该吸收液,逐滴加入
该吸收液,逐滴加入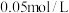 酸性高锰酸钾溶液,当滴入
酸性高锰酸钾溶液,当滴入 时恰好完全反应。则该厂废气中
时恰好完全反应。则该厂废气中 含量为
含量为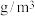 (提示:本题除
(提示:本题除 外,不考虑其它可能与酸性高锰酸钾反应的物质)。
外,不考虑其它可能与酸性高锰酸钾反应的物质)。
您最近一年使用:0次
解题方法
8 . 一种利用废旧镀锌铁皮制备磁性 纳米粒子的工艺流程如图所示:
纳米粒子的工艺流程如图所示:
回答下列问题:
(1)“碱洗”的目的是___________ 。
(2)“酸溶”发生反应的化学方程式___________ 。
(3)“氧化”操作的目的是___________ ,发生反应的离子方程式为___________ 。
(4)“氧化”后的溶液中金属阳离子主要有___________ 。
(5)用激光笔照射“加热沉铁”后所得分散系,可产生___________ 。
 纳米粒子的工艺流程如图所示:
纳米粒子的工艺流程如图所示: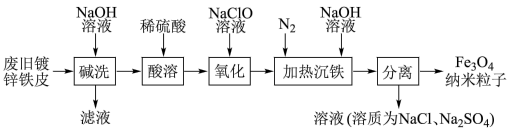
回答下列问题:
(1)“碱洗”的目的是
(2)“酸溶”发生反应的化学方程式
(3)“氧化”操作的目的是
(4)“氧化”后的溶液中金属阳离子主要有
(5)用激光笔照射“加热沉铁”后所得分散系,可产生
您最近一年使用:0次
解题方法
9 . 为保护环境,充分利用钴资源,一种以废旧锂离子二次电池材料(正极材料主要含有 、铝箔及金属钢壳)为原料回收钴的工艺流程如下:
、铝箔及金属钢壳)为原料回收钴的工艺流程如下:___________ 。
(2) 中Co的化合价为
中Co的化合价为___________ 。
(3)不同浸出剂“酸浸”结果如下表:
①浸出剂a的钴浸出率更高,但工业生产中一般不选用a的原因是___________ 。(答一点即可)
②工业生产中常选用浸出剂b,则“酸浸”时反应的离子方程式为___________ , 的作用是
的作用是___________ (填“做氧化剂”或“做还原剂”)
③选用浸出剂b时,“酸浸”的温度控制在80℃左右,其原因为___________ 。
(4)萃取是化学实验中常用分离方法,其操作过程为检查分液漏斗是否漏液→加萃取剂和萃取液→___________ →放气→静置→……
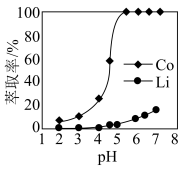
(5)“萃取分离”中钴、锂的萃取率与平衡时溶液pH的关系如图所示,为了实现钴锂分离效果较好,pH一般选择___________ (填整数)左右。
 、铝箔及金属钢壳)为原料回收钴的工艺流程如下:
、铝箔及金属钢壳)为原料回收钴的工艺流程如下: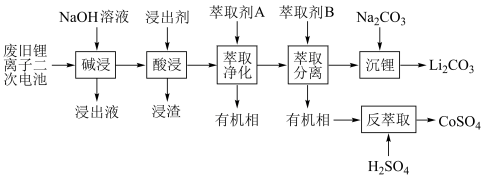
(2)
 中Co的化合价为
中Co的化合价为(3)不同浸出剂“酸浸”结果如下表:
| 浸出剂 | 浸出液中 的浓度/( 的浓度/( ) ) | 钴浸出率/% |
| a.盐酸 | 80.84 | 98.4 |
| b.硫酸与过氧化氢的混合溶液 | 84.91 | 98.0 |
②工业生产中常选用浸出剂b,则“酸浸”时反应的离子方程式为
 的作用是
的作用是③选用浸出剂b时,“酸浸”的温度控制在80℃左右,其原因为
(4)萃取是化学实验中常用分离方法,其操作过程为检查分液漏斗是否漏液→加萃取剂和萃取液→
(5)“萃取分离”中钴、锂的萃取率与平衡时溶液pH的关系如图所示,为了实现钴锂分离效果较好,pH一般选择
您最近一年使用:0次
名校
10 . 甲苯是重要的有机原料,某化学兴趣小组利用甲苯为主要原料,进行下列实验:
I.利用如图所示装置制备对溴甲苯(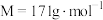 ),并证明该反应为取代反应。
),并证明该反应为取代反应。___________ ,实验过程中使用了40mL甲苯(约0.38mol)和30mL液溴(约0.58mol),则选用的仪器M的最合理规格为___________ (填字母)。
A.100mL B.200mL C.250mL D.500mL
(2)冷凝管中冷凝水从________ (填“a”或“b”)口进入,装置乙中 的作用为
的作用为________ ,能说明该反应为取代反应的实验现象为________ 。
(3)若最后得到对溴甲苯51.98g,则该实验中产品的产率约为______ (结果保留两位有效数字)。
II.利用如图实验步骤制取苯甲酸。___________ 。
(5)粗苯甲酸中主要杂质为KCl和 ,可采用下列步骤纯化:
,可采用下列步骤纯化:___________ 。
②最后得到的苯甲酸纯品晶体颗粒较小且晶体外形不规则,最可能的原因为___________ 。
I.利用如图所示装置制备对溴甲苯(
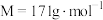 ),并证明该反应为取代反应。
),并证明该反应为取代反应。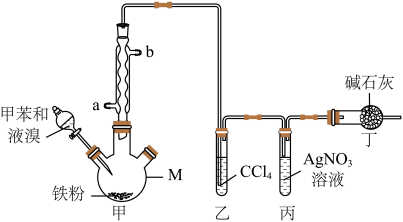
A.100mL B.200mL C.250mL D.500mL
(2)冷凝管中冷凝水从
 的作用为
的作用为(3)若最后得到对溴甲苯51.98g,则该实验中产品的产率约为
II.利用如图实验步骤制取苯甲酸。
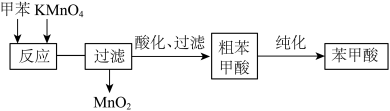
反应原理为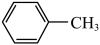
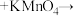
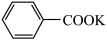
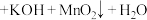 (未配平)。
(未配平)。
(5)粗苯甲酸中主要杂质为KCl和
 ,可采用下列步骤纯化:
,可采用下列步骤纯化: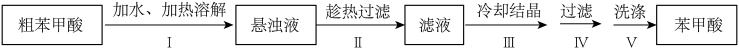
②最后得到的苯甲酸纯品晶体颗粒较小且晶体外形不规则,最可能的原因为
您最近一年使用:0次



