名校
解题方法
1 . 我国最新型055型万吨驱逐舰上使用了最新一代国产有源相控阵雷达,采用了最先进的氮化镓( )半导体技术。某工厂利用铝土矿(主要成分为
)半导体技术。某工厂利用铝土矿(主要成分为 、
、 、
、 )为原料制备
)为原料制备 的流程如下图所示。已知镓与铝同主族,其氧化物和氢氧化物均为两性化合物,能与强酸、强碱溶液反应,
的流程如下图所示。已知镓与铝同主族,其氧化物和氢氧化物均为两性化合物,能与强酸、强碱溶液反应, 为阿伏加德罗常数的值,下列说法错误的是
为阿伏加德罗常数的值,下列说法错误的是
 )半导体技术。某工厂利用铝土矿(主要成分为
)半导体技术。某工厂利用铝土矿(主要成分为 、
、 、
、 )为原料制备
)为原料制备 的流程如下图所示。已知镓与铝同主族,其氧化物和氢氧化物均为两性化合物,能与强酸、强碱溶液反应,
的流程如下图所示。已知镓与铝同主族,其氧化物和氢氧化物均为两性化合物,能与强酸、强碱溶液反应, 为阿伏加德罗常数的值,下列说法错误的是
为阿伏加德罗常数的值,下列说法错误的是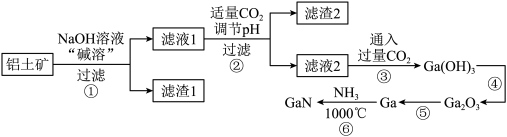
| A.可以通过粉碎铝土矿、搅拌等方法提高“碱溶”效率 |
B.由过程②、③可知, 的酸性比 的酸性比 强 强 |
C.已知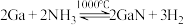 , , 与足量 与足量 反应,转移电子数为 反应,转移电子数为 |
D.滤渣1是 ,生成滤渣2的离子方程式可能为 ,生成滤渣2的离子方程式可能为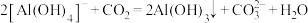 |
您最近一年使用:0次
2024-05-12更新
|
257次组卷
|
2卷引用:安徽师范大学附属中学2024届高三下学期5月测试化学试卷
名校
2 . 下列关于氨气的应用及性质说法正确的是
A.氨燃料动力集装箱船中氨气燃烧的化学方程式: |
B.足量的氨气和氯气反应,氧化剂和还原剂的物质的量之比为 |
C.氨气的中心原子采取 杂化,且氮原子提供空轨道与 杂化,且氮原子提供空轨道与 形成配位键 形成配位键 |
D.氨气可用于制备高能分子磷酰三叠氮,结构简式为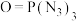 ,其分解产物 ,其分解产物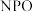 的电子式为 的电子式为 |
您最近一年使用:0次
2024-05-12更新
|
121次组卷
|
2卷引用:安徽师范大学附属中学2024届高三下学期5月测试化学试卷
名校
解题方法
3 . 铅酸蓄电池由于其技术成熟、安全性高、电压稳定及价格低廉等优势,在电池市场占据主导地位。以方铅可矿(PbS,含少量 )为原料制取
)为原料制取 的流程如图所示:
的流程如图所示:
(1)“酸浸”时温度一般控制在65~90℃,理由是___________ ,酸浸时发生反应的离子方程式为___________ 。
(2)从“酸浸”所得滤渣中回收的 ,可用于
,可用于___________ (任写两种)。
(3)“氧化”时参加反应的氧化剂与还原剂的物质的量之比为___________ 。
(4)若以100kg方铅矿(PbS的质量分数为70%)为原料,最终制得 59.75kg(假设反应过程中Pb无损失),则
59.75kg(假设反应过程中Pb无损失),则 的产率(产率
的产率(产率 )为
)为___________ (保留一位小数)。
(5)铅酸蓄电池为可充电电池,充放电时反应为 。
。
①放电时 电极的电极反应式为
电极的电极反应式为___________ 。
②充电时 电极发生
电极发生___________ (填“氧化”或“还原”)反应。
 )为原料制取
)为原料制取 的流程如图所示:
的流程如图所示: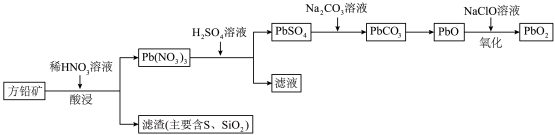
(1)“酸浸”时温度一般控制在65~90℃,理由是
(2)从“酸浸”所得滤渣中回收的
 ,可用于
,可用于(3)“氧化”时参加反应的氧化剂与还原剂的物质的量之比为
(4)若以100kg方铅矿(PbS的质量分数为70%)为原料,最终制得
 59.75kg(假设反应过程中Pb无损失),则
59.75kg(假设反应过程中Pb无损失),则 的产率(产率
的产率(产率 )为
)为(5)铅酸蓄电池为可充电电池,充放电时反应为
 。
。①放电时
 电极的电极反应式为
电极的电极反应式为②充电时
 电极发生
电极发生
您最近一年使用:0次
解题方法
4 . 某工厂以粗硅藻土 主要成分是
主要成分是 和有机质,并含有少量的
和有机质,并含有少量的 、
、 等杂质
等杂质 ,生产精制硅藻土并获得
,生产精制硅藻土并获得 及高铁酸钾
及高铁酸钾 的工艺流程如下:
的工艺流程如下:
(1)粗硅藻土在煅烧过程中,为了加快反应速率可以采取的措施有___________  写两条
写两条 。
。
(2)查阅资料得知:常温下 、
、 在浓度为
在浓度为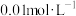 时,氢氧化物沉淀的
时,氢氧化物沉淀的 如下表:
如下表:
要使 与
与 分离,应调节溶液的
分离,应调节溶液的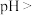
___________ ;根据表中数据,该温度下
___________ 。
(3)滤液 中通入过量
中通入过量 发生反应的离子方程式为
发生反应的离子方程式为___________ 。
(4)滤渣 与
与 溶液、
溶液、 反应的化学方程式为
反应的化学方程式为___________ ;在该反应中每生成 ,转移的电子数为
,转移的电子数为___________ 。
(5)工业可利用电解法制取高铁酸钾 ,装置示意图如下:
,装置示意图如下: 在电解时,镍电极接电源的
在电解时,镍电极接电源的___________ 极 填“正”或“负”
填“正”或“负” 。
。
 在电解过程中,阳极的电极反应式为
在电解过程中,阳极的电极反应式为___________ ;阴极区溶液的
___________ (填“增大”“减少”或“不变” 。
。
 主要成分是
主要成分是 和有机质,并含有少量的
和有机质,并含有少量的 、
、 等杂质
等杂质 ,生产精制硅藻土并获得
,生产精制硅藻土并获得 及高铁酸钾
及高铁酸钾 的工艺流程如下:
的工艺流程如下: 
(1)粗硅藻土在煅烧过程中,为了加快反应速率可以采取的措施有
 写两条
写两条 。
。(2)查阅资料得知:常温下
 、
、 在浓度为
在浓度为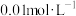 时,氢氧化物沉淀的
时,氢氧化物沉淀的 如下表:
如下表:| 氢氧化物 |  |  |  在 在 时开始溶解, 时开始溶解, 完全溶解 完全溶解 |
开始沉淀的 |  | 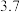 | |
完全沉淀的 |  | 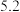 |
 与
与 分离,应调节溶液的
分离,应调节溶液的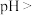

(3)滤液
 中通入过量
中通入过量 发生反应的离子方程式为
发生反应的离子方程式为(4)滤渣
 与
与 溶液、
溶液、 反应的化学方程式为
反应的化学方程式为 ,转移的电子数为
,转移的电子数为(5)工业可利用电解法制取高铁酸钾
 ,装置示意图如下:
,装置示意图如下:
 在电解时,镍电极接电源的
在电解时,镍电极接电源的 填“正”或“负”
填“正”或“负” 。
。 在电解过程中,阳极的电极反应式为
在电解过程中,阳极的电极反应式为
 。
。
您最近一年使用:0次
5 . 下列说法不正确的是
| A.铁元素在自然界中以化合态和游离态形式存在 |
B. 中铁的化合价有 中铁的化合价有 和 和 价,是一种混合物 价,是一种混合物 |
C.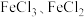 和 和 都可以通过化合反应制取 都可以通过化合反应制取 |
D. 铁与足量稀盐酸反应,转移电子数为 铁与足量稀盐酸反应,转移电子数为 |
您最近一年使用:0次
解题方法
6 . 某电镀厂产生的废水经预处理后含有 和少量的Cu2+、Ni2+,能够采用以下流程进行逐一分离,实现资源再利用。
和少量的Cu2+、Ni2+,能够采用以下流程进行逐一分离,实现资源再利用。
①常温下,物质的Ksp数据:
②Cr(OH)3性质与Al(OH)3相似。
③设H2S平衡浓度为1.0×10-6mol/L,已知H2S的K1=1.0×10-7,K2=7.0×10-15。
回答下列问题:
(1)还原池中溶液调pH___________ (填“能”或“否")使用盐酸。
(2)还原池中有Cr3+和CO2气体生成,反应的离子方程式为___________ 。
(3)沉淀池1中溶液的pH应为___________ 时才能使c(Cr3+)降至10-5mol/L,若溶液pH过高将会导致___________ 沉铬率下降。
(4)沉淀池2中加入的Na2S溶液呈碱性,原因是___________ (用主要反应的离子方程式表示),根据溶度积常数可确定沉淀2为___________ 。
(5)沉淀池3中沉淀结束,pH=7时,溶液中主要离子是___________ 。
 和少量的Cu2+、Ni2+,能够采用以下流程进行逐一分离,实现资源再利用。
和少量的Cu2+、Ni2+,能够采用以下流程进行逐一分离,实现资源再利用。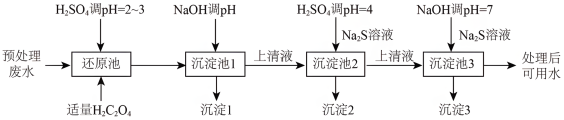
①常温下,物质的Ksp数据:
| 物质 | Cr(OH)3 | CuS | NiS |
| Ksp | 1×10-32 | 6.3×10-36 | 3.0×10-19 |
③设H2S平衡浓度为1.0×10-6mol/L,已知H2S的K1=1.0×10-7,K2=7.0×10-15。
回答下列问题:
(1)还原池中溶液调pH
(2)还原池中有Cr3+和CO2气体生成,反应的离子方程式为
(3)沉淀池1中溶液的pH应为
(4)沉淀池2中加入的Na2S溶液呈碱性,原因是
(5)沉淀池3中沉淀结束,pH=7时,溶液中主要离子是
您最近一年使用:0次
7 . 锂电池中一些金属的回收利用也是未来发展的一大方向。废弃的锂电池正极材料 进行氯化处理并回收利用的工艺流程如下:
进行氯化处理并回收利用的工艺流程如下:
(1) 在元素周期表的位置是
在元素周期表的位置是______ 。“烧渣”是 、
、 和
和 的混合物,滤饼2成分的化学式为
的混合物,滤饼2成分的化学式为______ 。
(2)碳酸锂的溶解度随温度变化如图所示。向滤液2中加入 ,将温度升至
,将温度升至 是为了提高沉淀反应速率和
是为了提高沉淀反应速率和______ 。得到碳酸锂沉淀的最佳操作为______ (填字母)。
(3)取 滤液2,其中
滤液2,其中 ,为使锂元素的回收率不低于
,为使锂元素的回收率不低于 ,则至少应加入
,则至少应加入 固体的物质的量为
固体的物质的量为______  [已知
[已知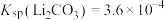 ]。
]。
(4)碳酸锂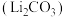 与
与 按
按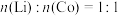 的比例配合,然后在空气中于
的比例配合,然后在空气中于 烧结可合成锂电池正极材料
烧结可合成锂电池正极材料 ,反应方程式为
,反应方程式为______ 。
(5)钴酸锂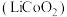 的晶胞结构示意图如图。晶体中
的晶胞结构示意图如图。晶体中 围绕
围绕 形成八面体,八面体共棱形成带负电的层状空间结构,与
形成八面体,八面体共棱形成带负电的层状空间结构,与 层交替排列,其中
层交替排列,其中 处于晶胞顶点或晶胞内部,
处于晶胞顶点或晶胞内部, 处于晶胞内部或晶胞侧棱上,可推断该晶胞中
处于晶胞内部或晶胞侧棱上,可推断该晶胞中 的个数为
的个数为______ 。
 进行氯化处理并回收利用的工艺流程如下:
进行氯化处理并回收利用的工艺流程如下: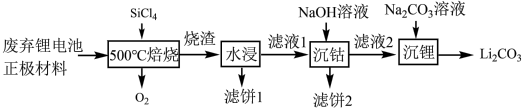
(1)
 在元素周期表的位置是
在元素周期表的位置是 、
、 和
和 的混合物,滤饼2成分的化学式为
的混合物,滤饼2成分的化学式为(2)碳酸锂的溶解度随温度变化如图所示。向滤液2中加入
 ,将温度升至
,将温度升至 是为了提高沉淀反应速率和
是为了提高沉淀反应速率和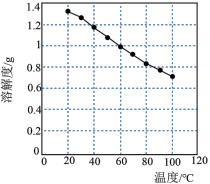
(3)取
 滤液2,其中
滤液2,其中 ,为使锂元素的回收率不低于
,为使锂元素的回收率不低于 ,则至少应加入
,则至少应加入 固体的物质的量为
固体的物质的量为 [已知
[已知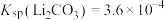 ]。
]。(4)碳酸锂
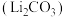 与
与 按
按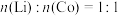 的比例配合,然后在空气中于
的比例配合,然后在空气中于 烧结可合成锂电池正极材料
烧结可合成锂电池正极材料 ,反应方程式为
,反应方程式为(5)钴酸锂
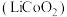 的晶胞结构示意图如图。晶体中
的晶胞结构示意图如图。晶体中 围绕
围绕 形成八面体,八面体共棱形成带负电的层状空间结构,与
形成八面体,八面体共棱形成带负电的层状空间结构,与 层交替排列,其中
层交替排列,其中 处于晶胞顶点或晶胞内部,
处于晶胞顶点或晶胞内部, 处于晶胞内部或晶胞侧棱上,可推断该晶胞中
处于晶胞内部或晶胞侧棱上,可推断该晶胞中 的个数为
的个数为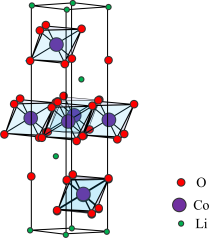
您最近一年使用:0次
解题方法
8 . 粗氢氧化钴Co(OH)3是以铜钴矿为原料湿法提取而得到的粗制钴盐中间品,含有MnOOH以及Al2O3、Fe3O4、Mg等杂质,粗氢氧化钴湿法制取精制硫酸钴流程如下:_______ (填元素名称)进行有效浸出。保持温度, 流速等条件不变,Co浸出率与时间关系如图所示,则
流速等条件不变,Co浸出率与时间关系如图所示,则 浓度最适宜为
浓度最适宜为_______ mol/L。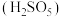 。
。 被
被 氧化为
氧化为 ,该反应的离子方程式为
,该反应的离子方程式为_______ (已知: 的电离第一步完全,第二步微弱)。生石灰调节
的电离第一步完全,第二步微弱)。生石灰调节
_______ (保留一位小数)时,检验反应后的滤液中恰好不存在 (已知:
(已知: 的
的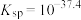 ,离子浓度
,离子浓度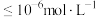 时沉淀完全)。
时沉淀完全)。
(3)在萃取剂一定量的情况下,提高萃取率的措施有_______ (答出一点即可),萃取后水相溶液中存在的金属离子有_______ 。
(4)硫酸钴的溶解度曲线如图所示,从溶液中获得CoSO4•7H2O的方法是_______ 。
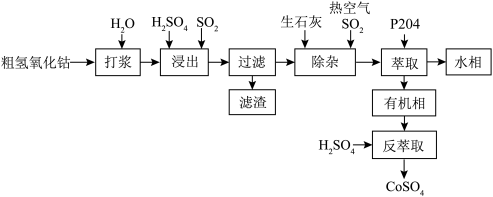
 流速等条件不变,Co浸出率与时间关系如图所示,则
流速等条件不变,Co浸出率与时间关系如图所示,则 浓度最适宜为
浓度最适宜为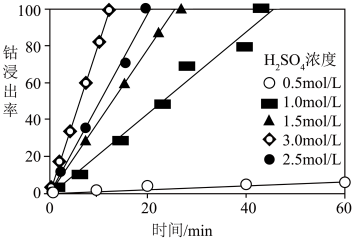
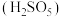 。
。 被
被 氧化为
氧化为 ,该反应的离子方程式为
,该反应的离子方程式为 的电离第一步完全,第二步微弱)。生石灰调节
的电离第一步完全,第二步微弱)。生石灰调节
 (已知:
(已知: 的
的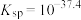 ,离子浓度
,离子浓度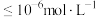 时沉淀完全)。
时沉淀完全)。(3)在萃取剂一定量的情况下,提高萃取率的措施有
(4)硫酸钴的溶解度曲线如图所示,从溶液中获得CoSO4•7H2O的方法是

您最近一年使用:0次
解题方法
9 . 钴一种非常稀缺的金属资源,素有“工业味精”和“工业牙齿”之称,是重要的战略资源之一、某工业废料中含稀土元素和少量 、
、 、
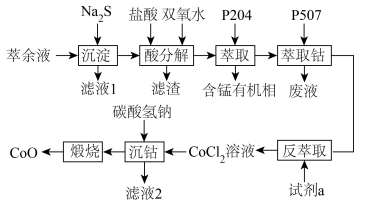
、 等金属离子,分离其中的稀土元素后,从萃余液中回收氧化钴的工艺流程如下:
等金属离子,分离其中的稀土元素后,从萃余液中回收氧化钴的工艺流程如下:
已知25℃时, ,
,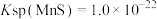 ,
,
萃取钴的原理: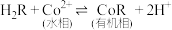
回答下列问题:
(1)钴元素在元素周期表中的位置___________ 。
(2)要使 完全沉淀,
完全沉淀, 至少为
至少为___________ 。
(3)酸分解时控制温度50~60℃,原因是___________ 。
(4)反萃取时最合适的试剂a是___________ 。
(5)写出“沉钴”时发生反应的离子方程式___________ 。
(6)“沉钴”后需将沉淀洗涤干净,实验室检验该沉淀是否洗净的方法是______ 。
(7)“煅烧”必须在氩气中进行,若在空气中煅烧,400℃时会生成另一种钴的氧化物,固体残留率为69.7%,则该反应的化学方程式为___________ 。
 、
、 、
、 等金属离子,分离其中的稀土元素后,从萃余液中回收氧化钴的工艺流程如下:
等金属离子,分离其中的稀土元素后,从萃余液中回收氧化钴的工艺流程如下:
已知25℃时,
 ,
,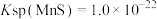 ,
,
萃取钴的原理:
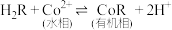
回答下列问题:
(1)钴元素在元素周期表中的位置
(2)要使
 完全沉淀,
完全沉淀, 至少为
至少为(3)酸分解时控制温度50~60℃,原因是
(4)反萃取时最合适的试剂a是
(5)写出“沉钴”时发生反应的离子方程式
(6)“沉钴”后需将沉淀洗涤干净,实验室检验该沉淀是否洗净的方法是
(7)“煅烧”必须在氩气中进行,若在空气中煅烧,400℃时会生成另一种钴的氧化物,固体残留率为69.7%,则该反应的化学方程式为
您最近一年使用:0次
10 . 柠檬酸亚铁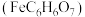 是一种高效补铁剂,实验室可通过铁粉制备,反应原理简示如下:
是一种高效补铁剂,实验室可通过铁粉制备,反应原理简示如下:
实验步骤:
①取15g铁粉,用 ,边搅拌边加热,至反应完全,过滤,以滤液制备
,边搅拌边加热,至反应完全,过滤,以滤液制备 (
(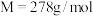 )晶体。
)晶体。
②取9g精制的 ,缓慢加入
,缓慢加入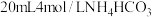 溶液,静置40min后有大量
溶液,静置40min后有大量
沉淀析出,过滤洗涤,得 晶体。
晶体。
③在烧杯中加入6g柠檬酸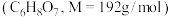 、80mL水、
、80mL水、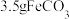 边加热边搅拌至晶体析出,过滤洗涤干燥得
边加热边搅拌至晶体析出,过滤洗涤干燥得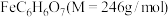 晶体。
晶体。
回答下列问题:
(1)请利用原子结构的相关知识解释三价铁比二价铁稳定原因_______ 。
(2) 溶液制备
溶液制备 晶体常用两种方法:
晶体常用两种方法:
方法ⅰ:先将滤液进行蒸发浓缩至稀糊状,可选用仪器有酒精灯、玻璃棒、_______ (从下列仪器中选择并填写名称,后一问相同要求)等,再将浓缩液冷却至室温,用_______ (仪器名称)过滤,其优点是_______ 。
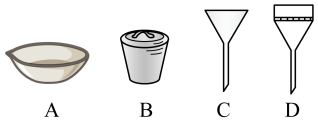
方法ⅱ:将滤液冷却静置后,用玻璃棒摩擦烧杯壁,先有少量规则晶体出现,后有大量晶体 晶体出现。试回答,用玻璃棒摩擦烧杯壁的作用
晶体出现。试回答,用玻璃棒摩擦烧杯壁的作用_______ 。
(3)写出制备碳酸亚铁的离子方程式_______ 。
(4)利用邻二氮菲 与
与 生成稳定橙红色配合物
生成稳定橙红色配合物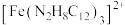 ,最大吸收波长为510nm这一特征可用来检测
,最大吸收波长为510nm这一特征可用来检测 含量,某同学将上述所制
含量,某同学将上述所制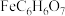 晶体全部溶解于试管中后,添加25mL3mol/L邻二氮菲溶液后,可获得最大吸收波长,则
晶体全部溶解于试管中后,添加25mL3mol/L邻二氮菲溶液后,可获得最大吸收波长,则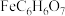 晶体质量为
晶体质量为_______ g。
(5)不用酸性高锰酸钾溶液滴定 最可能的原因是
最可能的原因是_______ 。
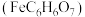 是一种高效补铁剂,实验室可通过铁粉制备,反应原理简示如下:
是一种高效补铁剂,实验室可通过铁粉制备,反应原理简示如下:
实验步骤:
①取15g铁粉,用
 ,边搅拌边加热,至反应完全,过滤,以滤液制备
,边搅拌边加热,至反应完全,过滤,以滤液制备 (
(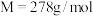 )晶体。
)晶体。②取9g精制的
 ,缓慢加入
,缓慢加入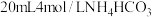 溶液,静置40min后有大量
溶液,静置40min后有大量
沉淀析出,过滤洗涤,得
 晶体。
晶体。③在烧杯中加入6g柠檬酸
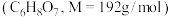 、80mL水、
、80mL水、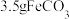 边加热边搅拌至晶体析出,过滤洗涤干燥得
边加热边搅拌至晶体析出,过滤洗涤干燥得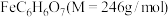 晶体。
晶体。回答下列问题:
(1)请利用原子结构的相关知识解释三价铁比二价铁稳定原因
(2)
 溶液制备
溶液制备 晶体常用两种方法:
晶体常用两种方法:方法ⅰ:先将滤液进行蒸发浓缩至稀糊状,可选用仪器有酒精灯、玻璃棒、

方法ⅱ:将滤液冷却静置后,用玻璃棒摩擦烧杯壁,先有少量规则晶体出现,后有大量晶体
 晶体出现。试回答,用玻璃棒摩擦烧杯壁的作用
晶体出现。试回答,用玻璃棒摩擦烧杯壁的作用(3)写出制备碳酸亚铁的离子方程式
(4)利用邻二氮菲
 与
与 生成稳定橙红色配合物
生成稳定橙红色配合物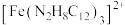 ,最大吸收波长为510nm这一特征可用来检测
,最大吸收波长为510nm这一特征可用来检测 含量,某同学将上述所制
含量,某同学将上述所制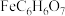 晶体全部溶解于试管中后,添加25mL3mol/L邻二氮菲溶液后,可获得最大吸收波长,则
晶体全部溶解于试管中后,添加25mL3mol/L邻二氮菲溶液后,可获得最大吸收波长,则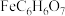 晶体质量为
晶体质量为(5)不用酸性高锰酸钾溶液滴定
 最可能的原因是
最可能的原因是
您最近一年使用:0次



