1 . Ⅰ.化学反应速率和化学平衡影响因素较多,经常采用变量控制思想分析问题。某小组利用 溶液和酸性
溶液和酸性 溶液反应来探究“条件对化学反应速率的影响”,进行如表中的实验:
溶液反应来探究“条件对化学反应速率的影响”,进行如表中的实验:
请回答:
(1)已知 酸性溶液与
酸性溶液与 溶液反应有
溶液反应有 生成,用化学方程式表示该实验的实验原理:
生成,用化学方程式表示该实验的实验原理:___________ 。
(2)根据表中的实验数据,可以得到的结论是___________ 。
(3)利用实验3中数据计算,用 溶液的浓度变化表示的反应速率为
溶液的浓度变化表示的反应速率为
___________ 。
Ⅱ.研究 的综合利用对促进“低碳经济”的发展有重要意义。工业上以
的综合利用对促进“低碳经济”的发展有重要意义。工业上以 、,为原料生产尿素
、,为原料生产尿素 ,
,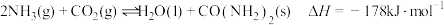 ,
,
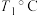 时,在1L的密闭容器中充入
时,在1L的密闭容器中充入 和模拟工业生产,
和模拟工业生产, ,图中是
,图中是 平衡转化率
平衡转化率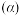 与
与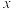 的关系。
的关系。
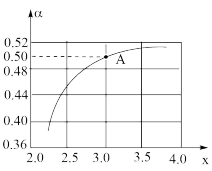
(4)图中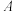 点
点 的平衡转化率
的平衡转化率
___________ %(结果保留3位有效数字)。
(5)当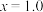 时,若起始的压强为
时,若起始的压强为 ,水为液态平衡时压强变为起始的
,水为液态平衡时压强变为起始的 ,则该反应的平衡常数
,则该反应的平衡常数 =
=___________ ( 为以分压表示的平衡常数,分压=总压
为以分压表示的平衡常数,分压=总压 体积分数)。
体积分数)。
 溶液和酸性
溶液和酸性 溶液反应来探究“条件对化学反应速率的影响”,进行如表中的实验:
溶液反应来探究“条件对化学反应速率的影响”,进行如表中的实验:| 实验编号 | 室温下,试管中所加试剂及其用量/mL | 室温下溶液颜色褪至无色所需时间/min | |||
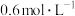  溶液 溶液 |  |   溶液 溶液 |  稀硫酸 稀硫酸 | ||
| 1 | 3.0 | 4.0 | 1.0 | 2.0 | 6.4 |
| 2 | 3.0 | 3.0 | 2.0 | 2.0 | 5.2 |
| 3 | 3.0 | 2.0 | 3.0 | 2.0 | 4.0 |
请回答:
(1)已知
 酸性溶液与
酸性溶液与 溶液反应有
溶液反应有 生成,用化学方程式表示该实验的实验原理:
生成,用化学方程式表示该实验的实验原理:(2)根据表中的实验数据,可以得到的结论是
(3)利用实验3中数据计算,用
 溶液的浓度变化表示的反应速率为
溶液的浓度变化表示的反应速率为
Ⅱ.研究
 的综合利用对促进“低碳经济”的发展有重要意义。工业上以
的综合利用对促进“低碳经济”的发展有重要意义。工业上以 、,为原料生产尿素
、,为原料生产尿素 ,
,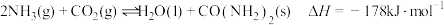 ,
,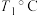 时,在1L的密闭容器中充入
时,在1L的密闭容器中充入 和模拟工业生产,
和模拟工业生产, ,图中是
,图中是 平衡转化率
平衡转化率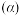 与
与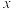 的关系。
的关系。
(4)图中
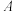 点
点 的平衡转化率
的平衡转化率
(5)当
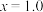 时,若起始的压强为
时,若起始的压强为 ,水为液态平衡时压强变为起始的
,水为液态平衡时压强变为起始的 ,则该反应的平衡常数
,则该反应的平衡常数 =
= 为以分压表示的平衡常数,分压=总压
为以分压表示的平衡常数,分压=总压 体积分数)。
体积分数)。
您最近半年使用:0次
解题方法
2 . 用一种硫化矿(含45%SiO2、20.4% Al2O3、30%FeS和少量GeS2等)制取盆景肥料NH4Fe(SO4)2及铝硅合金材料的工艺流程如下 :
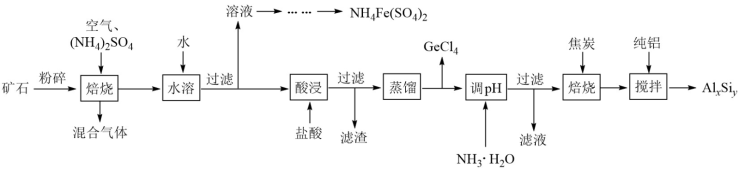
(1)“矿石”粉碎的目的是_____________________ 。
(2)“混合气体”经过水吸收和空气氧化能再次利用。
①“焙烧”时,GeS2发生反应的化学方程式为____________________ 。
②“混合气体”的主要成分是_______________ (填化学式).
③FeS焙烧产生的Fe2O3会与(NH4)2SO4反应生成NH4Fe(SO4)2,该反应的化学方程式为_______________ 。 Al2O3也能发生类似反应.这两种氧化物转化为硫酸盐的转化率与温度的关系如图,上述流程中最适宜的“焙烧” 温度为_____________________ 。

(3)GeCl4的沸点低,可在酸性条件下利用蒸馏的方法进行分离,酸性条件的目的是_________ 。
(4)用电解氧化法可以增强合金 AlxSiy的防腐蚀能力,电解后在合金表面形成致密、耐腐蚀的氧化膜(主要成分为Al2O3), 电解质溶液为 H2SO4-H2C2O4混合溶液,阳极的电极反应式为______________________ 。
(5)假设流程中SiO2损失了20%,Al2O3损失了25%,当投入1 t硫化矿,加入了54kg纯铝时,铝硅合金中x:y=______________ 。

(1)“矿石”粉碎的目的是
(2)“混合气体”经过水吸收和空气氧化能再次利用。
①“焙烧”时,GeS2发生反应的化学方程式为
②“混合气体”的主要成分是
③FeS焙烧产生的Fe2O3会与(NH4)2SO4反应生成NH4Fe(SO4)2,该反应的化学方程式为

(3)GeCl4的沸点低,可在酸性条件下利用蒸馏的方法进行分离,酸性条件的目的是
(4)用电解氧化法可以增强合金 AlxSiy的防腐蚀能力,电解后在合金表面形成致密、耐腐蚀的氧化膜(主要成分为Al2O3), 电解质溶液为 H2SO4-H2C2O4混合溶液,阳极的电极反应式为
(5)假设流程中SiO2损失了20%,Al2O3损失了25%,当投入1 t硫化矿,加入了54kg纯铝时,铝硅合金中x:y=
您最近半年使用:0次
2020-06-11更新
|
298次组卷
|
2卷引用:甘肃省陇南市2020届高三第二次诊断考试理科综合化学试题
9-10高二下·甘肃陇南·期末
3 . 配平下列氧化还原反应方程式:
____ K2S +____ HNO3=____ KNO3+_____ NO↑+____ S +____ H2O
当反应中有3mol电子发生转移时,有____ mol HNO3参加反应。
当反应中有3mol电子发生转移时,有
您最近半年使用:0次



