名校
1 . 几种中学化学常见的单质及其化合物相互转化的关系如图:
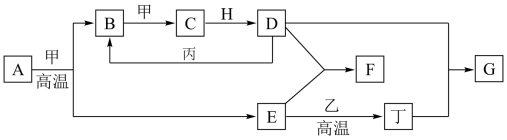
已知:
①甲、乙、丙、丁为单质,乙中元素在地壳中的含量占第三位,丙为红色固体,其余为化合物。
②A由X和Y两种元素组成,其原子个数比为1∶2,元素质量之比为7∶8。
③H常温下为无色、无味的液体,E常用作油漆、涂料的红色颜料。
回答下列问题:
(1)高温下,A和甲反应生成B和E的化学方程式为___________ ,每生成1 mol B,转移___________ mol电子。
(2)F的水溶液与丁单质反应也可以生成G,反应的离子方程式为___________ 。
(3)少量F的饱和溶液分别滴加到下列物质中,得到三种分散系①②③。
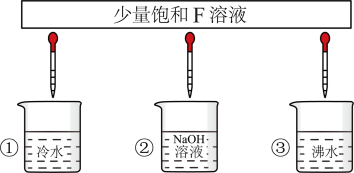
分散系②是___________ (填“胶体”“悬浊液”“乳浊液”或“溶液”),能鉴别分散系①③的实验现象称为___________ 。
(4)一定条件下,丙和D反应生成B的化学方程式为___________ 。

已知:
①甲、乙、丙、丁为单质,乙中元素在地壳中的含量占第三位,丙为红色固体,其余为化合物。
②A由X和Y两种元素组成,其原子个数比为1∶2,元素质量之比为7∶8。
③H常温下为无色、无味的液体,E常用作油漆、涂料的红色颜料。
回答下列问题:
(1)高温下,A和甲反应生成B和E的化学方程式为
(2)F的水溶液与丁单质反应也可以生成G,反应的离子方程式为
(3)少量F的饱和溶液分别滴加到下列物质中,得到三种分散系①②③。

分散系②是
(4)一定条件下,丙和D反应生成B的化学方程式为
您最近半年使用:0次
名校
解题方法
2 . 工业综合处理含NH 废水和含N2、CO2、SO2、NO、CO的废气,得到无毒气体b,流程如下:
废水和含N2、CO2、SO2、NO、CO的废气,得到无毒气体b,流程如下:
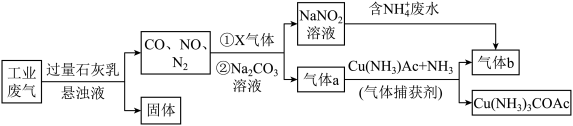
下列说法正确的是
 废水和含N2、CO2、SO2、NO、CO的废气,得到无毒气体b,流程如下:
废水和含N2、CO2、SO2、NO、CO的废气,得到无毒气体b,流程如下:
下列说法正确的是
| A.“固体”中含有CaSO4、CaSO3和CaCO3 |
B.X气体、NO与Na2CO3溶液的离子反应:4NO+O2+CO = 4NO = 4NO +CO2 +CO2 |
C.处理含NH 的废水时,离子方程式为NH 的废水时,离子方程式为NH +NO +NO = N2↑+2H2O = N2↑+2H2O |
| D.捕获剂捕获气体a中发生络合反应Cu(NH3)Ac+CO+NH3=Cu(NH3)3COAc |
您最近半年使用:0次
名校
3 . 为消除燃煤烟气中含有的 、
、 ,研究者提出若干烟气“脱硫”“脱硝”的方法。
,研究者提出若干烟气“脱硫”“脱硝”的方法。
【方法一】以NaClO作为吸收剂进行一体化“脱硫”“脱硝”,将烟气中的 、NO转化为
、NO转化为 、
、 。
。
(1)

 溶液理论上最多能吸收标准状况下NO的体积为
溶液理论上最多能吸收标准状况下NO的体积为_______ L。
(2)实验室利用模拟烟气(模拟烟气中 和NO的物质的量之比为
和NO的物质的量之比为 )探究该方法“脱硫”“脱硝”的效果,一定时间内,温度对硫、硝脱除率的影响曲线如图所示。
)探究该方法“脱硫”“脱硝”的效果,一定时间内,温度对硫、硝脱除率的影响曲线如图所示。

①此方法“脱硫”“脱硝”探究实验的最佳温度为_______ ; 的脱除率高于
的脱除率高于 ,其原因除
,其原因除 的还原性比
的还原性比 强外,还可能是
强外,还可能是_______ 。
② 时,吸收液中烟气转化生成的
时,吸收液中烟气转化生成的 和
和 的物质的量之比为
的物质的量之比为_______ 。
【方法二】 技术(选择性催化还原氮氧化物)
技术(选择性催化还原氮氧化物)
研究表明,铁基催化剂在260~300℃范围内实现 技术的过程如图所示。
技术的过程如图所示。
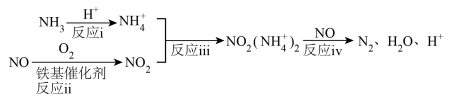
(3)根据上述机理, 在反应过程中的作用为
在反应过程中的作用为_______ ;等物质的量的 、
、 在有氧条件下转化为
在有氧条件下转化为 的总反应化学方程式为
的总反应化学方程式为_______ ;
(4)若使用锰基催化剂(活性物质为 )代替铁基催化剂,烟气中含有的
)代替铁基催化剂,烟气中含有的 会使催化剂失效而降低
会使催化剂失效而降低 脱除率,用化学方程式表示催化剂失效的原因:
脱除率,用化学方程式表示催化剂失效的原因:_______ 。
(5)向反应体系中添加 可显著提高
可显著提高 脱除率,原因是
脱除率,原因是 与
与 反应生成
反应生成 和阴离子M;阴离子M再与
和阴离子M;阴离子M再与 发生反应转化为
发生反应转化为 ,则阴离子M为
,则阴离子M为_______ 。
 、
、 ,研究者提出若干烟气“脱硫”“脱硝”的方法。
,研究者提出若干烟气“脱硫”“脱硝”的方法。【方法一】以NaClO作为吸收剂进行一体化“脱硫”“脱硝”,将烟气中的
 、NO转化为
、NO转化为 、
、 。
。(1)


 溶液理论上最多能吸收标准状况下NO的体积为
溶液理论上最多能吸收标准状况下NO的体积为(2)实验室利用模拟烟气(模拟烟气中
 和NO的物质的量之比为
和NO的物质的量之比为 )探究该方法“脱硫”“脱硝”的效果,一定时间内,温度对硫、硝脱除率的影响曲线如图所示。
)探究该方法“脱硫”“脱硝”的效果,一定时间内,温度对硫、硝脱除率的影响曲线如图所示。
①此方法“脱硫”“脱硝”探究实验的最佳温度为
 的脱除率高于
的脱除率高于 ,其原因除
,其原因除 的还原性比
的还原性比 强外,还可能是
强外,还可能是②
 时,吸收液中烟气转化生成的
时,吸收液中烟气转化生成的 和
和 的物质的量之比为
的物质的量之比为【方法二】
 技术(选择性催化还原氮氧化物)
技术(选择性催化还原氮氧化物)研究表明,铁基催化剂在260~300℃范围内实现
 技术的过程如图所示。
技术的过程如图所示。
(3)根据上述机理,
 在反应过程中的作用为
在反应过程中的作用为 、
、 在有氧条件下转化为
在有氧条件下转化为 的总反应化学方程式为
的总反应化学方程式为(4)若使用锰基催化剂(活性物质为
 )代替铁基催化剂,烟气中含有的
)代替铁基催化剂,烟气中含有的 会使催化剂失效而降低
会使催化剂失效而降低 脱除率,用化学方程式表示催化剂失效的原因:
脱除率,用化学方程式表示催化剂失效的原因:(5)向反应体系中添加
 可显著提高
可显著提高 脱除率,原因是
脱除率,原因是 与
与 反应生成
反应生成 和阴离子M;阴离子M再与
和阴离子M;阴离子M再与 发生反应转化为
发生反应转化为 ,则阴离子M为
,则阴离子M为
您最近半年使用:0次
2022-11-19更新
|
206次组卷
|
2卷引用:甘肃省永昌县第一高级中学2023-2024学年高三上学期期中考试化学试题
名校
4 . 二氧化氯(ClO2)是一种新型高效安全消毒剂,易溶于水,沸点为 ,遇热不稳定,易分解并发生爆炸。工业上利用硫铁矿[主要成分为二硫化亚铁(FeS2)]还原氯酸钠(NaClO3)制取二氧化氯。某研究小组利用如图装置模拟工业制备
,遇热不稳定,易分解并发生爆炸。工业上利用硫铁矿[主要成分为二硫化亚铁(FeS2)]还原氯酸钠(NaClO3)制取二氧化氯。某研究小组利用如图装置模拟工业制备 :向三颈烧瓶中加入
:向三颈烧瓶中加入 溶液、浓
溶液、浓 并通入空气,调节恒温器至
并通入空气,调节恒温器至 ,通过固体加料器缓慢匀速加入硫铁矿粉末。
,通过固体加料器缓慢匀速加入硫铁矿粉末。
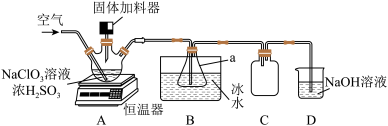
回答下列问题:
(1)仪器a的名称是_______ 。
(2)A装置中生成 的离子方程式为
的离子方程式为_______ ( 对应的产物为
对应的产物为 和
和 ),此离子反应中氧化产物与还原产物的物质的量之比为
),此离子反应中氧化产物与还原产物的物质的量之比为_______ 。
(3)装置C的作用是_______ 。
(4)装置D中 与NaOH溶液反应生成二种盐,其中一种为
与NaOH溶液反应生成二种盐,其中一种为 且二者物质的量之比为
且二者物质的量之比为 ,则另一种盐的化学式为
,则另一种盐的化学式为_______ 。
(5)一种主要成分为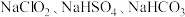 的“
的“ 泡腾片”,能快速溶于水,并产生大量气泡,得到含有
泡腾片”,能快速溶于水,并产生大量气泡,得到含有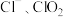 的溶液。上述过程中,每生成
的溶液。上述过程中,每生成 消耗
消耗 的物质的量为
的物质的量为_______ mol。
(6)工业上可用 与水中的
与水中的 在常温下反应,生成
在常温下反应,生成 和盐酸,以除去水中
和盐酸,以除去水中 。写出该反应的离子方程式:
。写出该反应的离子方程式:_______ 。
 ,遇热不稳定,易分解并发生爆炸。工业上利用硫铁矿[主要成分为二硫化亚铁(FeS2)]还原氯酸钠(NaClO3)制取二氧化氯。某研究小组利用如图装置模拟工业制备
,遇热不稳定,易分解并发生爆炸。工业上利用硫铁矿[主要成分为二硫化亚铁(FeS2)]还原氯酸钠(NaClO3)制取二氧化氯。某研究小组利用如图装置模拟工业制备 :向三颈烧瓶中加入
:向三颈烧瓶中加入 溶液、浓
溶液、浓 并通入空气,调节恒温器至
并通入空气,调节恒温器至 ,通过固体加料器缓慢匀速加入硫铁矿粉末。
,通过固体加料器缓慢匀速加入硫铁矿粉末。
回答下列问题:
(1)仪器a的名称是
(2)A装置中生成
 的离子方程式为
的离子方程式为 对应的产物为
对应的产物为 和
和 ),此离子反应中氧化产物与还原产物的物质的量之比为
),此离子反应中氧化产物与还原产物的物质的量之比为(3)装置C的作用是
(4)装置D中
 与NaOH溶液反应生成二种盐,其中一种为
与NaOH溶液反应生成二种盐,其中一种为 且二者物质的量之比为
且二者物质的量之比为 ,则另一种盐的化学式为
,则另一种盐的化学式为(5)一种主要成分为
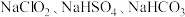 的“
的“ 泡腾片”,能快速溶于水,并产生大量气泡,得到含有
泡腾片”,能快速溶于水,并产生大量气泡,得到含有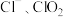 的溶液。上述过程中,每生成
的溶液。上述过程中,每生成 消耗
消耗 的物质的量为
的物质的量为(6)工业上可用
 与水中的
与水中的 在常温下反应,生成
在常温下反应,生成 和盐酸,以除去水中
和盐酸,以除去水中 。写出该反应的离子方程式:
。写出该反应的离子方程式:
您最近半年使用:0次
2022-10-08更新
|
212次组卷
|
3卷引用:甘肃省永昌县第一高级中学2023-2024学年高三上学期期中考试化学试题
名校
解题方法
5 . 硫铁矿烧渣主要成分是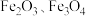 、少量
、少量 和CaO等。铁黄(FeOOH)主要用于涂料、水泥制件等。以硫铁矿烧渣为原料制备铁黄的工艺流程如下:
和CaO等。铁黄(FeOOH)主要用于涂料、水泥制件等。以硫铁矿烧渣为原料制备铁黄的工艺流程如下:
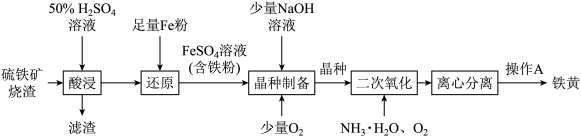
回答下列问题:
(1)“滤渣”的主要成分是_______ (填化学式)。
(2)操作A为_______ 。
(3)晶种制备过程中溶液pH与时间的关系如图:
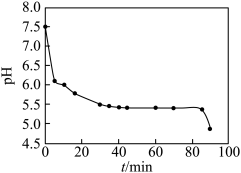
在反应前期(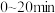 )溶液的pH随时间的延长而直线下降,是因为通入
)溶液的pH随时间的延长而直线下降,是因为通入 后,溶液中
后,溶液中 生成FeOOH晶种时发生反应
生成FeOOH晶种时发生反应_______ (写离子方程式),使溶液pH降低,同时NaOH与 反应生成
反应生成 絮状物。
絮状物。
(4)二次氧化的目的是将 和
和 进一步转化为铁黄,写出
进一步转化为铁黄,写出 转化为铁黄的离子方程式:
转化为铁黄的离子方程式:_______ ,此过程要使溶液的pH控制在3~4比较合适,如果溶液pH大于5,则可能产生的后果是_______ 。
(5)铁黄纯度可以通过产品的耗酸量确定。
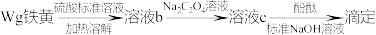
资料: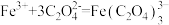 ,
,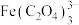 不与稀碱液反应
不与稀碱液反应
①写出铁黄溶解于硫酸溶液的化学方程式:_______ 。
②加入的 ,溶液必须过量,原因是
,溶液必须过量,原因是_______ 。
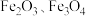 、少量
、少量 和CaO等。铁黄(FeOOH)主要用于涂料、水泥制件等。以硫铁矿烧渣为原料制备铁黄的工艺流程如下:
和CaO等。铁黄(FeOOH)主要用于涂料、水泥制件等。以硫铁矿烧渣为原料制备铁黄的工艺流程如下:
回答下列问题:
(1)“滤渣”的主要成分是
(2)操作A为
(3)晶种制备过程中溶液pH与时间的关系如图:

在反应前期(
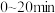 )溶液的pH随时间的延长而直线下降,是因为通入
)溶液的pH随时间的延长而直线下降,是因为通入 后,溶液中
后,溶液中 生成FeOOH晶种时发生反应
生成FeOOH晶种时发生反应 反应生成
反应生成 絮状物。
絮状物。(4)二次氧化的目的是将
 和
和 进一步转化为铁黄,写出
进一步转化为铁黄,写出 转化为铁黄的离子方程式:
转化为铁黄的离子方程式:(5)铁黄纯度可以通过产品的耗酸量确定。
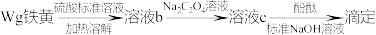
资料:
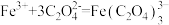 ,
, 不与稀碱液反应
不与稀碱液反应①写出铁黄溶解于硫酸溶液的化学方程式:
②加入的
 ,溶液必须过量,原因是
,溶液必须过量,原因是
您最近半年使用:0次
2022-10-08更新
|
203次组卷
|
5卷引用:甘肃省永昌县第一高级中学2023-2024学年高三上学期期中考试化学试题
甘肃省永昌县第一高级中学2023-2024学年高三上学期期中考试化学试题河北省九师联盟2022-2023学年高三上学期10月月考化学试题(已下线)2022年河北省高考真题变式题(14-18)(已下线)T26-工业流程题贵州省顶效开发区顶兴学校2023-2024学年高三第三次月考化学试题
名校
解题方法
6 . 某同学用如图装置(夹持装置略)探究铜丝与过量浓硫酸的反应,回答下列问题:

(1)写出铜与浓硫酸反应的化学方程式为____ 。
(2)B中观察到的现象为____ ;C中应加入的试剂为____ ;倒置漏斗的作用是____ 。
(3)某学习小组设计了如图所示装置来验证二氧化硫的化学性质。
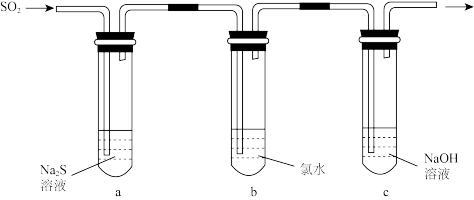
①能说明二氧化硫具有氧化性的实验现象为____ 。
②为验证二氧化硫的还原性,反应一段时间后,取试管b中的溶液分成三份,分别进行如下实验。
方案I:向第一份溶液中加入AgNO3溶液,有白色沉淀生成
方案II:向第二份溶液中加入品红溶液,红色褪去
方案III:向第三份溶液中加入BaCl2溶液,产生白色沉淀
上述方案合理的是____ (填I、II或III);试管b中发生反应的离子方程式为____ 。
(4)将铜丝与浓硫酸反应后的溶液冷却后加水稀释,取少许于试管中作为待测液,加____ (填化学式)溶液酸化,再取上层清液加____ (填化学式)溶液出现白色沉淀,即可确定存在SO 。写出产生白色沉淀的离子方程式
。写出产生白色沉淀的离子方程式____ 。

(1)写出铜与浓硫酸反应的化学方程式为
(2)B中观察到的现象为
(3)某学习小组设计了如图所示装置来验证二氧化硫的化学性质。

①能说明二氧化硫具有氧化性的实验现象为
②为验证二氧化硫的还原性,反应一段时间后,取试管b中的溶液分成三份,分别进行如下实验。
方案I:向第一份溶液中加入AgNO3溶液,有白色沉淀生成
方案II:向第二份溶液中加入品红溶液,红色褪去
方案III:向第三份溶液中加入BaCl2溶液,产生白色沉淀
上述方案合理的是
(4)将铜丝与浓硫酸反应后的溶液冷却后加水稀释,取少许于试管中作为待测液,加
 。写出产生白色沉淀的离子方程式
。写出产生白色沉淀的离子方程式
您最近半年使用:0次
名校
解题方法
7 . 某同学为了检验浓硫酸与木炭粉在加热条件下反应产生的所有产物,用如图所示实验装置。
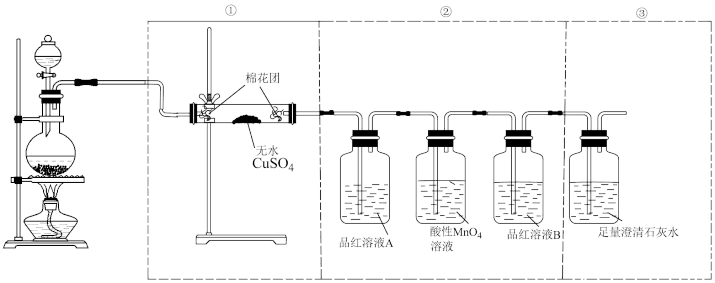
(1)写出浓硫酸和木炭粉在加热条件下发生反应的化学方程式____ 。
(2)装置①中无水硫酸铜表面现象是____ ,作用是____ 。
(3)装置②中酸性KMnO4溶液的现象是____ ,作用是____ 。
(4)写出装置③中发生反应的方程式____ 。
(5)某校科学小组为探究浓硫酸与木炭反应中定会产生二氧化碳,将发生装置产生的混合气体从a端通入(按如图所示)①A中的现象____ ;②C中的现象____ ;③D中的现象____ ,由上述现象该小组同学就能确认该气体的成分为CO2。
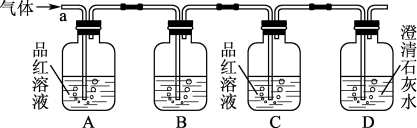
(6)利用SO2的还原性用KMnO4溶液可除去CO2混有SO2,写出发生反应的方程式____ 。

(1)写出浓硫酸和木炭粉在加热条件下发生反应的化学方程式
(2)装置①中无水硫酸铜表面现象是
(3)装置②中酸性KMnO4溶液的现象是
(4)写出装置③中发生反应的方程式
(5)某校科学小组为探究浓硫酸与木炭反应中定会产生二氧化碳,将发生装置产生的混合气体从a端通入(按如图所示)①A中的现象

(6)利用SO2的还原性用KMnO4溶液可除去CO2混有SO2,写出发生反应的方程式
您最近半年使用:0次
名校
8 . 研究氮及其化合物的性质,可以有效改善人类的生存环境。下图是有关氮的循环示意图。请回答:
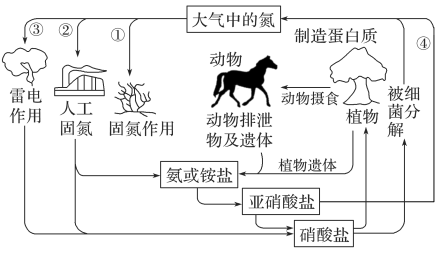
(1)请写出②中实现人工固氮的化学方程式:_______ 。
(2)氮氧化物进入大气后,不仅会形成硝酸型酸雨,还可能形成光化学烟雾。因此必须对含有氮氧化物的废气进行处理。某科研小组研究发现在一定条件下氨气可用来将氮氧化物转化为无污染的物质,请写出氨气和二氧化氮在一定条件下反应的化学方程式_______ 。

(1)请写出②中实现人工固氮的化学方程式:
(2)氮氧化物进入大气后,不仅会形成硝酸型酸雨,还可能形成光化学烟雾。因此必须对含有氮氧化物的废气进行处理。某科研小组研究发现在一定条件下氨气可用来将氮氧化物转化为无污染的物质,请写出氨气和二氧化氮在一定条件下反应的化学方程式
您最近半年使用:0次
名校
9 . 教材中用酸性KMnO4和H2C2O4(草酸)反应研究影响反应速率的因素,某实验小组欲通过测定单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计实验方案如下(KMnO4溶液已酸化):

(1)试写出酸性KMnO4和H2C2O4的离子反应方程式为:___________ 。
(2)该实验探究的是___________ 因素对化学反应速率的影响。相同时间内针筒中所得CO2的体积大小关系是:___________>___________,___________ (填实验序号)。
(3)若实验①在2min末收集了4.48mLCO2(标准状况下),用CO2表示2min内的反应速率为___________ ,则在2min末c(MnO )=
)=___________ (假设混合液体积为50mL)。
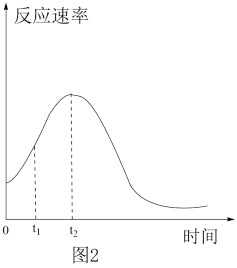
(4)实验小组同学发现反应速率总是如图2,其中t1~t2时间内速率变快的主要原因可能是:产物Mn2+(或MnSO4)是反应的催化剂;②___________ 。

| 实验序号 | A溶液 | B溶液 |
| ① | 20mL0.1mol•L-1H2C2O4溶液 | 30mL0.01mol•L-1KMnO4溶液 |
| ② | 20mL0.2mol•L-1H2C2O4溶液 | 30mL0.01mol•L-1KMnO4溶液 |
(2)该实验探究的是
(3)若实验①在2min末收集了4.48mLCO2(标准状况下),用CO2表示2min内的反应速率为
 )=
)=(4)实验小组同学发现反应速率总是如图2,其中t1~t2时间内速率变快的主要原因可能是:产物Mn2+(或MnSO4)是反应的催化剂;②

您最近半年使用:0次
10 . (1)NA表示阿伏加 德罗常数的数值.46g NO2和N2O4的混合气体中含有_____ NA个氧原子;2L0.6 mol·L−1 Fe(NO3)3溶液中含_____ NA个NO 离子.
离子.
(2)三氟化氮(NF3)是一种气体,它是微电子工业技术的关键原料之一,三氟化氮在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有:HF、NO和HNO3,
①写出该反应的化学方程式_________________________________
②三氟化氮可由氨气和氟气反应得到:4NH3+3F2=NF3+3NH4F;据题意推测NF3,F2,NO三种气体中,氧化性由强到弱的顺序为________________________
(3)氨和联氨(N2H4)是氮的两种常见化合物,制备联氨可用丙酮为催化剂,将次氯酸钠与氨气反应,该反应中还原剂与氧化剂的物质的量之比为2∶1,写出该反应的化学方程式_________________________
 离子.
离子.(2)三氟化氮(NF3)是一种气体,它是微电子工业技术的关键原料之一,三氟化氮在潮湿的空气中与水蒸气能发生氧化还原反应,其反应的产物有:HF、NO和HNO3,
①写出该反应的化学方程式
②三氟化氮可由氨气和氟气反应得到:4NH3+3F2=NF3+3NH4F;据题意推测NF3,F2,NO三种气体中,氧化性由强到弱的顺序为
(3)氨和联氨(N2H4)是氮的两种常见化合物,制备联氨可用丙酮为催化剂,将次氯酸钠与氨气反应,该反应中还原剂与氧化剂的物质的量之比为2∶1,写出该反应的化学方程式
您最近半年使用:0次



