名校
解题方法
1 . 请默写下列方程式。
(1)写出NH3与氧气发生催化氧化反应的化学方程式:_______ 。
(2)浓硝酸见光分解的化学方程式:_______ 。
(3)浓硝酸和铜反应的化学方程式:_______ 。
(4)硫化氢和二氧化硫气体混合的化学方程式:_______ 。
(5)二氧化氮通入水中反应的离子方程式:_______ 。
(1)写出NH3与氧气发生催化氧化反应的化学方程式:
(2)浓硝酸见光分解的化学方程式:
(3)浓硝酸和铜反应的化学方程式:
(4)硫化氢和二氧化硫气体混合的化学方程式:
(5)二氧化氮通入水中反应的离子方程式:
您最近一年使用:0次
解题方法
2 . 某同学利用钠与硫酸铜溶液进行实验,并对其现象进行分析,研究其产物组成。
(1)硫酸铜溶液的配制:准确称取五水硫酸铜(CuSO4·5H2O)晶体2.5000g,溶解后转移至100mL容量瓶中。
①上述实验过程中,用不到的实验仪器有____ (填标号)。

②该CuSO4溶液的浓度为__________ mo/L。
③通过理论计算,当上述硫酸铜与钠完全反应,溶液质量变化为___ g。
(2)将配好的CuSO4溶液,分3组进行实验,实验结果如下图所示:
查阅资料得知:极细的铜粉,外观呈现黑色
①a组中的蓝色沉淀成分主要是_________ 。
②将c组中黑色沉淀进行抽滤,干燥,对其成分进行初步的猜想
猜想ⅰ:金属钠将铜置换出来,以极细的铜粉存在;
猜想ⅱ:金属钠与水反应剧烈放热,______________ 。
设计一个简单的实验,证明猜想ⅰ是错误的______________ 。
(3)为进一步验证黑色固体的成分,该同学求助实验室检测,得到黑色固体中含铜化合物主要有硫酸氧化铜[Cu2O(SO4)]、碱式硫酸铜[Cu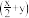 (OH)x(SO4)y]、氧化铜[CuO]三种。写出钠与硫酸铜反应生成碱式硫酸铜的化学方程式
(OH)x(SO4)y]、氧化铜[CuO]三种。写出钠与硫酸铜反应生成碱式硫酸铜的化学方程式____________ 。
(4)根据实验结果,可以得到的结论为____________ (写一条)。
(1)硫酸铜溶液的配制:准确称取五水硫酸铜(CuSO4·5H2O)晶体2.5000g,溶解后转移至100mL容量瓶中。
①上述实验过程中,用不到的实验仪器有

②该CuSO4溶液的浓度为
③通过理论计算,当上述硫酸铜与钠完全反应,溶液质量变化为
(2)将配好的CuSO4溶液,分3组进行实验,实验结果如下图所示:
| 序号 | CuSO4溶液体积/mL | 金属钠质量/g | 实验现象 |
| a | 15 | 0.01g | 迅速产生大量蓝色沉淀 |
| b | 15 | 0.1g | 蓝色沉淀和黑色沉淀共存 |
| c | 15 | 1.0g | 出现大量黑色沉淀 |
①a组中的蓝色沉淀成分主要是
②将c组中黑色沉淀进行抽滤,干燥,对其成分进行初步的猜想
猜想ⅰ:金属钠将铜置换出来,以极细的铜粉存在;
猜想ⅱ:金属钠与水反应剧烈放热,
设计一个简单的实验,证明猜想ⅰ是错误的
(3)为进一步验证黑色固体的成分,该同学求助实验室检测,得到黑色固体中含铜化合物主要有硫酸氧化铜[Cu2O(SO4)]、碱式硫酸铜[Cu
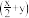 (OH)x(SO4)y]、氧化铜[CuO]三种。写出钠与硫酸铜反应生成碱式硫酸铜的化学方程式
(OH)x(SO4)y]、氧化铜[CuO]三种。写出钠与硫酸铜反应生成碱式硫酸铜的化学方程式(4)根据实验结果,可以得到的结论为
您最近一年使用:0次
3 . 活化二氧化锰在能源化学上有着重要作用,工业上利用精制软锰矿粉(MnO2)通过下列流程制备:
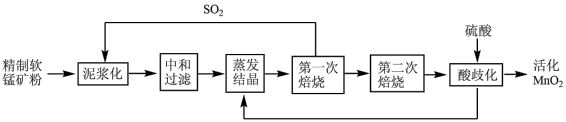
已知:蒸发结晶得到MnSO4。
(1)将软锰矿粉泥浆化的目的是________ ;反应方程式为_____________ ;
(2)“第一次焙烧”温度是1000℃,生成Mn3O4、SO2和O2,“第二次焙烧”温度为700℃,产物为Mn2O3;700℃时焙烧的氧化剂与还原剂物质的量比为_____________ 。
(3)“酸歧化”的离子方程式为________________ 。
(4)活化MnO2中不能含有铜、铅等重金属元素,在“中和过滤”前需要加入某种盐溶液除去重金属离子,该盐的化学式是___________ 。(已知CuS、PbS、PbSO4均为难溶物)
(5)“第一次焙烧”每产生3molSO2,若完全转化为硫酸,理论上需要再充入空气_____ L。(标准状况下)

已知:蒸发结晶得到MnSO4。
(1)将软锰矿粉泥浆化的目的是
(2)“第一次焙烧”温度是1000℃,生成Mn3O4、SO2和O2,“第二次焙烧”温度为700℃,产物为Mn2O3;700℃时焙烧的氧化剂与还原剂物质的量比为
(3)“酸歧化”的离子方程式为
(4)活化MnO2中不能含有铜、铅等重金属元素,在“中和过滤”前需要加入某种盐溶液除去重金属离子,该盐的化学式是
(5)“第一次焙烧”每产生3molSO2,若完全转化为硫酸,理论上需要再充入空气
您最近一年使用:0次
解题方法
4 . 亚硝酸钠(NaNO2)用途很广泛:可制药,作食品防腐剂、显色剂,作印染工业的媒染剂、漂白剂、缓蚀剂等,某兴趣小组欲制备亚硝酸钠并进行一定的实验探究,查阅资料可知:①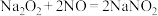 ;②
;②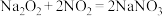 ;③
;③ 可被酸性
可被酸性 氧化成
氧化成 ,现用下图所示装置制备
,现用下图所示装置制备 :
:
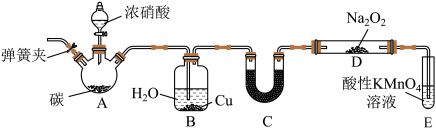
(1)连接仪器之后,加入药品之前需要进行的操作是_____ ;过氧化钠的电子式是_____ 。
(2)仪器B中Cu的作用是_____ 。(用离子方程式表示)
(3)U形管C中的试剂可以是_____ 。
(4)试管E中反应的离子方程式为_____ 。
(5)以上装置有设计缺陷,会使产品NaNO2中杂质增多,改进方法是_____ 。
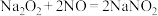 ;②
;②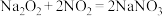 ;③
;③ 可被酸性
可被酸性 氧化成
氧化成 ,现用下图所示装置制备
,现用下图所示装置制备 :
:
(1)连接仪器之后,加入药品之前需要进行的操作是
(2)仪器B中Cu的作用是
(3)U形管C中的试剂可以是
(4)试管E中反应的离子方程式为
(5)以上装置有设计缺陷,会使产品NaNO2中杂质增多,改进方法是
您最近一年使用:0次
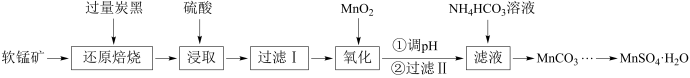
5 . 以软锰矿(主要成分是MnO2,还含有Fe2O3、SiO2、CuO、CaO等少量杂质)为主要原料制备硫酸锰晶体的工艺流程如图:
已知:①还原焙烧的主反应为 ;
;
②Mn2+在酸性条件下比较稳定,pH高于5.5时易被O2氧化;
③ 溶于1份冷水、0.6份沸水,不溶于乙醇。
溶于1份冷水、0.6份沸水,不溶于乙醇。
回答下列问题:
(1)还原焙烧时软锰矿要粉碎,其目的是___________ 。过滤I得到的滤渣主要成分的化学式是___________ 。
(2)“氧化”时发生反应的离子方程式为___________ 。
(3)调溶液pH时,可使用的物质是___________ (填一种即可,写化学式)。
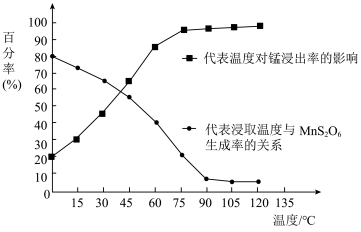
(4)“浸取”时,反应中往往有副产物MnS2O6生成,温度对浸取反应的影响如图所示,为减少MnS2O6的生成,“浸取”的适宜温度是___________ ;过滤Ⅱ所得的滤液中加入NH4HCO3溶液时,温度不宜太高的原因是___________ 。
(5)向滤液中加入NH4HCO3溶液生成MnCO3的同时会产生一种无色无味的气体,写出其离子方程式___________ 。
(6)获得 后常用乙醇洗涤,主要目的是
后常用乙醇洗涤,主要目的是___________ ;洗涤 的操作为
的操作为___________ 。

已知:①还原焙烧的主反应为
 ;
;②Mn2+在酸性条件下比较稳定,pH高于5.5时易被O2氧化;
③
 溶于1份冷水、0.6份沸水,不溶于乙醇。
溶于1份冷水、0.6份沸水,不溶于乙醇。回答下列问题:
(1)还原焙烧时软锰矿要粉碎,其目的是
(2)“氧化”时发生反应的离子方程式为
(3)调溶液pH时,可使用的物质是
(4)“浸取”时,反应中往往有副产物MnS2O6生成,温度对浸取反应的影响如图所示,为减少MnS2O6的生成,“浸取”的适宜温度是

(5)向滤液中加入NH4HCO3溶液生成MnCO3的同时会产生一种无色无味的气体,写出其离子方程式
(6)获得
 后常用乙醇洗涤,主要目的是
后常用乙醇洗涤,主要目的是 的操作为
的操作为
您最近一年使用:0次
名校
解题方法
6 . 采用废铁屑还原软锰矿(软锰矿主要成分是 ,还含少量
,还含少量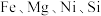 等元素的氧化物杂质)来制备
等元素的氧化物杂质)来制备 的工艺流程如图所示:
的工艺流程如图所示: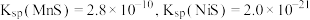 ;
;
②假设溶液中某离子浓度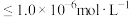 时,该离子沉淀完全;
时,该离子沉淀完全;
③室温时生成氢氧化物的 见下表。
见下表。
回答下列问题:
(1)“酸浸”时,为提高浸取效率,可采取的措施有_____ (任写一点)。
(2)在“浸出液”中加入 时发生反应的离子方程式为
时发生反应的离子方程式为_____ 。
(3)“除杂”过程中有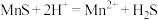 反应发生,其平衡常数
反应发生,其平衡常数 与
与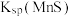 、
、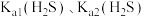 的代数关系式为
的代数关系式为
_____ 。加入 “除杂”后的滤渣为
“除杂”后的滤渣为_____ (填化学式),“除杂”后的滤液中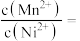
_____ 。
(4)“沉锰”过程中温度和 对
对 和
和 沉淀率的影响如图所示。则“沉锰”的合适条件是
沉淀率的影响如图所示。则“沉锰”的合适条件是_____ 。“沉锰”时发生反应的离子方程式为_____ 。
 ,还含少量
,还含少量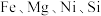 等元素的氧化物杂质)来制备
等元素的氧化物杂质)来制备 的工艺流程如图所示:
的工艺流程如图所示: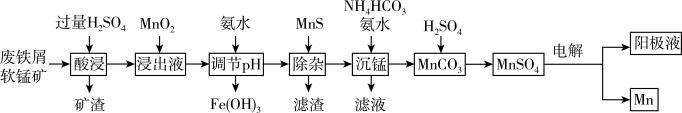
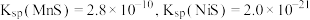 ;
;②假设溶液中某离子浓度
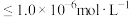 时,该离子沉淀完全;
时,该离子沉淀完全;③室温时生成氢氧化物的
 见下表。
见下表。| 离子 |  |  |  |  |  |
开始沉淀的 | 7.5 | 1.8 | 8.1 | 7.7 | 8.3 |
完全沉淀的 | 9.7 | 3 | 9.4 | 8.4 | 9.8 |
(1)“酸浸”时,为提高浸取效率,可采取的措施有
(2)在“浸出液”中加入
 时发生反应的离子方程式为
时发生反应的离子方程式为(3)“除杂”过程中有
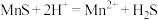 反应发生,其平衡常数
反应发生,其平衡常数 与
与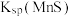 、
、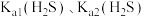 的代数关系式为
的代数关系式为
 “除杂”后的滤渣为
“除杂”后的滤渣为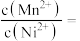
(4)“沉锰”过程中温度和
 对
对 和
和 沉淀率的影响如图所示。则“沉锰”的合适条件是
沉淀率的影响如图所示。则“沉锰”的合适条件是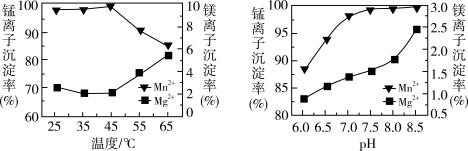
您最近一年使用:0次
2024-03-11更新
|
155次组卷
|
3卷引用:广东省佛山市顺德区勒流中学、均安中学、龙江中学等十五校2023-2024学年高二上学期12月联考化学试题
名校
解题方法
7 . 钒的用途十分广泛,有金属“维生素”之称。以含钒石煤(主要成分是V2O3、V2O4,含有的杂质有SiO2、FeS2及Mg、Al、Mn等的化合物)制备单质钒的工艺流程如图所示。
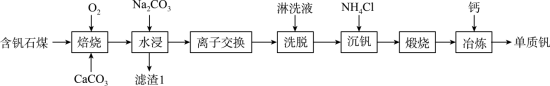
已知:①该工艺条件下,溶液中金属离子开始沉淀时和完全沉淀时的pH如下表所示:
②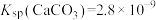 ,
,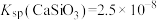 ,
,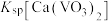 远大于
远大于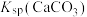 。
。
回答下列问题:
(1)基态Fe3+的价电子排布式为___________ 。
(2)为了提高“焙烧”效率,可采取的措施有___________ 、___________ 。
(3)“焙烧”时,V2O3、V2O4都转化为Ca(VO3)3,写出V2O4转化为Ca(VO3)3的化学方程式:___________ 。
(4)“水浸”加入Na2CO3调节溶液的pH为8.5,可完全除去的金属离子有___________ ;“水浸”加入过量Na2CO3不能使CaSiO3完全转化为CaCO3,原因是___________ 。(列式计算平衡常数分析该反应进行的趋势,一般认为,K>105时反应进行较完全,K<10-5时反应难以进行)
(5)“离子交换”与“洗脱”可表示为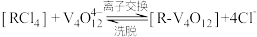 (
( 为强碱性阴离子交换树脂,
为强碱性阴离子交换树脂,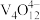 为VO
为VO 在水溶液中的实际存在形式),则“洗脱”过程中“淋洗液”最好选用
在水溶液中的实际存在形式),则“洗脱”过程中“淋洗液”最好选用___________ 。
(6)“沉钒”过程析出NH4VO3晶体,需要加入过量NH4Cl,目的是___________ 。
(7)下列金属冶炼方法中,与本工艺流程中冶炼钒的方法相似的是___________(填字母)。

已知:①该工艺条件下,溶液中金属离子开始沉淀时和完全沉淀时的pH如下表所示:
| 金属离子 | Fe3+ | Mg2+ | Al3+ | Mn2+ |
| 开始沉淀时的pH | 1.9 | 7.0 | 3.0 | 8.1 |
| 完全沉淀时的pH | 3.2 | 9.0 | 4.7 | 10.1 |
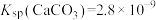 ,
,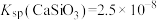 ,
,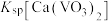 远大于
远大于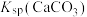 。
。回答下列问题:
(1)基态Fe3+的价电子排布式为
(2)为了提高“焙烧”效率,可采取的措施有
(3)“焙烧”时,V2O3、V2O4都转化为Ca(VO3)3,写出V2O4转化为Ca(VO3)3的化学方程式:
(4)“水浸”加入Na2CO3调节溶液的pH为8.5,可完全除去的金属离子有
(5)“离子交换”与“洗脱”可表示为
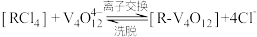 (
( 为强碱性阴离子交换树脂,
为强碱性阴离子交换树脂,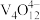 为VO
为VO 在水溶液中的实际存在形式),则“洗脱”过程中“淋洗液”最好选用
在水溶液中的实际存在形式),则“洗脱”过程中“淋洗液”最好选用(6)“沉钒”过程析出NH4VO3晶体,需要加入过量NH4Cl,目的是
(7)下列金属冶炼方法中,与本工艺流程中冶炼钒的方法相似的是___________(填字母)。
| A.高炉炼铁 | B.电解熔融氯化钠制钠 |
| C.铝热反应制锰 | D.氧化汞分解制汞 |
您最近一年使用:0次
解题方法
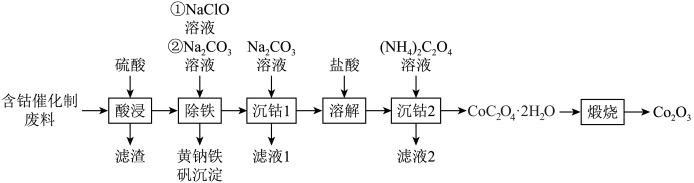
8 . Co2O3主要用作颜料、釉料及磁性材料,一种利用含钴催化剂废料(主要含Co、Fe,还含有少量的CoO、FeO,Fe2O3、CaO、SiO2)制备氧化钴(Co2O3)的工艺流程如图所示。
已知:ⅰ.黄钠铁矾的化学式为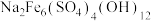 ;
;
ⅱ.金属钴与铁具有相似的化学性质;
ⅲ.氧化性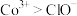 。
。
回答下列问题:
(1)钴元素基态原子的电子排布式为_______ 。
(2)“酸浸”时滤渣的主要成分为_______ (填化学式)。
(3)“除铁”时先加入NaClO溶液,主要发生反应的离子方程式为_______ ,再加入 溶液调节pH为2.5~3.0,生成黄钠铁矾沉淀。
溶液调节pH为2.5~3.0,生成黄钠铁矾沉淀。
(4)常温下,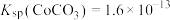 ,
,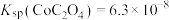 ,向
,向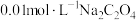 溶液中加入足量
溶液中加入足量 固体,能否生成
固体,能否生成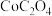 沉淀?
沉淀?_______ (通过计算说明)。
(5)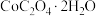 在空气中加热煅烧得到
在空气中加热煅烧得到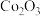 的化学方程式为
的化学方程式为_______ 。
(6)(a)钴被称为无机配合物之王,配合物 的中心离子的配位数为
的中心离子的配位数为_______ 。
(b)钴的一种化合物的晶胞结构如图所示。
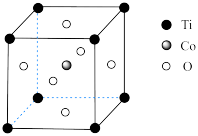
①晶体中一个Ti周围与其最近的O的个数为_______ 。
②在该晶胞中氧、钴、钛的粒子个数比为_______ 。

已知:ⅰ.黄钠铁矾的化学式为
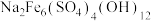 ;
;ⅱ.金属钴与铁具有相似的化学性质;
ⅲ.氧化性
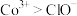 。
。回答下列问题:
(1)钴元素基态原子的电子排布式为
(2)“酸浸”时滤渣的主要成分为
(3)“除铁”时先加入NaClO溶液,主要发生反应的离子方程式为
 溶液调节pH为2.5~3.0,生成黄钠铁矾沉淀。
溶液调节pH为2.5~3.0,生成黄钠铁矾沉淀。(4)常温下,
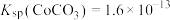 ,
,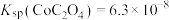 ,向
,向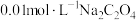 溶液中加入足量
溶液中加入足量 固体,能否生成
固体,能否生成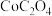 沉淀?
沉淀?(5)
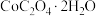 在空气中加热煅烧得到
在空气中加热煅烧得到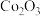 的化学方程式为
的化学方程式为(6)(a)钴被称为无机配合物之王,配合物
 的中心离子的配位数为
的中心离子的配位数为(b)钴的一种化合物的晶胞结构如图所示。

①晶体中一个Ti周围与其最近的O的个数为
②在该晶胞中氧、钴、钛的粒子个数比为
您最近一年使用:0次
名校
解题方法
9 . 氨氮废水是造成水体富营养化的原因之一,下图为处理氨氮废水的流程。错误 的是

A.过程①: |
B.过程②总反应式: |
C.过程③: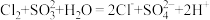 |
D. 溶于水: 溶于水: |
您最近一年使用:0次
2024-03-06更新
|
1113次组卷
|
5卷引用:广东省广州市黄广中学2023-2024学年高一下学期3月月考化学试题
广东省广州市黄广中学2023-2024学年高一下学期3月月考化学试题云南省云南师范大学实验中学2023-2024学年高一下学期三月月考化学试题福建省泉州市2024届高三下学期高中毕业班质量监测(三)化学试卷(已下线)通关练01 化学基本概念再回归-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)(已下线)压轴题01?离子方程式与离子共存的判断(5大题型+方法总结+压轴题速练)-2024年高考化学压轴题专项训练(新高考通用)
名校
解题方法
10 . 构建知识网络是一种有效的学习方法,化学学习中的“价-类”二维图就是其中一种,如图所示是铁及其化合物的“价-类”二维图,请回答下列问题:_____ 。
(2)下列各图示中能较长时间观察到 的是
的是_____ 。_____ ,当生成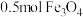 时,转移电子数为
时,转移电子数为_____ 。
(4)将 溶于盐酸后再加入1滴
溶于盐酸后再加入1滴 溶液,则溶液变红时发生反应的离子方程式为
溶液,则溶液变红时发生反应的离子方程式为_____ 。
(5)绿矾 是补血剂的原料,易变质。将硫酸亚铁溶液加热浓缩,冷却结晶,之后
是补血剂的原料,易变质。将硫酸亚铁溶液加热浓缩,冷却结晶,之后_____ 可获得绿矾晶体,如何检验绿矾是否完全变质_____ 。
(6)将硫酸亚铁固体隔绝空气煅烧,可发生以下反应,请将方程式配平:_____ 。
_____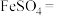 _____
_____ _____
_____ _____
_____

(2)下列各图示中能较长时间观察到
 的是
的是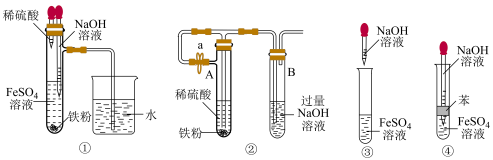
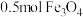 时,转移电子数为
时,转移电子数为(4)将
 溶于盐酸后再加入1滴
溶于盐酸后再加入1滴 溶液,则溶液变红时发生反应的离子方程式为
溶液,则溶液变红时发生反应的离子方程式为(5)绿矾
 是补血剂的原料,易变质。将硫酸亚铁溶液加热浓缩,冷却结晶,之后
是补血剂的原料,易变质。将硫酸亚铁溶液加热浓缩,冷却结晶,之后(6)将硫酸亚铁固体隔绝空气煅烧,可发生以下反应,请将方程式配平:
_____
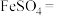 _____
_____ _____
_____ _____
_____
您最近一年使用:0次
2024-03-02更新
|
162次组卷
|
2卷引用:广东省清远市五校(清新一中、佛冈一中、南阳中学、连山中学、连州中学)2023-2024学年高二下学期5月联考化学试卷



