名校
1 . 按要求完成下列题目。
(1)书写对应的化学方程式:
①用氯气制备漂白粉:___________ 。
②固体管道疏通剂(主要成分有氢氧化钠和铝粉)的疏通原理:___________ 。
③呼吸面具中过氧化钠与二氧化碳反应:___________ 。
④KClO3可以和草酸(H2C2O4)、硫酸反应生成高效的消毒杀菌剂ClO2气体,还生成CO2和KHSO4等物质。写出该反应的化学方程式___________ 。
(2)书写对应的离子方程式:
⑤制作印刷电路板时氯化铁溶液腐蚀铜:___________ 。
⑥用高锰酸钾酸性溶液检验溶液中的亚铁离子(还原产物为Mn2+):___________ 。
⑦在酸性条件下,向含铬废水中加入FeSO4,可将 还原为Cr3+,该过程的离子反应方程式为
还原为Cr3+,该过程的离子反应方程式为___________ 。
(1)书写对应的化学方程式:
①用氯气制备漂白粉:
②固体管道疏通剂(主要成分有氢氧化钠和铝粉)的疏通原理:
③呼吸面具中过氧化钠与二氧化碳反应:
④KClO3可以和草酸(H2C2O4)、硫酸反应生成高效的消毒杀菌剂ClO2气体,还生成CO2和KHSO4等物质。写出该反应的化学方程式
(2)书写对应的离子方程式:
⑤制作印刷电路板时氯化铁溶液腐蚀铜:
⑥用高锰酸钾酸性溶液检验溶液中的亚铁离子(还原产物为Mn2+):
⑦在酸性条件下,向含铬废水中加入FeSO4,可将
 还原为Cr3+,该过程的离子反应方程式为
还原为Cr3+,该过程的离子反应方程式为
您最近一年使用:0次
解题方法
2 . 铜镉渣主要含锌、铜、铁、镉(Cd)、钴(Co)等单质。湿法炼锌产生的铜镉渣用于生产金属镉的工艺流程如图:
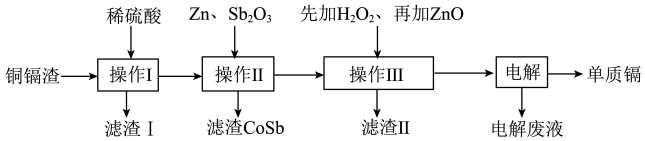
表中列出了相关金属离子生成氢氧化物沉淀的pH(金属离子的起始浓度为0.1 )
)
(1)酸浸铜镉渣时,加快反应速率的措施有_______ (写一条)。滤渣Ⅰ的主要成分是_______ (填化学式)。
(2)操作III中先加入适量 ,发生反应的离子方程式
,发生反应的离子方程式_______ ;再加入ZnO调节反应液的pH,pH范围为_______ ;选择_______ (填“铁氰化钾”或“硫氰化钾”)试剂,能证明添加的 已过量。
已过量。
(3)常用沉淀转化法处理含 废水,写出碳酸钙处理
废水,写出碳酸钙处理 的离子方程式
的离子方程式______ ;若反应达到平衡后溶液中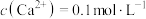 ,溶液中
,溶液中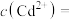
______  。[已知25℃,
。[已知25℃,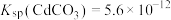 ,
,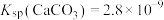 ]
]

表中列出了相关金属离子生成氢氧化物沉淀的pH(金属离子的起始浓度为0.1
 )
)(1)酸浸铜镉渣时,加快反应速率的措施有
| 氢氧化物 |  |  | 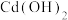 |  |
| 开始沉淀的pH | 1.5 | 6.5 | 7.2 | 8.0 |
| 沉淀完全的pH | 3.3 | 9.9 | 9.5 | 11.1 |
(2)操作III中先加入适量
 ,发生反应的离子方程式
,发生反应的离子方程式 已过量。
已过量。(3)常用沉淀转化法处理含
 废水,写出碳酸钙处理
废水,写出碳酸钙处理 的离子方程式
的离子方程式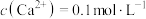 ,溶液中
,溶液中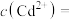
 。[已知25℃,
。[已知25℃,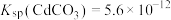 ,
,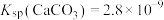 ]
]
您最近一年使用:0次
名校
解题方法
3 . 镍、钴是重要的战略物资,但资源匮乏。一种利用酸浸出法从冶金厂废炉渣中提取镍和钴的工艺流程如下:
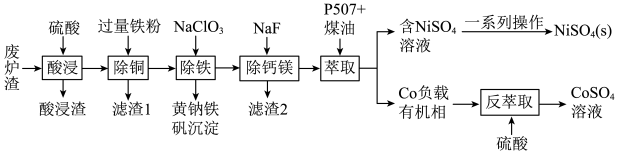
已知:i.酸浸液中的金属阳离子有Ni2+、Co2+、Cu2+、Mg2+、Ca2+等
ii.NiSO4在水中的溶解度随温度升高而增大
回答下列问题:
(1)“滤渣1”的主要成分是___________ 。(写化学式)
(2)黄钠铁矾的化学式为Na2Fe6(SO4)4(OH)12,“除铁”的离子方程式为___________ 。
(3)“除钙镁”时,随pH降低,NaF用量急剧增加,原因是___________ (结合平衡理论解释)。Ca2+和Mg2+沉淀完全时,溶液中F-的浓度c(F-)最小为___________ mol·L-1。[已知离子浓度≤10-5mol/L时,认为该离子沉淀完全,Ksp(CaF2)=1.0×10-10(mol/L)3,Ksp(MgF2)=7.5×10-11(mol/L)3]
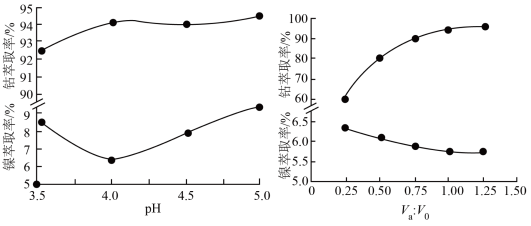
(4)镍、钴萃取率与料液pH、萃取剂体积与料液体积比Va:V0的关系曲线如下图所示,则“萃取”时应选择的pH和Va:V0分别为___________ 、___________ 。
(5)获得NiSO4(s)的“一系列操作”是___________ 。
(6)该工艺流程中,可循环利用的物质是___________ 。

已知:i.酸浸液中的金属阳离子有Ni2+、Co2+、Cu2+、Mg2+、Ca2+等
ii.NiSO4在水中的溶解度随温度升高而增大
回答下列问题:
(1)“滤渣1”的主要成分是
(2)黄钠铁矾的化学式为Na2Fe6(SO4)4(OH)12,“除铁”的离子方程式为
(3)“除钙镁”时,随pH降低,NaF用量急剧增加,原因是
(4)镍、钴萃取率与料液pH、萃取剂体积与料液体积比Va:V0的关系曲线如下图所示,则“萃取”时应选择的pH和Va:V0分别为

(5)获得NiSO4(s)的“一系列操作”是
(6)该工艺流程中,可循环利用的物质是
您最近一年使用:0次
2023-12-27更新
|
605次组卷
|
4卷引用:广东省深圳市实验学校高中部2023-2024学年高二上学期第三阶段考试化学试题
广东省深圳市实验学校高中部2023-2024学年高二上学期第三阶段考试化学试题山东省实验中学2023-2024学年高三上学期11月二诊化学试题山东省淄博市部分学校2023-2024学年高三上学期联考化学试卷(已下线)题型16 无机化工流程综合分析-2024年高考化学二轮热点题型归纳与变式演练(新高考通用)
4 . Operando光谱和DFT计算明确了在负载WO3的CeO2上NH3(NH3-SCR)选择性催化还原NO的还原/氧化半循环的过程如下。下列说法正确的是
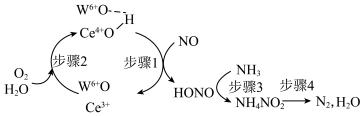

A.步骤1中氧化剂与还原剂的物质的量之比: |
B.氧化性强弱顺序: |
C.每生成 理论上消耗 理论上消耗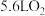 |
D.上述过程的总反应方程式: |
您最近一年使用:0次
2023-12-19更新
|
153次组卷
|
2卷引用:广东省深圳市实验学校高中部2023-2024学年高二上学期第三阶段考试化学试题
名校
5 . 电石渣[主要成分为 ,杂质不参与反应]是氯碱工业中的废料,以电石渣为原料制取
,杂质不参与反应]是氯碱工业中的废料,以电石渣为原料制取 的工艺流程如图所示:已知:
的工艺流程如图所示:已知: 易溶于水。
易溶于水。

(1)工业生产电石的反应为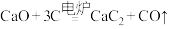 ,该反应每消耗
,该反应每消耗 转移电子数为
转移电子数为_______ 。
(2)流程中的 可由
可由 反应制得,离子方程式为
反应制得,离子方程式为_______ ,其中盐酸体现的性质有_______ 。
(3)写出 与
与 反应生成
反应生成 的化学方程式
的化学方程式_______ 。
(4)制 时要控制温度
时要控制温度 上,原因可能是
上,原因可能是_______ ,反应结束以后通常会加入适量活性炭,再过滤。从绿色化学的角度分析,活性炭的作用是_______ 。
(5)“转化”时加入 的目的是
的目的是_______ 。
 ,杂质不参与反应]是氯碱工业中的废料,以电石渣为原料制取
,杂质不参与反应]是氯碱工业中的废料,以电石渣为原料制取 的工艺流程如图所示:已知:
的工艺流程如图所示:已知: 易溶于水。
易溶于水。
(1)工业生产电石的反应为
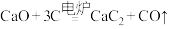 ,该反应每消耗
,该反应每消耗 转移电子数为
转移电子数为(2)流程中的
 可由
可由 反应制得,离子方程式为
反应制得,离子方程式为(3)写出
 与
与 反应生成
反应生成 的化学方程式
的化学方程式(4)制
 时要控制温度
时要控制温度 上,原因可能是
上,原因可能是(5)“转化”时加入
 的目的是
的目的是
您最近一年使用:0次
名校
6 . 高铁酸钾( ,其中Fe元素为
,其中Fe元素为 价)是新型绿色水处理剂,其制备方法如下图所示(部分步骤已略去)。已知:在碱性溶液中的溶解度:
价)是新型绿色水处理剂,其制备方法如下图所示(部分步骤已略去)。已知:在碱性溶液中的溶解度: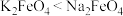 。
。
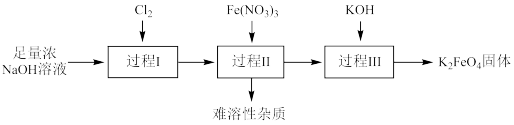
(1)过程Ⅰ的目的是制备 ,反应的离子方程式为
,反应的离子方程式为_______ 。
(2)过程Ⅱ为碱性条件下制备高铁酸钠 。
。
①补全过程Ⅱ中发生反应的离子方程式:_______ 。
_______ _______
_______ _______= _______
_______= _______ _______
_______ _______
_______
②除 外,过程Ⅱ中还可能生成一种含铁元素的难溶性杂质,该物质的化学式为
外,过程Ⅱ中还可能生成一种含铁元素的难溶性杂质,该物质的化学式为_______ 。
(3)过程Ⅲ中,发生反应的化学方程式为_______ 。
(4)过程Ⅰ~Ⅲ中,需要进行过滤操作的是_______ (填序号)。
(5) 可将氨氮废水中的
可将氨氮废水中的 转化为
转化为 除去,Fe元素被还原为
除去,Fe元素被还原为 价。每处理1个
价。每处理1个 理论上转移的电子个数为
理论上转移的电子个数为_______ 。
 ,其中Fe元素为
,其中Fe元素为 价)是新型绿色水处理剂,其制备方法如下图所示(部分步骤已略去)。已知:在碱性溶液中的溶解度:
价)是新型绿色水处理剂,其制备方法如下图所示(部分步骤已略去)。已知:在碱性溶液中的溶解度: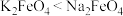 。
。
(1)过程Ⅰ的目的是制备
 ,反应的离子方程式为
,反应的离子方程式为(2)过程Ⅱ为碱性条件下制备高铁酸钠
 。
。①补全过程Ⅱ中发生反应的离子方程式:
_______
 _______
_______ _______= _______
_______= _______ _______
_______ _______
_______②除
 外,过程Ⅱ中还可能生成一种含铁元素的难溶性杂质,该物质的化学式为
外,过程Ⅱ中还可能生成一种含铁元素的难溶性杂质,该物质的化学式为(3)过程Ⅲ中,发生反应的化学方程式为
(4)过程Ⅰ~Ⅲ中,需要进行过滤操作的是
(5)
 可将氨氮废水中的
可将氨氮废水中的 转化为
转化为 除去,Fe元素被还原为
除去,Fe元素被还原为 价。每处理1个
价。每处理1个 理论上转移的电子个数为
理论上转移的电子个数为
您最近一年使用:0次
名校
7 . 某化学兴趣小组模拟“侯氏制碱法”制纯碱并进行后续实验。
Ⅰ.制备纯碱:先以NaCl、NH3、CO2 和水等为原料,用如图所示装置制取NaHCO3,然后再将NaHCO3 制备成Na2CO3。
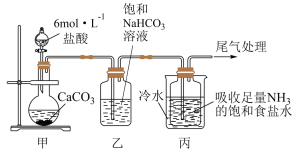
(1)装置甲中反应的离子方程式 为______________ ,装置乙的作用是__________ ,反应的化学方程式为__________________ 。
(2)反应进行一段时间后,观察到装置丙中试剂瓶内溶液中有白色固体析出,经检验该白色固体是NaHCO3,装置丙中反应的化学方程式为_________________ 。
(3)用装置丙中产生的NaHCO3 制取Na2CO3 时,需要进行的实验操作有__________ 、洗涤、干燥、灼烧固体, 化学方程式为_______________ 。
Ⅱ.测定所得产品的组成和纯度
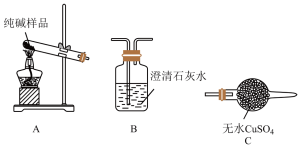
(4)检验纯碱样品中是否混有NaHCO3,请完成下表:
(5)测定该纯碱样品的纯度:称取m1 g 样品,置于试管中,充分加热,得到固体的质量为m2 g。则该纯碱样品的纯度为_______。(填字母代号)
Ⅰ.制备纯碱:先以NaCl、NH3、CO2 和水等为原料,用如图所示装置制取NaHCO3,然后再将NaHCO3 制备成Na2CO3。

(1)装置甲中反应的
(2)反应进行一段时间后,观察到装置丙中试剂瓶内溶液中有白色固体析出,经检验该白色固体是NaHCO3,装置丙中反应的化学方程式为
(3)用装置丙中产生的NaHCO3 制取Na2CO3 时,需要进行的实验操作有
Ⅱ.测定所得产品的组成和纯度

(4)检验纯碱样品中是否混有NaHCO3,请完成下表:
| 装置的顺序(填编号) | 实验现象 | 实验结论 |
| 样品中含NaHCO3 |
(5)测定该纯碱样品的纯度:称取m1 g 样品,置于试管中,充分加热,得到固体的质量为m2 g。则该纯碱样品的纯度为_______。(填字母代号)
A.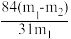 | B.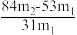 |
C. | D.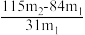 |
您最近一年使用:0次
8 . “绿色化学”又称环境友好化学,主张“回收利用、变废为宝、循环使用∙∙∙∙∙∙”,有利于资源利用的可持续发展。工业合金废料(含铝、铁、铜)回收利用的流程如下图所示:
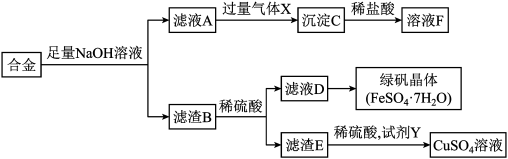
(1)写出合金与足量 溶液反应的化学方程式
溶液反应的化学方程式___________ ;向滤液A中通入过量气体X,X的化学式是___________ ;
(2)若要从滤液D得到绿矾晶体,必须进行的实验操作步骤:___________ 、___________ 、过滤、自然干燥。
(3)若试剂Y为具有强氧化性的双氧水,请在答题卡上相应位置写出滤渣E发生的离子方程式并用单线桥表示出电子转移的方向与数目__________________ 。
(4)已知:稀硝酸具有强氧化性,故可以溶解铜,也可以溶解上述合金。若用稀硝酸处理该合金废料,固体未完全溶解,则滤液D中 元素将以
元素将以_________ (填“ ”或“
”或“ )离子形式存在,检验该离子的试剂可选择
)离子形式存在,检验该离子的试剂可选择_________ (填序号)。
A. B.
B. C.氯水 D.
C.氯水 D.

(1)写出合金与足量
 溶液反应的化学方程式
溶液反应的化学方程式(2)若要从滤液D得到绿矾晶体,必须进行的实验操作步骤:
(3)若试剂Y为具有强氧化性的双氧水,请在答题卡上相应位置写出滤渣E发生的离子方程式并用单线桥表示出电子转移的方向与数目
(4)已知:稀硝酸具有强氧化性,故可以溶解铜,也可以溶解上述合金。若用稀硝酸处理该合金废料,固体未完全溶解,则滤液D中
 元素将以
元素将以 ”或“
”或“ )离子形式存在,检验该离子的试剂可选择
)离子形式存在,检验该离子的试剂可选择A.
 B.
B. C.氯水 D.
C.氯水 D.
您最近一年使用:0次
名校
9 . 通过 CO2 捕获和转化技术可实现 CO2 资源化利用,其物质转化关系如图所示。
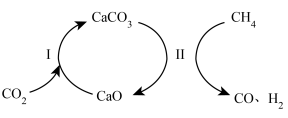
| A.过程Ⅰ属于氧化还原反应 |
| B.过程Ⅱ中的反应为CaCO3+CH4=CaO+2CO+2H2 |
| C.捕获和转化 CO2的过程中,CaO 可以循环利用 |
| D.CO2的捕获和转化有助于减弱温室效应 |
您最近一年使用:0次
2023-12-11更新
|
189次组卷
|
6卷引用:广东省 深圳实验学校高中部2023-2024学年高一上学期化学培优考试 2
名校
解题方法
10 . 某化学小组为了研究外界条件对化学反应速率的影响,进行了如下实验:
(1)该实验还需要测量的数据是_______ 。该实验的原理是:_______ (用化学方程式表示)。
(2)
_______ ,
_______ 。
(3)探究温度对化学反应速率的影响,应选择实验_______ (填实验编号)。
(4)若实验①用时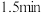 则第一组实验的化学反应速率(用草酸表示)为
则第一组实验的化学反应速率(用草酸表示)为_______ 。
(5)某同学绘制了瞬时速率 和时间
和时间 的图像
的图像
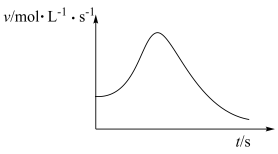
①该同学提出猜想
猜想a:温度上升导致速率快速上升
猜想b:反应产生了催化剂
该同学发现该反应前后体系温度上升了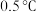 ,因此
,因此_______ 不成立(猜想a或猜想b)
②该同学推测可能的催化剂是_______ (填物质化学式)。
③验证猜想的方法是_______ 。
| 实验编号 | 实验温度 | 试管中所加试剂及其用量 | |||
  溶液 溶液 |  |  稀 稀 溶液 溶液 | 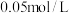  溶液 溶液 | ||
| ① | 25 | 3.0 |  | 2.0 | 3.0 |
| ② | 25 | 2.0 | 3.0 | 2.0 | 3.0 |
| ③ | 30 | 2.0 |  | 2.0 | 3.0 |
(1)该实验还需要测量的数据是
(2)


(3)探究温度对化学反应速率的影响,应选择实验
(4)若实验①用时
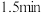 则第一组实验的化学反应速率(用草酸表示)为
则第一组实验的化学反应速率(用草酸表示)为(5)某同学绘制了瞬时速率
 和时间
和时间 的图像
的图像
①该同学提出猜想
猜想a:温度上升导致速率快速上升
猜想b:反应产生了催化剂
该同学发现该反应前后体系温度上升了
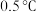 ,因此
,因此②该同学推测可能的催化剂是
③验证猜想的方法是
您最近一年使用:0次



