名校
1 . 实验室以 溶液和碳酸氢铵溶液制备氧钒(IV)碱式碳酸铵晶体
溶液和碳酸氢铵溶液制备氧钒(IV)碱式碳酸铵晶体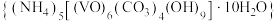 ,装置如图所示。已知:
,装置如图所示。已知: 能被
能被 氧化。下列说法不正确的是
氧化。下列说法不正确的是
 溶液和碳酸氢铵溶液制备氧钒(IV)碱式碳酸铵晶体
溶液和碳酸氢铵溶液制备氧钒(IV)碱式碳酸铵晶体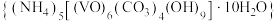 ,装置如图所示。已知:
,装置如图所示。已知: 能被
能被 氧化。下列说法不正确的是
氧化。下列说法不正确的是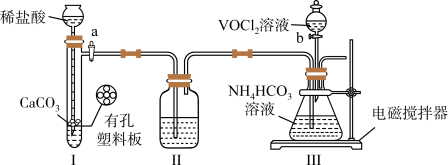
A.Ⅱ中的试剂为饱和 溶液 溶液 |
B.实验开始时应先打开活塞 ,一段时间后,再打开活塞 ,一段时间后,再打开活塞 |
| C.Ⅲ中的反应为氧化还原反应 |
D.反应完全,小心取下分液漏斗,停止通气,立即塞上橡胶塞,将锥形瓶置于 保护下的干燥器中,静置过夜,得到晶体 保护下的干燥器中,静置过夜,得到晶体 |
您最近一年使用:0次
2024-05-13更新
|
299次组卷
|
2卷引用:湖南省新高考教学教研联盟2023-2024学年高三下学期第二次联考化学试题
2 . 正高碘酸(H5IO6)是白色结晶性粉末,可溶于水,主要用作氧化剂和分析试剂。由NaI制取H5IO6的实验流程如图所示:
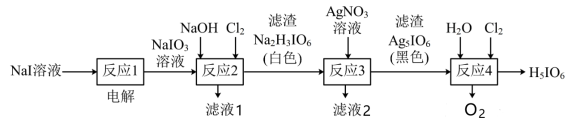
A.“反应1”中: |
B.“反应2”中: |
C.“反应3”中: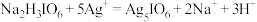 |
D.“反应4”中: |
您最近一年使用:0次
3 . 氧钒(Ⅳ)碱式碳酸铵晶体{化学式为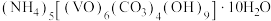 ,
,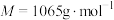 }是一种难溶于水的化合物,它是制备热敏材料VO2的原料。实验室以V2O5为原料,通过还原、转化、沉淀等步骤合成该晶体的流程如下:
}是一种难溶于水的化合物,它是制备热敏材料VO2的原料。实验室以V2O5为原料,通过还原、转化、沉淀等步骤合成该晶体的流程如下:

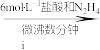
 溶液
溶液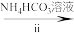 氧钒(Ⅳ)碱式碳酸铵晶体
氧钒(Ⅳ)碱式碳酸铵晶体
已知:+4价钒在弱酸性条件下具有还原性。
回答下列问题:
(1)N2H4为二元弱碱,其在水中的电离过程与NH3类似,其第一步电离方程式为_____ ,第二步电离方程式为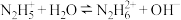 ;N2H4与液氧接触能自燃,产物对环境无污染,写出发生反应的化学方程式:
;N2H4与液氧接触能自燃,产物对环境无污染,写出发生反应的化学方程式:_____ 。
(2)步骤ii可通过如图装置完成。 的优点为
的优点为_____ ,检查其气密性的操作为_____ 。
②实验开始时,先打开_____ (填“K1”或“K2”)。
③盛装NH4HCO3溶液的仪器名称为_____ 。
(3)测定氧钒(Ⅳ)碱式碳酸铵晶体粗产品的纯度。
实验步骤:粗产品wg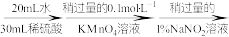
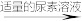
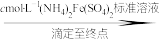 再重复实验两次。
再重复实验两次。
已知: 。
。
①滴入NaNO2溶液的目的是除去KMnO4,写出其反应的离子方程式:_____ 。
②若平均消耗cmol/L(NH4)2Fe(SO4)2标准溶液的体积为amL,则氧钒(Ⅳ)碱式碳酸铵晶体粗产品的纯度为_____  。
。
③若其他操作均正确,但NaNO2的加入量不足,会引起测定结果_____ (填“偏大”“偏小”或“无影响”)。
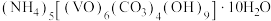 ,
,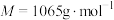 }是一种难溶于水的化合物,它是制备热敏材料VO2的原料。实验室以V2O5为原料,通过还原、转化、沉淀等步骤合成该晶体的流程如下:
}是一种难溶于水的化合物,它是制备热敏材料VO2的原料。实验室以V2O5为原料,通过还原、转化、沉淀等步骤合成该晶体的流程如下:
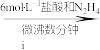
 溶液
溶液 氧钒(Ⅳ)碱式碳酸铵晶体
氧钒(Ⅳ)碱式碳酸铵晶体已知:+4价钒在弱酸性条件下具有还原性。
回答下列问题:
(1)N2H4为二元弱碱,其在水中的电离过程与NH3类似,其第一步电离方程式为
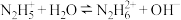 ;N2H4与液氧接触能自燃,产物对环境无污染,写出发生反应的化学方程式:
;N2H4与液氧接触能自燃,产物对环境无污染,写出发生反应的化学方程式:(2)步骤ii可通过如图装置完成。
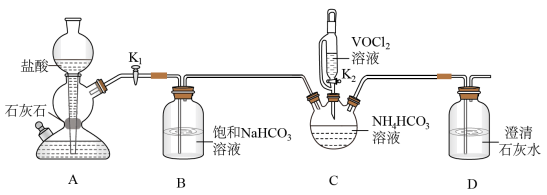
 的优点为
的优点为②实验开始时,先打开
③盛装NH4HCO3溶液的仪器名称为
(3)测定氧钒(Ⅳ)碱式碳酸铵晶体粗产品的纯度。
实验步骤:粗产品wg
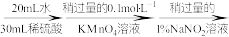
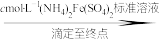 再重复实验两次。
再重复实验两次。已知:
 。
。①滴入NaNO2溶液的目的是除去KMnO4,写出其反应的离子方程式:
②若平均消耗cmol/L(NH4)2Fe(SO4)2标准溶液的体积为amL,则氧钒(Ⅳ)碱式碳酸铵晶体粗产品的纯度为
 。
。③若其他操作均正确,但NaNO2的加入量不足,会引起测定结果
您最近一年使用:0次
2024-05-08更新
|
218次组卷
|
2卷引用:湖南省衡阳市祁东县2024届高三第三次联考(三模)化学试题
名校
4 . 锌是一种重要的金属,锌及其化合物被广泛应用于汽车、建筑、船舶、电池等行业。现某科研小组以固体废锌催化剂(主要成分是 ,含少量
,含少量 、
、 、
、 、
、 等杂质)为原料制备锌的工艺流程如图所示:
等杂质)为原料制备锌的工艺流程如图所示: 和
和 转化为
转化为 、
、 进入溶液。
进入溶液。
②25℃时,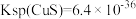 ,
,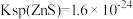
③深度除杂标准:溶液中 ≤2.0×10-6
≤2.0×10-6
(1)“浸取”温度为30℃,锌的浸出率可达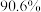 ,继续升温浸出率反而下降,其原因为
,继续升温浸出率反而下降,其原因为___________ 。
(2)“滤渣1”的主要成分为 、
、___________ 。
(3)“深度除锰”是将残留的 转化为
转化为 ,写出该过程的离子方程式
,写出该过程的离子方程式___________ 。
(4)“深度除铜”时,锌的最终回收率,除铜效果(用反应后溶液中的铜锌比 表示)与
表示)与 加入量的关系曲线如图所示。
加入量的关系曲线如图所示。 加入量最优选择
加入量最优选择___________ (填标号)
A.100% B.110% C.120% D.130%
②由图可知,当 达到一定量的时候,锌的最终回收率下降的原因是
达到一定量的时候,锌的最终回收率下降的原因是___________ (用离子方程式解释)。
(5) 原子能形成多种配位化合物,一种锌的配合物结构如图:
原子能形成多种配位化合物,一种锌的配合物结构如图:___________ 。
②键角③___________ 120°(填“<”或“=”)。
 ,含少量
,含少量 、
、 、
、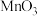 、
、 等杂质)为原料制备锌的工艺流程如图所示:
等杂质)为原料制备锌的工艺流程如图所示: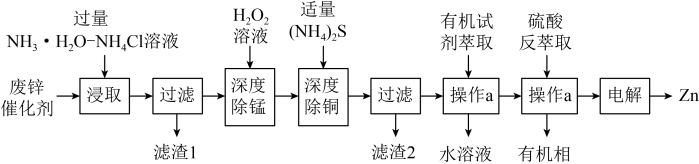
 和
和 转化为
转化为 、
、 进入溶液。
进入溶液。②25℃时,
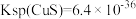 ,
,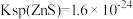
③深度除杂标准:溶液中
 ≤2.0×10-6
≤2.0×10-6(1)“浸取”温度为30℃,锌的浸出率可达
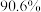 ,继续升温浸出率反而下降,其原因为
,继续升温浸出率反而下降,其原因为(2)“滤渣1”的主要成分为
 、
、(3)“深度除锰”是将残留的
 转化为
转化为 ,写出该过程的离子方程式
,写出该过程的离子方程式(4)“深度除铜”时,锌的最终回收率,除铜效果(用反应后溶液中的铜锌比
 表示)与
表示)与 加入量的关系曲线如图所示。
加入量的关系曲线如图所示。
 加入量最优选择
加入量最优选择A.100% B.110% C.120% D.130%
②由图可知,当
 达到一定量的时候,锌的最终回收率下降的原因是
达到一定量的时候,锌的最终回收率下降的原因是(5)
 原子能形成多种配位化合物,一种锌的配合物结构如图:
原子能形成多种配位化合物,一种锌的配合物结构如图: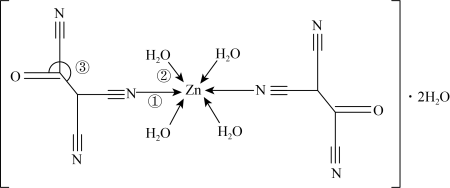
②键角③
您最近一年使用:0次
解题方法
5 . 某煤矸石经化学成分分析可知,其含有大量的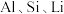 元素,还含有少量
元素,还含有少量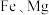 等杂质。下图为硝酸浸出铝、铁、锂等工业流程。按要求回答下列问题:
等杂质。下图为硝酸浸出铝、铁、锂等工业流程。按要求回答下列问题: 的操作是
的操作是______ 。
(2)富铁渣中的主要成分是______ (填化学式)。
(3)低温热解过程中有红棕色气体放出,则铝盐发生反应的化学方程式为______ (假设热解过程中只有一种含氮化合物生成);此时热解温度不宜过高的原因是______ 。
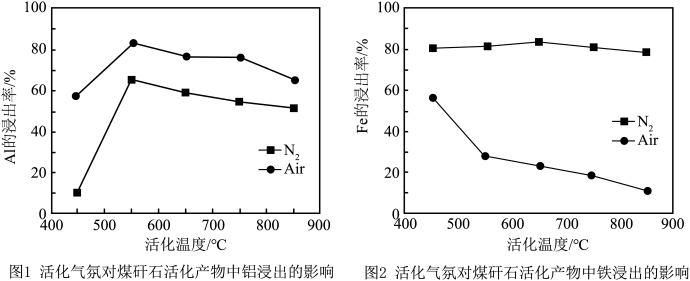
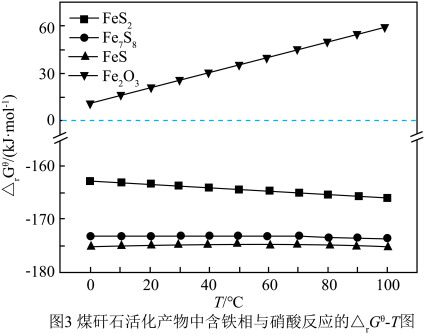
(4)热活化过程可在氮气或空气气氛中进行,其活化气氛在不同温度下对铝(图1)、铁(图2)浸出的影响,以及铁的活化产物与硝酸反应的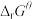 与温度的关系(图3)如下图所示。则热活化过程所选用的合适的条件是
与温度的关系(图3)如下图所示。则热活化过程所选用的合适的条件是______ (填标号)。
A. 气氛、
气氛、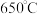 B.空气气氛、
B.空气气氛、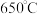 C.
C. 气氛、
气氛、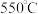 D.空气气氛、
D.空气气氛、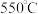
空气气氛中温度越高,铁的浸出率越小的原因可能是______ 。 )和碳酸酯类有机溶剂组成,充电过程中,石墨
)和碳酸酯类有机溶剂组成,充电过程中,石墨 电极发生阴离子插层反应得
电极发生阴离子插层反应得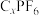 。则碳酸酯类为
。则碳酸酯类为______ (填“极性”或“非极性”)溶剂,放电时,正极发生的电极反应方程式为______ 。
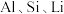 元素,还含有少量
元素,还含有少量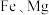 等杂质。下图为硝酸浸出铝、铁、锂等工业流程。按要求回答下列问题:
等杂质。下图为硝酸浸出铝、铁、锂等工业流程。按要求回答下列问题: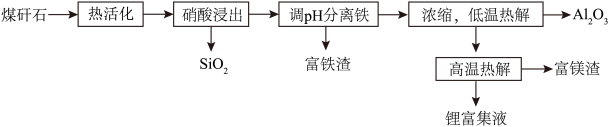
 的操作是
的操作是(2)富铁渣中的主要成分是
(3)低温热解过程中有红棕色气体放出,则铝盐发生反应的化学方程式为
(4)热活化过程可在氮气或空气气氛中进行,其活化气氛在不同温度下对铝(图1)、铁(图2)浸出的影响,以及铁的活化产物与硝酸反应的
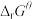 与温度的关系(图3)如下图所示。则热活化过程所选用的合适的条件是
与温度的关系(图3)如下图所示。则热活化过程所选用的合适的条件是A.
 气氛、
气氛、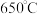 B.空气气氛、
B.空气气氛、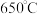 C.
C. 气氛、
气氛、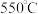 D.空气气氛、
D.空气气氛、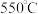
空气气氛中温度越高,铁的浸出率越小的原因可能是
 )和碳酸酯类有机溶剂组成,充电过程中,石墨
)和碳酸酯类有机溶剂组成,充电过程中,石墨 电极发生阴离子插层反应得
电极发生阴离子插层反应得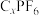 。则碳酸酯类为
。则碳酸酯类为
您最近一年使用:0次
名校
解题方法
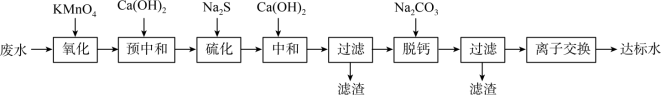
6 . 湿法炼锌的工业废水中主要阳离子有Zn2+、H+、Tl+、Tl3+,废水除铊的工艺流程如图。 能够在pH为0~14的范围内以离子态稳定存在,不易与
能够在pH为0~14的范围内以离子态稳定存在,不易与 形成沉淀。
形成沉淀。
②部分物质的 如表:
如表:
③排放标准:Tl的含量低于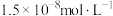 。
。
回答下列问题:
(1)Tl的原子序数为81,在元素周期表中的位置为___________ ,价电子排布式为___________ 。
(2)已知“氧化”步骤中 被还原为
被还原为 ,请写出该反应的离子方程式:
,请写出该反应的离子方程式:___________ ,反应后仍存在少量的 。
。
(3)“预中和”步骤中加入 至溶液的pH约为7,可减少“硫化”步骤中
至溶液的pH约为7,可减少“硫化”步骤中 的使用量,还能减少
的使用量,还能减少___________ (填化学式)污染物的生成。
(4)“硫化”步骤的主要目的是除去___________ (填离子符号)。
(5)在“中和”步骤中,若要使溶液中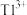 的含量低于排放标准,请根据
的含量低于排放标准,请根据 计算溶液的pH应大于
计算溶液的pH应大于___________ 。
(6)“离子交换”步骤中可用普鲁士蓝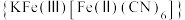 (其摩尔质量为
(其摩尔质量为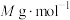 )中的
)中的 与残余铊离子进行离子交换,进一步实现废水中铊的去除。普鲁士蓝晶胞的如下[
与残余铊离子进行离子交换,进一步实现废水中铊的去除。普鲁士蓝晶胞的如下[ 未标出,其占据四个互不相邻的小立方体(晶胞的部分)的体心]。若该晶体的密度为
未标出,其占据四个互不相邻的小立方体(晶胞的部分)的体心]。若该晶体的密度为 ,则
,则 和
和 的最短距离为
的最短距离为___________ cm(设 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
 能够在pH为0~14的范围内以离子态稳定存在,不易与
能够在pH为0~14的范围内以离子态稳定存在,不易与 形成沉淀。
形成沉淀。②部分物质的
 如表:
如表:| 物质 |  | 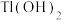 | ZnS |  |
 | 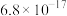 |  |  |  |
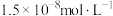 。
。回答下列问题:
(1)Tl的原子序数为81,在元素周期表中的位置为
(2)已知“氧化”步骤中
 被还原为
被还原为 ,请写出该反应的离子方程式:
,请写出该反应的离子方程式: 。
。(3)“预中和”步骤中加入
 至溶液的pH约为7,可减少“硫化”步骤中
至溶液的pH约为7,可减少“硫化”步骤中 的使用量,还能减少
的使用量,还能减少(4)“硫化”步骤的主要目的是除去
(5)在“中和”步骤中,若要使溶液中
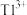 的含量低于排放标准,请根据
的含量低于排放标准,请根据 计算溶液的pH应大于
计算溶液的pH应大于(6)“离子交换”步骤中可用普鲁士蓝
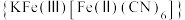 (其摩尔质量为
(其摩尔质量为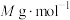 )中的
)中的 与残余铊离子进行离子交换,进一步实现废水中铊的去除。普鲁士蓝晶胞的如下[
与残余铊离子进行离子交换,进一步实现废水中铊的去除。普鲁士蓝晶胞的如下[ 未标出,其占据四个互不相邻的小立方体(晶胞的部分)的体心]。若该晶体的密度为
未标出,其占据四个互不相邻的小立方体(晶胞的部分)的体心]。若该晶体的密度为 ,则
,则 和
和 的最短距离为
的最短距离为 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。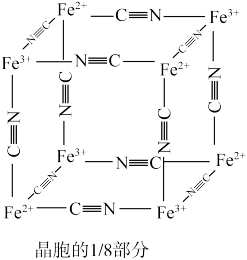
您最近一年使用:0次
解题方法
7 . 碲、锑广泛应用光伏、半导体领域。某科研小组从阳极泥分铜液净化渣[主要含铜、碲(Te)、锑(Sb)等元素的化合物]分别回收碲和锑的工艺流程如下图所示: 浸渣。
浸渣。
②“碱浸”时,铜、锑转化为难溶氢氧化物或氧化物,碱浸液含有 。
。
回答下列问题:
(1)基态Sb原子的价层电子排布式为___________ 。
(2)“碱浸”时,二氧化碲与碱溶液反应的离子方程式为___________ 。
(3)“氯盐酸浸”时,通入 的目的是
的目的是___________ ;“氯盐酸浸”时温度过高会使Sb的浸出率降低,原因是___________ 。
(4)向“碱浸液”中加双氧水需分批加入,目的是___________ 。
(5)写出“热还原”时发生反应的化学方程式___________ 。
(6)粗碲粉中碲质量分数的测定:取3.2g粗碲粉,加入硝酸使其转化为亚碲酸(H2TeO3),将溶液置于冰盐冷剂中冷却至273K过滤、冰水洗涤等得到亚碲酸。将亚碲酸配制成250mL溶液,取25.00mL于锥形瓶中。向锥形瓶中加入20.00mL0.04mol·L-1酸性K2Cr2O7溶液,充分反应使亚碲酸转化为原碲酸(H6TeO6)。用0.03mol·L-1硫酸亚铁铵[ (NH4)2 Fe(SO4)2 ]标准溶液滴定剩余的酸性K2Cr2O7溶液,滴定至终点时消耗20.00mL硫酸亚铁铵标准溶液。则粗碲粉中碲的质量分数为___________ ;如滴定前滴定管尖嘴部分有气泡,滴定后气泡消失,则测定结果___________ (填“偏高”、“偏低”或“无影响”)。

 浸渣。
浸渣。②“碱浸”时,铜、锑转化为难溶氢氧化物或氧化物,碱浸液含有
 。
。回答下列问题:
(1)基态Sb原子的价层电子排布式为
(2)“碱浸”时,二氧化碲与碱溶液反应的离子方程式为
(3)“氯盐酸浸”时,通入
 的目的是
的目的是(4)向“碱浸液”中加双氧水需分批加入,目的是
(5)写出“热还原”时发生反应的化学方程式
(6)粗碲粉中碲质量分数的测定:取3.2g粗碲粉,加入硝酸使其转化为亚碲酸(H2TeO3),将溶液置于冰盐冷剂中冷却至273K过滤、冰水洗涤等得到亚碲酸。将亚碲酸配制成250mL溶液,取25.00mL于锥形瓶中。向锥形瓶中加入20.00mL0.04mol·L-1酸性K2Cr2O7溶液,充分反应使亚碲酸转化为原碲酸(H6TeO6)。用0.03mol·L-1硫酸亚铁铵[ (NH4)2 Fe(SO4)2 ]标准溶液滴定剩余的酸性K2Cr2O7溶液,滴定至终点时消耗20.00mL硫酸亚铁铵标准溶液。则粗碲粉中碲的质量分数为
您最近一年使用:0次
8 . 湿法炼锌具有能耗低,生成产品纯度高等特点,其主要原料为锌精矿(主要成分为硫化锌,还含有铁、钴、铜、镉、铅等元素的杂质),获得较纯锌锭的工艺流程如图: 、
、 、CdO。
、CdO。
(1)铜原子的价层电子排布图为___________ 。
(2)“酸浸”中滤渣主要成分为___________ 。
(3)“一段沉积”和“二段沉积”刚开始加入锌粉时,反应速率较小,然后反应速率显著增大,请解释产生此现象的原因:___________ 。
(4)写出“赤铁矿除铁”过程中反应的离子方程式:___________ 。
(5)“ —萘酚净化除钴”先是
—萘酚净化除钴”先是 把
把 氧化成
氧化成 ,并生成NO,
,并生成NO, 与有机物发生化学反应生成红褐色稳定鳌合物沉淀。写出
与有机物发生化学反应生成红褐色稳定鳌合物沉淀。写出 被氧化的离子方程式:
被氧化的离子方程式:___________ 。
(6)“电解”工艺中,电解液常有较高浓度的 会腐蚀阳极而增大电解能耗。可向溶液中同时加入Cu和
会腐蚀阳极而增大电解能耗。可向溶液中同时加入Cu和 ,生成CuCl沉淀从而除去
,生成CuCl沉淀从而除去 。已知:
。已知: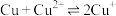
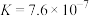 ;
;
 。请通过具体数据说明上述的反应能完全进行的原因:
。请通过具体数据说明上述的反应能完全进行的原因:___________ 。
(7)纯净的硫化锌是半导体锂离子电池负极材料。在充电过程中,发生合金化反应生成LiZn(合金相),同时负极材料晶胞的组成变化如图所示。 的电极方程式为
的电极方程式为___________ (x和y用具体数字表示)。
②若 的晶胞参数为a nm,则EF间的距离为
的晶胞参数为a nm,则EF间的距离为___________ nm。

 、
、 、CdO。
、CdO。(1)铜原子的价层电子排布图为
(2)“酸浸”中滤渣主要成分为
(3)“一段沉积”和“二段沉积”刚开始加入锌粉时,反应速率较小,然后反应速率显著增大,请解释产生此现象的原因:
(4)写出“赤铁矿除铁”过程中反应的离子方程式:
(5)“
 —萘酚净化除钴”先是
—萘酚净化除钴”先是 把
把 氧化成
氧化成 ,并生成NO,
,并生成NO, 与有机物发生化学反应生成红褐色稳定鳌合物沉淀。写出
与有机物发生化学反应生成红褐色稳定鳌合物沉淀。写出 被氧化的离子方程式:
被氧化的离子方程式:(6)“电解”工艺中,电解液常有较高浓度的
 会腐蚀阳极而增大电解能耗。可向溶液中同时加入Cu和
会腐蚀阳极而增大电解能耗。可向溶液中同时加入Cu和 ,生成CuCl沉淀从而除去
,生成CuCl沉淀从而除去 。已知:
。已知: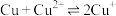
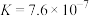 ;
;
 。请通过具体数据说明上述的反应能完全进行的原因:
。请通过具体数据说明上述的反应能完全进行的原因:(7)纯净的硫化锌是半导体锂离子电池负极材料。在充电过程中,发生合金化反应生成LiZn(合金相),同时负极材料晶胞的组成变化如图所示。
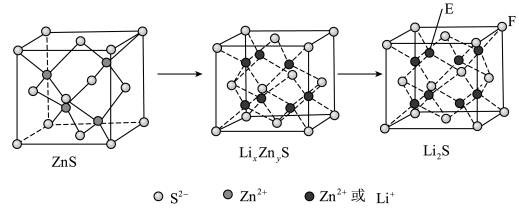
 的电极方程式为
的电极方程式为②若
 的晶胞参数为a nm,则EF间的距离为
的晶胞参数为a nm,则EF间的距离为
您最近一年使用:0次
9 . 高锰酸钾在工业中广泛用作氧化剂。以软锰矿(主要成分是 ,含有
,含有 和
和 等杂质)为原料制备高锰酸钾的工艺流程如图所示:
等杂质)为原料制备高锰酸钾的工艺流程如图所示:
①“焙烧”中有 生成。
生成。
②20℃时各物质的溶解度如下表。
下列说法错误的是
 ,含有
,含有 和
和 等杂质)为原料制备高锰酸钾的工艺流程如图所示:
等杂质)为原料制备高锰酸钾的工艺流程如图所示: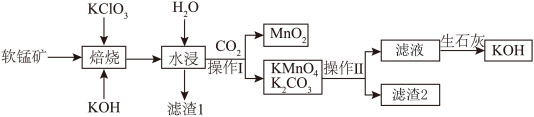
①“焙烧”中有
 生成。
生成。②20℃时各物质的溶解度如下表。
| 物质 |  |  |  |
| 溶解度/g | 6.38 | 111 | 11.1 |
A.“焙烧”时,主要反应的化学方程式为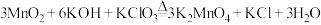 |
B.操作Ⅰ,若通入4mol  时,理论上转移电子数为2 时,理论上转移电子数为2 |
C.“焙烧”时加入的KOH应适量,否则制得的 中混有含Si元素的杂质 中混有含Si元素的杂质 |
D.操作Ⅱ为蒸发浓缩、冷却结晶、过滤,滤渣2的主要成分为 |
您最近一年使用:0次
10 . 联氨 是一种绿色环保还原剂,为二元弱碱,在水中的电离方程式与氨相似,可用于处理锅炉水中的溶解氧,防止锅炉被腐蚀,下列说法错误的是
是一种绿色环保还原剂,为二元弱碱,在水中的电离方程式与氨相似,可用于处理锅炉水中的溶解氧,防止锅炉被腐蚀,下列说法错误的是
 是一种绿色环保还原剂,为二元弱碱,在水中的电离方程式与氨相似,可用于处理锅炉水中的溶解氧,防止锅炉被腐蚀,下列说法错误的是
是一种绿色环保还原剂,为二元弱碱,在水中的电离方程式与氨相似,可用于处理锅炉水中的溶解氧,防止锅炉被腐蚀,下列说法错误的是A.向装有少量 的试管中加入联氨溶液,可观察到固体逐渐变黑,发生的反应为 的试管中加入联氨溶液,可观察到固体逐渐变黑,发生的反应为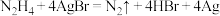 |
B.碱性: |
C.理论上1mol 可处理水中1mol 可处理水中1mol |
D. 是极性分子 是极性分子 |
您最近一年使用:0次



