解题方法
1 . 海水中蕴藏着大量资源,利用海水可提取溴和镁,主要工业生产流程如下图所示:
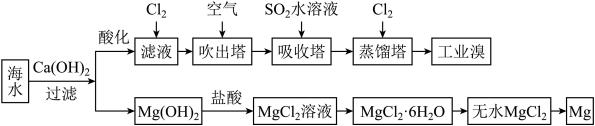
请回答下列问题。
(1)吸收塔中发生的主要反应的离子方程式为___________ 。
(2)提取溴的过程中,经过两次 的转化,其目的是
的转化,其目的是___________ 。
(3)吹出塔吹出的含溴空气经由吸收塔吸收溴后回到吹出塔进行循环利用。吹出塔中 吹出率与吸收塔中
吹出率与吸收塔中 流量的关系如图所示。
流量的关系如图所示。
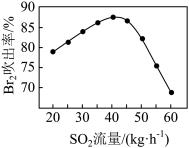
 流量过大,
流量过大, 吹出率反而下降的原因是
吹出率反而下降的原因是___________ 。
(4)工业上也可用 溶液吸收吹出的
溶液吸收吹出的 ,将以下方程式补充完整。
,将以下方程式补充完整。________
___________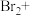 ___________
___________ ___________
___________ __________
__________
 ___________
___________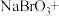 ___________
___________
(5)从 溶液中得到
溶液中得到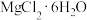 晶体的主要操作为
晶体的主要操作为___________ 、___________ 、过滤、洗涤、干燥(在HCl气流的保护下)。
(6)工业上用无水氯化镁得到金属镁的冶炼方法为___________ 。
(7)请写出上述过程中可以循环利用的一种物质___________ 。(写出化学式)。

请回答下列问题。
(1)吸收塔中发生的主要反应的离子方程式为
(2)提取溴的过程中,经过两次
 的转化,其目的是
的转化,其目的是(3)吹出塔吹出的含溴空气经由吸收塔吸收溴后回到吹出塔进行循环利用。吹出塔中
 吹出率与吸收塔中
吹出率与吸收塔中 流量的关系如图所示。
流量的关系如图所示。
 流量过大,
流量过大, 吹出率反而下降的原因是
吹出率反而下降的原因是(4)工业上也可用
 溶液吸收吹出的
溶液吸收吹出的 ,将以下方程式补充完整。
,将以下方程式补充完整。___________
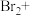 ___________
___________ ___________
___________ __________
__________
 ___________
___________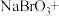 ___________
___________
(5)从
 溶液中得到
溶液中得到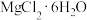 晶体的主要操作为
晶体的主要操作为(6)工业上用无水氯化镁得到金属镁的冶炼方法为
(7)请写出上述过程中可以循环利用的一种物质
您最近一年使用:0次
解题方法
2 . 为治理雾霾天气,可采用多种方法实现工业废气脱硫。
Ⅰ.软锰矿浆(主要成分 ,含有少量铁、铝等氧化物)可脱除燃煤烟气中的
,含有少量铁、铝等氧化物)可脱除燃煤烟气中的 ,又可制得电池材料
,又可制得电池材料 。主要流程如图:
。主要流程如图:
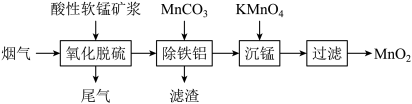
(1)提高烟气吸收效率的可行措施有___________ (写出两点)。
(2)写出“沉锰”步骤发生反应的离子方程式:___________ 。
(3)现将该烟气以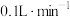 的流量通入到装有
的流量通入到装有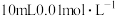 的
的 溶液的装置中,
溶液的装置中, 后,
后, 恰好完全反应。计算该烟气中
恰好完全反应。计算该烟气中 含量:
含量:___________  。
。
II.活性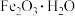 是一种固体脱硫剂(无水
是一种固体脱硫剂(无水 无脱硫作用),其原理是将废气中的含硫化合物化学吸附到脱硫剂的孔隙中,发生反应改变其化学组成。利用活性
无脱硫作用),其原理是将废气中的含硫化合物化学吸附到脱硫剂的孔隙中,发生反应改变其化学组成。利用活性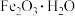 脱除沼气中的
脱除沼气中的 可转化成
可转化成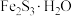 。
。
(4)“脱除沼气中 ”反应的化学方程式为
”反应的化学方程式为___________ 。
(5)工业上要求脱除过程温度不能超过 ,原因是
,原因是___________ 。
Ⅲ.有人设想利用电化学原理除去 ,并将化学能转化为电能。装置图如下。
,并将化学能转化为电能。装置图如下。
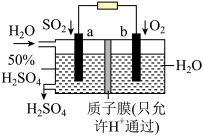
(6)电池的正极是___________ 。(填“a”或“b”)
(7)写出a电极的电极反应___________ 。
Ⅰ.软锰矿浆(主要成分
 ,含有少量铁、铝等氧化物)可脱除燃煤烟气中的
,含有少量铁、铝等氧化物)可脱除燃煤烟气中的 ,又可制得电池材料
,又可制得电池材料 。主要流程如图:
。主要流程如图:
(1)提高烟气吸收效率的可行措施有
(2)写出“沉锰”步骤发生反应的离子方程式:
(3)现将该烟气以
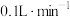 的流量通入到装有
的流量通入到装有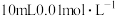 的
的 溶液的装置中,
溶液的装置中, 后,
后, 恰好完全反应。计算该烟气中
恰好完全反应。计算该烟气中 含量:
含量: 。
。II.活性
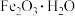 是一种固体脱硫剂(无水
是一种固体脱硫剂(无水 无脱硫作用),其原理是将废气中的含硫化合物化学吸附到脱硫剂的孔隙中,发生反应改变其化学组成。利用活性
无脱硫作用),其原理是将废气中的含硫化合物化学吸附到脱硫剂的孔隙中,发生反应改变其化学组成。利用活性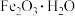 脱除沼气中的
脱除沼气中的 可转化成
可转化成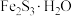 。
。(4)“脱除沼气中
 ”反应的化学方程式为
”反应的化学方程式为(5)工业上要求脱除过程温度不能超过
 ,原因是
,原因是Ⅲ.有人设想利用电化学原理除去
 ,并将化学能转化为电能。装置图如下。
,并将化学能转化为电能。装置图如下。
(6)电池的正极是
(7)写出a电极的电极反应
您最近一年使用:0次
2023-07-13更新
|
418次组卷
|
2卷引用:辽宁省五校(大连二十四中、东北育才等)2022-2023学年高一下学期期末考试化学试题
解题方法
3 . 某含镁废弃物中主要含有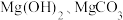 ,还含有少量的
,还含有少量的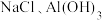 、
、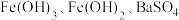 ,以该固体废弃物为原料制备
,以该固体废弃物为原料制备 的流程如下:
的流程如下:

已知:部分离子开始沉淀和完全沉淀的
回答下列问题:
(1)滤渣1的主要成分为_______ (填化学式),其阴离子空间构型为_______ 。
(2)“酸浸”时,发生反应的基本反应类型均为_______ ,所使用的稀盐酸的质量浓度为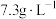 ,则其物质的量浓度为
,则其物质的量浓度为_______  。
。
(3)“氧化”时,反应的离子方程式为_______ 。
(4)“调 ”时,
”时, 的调节范围为
的调节范围为_______ (滤渣2中有两种氢氧化物)。
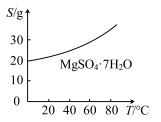
(5)已知 的溶解度曲线如图所示。“操作”应包括
的溶解度曲线如图所示。“操作”应包括_______ 、过滤、洗涤、干燥。
(6)若测定 晶体中结晶水的含量,下列仪器一定不需要的是_______(填字母)。
晶体中结晶水的含量,下列仪器一定不需要的是_______(填字母)。
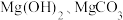 ,还含有少量的
,还含有少量的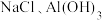 、
、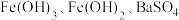 ,以该固体废弃物为原料制备
,以该固体废弃物为原料制备 的流程如下:
的流程如下:
已知:部分离子开始沉淀和完全沉淀的

| 氢氧化物 |  |  |  |
开始沉淀时的 | 4.0 | 8.4 | 1.9 |
完全沉淀时的 | 5.2 | 11.2 | 3.2 |
(1)滤渣1的主要成分为
(2)“酸浸”时,发生反应的基本反应类型均为
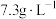 ,则其物质的量浓度为
,则其物质的量浓度为 。
。(3)“氧化”时,反应的离子方程式为
(4)“调
 ”时,
”时, 的调节范围为
的调节范围为(5)已知
 的溶解度曲线如图所示。“操作”应包括
的溶解度曲线如图所示。“操作”应包括
(6)若测定
 晶体中结晶水的含量,下列仪器一定不需要的是_______(填字母)。
晶体中结晶水的含量,下列仪器一定不需要的是_______(填字母)。| A | B | C | D |
 |  |  |  |
| 天平 | 坩埚 | 马弗炉(一种加热设备) | 分液漏斗 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-07-12更新
|
106次组卷
|
2卷引用:辽宁省朝阳市2022-2023学年高二下学期期末联考化学试题
解题方法
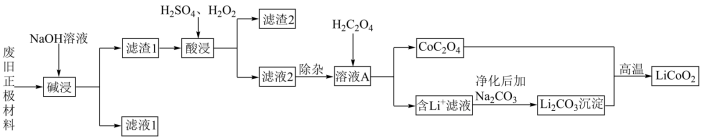
4 . 废旧锂离子电池材料的回收再生意义重大。一种回收废旧锂离子电池正极材料[含有钴酸锂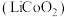 、石墨、铝箔及少量其它杂质]中钴酸锂的工艺流程如下图所示:
、石墨、铝箔及少量其它杂质]中钴酸锂的工艺流程如下图所示:
已知:常温下①草酸 的电离常数
的电离常数 ,
, ;
;
②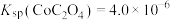 。
。
请回答下列问题:
(1)基态Co原子价层电子的轨道表示式为_______ 。
(2)为提高“碱浸”效率可采取的措施有_______ (任写一条)。
(3)“滤渣2”的主要成分为_______ 。
(4)“酸浸”中发生反应的离子方程式为_______ 。
(5)相同条件下,“酸浸”时钴的浸出率随温度变化如表所示,请解释温度高于80℃,钴的浸出率降低的原因是_______ 。
(6)常温下,溶液A中加入 产生
产生 沉淀:
沉淀: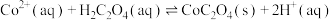 ,该反应的化学平衡常数
,该反应的化学平衡常数
_______ 。
(7)在空气中, 与
与 高温下生成
高温下生成 的化学方程式为
的化学方程式为_______ 。
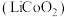 、石墨、铝箔及少量其它杂质]中钴酸锂的工艺流程如下图所示:
、石墨、铝箔及少量其它杂质]中钴酸锂的工艺流程如下图所示:
已知:常温下①草酸
 的电离常数
的电离常数 ,
, ;
;②
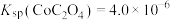 。
。请回答下列问题:
(1)基态Co原子价层电子的轨道表示式为
(2)为提高“碱浸”效率可采取的措施有
(3)“滤渣2”的主要成分为
(4)“酸浸”中发生反应的离子方程式为
(5)相同条件下,“酸浸”时钴的浸出率随温度变化如表所示,请解释温度高于80℃,钴的浸出率降低的原因是
| 反应温度/℃ | 60 | 70 | 80 | 90 |
| 钴的浸出率/% | 88 | 90.5 | 93 | 89 |
(6)常温下,溶液A中加入
 产生
产生 沉淀:
沉淀: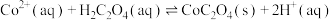 ,该反应的化学平衡常数
,该反应的化学平衡常数
(7)在空气中,
 与
与 高温下生成
高温下生成 的化学方程式为
的化学方程式为
您最近一年使用:0次
解题方法
5 . I.A、B、C、D、E为中学常见化学物质,它们之间可发生如图所示的转化,反应条件和部分产物已略去。其中A、C、E含有同一种元素X;A、D是常见金属单质,B是一种黄绿色气体。
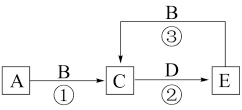
(1)物质B的化学式为_______ ;物质C中元素X的价态为_______ 。
(2)反应②可用于蚀刻铜电路板,其化学方程式为_______ 。
II.高铁酸钠是钠的六价铁酸盐,化学式为 ,具有强烈的氧化和絮凝作用,对水的消毒和净化过程中,不会产生对人体有害的物质,因此可以作为绿色消毒剂。某实验小组设计如图所示装置制备
,具有强烈的氧化和絮凝作用,对水的消毒和净化过程中,不会产生对人体有害的物质,因此可以作为绿色消毒剂。某实验小组设计如图所示装置制备 ,根据所学知识回答下列问题:
,根据所学知识回答下列问题:
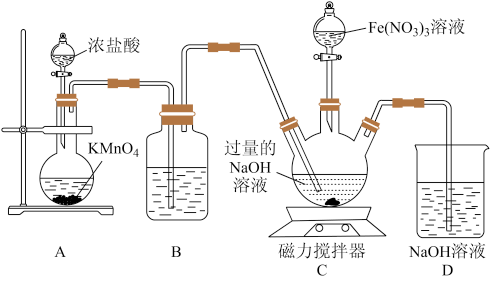
(3)装置A中,盛装浓盐酸的仪器名称为_______ ;若不考虑本实验条件限制,制备 时还可以将
时还可以将 替换为
替换为_______ (写出一种即可)。
(4)装置B中盛装液体的作用为_______ 。
(5)先向装置C的三颈烧瓶中通入一段时间 制备
制备 ,再滴加
,再滴加 溶液制备
溶液制备 ,则生成
,则生成 时发生反应的离子方程式为
时发生反应的离子方程式为_______ 。

(1)物质B的化学式为
(2)反应②可用于蚀刻铜电路板,其化学方程式为
II.高铁酸钠是钠的六价铁酸盐,化学式为
 ,具有强烈的氧化和絮凝作用,对水的消毒和净化过程中,不会产生对人体有害的物质,因此可以作为绿色消毒剂。某实验小组设计如图所示装置制备
,具有强烈的氧化和絮凝作用,对水的消毒和净化过程中,不会产生对人体有害的物质,因此可以作为绿色消毒剂。某实验小组设计如图所示装置制备 ,根据所学知识回答下列问题:
,根据所学知识回答下列问题:
(3)装置A中,盛装浓盐酸的仪器名称为
 时还可以将
时还可以将 替换为
替换为(4)装置B中盛装液体的作用为
(5)先向装置C的三颈烧瓶中通入一段时间
 制备
制备 ,再滴加
,再滴加 溶液制备
溶液制备 ,则生成
,则生成 时发生反应的离子方程式为
时发生反应的离子方程式为
您最近一年使用:0次
解题方法
6 . 纳米 是一种用途广泛的光电材料,工业上可以以氯化铁溶液腐蚀铜电路板废液(以下称“腐蚀液”,主要含
是一种用途广泛的光电材料,工业上可以以氯化铁溶液腐蚀铜电路板废液(以下称“腐蚀液”,主要含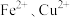 )为原料制备,实现变废为宝,路线如下:
)为原料制备,实现变废为宝,路线如下:
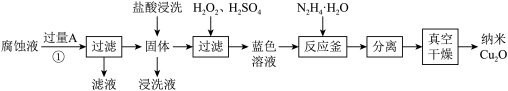
已知:a.当温度为60℃时,过氧化氢分解率为50%左右;
b. 中的
中的 元素为
元素为 价。
价。
请回答下列问题
(1)流程中的 为
为_______ (填化学式),①发生的反应的离子方程式为_______ ;
(2)“氧化”步骤为了加快反应速率可以适当升温,但不宜加热温度过高,原因是_______ ;
(3)为验证“反应釜”中反应已发生,可采用的实验操作是_______ ,从反应体系中分离出分散质_______ (填“能”或“不能”)选择过滤操作,理由是_______ ;
(4)发生反应时,“反应釜”中获得一种气体为空气主要成分,写出其中发生反应的离子方程式,并用单线桥法表示电子转移情况_______ ;
 是一种用途广泛的光电材料,工业上可以以氯化铁溶液腐蚀铜电路板废液(以下称“腐蚀液”,主要含
是一种用途广泛的光电材料,工业上可以以氯化铁溶液腐蚀铜电路板废液(以下称“腐蚀液”,主要含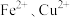 )为原料制备,实现变废为宝,路线如下:
)为原料制备,实现变废为宝,路线如下:
已知:a.当温度为60℃时,过氧化氢分解率为50%左右;
b.
 中的
中的 元素为
元素为 价。
价。请回答下列问题
(1)流程中的
 为
为(2)“氧化”步骤为了加快反应速率可以适当升温,但不宜加热温度过高,原因是
(3)为验证“反应釜”中反应已发生,可采用的实验操作是
(4)发生反应时,“反应釜”中获得一种气体为空气主要成分,写出其中发生反应的离子方程式,并用单线桥法表示电子转移情况
您最近一年使用:0次
7 . 某工厂采用联合焙烧法以辉铋矿(主要成分为 ,含有
,含有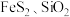 杂质)与软锰矿(主要成分为
杂质)与软锰矿(主要成分为 )为原料制备
)为原料制备 和
和 ,工艺流程如下:
,工艺流程如下:
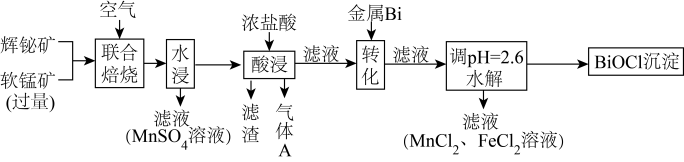
已知:①焙烧时过量的 分解为
分解为 ,
,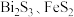 转变为
转变为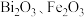 ;
;
②金属活动性: ;
;
③常温下,相关金属离子形成氢氧化物的 范围如下:
范围如下:
回答下列问题:
(1)写出“联合焙烧”时 和
和 反应生成
反应生成 的化学方程式:
的化学方程式:_______ 。
(2) 在空气中单独焙烧生成
在空气中单独焙烧生成 ,同时产生一种气体产物,若用过量的
,同时产生一种气体产物,若用过量的 溶液吸收该气体,则所得溶液的溶质为
溶液吸收该气体,则所得溶液的溶质为_______ 。
(3)“酸浸”时 转化为
转化为 ,则生成的气体A为
,则生成的气体A为_______ (填化学式)
(4)“转化”时加入金属 的目的是
的目的是_______ (用离子方程式表示)
(5)若沉淀完全时溶液中的金属离子浓度为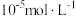 ,则由表中数据计算可得:
,则由表中数据计算可得: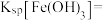
_______ 。
(6)水解生成 的离子方程式为
的离子方程式为_______ 、
(7)若取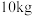 铋含量为
铋含量为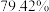 的辉铋矿,经过上述流程(铋元素在整个流程中损失率为
的辉铋矿,经过上述流程(铋元素在整个流程中损失率为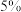 ),计算可制得
),计算可制得 固体的质量约为
固体的质量约为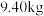 ,实测干燥的
,实测干燥的 产品产量高于计算值的原因是
产品产量高于计算值的原因是_______ 。
 ,含有
,含有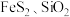 杂质)与软锰矿(主要成分为
杂质)与软锰矿(主要成分为 )为原料制备
)为原料制备 和
和 ,工艺流程如下:
,工艺流程如下:
已知:①焙烧时过量的
 分解为
分解为 ,
,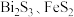 转变为
转变为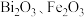 ;
;②金属活动性:
 ;
;③常温下,相关金属离子形成氢氧化物的
 范围如下:
范围如下:| 离子 | 开始沉淀 | 完全沉淀 |
 | 6.3 | 8.3 |
 | 1.6 | 3.1 |
 | 8.1 | 10.1 |
(1)写出“联合焙烧”时
 和
和 反应生成
反应生成 的化学方程式:
的化学方程式:(2)
 在空气中单独焙烧生成
在空气中单独焙烧生成 ,同时产生一种气体产物,若用过量的
,同时产生一种气体产物,若用过量的 溶液吸收该气体,则所得溶液的溶质为
溶液吸收该气体,则所得溶液的溶质为(3)“酸浸”时
 转化为
转化为 ,则生成的气体A为
,则生成的气体A为(4)“转化”时加入金属
 的目的是
的目的是(5)若沉淀完全时溶液中的金属离子浓度为
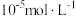 ,则由表中数据计算可得:
,则由表中数据计算可得: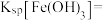
(6)水解生成
 的离子方程式为
的离子方程式为(7)若取
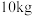 铋含量为
铋含量为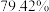 的辉铋矿,经过上述流程(铋元素在整个流程中损失率为
的辉铋矿,经过上述流程(铋元素在整个流程中损失率为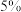 ),计算可制得
),计算可制得 固体的质量约为
固体的质量约为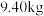 ,实测干燥的
,实测干燥的 产品产量高于计算值的原因是
产品产量高于计算值的原因是
您最近一年使用:0次
名校
解题方法
8 . 二氧化氯( )是目前国际上公认的第四代高效、无毒的广谱消毒剂,是一种黄绿色气体,易溶于水,浓度过大时易发生分解爆炸。近来有学者发现使用复合法
)是目前国际上公认的第四代高效、无毒的广谱消毒剂,是一种黄绿色气体,易溶于水,浓度过大时易发生分解爆炸。近来有学者发现使用复合法 发生器进行消毒的水中含有中等毒性的
发生器进行消毒的水中含有中等毒性的 ,进一步研究表明
,进一步研究表明 是由于
是由于 制备过程中未完全反应的
制备过程中未完全反应的 原料液进入水体引起的。实验室模拟复合法二氧化氯发生器反应工艺,探索反应温度对氯酸盐残留量的影响。
原料液进入水体引起的。实验室模拟复合法二氧化氯发生器反应工艺,探索反应温度对氯酸盐残留量的影响。
实验原理: 溶液(质量分数
溶液(质量分数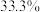 )与盐酸溶液(
)与盐酸溶液( 质量分数
质量分数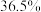 )经计量泵按
)经计量泵按 比例进入发生器连续进行反应,并在水射器的抽吸作用下,将
比例进入发生器连续进行反应,并在水射器的抽吸作用下,将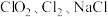 等产物和含有
等产物和含有 与盐酸的反应残液一同混合形成二氧化氯复合消毒液模拟实验装置:
与盐酸的反应残液一同混合形成二氧化氯复合消毒液模拟实验装置:
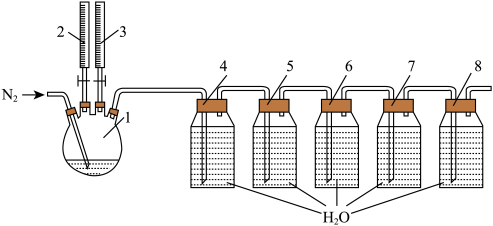
实验步骤:
i.将 溶液与盐酸溶液按
溶液与盐酸溶液按 比例加入烧瓶1中,产生黄绿色气体后通入高纯
比例加入烧瓶1中,产生黄绿色气体后通入高纯 ;
;
ⅱ.反应90分钟,将5个广口瓶内的液体和烧瓶内的反应残液一同倒入一个棕色广口瓶内,形成浓度均匀的复合二氧化氯消毒液;
iii.分别在反应温度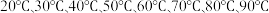 重复上述过程;
重复上述过程;
iv.测试复合二氧化氯消毒液中各组分浓度,收集整理数据。
(1)用来滴加反应液的仪器名称:_______ ;为确保实验准确性,控制反应温度,发生装置选择的加热方式:_______ 。
(2)烧瓶1中反应的化学方程式:_______ 。
(3)若已知所用盐酸的密度是 。则盐酸的浓度是:
。则盐酸的浓度是:_______ 。
(4)通入高纯 的作用:
的作用:_______ 。
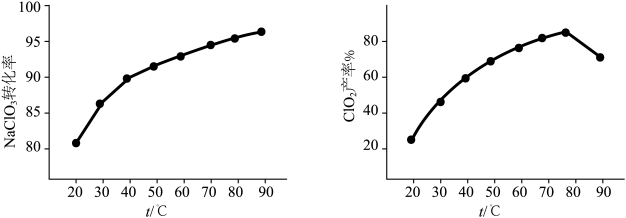
(5) 转化率及
转化率及 产率随温度的变化如下图,据图可知,随反应温度的提高,氯酸盐残留量
产率随温度的变化如下图,据图可知,随反应温度的提高,氯酸盐残留量_______ (填“升高”或“降低”):改变反应时间,重复实验, 产率随温度变化趋势均如下图所示,不考虑有副反应发生,试从装置角度分析
产率随温度变化趋势均如下图所示,不考虑有副反应发生,试从装置角度分析 时
时 产率降低的可能原因
产率降低的可能原因_______ 。
(6)二氧化氯可氧化 等金属离子,还可杀菌消毒,下列与二氧化氯杀菌消毒原理一致的是
等金属离子,还可杀菌消毒,下列与二氧化氯杀菌消毒原理一致的是_______ 。
a.含二氧化氯漱口水去除口腔异味 b.酒精消毒 c.明矾净水
 )是目前国际上公认的第四代高效、无毒的广谱消毒剂,是一种黄绿色气体,易溶于水,浓度过大时易发生分解爆炸。近来有学者发现使用复合法
)是目前国际上公认的第四代高效、无毒的广谱消毒剂,是一种黄绿色气体,易溶于水,浓度过大时易发生分解爆炸。近来有学者发现使用复合法 发生器进行消毒的水中含有中等毒性的
发生器进行消毒的水中含有中等毒性的 ,进一步研究表明
,进一步研究表明 是由于
是由于 制备过程中未完全反应的
制备过程中未完全反应的 原料液进入水体引起的。实验室模拟复合法二氧化氯发生器反应工艺,探索反应温度对氯酸盐残留量的影响。
原料液进入水体引起的。实验室模拟复合法二氧化氯发生器反应工艺,探索反应温度对氯酸盐残留量的影响。实验原理:
 溶液(质量分数
溶液(质量分数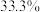 )与盐酸溶液(
)与盐酸溶液( 质量分数
质量分数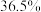 )经计量泵按
)经计量泵按 比例进入发生器连续进行反应,并在水射器的抽吸作用下,将
比例进入发生器连续进行反应,并在水射器的抽吸作用下,将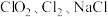 等产物和含有
等产物和含有 与盐酸的反应残液一同混合形成二氧化氯复合消毒液模拟实验装置:
与盐酸的反应残液一同混合形成二氧化氯复合消毒液模拟实验装置:
实验步骤:
i.将
 溶液与盐酸溶液按
溶液与盐酸溶液按 比例加入烧瓶1中,产生黄绿色气体后通入高纯
比例加入烧瓶1中,产生黄绿色气体后通入高纯 ;
;ⅱ.反应90分钟,将5个广口瓶内的液体和烧瓶内的反应残液一同倒入一个棕色广口瓶内,形成浓度均匀的复合二氧化氯消毒液;
iii.分别在反应温度
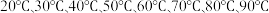 重复上述过程;
重复上述过程;iv.测试复合二氧化氯消毒液中各组分浓度,收集整理数据。
(1)用来滴加反应液的仪器名称:
(2)烧瓶1中反应的化学方程式:
(3)若已知所用盐酸的密度是
 。则盐酸的浓度是:
。则盐酸的浓度是:(4)通入高纯
 的作用:
的作用:(5)
 转化率及
转化率及 产率随温度的变化如下图,据图可知,随反应温度的提高,氯酸盐残留量
产率随温度的变化如下图,据图可知,随反应温度的提高,氯酸盐残留量 产率随温度变化趋势均如下图所示,不考虑有副反应发生,试从装置角度分析
产率随温度变化趋势均如下图所示,不考虑有副反应发生,试从装置角度分析 时
时 产率降低的可能原因
产率降低的可能原因
(6)二氧化氯可氧化
 等金属离子,还可杀菌消毒,下列与二氧化氯杀菌消毒原理一致的是
等金属离子,还可杀菌消毒,下列与二氧化氯杀菌消毒原理一致的是a.含二氧化氯漱口水去除口腔异味 b.酒精消毒 c.明矾净水
您最近一年使用:0次
名校
9 . 铁及其化合物在生产和生活中起到重要的作用。请回答下列问题:
(1)人体对 的吸收效果更好,但人体中时刻进行着
的吸收效果更好,但人体中时刻进行着 、
、 的转化。服用补铁口服剂时,配合服用维生素C会增强人体对铁的吸收效果,在此过程中维生素C的作用是起
的转化。服用补铁口服剂时,配合服用维生素C会增强人体对铁的吸收效果,在此过程中维生素C的作用是起_______ 剂。
(2)钢铁烤蓝是在钢铁表面形成一层一定厚度和强度的致密氧化膜,古代铁匠常用红热的铁浸入水中形成烤蓝,体现该反应原理的化学方程式为_______ 。
(3)实验室中储存 溶液时,为了防止其被空气中氧气氧化变质,会在溶液中加入一定量的
溶液时,为了防止其被空气中氧气氧化变质,会在溶液中加入一定量的_______ 。
(4)某小组同学欲用废铁屑(主要成分为Fe,还含有少量 )制备
)制备 。操作过程如下:
。操作过程如下:
i.用稀盐酸溶解废铁屑。
ii.在所得溶液中先加入过量氧化剂 ,再加入过量NaOH溶液,过滤,将沉淀洗涤、干燥、煅烧得
,再加入过量NaOH溶液,过滤,将沉淀洗涤、干燥、煅烧得 。
。
①步骤ii中加入过量氧化剂 的目的是
的目的是_______ 。离子方程式为_______ 。
②设计实验验证操作i所得溶液中不含 ,简述实验操作及现象:
,简述实验操作及现象:_______ 。
③该小组同学认为即使操作i所得溶液中不含 ,也不需要加入
,也不需要加入 ,若直接加入NaOH溶液可观察到的实验现象为
,若直接加入NaOH溶液可观察到的实验现象为_______ 。
(5)羟基氧化铁 是一种重要的化工原料,一种以工厂废料(含FeO、
是一种重要的化工原料,一种以工厂废料(含FeO、 、
、 、CuO)为原料生产
、CuO)为原料生产 的工艺流程如下:
的工艺流程如下:
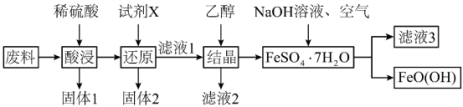
已知: 为酸性氧化物,不与硫酸等强酸反应;
为酸性氧化物,不与硫酸等强酸反应; 易溶于水,难溶于乙醇。
易溶于水,难溶于乙醇。
①“固体1”的主要成分是_______ 。
②“酸浸”时CuO与硫酸发生反应的离子方程式为_______ 。“试剂X”宜选择的是_______ 。
A.双氧水 B.铜粉 C.铁粉 D.钠块
(1)人体对
 的吸收效果更好,但人体中时刻进行着
的吸收效果更好,但人体中时刻进行着 、
、 的转化。服用补铁口服剂时,配合服用维生素C会增强人体对铁的吸收效果,在此过程中维生素C的作用是起
的转化。服用补铁口服剂时,配合服用维生素C会增强人体对铁的吸收效果,在此过程中维生素C的作用是起(2)钢铁烤蓝是在钢铁表面形成一层一定厚度和强度的致密氧化膜,古代铁匠常用红热的铁浸入水中形成烤蓝,体现该反应原理的化学方程式为
(3)实验室中储存
 溶液时,为了防止其被空气中氧气氧化变质,会在溶液中加入一定量的
溶液时,为了防止其被空气中氧气氧化变质,会在溶液中加入一定量的(4)某小组同学欲用废铁屑(主要成分为Fe,还含有少量
 )制备
)制备 。操作过程如下:
。操作过程如下:i.用稀盐酸溶解废铁屑。
ii.在所得溶液中先加入过量氧化剂
 ,再加入过量NaOH溶液,过滤,将沉淀洗涤、干燥、煅烧得
,再加入过量NaOH溶液,过滤,将沉淀洗涤、干燥、煅烧得 。
。①步骤ii中加入过量氧化剂
 的目的是
的目的是②设计实验验证操作i所得溶液中不含
 ,简述实验操作及现象:
,简述实验操作及现象:③该小组同学认为即使操作i所得溶液中不含
 ,也不需要加入
,也不需要加入 ,若直接加入NaOH溶液可观察到的实验现象为
,若直接加入NaOH溶液可观察到的实验现象为(5)羟基氧化铁
 是一种重要的化工原料,一种以工厂废料(含FeO、
是一种重要的化工原料,一种以工厂废料(含FeO、 、
、 、CuO)为原料生产
、CuO)为原料生产 的工艺流程如下:
的工艺流程如下:
已知:
 为酸性氧化物,不与硫酸等强酸反应;
为酸性氧化物,不与硫酸等强酸反应; 易溶于水,难溶于乙醇。
易溶于水,难溶于乙醇。①“固体1”的主要成分是
②“酸浸”时CuO与硫酸发生反应的离子方程式为
A.双氧水 B.铜粉 C.铁粉 D.钠块
您最近一年使用:0次
10 . 肼(N2H4),又称联氨,为无色油状液体,能很好地混溶于水中,与卤素、过氧化氢等强氧化剂作用能自燃,长期暴露在空气中或短时间受高温作用会爆炸分解,具有强烈的吸水性。实验室设计如图装置用氨和次氯酸钠反应制备肼,并探究肼的性质。
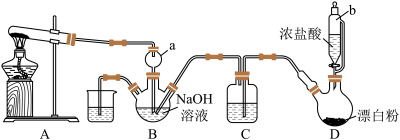
已知:硫酸肼(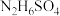 )为无色无味鳞状结晶或斜方结晶,微溶于冷水,易溶于热水。
)为无色无味鳞状结晶或斜方结晶,微溶于冷水,易溶于热水。
回答下列问题:
(1)仪器a的作用是_______ 。
(2)装置A的试管中盛放的试剂为_______ (填化学式)。
(3)装置C中盛放的试剂为_______ (填名称),其作用是_______ 。
(4)装置D中发生反应的化学方程式为_______ 。
(5)①探究性质。取装置B中溶液于试管中,加入适量稀硫酸振荡,置于冰水浴冷却,试管底部得到结晶。写出生成结晶的离子方程式:_______ 。
②测定产品中肼的质量分数。称取 g装置B中溶液,加入适量
g装置B中溶液,加入适量 固体(滴定过程中,调节溶液的
固体(滴定过程中,调节溶液的 保持在6.5左右),加水配成100
保持在6.5左右),加水配成100 溶液,移取25.00
溶液,移取25.00 置于锥形瓶中,并滴加2~3滴淀粉溶液作指示剂,用c
置于锥形瓶中,并滴加2~3滴淀粉溶液作指示剂,用c 的碘溶液滴定,滴定过程中有无色无味无毒气体产生。滴定终点的颜色变化为
的碘溶液滴定,滴定过程中有无色无味无毒气体产生。滴定终点的颜色变化为_______ ,滴定终点平均消耗标准溶液V ,产品中肼的质量分数的表达式为
,产品中肼的质量分数的表达式为_______ 。

已知:硫酸肼(
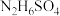 )为无色无味鳞状结晶或斜方结晶,微溶于冷水,易溶于热水。
)为无色无味鳞状结晶或斜方结晶,微溶于冷水,易溶于热水。回答下列问题:
(1)仪器a的作用是
(2)装置A的试管中盛放的试剂为
(3)装置C中盛放的试剂为
(4)装置D中发生反应的化学方程式为
(5)①探究性质。取装置B中溶液于试管中,加入适量稀硫酸振荡,置于冰水浴冷却,试管底部得到结晶。写出生成结晶的离子方程式:
②测定产品中肼的质量分数。称取
 g装置B中溶液,加入适量
g装置B中溶液,加入适量 固体(滴定过程中,调节溶液的
固体(滴定过程中,调节溶液的 保持在6.5左右),加水配成100
保持在6.5左右),加水配成100 溶液,移取25.00
溶液,移取25.00 置于锥形瓶中,并滴加2~3滴淀粉溶液作指示剂,用c
置于锥形瓶中,并滴加2~3滴淀粉溶液作指示剂,用c 的碘溶液滴定,滴定过程中有无色无味无毒气体产生。滴定终点的颜色变化为
的碘溶液滴定,滴定过程中有无色无味无毒气体产生。滴定终点的颜色变化为 ,产品中肼的质量分数的表达式为
,产品中肼的质量分数的表达式为
您最近一年使用:0次



