名校
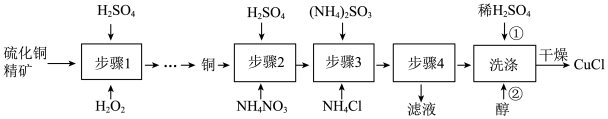
1 . 氯化亚铜(CuCl)广泛应用于冶金工业,也用作催化剂和杀菌剂。以硫化铜精矿为原料生产CuCl的工艺如图:
已知:CuCl难溶于醇和水,溶于 较大的体系
较大的体系 ,潮湿空气中易水解氧化。
,潮湿空气中易水解氧化。
(1)步骤1是“氧化酸浸”的过程,该过程生成蓝色溶液和浅黄色沉淀,化学方程式是___________ 。
(2)步骤4进行的实验操作是___________ 。
(3)洗涤过程中不能用硝酸代替硫酸进行“酸洗”,理由是___________ 。用乙醇洗涤的目的是___________ 。
(4)产品纯度测定:称取CuCl产品ag于锥形瓶中,加入足量的酸性Fe2(SO4)3溶液使其充分溶解,然后用0.1000mol/LKMnO4标准溶液滴定Fe2+,消耗KMnO4溶液bmL(本实验中 的被还原为Mn2+,不与产品中杂质和Cl﹣反应)。
的被还原为Mn2+,不与产品中杂质和Cl﹣反应)。
①CuCl溶于Fe2(SO4)3溶液的离子方程式是___________ 。
②产品中CuCl的质量分数为___________ (列计算式即可)。

已知:CuCl难溶于醇和水,溶于
 较大的体系
较大的体系 ,潮湿空气中易水解氧化。
,潮湿空气中易水解氧化。(1)步骤1是“氧化酸浸”的过程,该过程生成蓝色溶液和浅黄色沉淀,化学方程式是
(2)步骤4进行的实验操作是
(3)洗涤过程中不能用硝酸代替硫酸进行“酸洗”,理由是
(4)产品纯度测定:称取CuCl产品ag于锥形瓶中,加入足量的酸性Fe2(SO4)3溶液使其充分溶解,然后用0.1000mol/LKMnO4标准溶液滴定Fe2+,消耗KMnO4溶液bmL(本实验中
 的被还原为Mn2+,不与产品中杂质和Cl﹣反应)。
的被还原为Mn2+,不与产品中杂质和Cl﹣反应)。①CuCl溶于Fe2(SO4)3溶液的离子方程式是
②产品中CuCl的质量分数为
您最近半年使用:0次
解题方法
2 . 钠、铁、铜等金属在空气中容易变质腐蚀。下列说法错误的是
A. 很活泼,在湿润空气中久置变质为 很活泼,在湿润空气中久置变质为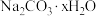 |
B. 表面包裹一层植物油可以减缓锈蚀 表面包裹一层植物油可以减缓锈蚀 |
C.生活中大量使用铝制品的原因是 常温下不与氧气反应 常温下不与氧气反应 |
D.古铜器表面生成铜绿 ,说明铜在空气中腐蚀时 ,说明铜在空气中腐蚀时 和 和 参与反应 参与反应 |
您最近半年使用:0次
3 . 燃煤火电厂产生的尾气(主要成分为 、NO)可以按如图所示流程脱除或利用。
、NO)可以按如图所示流程脱除或利用。
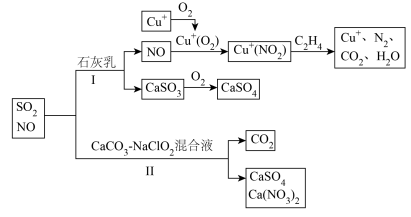
(1)写出途径Ⅰ中 转化成
转化成 的总反应化学方程式:
的总反应化学方程式:___________ 。
(2)途径Ⅰ中 的作用是
的作用是___________ ,途径Ⅰ中 的作用是
的作用是___________ 。
(3)写出途径Ⅱ中 与
与 、
、 混合液反应的化学方程式:
混合液反应的化学方程式:________ 。
(4)下列物质有可能代替途径Ⅱ中 的是______(填序号)。
的是______(填序号)。
(5)设计实验验证固体 有还原性(可供选择的试剂有:酸性
有还原性(可供选择的试剂有:酸性 溶液、
溶液、 溶液、
溶液、 溶液、
溶液、 溶液)
溶液)____ ;写出实验过程中涉及的离子反应方程式:________ 。
 、NO)可以按如图所示流程脱除或利用。
、NO)可以按如图所示流程脱除或利用。
(1)写出途径Ⅰ中
 转化成
转化成 的总反应化学方程式:
的总反应化学方程式:(2)途径Ⅰ中
 的作用是
的作用是 的作用是
的作用是(3)写出途径Ⅱ中
 与
与 、
、 混合液反应的化学方程式:
混合液反应的化学方程式:(4)下列物质有可能代替途径Ⅱ中
 的是______(填序号)。
的是______(填序号)。A. | B. | C. | D. |
(5)设计实验验证固体
 有还原性(可供选择的试剂有:酸性
有还原性(可供选择的试剂有:酸性 溶液、
溶液、 溶液、
溶液、 溶液、
溶液、 溶液)
溶液)
您最近半年使用:0次
解题方法
4 . 下列物质之间转化均要求一步完成,其中不符合 要求的是
A. | B.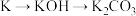 |
C.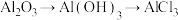 | D.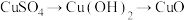 |
您最近半年使用:0次
名校
解题方法
5 . 硫酸铜是一种重要的盐,下列说法不正确 的是
| A.可用于泳池的消毒 | B.可以用来检验酒精中是否含少量水 |
| C.可以和石灰乳混合配制农药波尔多液 | D.可以通过Cu与稀硫酸反应制备 |
您最近半年使用:0次
名校
解题方法
6 . 云南省博物馆收藏的“四牛鎏金骑士铜贮贝器”,是滇青铜文明的代表性文物之一、下列有关该文物的说法正确的是


| A.青铜是合金 | B.青铜的熔点高于纯净的铜单质 |
C.表面的铜绿是 | D.在青铜器上鎏金是化学变化 |
您最近半年使用:0次
名校
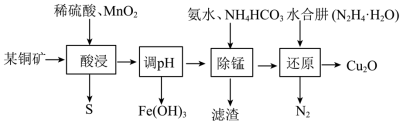
7 . 氧化亚铜主要用于制造船底防污漆(用来杀死低级海生动物)、杀虫剂,以及各种铜盐、分析试剂、红色玻璃,还用于镀铜及镀铜合金溶液的配制。用某铜矿(主要含CuS、FeO)制备Cu2O的一种工艺流程如下图:
已知:常温下,相关金属离子生成氢氧化物沉淀的pH见表:
请回答下列问题:
(1)基态Cu原子价层电子的排布图为_______ 。
(2)滤渣的主要成分是_______ (填化学式)。
(3)“酸浸”中加入MnO2的作用是_______ ;写出其中生成单质S的化学方程式_______ 。
(4)“调pH”的范围是_______ 。
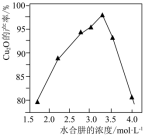
(5)“还原”前Cu元素以[Cu(NH3)4](OH)2的形式存在,水合肼被氧化的化学方程式为_______ ;一定体积下,保持其它条件不变,水合肼浓度对Cu2O的产率的影响如图所示。当水合肼浓度大于3.25mol·L-1时,[Cu(NH3)4]2+的转化率仍增大,但Cu2O的产率下降,其可能的原因是_______ 。

已知:常温下,相关金属离子生成氢氧化物沉淀的pH见表:
| 氢氧化物 | Cu(OH)2 | Fe(OH)3 | Fe(OH)2 | Mn(OH)2 |
| 开始沉淀的pH | 4.8 | 1.9 | 7.5 | 8.8 |
| 沉淀完全的pH | 6.4 | 3.2 | 9.7 | 10.4 |
(1)基态Cu原子价层电子的排布图为
(2)滤渣的主要成分是
(3)“酸浸”中加入MnO2的作用是
(4)“调pH”的范围是
(5)“还原”前Cu元素以[Cu(NH3)4](OH)2的形式存在,水合肼被氧化的化学方程式为

您最近半年使用:0次
名校
解题方法
8 . 铜广泛应用于电气、轻工、机械制造、国防工业等领域。回答下列问题:
(1)用黄铜矿冶炼铜的原理如图所示。
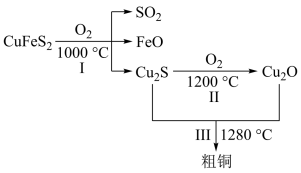
① 中Fe的化合价为
中Fe的化合价为__________ 。
②反应Ⅲ的化学方程式为____________________________ 。
(2)铜器久置于空气中会与空气中的水蒸气、 、
、 反应生成铜锈,其中有无害的“铜绿”
反应生成铜锈,其中有无害的“铜绿”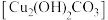 和有害的“粉状锈”
和有害的“粉状锈” 。
。
① 和
和 均属于
均属于_____________ (填“正”、“酸式”或“碱式”)盐。
②“铜绿”能与酸反应生成铜盐和 、
、 。某同学利用下述系列反应实现了:“铜→铜绿→……→铜”的转化:
。某同学利用下述系列反应实现了:“铜→铜绿→……→铜”的转化:
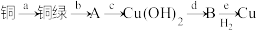
请写出“铜绿”与盐酸反应的化学方程式:_______________________ 。上述转化过程中属于化合反应的是________________ (填字母)。
(1)用黄铜矿冶炼铜的原理如图所示。

①
 中Fe的化合价为
中Fe的化合价为②反应Ⅲ的化学方程式为
(2)铜器久置于空气中会与空气中的水蒸气、
 、
、 反应生成铜锈,其中有无害的“铜绿”
反应生成铜锈,其中有无害的“铜绿”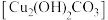 和有害的“粉状锈”
和有害的“粉状锈” 。
。①
 和
和 均属于
均属于②“铜绿”能与酸反应生成铜盐和
 、
、 。某同学利用下述系列反应实现了:“铜→铜绿→……→铜”的转化:
。某同学利用下述系列反应实现了:“铜→铜绿→……→铜”的转化: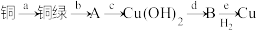
请写出“铜绿”与盐酸反应的化学方程式:
您最近半年使用:0次
9 . 下列实验方案设计不能达到实验目的的是
| 选项 | 实验目的 | 实验方案 |
| A | 检验FeCl2溶液中的FeCl2是否被氧化 | 向该溶液中滴加硫氰化钾溶液 |
| B | 比较Cl与S非金属性强弱 | 比较HCl与H2SO4酸性强弱 |
| C | 除去Cu粉中混有的CuO | 向混合物中滴加适量稀硫酸 |
| D | 证明CH2=CHCHO中含有醛基 | 向新制银氨溶液中滴少量丙烯醛并用水浴加热 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
10 . 某固体粉末可能含有KCl、K2CO3、Ba(NO3)2、CuSO4和Na2SO4,进行如下实验:
①取固体粉末加足量的水,振荡,有白色沉淀生成;
②向此悬浊液中加稀盐酸,沉淀不溶解,过滤,得到无色滤液;
③取无色滤液,滴加AgNO3溶液,产生白色沉淀。
依据实验现象,下列关于固体粉末的判断正确的是
| A.可能含K2CO3和CuSO4 |
| B.可能含KCl,一定含Ba(NO3)2和Na2SO4 |
| C.一定含KCl、Ba(NO3)2和Na2SO4 |
| D.一定含Ba(NO3)2、Na2SO4和K2CO3 |
您最近半年使用:0次
2024-01-20更新
|
177次组卷
|
4卷引用:北京市西城区2023-2024学年高一上学期期末考试化学试卷



