1 . 将1.92gCu投入到一定量的浓硝酸中,随着反应的进行,生成气体的颜色逐渐变浅,当铜完全溶解后,共收集到XmL气体(标准状况)。将盛有等量该气体的容器倒入水中,欲使容器内气体恰好完全溶解于水,需通入氧气的体积(标准状况)是
| A.224mL | B.336mL | C.448mL | D.672mL |
您最近一年使用:0次
2021-01-29更新
|
537次组卷
|
7卷引用:首都师范大学附属中学2020-2021学年高一上学期期末考试化学试题
2 . 下列化学用语对事实的表述正确的是
A.在加热条件下铜可与浓硫酸反应:Cu+2H+ Cu2++H2↑ Cu2++H2↑ |
B.碳酸氢钠水解离子方程式:HCO +H2O +H2O CO CO +H3O+ +H3O+ |
| C.实验室制备氢氧化铁胶体:Fe3++3H2O=Fe(OH)3↓+3H+ |
D.乙酸与乙醇发生酯化反应:CH3COOH+C2H518OH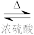 CH3CO18OC2H5+H2O CH3CO18OC2H5+H2O |
您最近一年使用:0次
解题方法
3 . 下列反应的离子方程式书写正确的是
A.碳酸钙与稀盐酸反应: |
B.氯化亚铁溶液与氯水反应: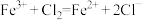 |
C.氯化铁溶液与氢氧化钠溶液反应: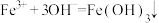 |
D.铜与稀硝酸反应: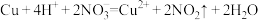 |
您最近一年使用:0次
2011高三·河南洛阳·专题练习
名校
解题方法
4 . 同学们在做铜与浓硝酸反应的实验时,发现反应后的溶液呈绿色,而不显蓝色。甲同学认为是该溶液中硝酸铜的质量分数较高所致,而乙同学认为是该溶液中溶解了生成的气体。同学们分别设计了以下4个实验来判断两种说法是否正确,这些方案中不可行的是
| A.加水稀释该绿色溶液,观察溶液颜色变化 |
| B.加热该绿色溶液,观察溶液颜色变化 |
| C.向该绿色溶液中通入氮气,观察溶液颜色变化 |
| D.向饱和硝酸铜溶液中通入浓硝酸与铜反应产生的气体,观察溶液颜色变化 |
您最近一年使用:0次
2020-09-23更新
|
561次组卷
|
6卷引用:北京市第四中学2022~2023学年高一下学期期中考试化学试题
(已下线)北京市第四中学2022~2023学年高一下学期期中考试化学试题(已下线)2012届河南省洛阳市高三“一练”考试化学试卷【全国百强校】湖南师范大学附属中学2018-2019学年高二下学期期中考试化学试题高一必修第一册(鲁科2019)第3章 第3节 氮的循环 教材帮(人教版2019)必修第二册 第五章 化工生产中的重要非金属元素 第二节 氮及其化合物(已下线)合格考汇编5金属及其化合物二
5 . 将铜粉放入稀硫酸中,加热后无明显现象,但加入某盐一段时间后,发现铜粉质量减少,则该盐不可能是
A. | B.NaCl | C. | D. |
您最近一年使用:0次
2020-09-23更新
|
237次组卷
|
4卷引用:北京第一〇一中学怀柔分校2020-2021学年高一上学期期末考试化学试题
北京第一〇一中学怀柔分校2020-2021学年高一上学期期末考试化学试题高一必修第一册(鲁科2019)第3章 第3节 氮的循环(已下线)第12讲 氮及其化合物(练)-2023年高考化学一轮复习讲练测(新教材新高考)江西省丰城市东煌学校2021-2022学年高一下学期5月月考化学试题
名校
解题方法
6 . 铜和镁的合金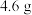 完全溶于足量的硝酸后,再加入过量的NaOH溶液,生成
完全溶于足量的硝酸后,再加入过量的NaOH溶液,生成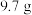 沉淀,则合金与硝酸反应时,放出的气体可能是( )
沉淀,则合金与硝酸反应时,放出的气体可能是( )
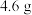 完全溶于足量的硝酸后,再加入过量的NaOH溶液,生成
完全溶于足量的硝酸后,再加入过量的NaOH溶液,生成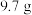 沉淀,则合金与硝酸反应时,放出的气体可能是( )
沉淀,则合金与硝酸反应时,放出的气体可能是( )A.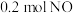 |
B.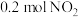 和 和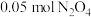 |
C.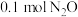 |
D.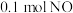 、 、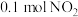 和 和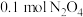 |
您最近一年使用:0次
2020-09-23更新
|
648次组卷
|
7卷引用:2006年北京市高中学生化学竞赛高中一年级试题
名校
解题方法
7 . 下列反应的离子方程式书写正确的是
A.碳酸钙与稀盐酸反应:CO +2H+=CO2↑+H2O +2H+=CO2↑+H2O |
B.硫酸与氢氧化钡反应:Ba2++SO =BaSO4↓ =BaSO4↓ |
| C.铁与氯化铁溶液反应:Fe+2Fe3+=3Fe2+ |
D.铜与稀硝酸反应:Cu+4H++2NO =Cu2++2NO2↑+2H2O =Cu2++2NO2↑+2H2O |
您最近一年使用:0次
2020-09-21更新
|
372次组卷
|
2卷引用:北京市海淀区2020年第一次合格性考试模拟化学试题
名校
解题方法
8 . 向Fe2(SO4)3溶液中加入a g铜,铜完全溶解后,再加入b g铁,充分反应后得到c g残余固体,且a>c,则下列说法正确的是( )
| A.残余固体是铜和铁 | B.最后得到的溶液中一定含有Cu2+ |
| C.将残余固体加入到稀硫酸中,无气泡产生 | D.最后得到的溶液中可能含有Fe3+ |
您最近一年使用:0次
2020-09-10更新
|
71次组卷
|
2卷引用:北京市育英学校2023-2024学年高一上学期期末考试化学试题
解题方法
9 . 某同学在实验室中进行如图所示实验。

(1)铜丝与浓硝酸发生反应的离子方程式是________ 。
(2)烧杯中NaOH溶液的作用是________ 。
(3)铜丝下端弯成螺旋状的原因是________ 。
(4)根据反应产生的现象,从不同角度推断该反应所属反应类型:
①根据________ 现象,可推断该反应为氧化还原反应。
②根据反应后试管壁发热的现象,可推断该反应属于________ 反应。

(1)铜丝与浓硝酸发生反应的离子方程式是
(2)烧杯中NaOH溶液的作用是
(3)铜丝下端弯成螺旋状的原因是
(4)根据反应产生的现象,从不同角度推断该反应所属反应类型:
①根据
②根据反应后试管壁发热的现象,可推断该反应属于
您最近一年使用:0次
名校
解题方法
10 . 某校化学小组同学研究 Cu与H2SO4 溶液反应,小伟同学实验记录如下:
(1)实验一:探究白雾的成分
①波波同学收集实验Ⅰ中白雾,加入品红溶液,溶液褪色,得出结论:白雾成分包含 SO2。可能是因为局部温度过高产生,写出有关化学方程式________ 。
②艳艳同学认为不妥,补充实验Ⅲ:
根据实验Ⅲ,可推断白雾成分是______ ,而并非SO2。
(2)实验二:探究红色固体的成分。经过分析,实验Ⅰ和实验Ⅱ中的红色浑浊成分相同。
【资料】Cu2O能溶在浓氨水中形成无色Cu(NH3)2+,很容易被氧气氧化为蓝色Cu(NH3)22+;Cu2O能与一定浓度的酸溶液发生反应:Cu2O+2H+=Cu2++Cu+H2O。
①写出Cu2O溶在浓氨水中的离子方程式_______ 。
②对于红色浑浊的成分,谷哥设计实验并实施,证实了红色固体中只有Cu2O。他的实验是:将实验Ⅰ试管中固体过滤洗涤,得红色固体,__________ 。
③结合实验Ⅰ和Ⅱ,吉吉同学确定铜丝烧至红热时生成了______ 。
(3)实验三:探究红色固体不溶的原因。经过检验,实验Ⅰ和实验Ⅱ反应后的溶液均显酸性,对于体系中有Cu2O固体的原因:
龙校假设:在实验条件下,随着溶液酸性降低,Cu2O与酸无法反应。
乔博假设:在实验条件下,随着溶液酸性降低,Cu2O与酸反应速率变小。
邹邹同学继续实验:
①实验Ⅴ的目的是 ______ 。
②通过以上实验,臧臧同学得出的结论是______ 。
| 实验编号 | 实验操作 | 实验现象 |
| Ⅰ | 取螺旋状铜丝在酒精灯上烧至红热,迅速伸入装有 10 mL 3 mol/L H2SO4溶液的试管中 | 产生大量白雾;溶液颜色变为浅蓝色;试管中出现红色浑浊 |
| Ⅱ | 步骤一:取螺旋状铜丝在酒精灯上烧至红热, 迅速伸入装有10 mL蒸馏水的试管中; 步骤二:冷却后加入5 mL 3 mol/L H2SO4 | 步骤一:产生少量白雾;试管中出现黑色浑浊,略带红色 步骤二:浑浊全部为红色;溶液略显蓝色 |
①波波同学收集实验Ⅰ中白雾,加入品红溶液,溶液褪色,得出结论:白雾成分包含 SO2。可能是因为局部温度过高产生,写出有关化学方程式
②艳艳同学认为不妥,补充实验Ⅲ:
| 实验编号 | 实验操作 | 实验现象 |
| Ⅲ | 步骤一:取品红溶液,加 3 mol/L H2SO4溶液,加热; 步骤二:收集实验Ⅰ中白雾,加入品红溶液,加热 | 步骤一:溶液褪色,加热无颜色变化; 步骤二:溶液褪色,加热无颜色变化 |
(2)实验二:探究红色固体的成分。经过分析,实验Ⅰ和实验Ⅱ中的红色浑浊成分相同。
【资料】Cu2O能溶在浓氨水中形成无色Cu(NH3)2+,很容易被氧气氧化为蓝色Cu(NH3)22+;Cu2O能与一定浓度的酸溶液发生反应:Cu2O+2H+=Cu2++Cu+H2O。
①写出Cu2O溶在浓氨水中的离子方程式
②对于红色浑浊的成分,谷哥设计实验并实施,证实了红色固体中只有Cu2O。他的实验是:将实验Ⅰ试管中固体过滤洗涤,得红色固体,
③结合实验Ⅰ和Ⅱ,吉吉同学确定铜丝烧至红热时生成了
(3)实验三:探究红色固体不溶的原因。经过检验,实验Ⅰ和实验Ⅱ反应后的溶液均显酸性,对于体系中有Cu2O固体的原因:
龙校假设:在实验条件下,随着溶液酸性降低,Cu2O与酸无法反应。
乔博假设:在实验条件下,随着溶液酸性降低,Cu2O与酸反应速率变小。
邹邹同学继续实验:
| 实验编号 | 实验操作 | 实验现象 |
| Ⅳ | 取Cu2O固体少量,加入到装有 10 mL3 mol/L H2SO4 溶液的试管中 | 溶液迅速变为蓝色;试管中出现少量亮红色固体 |
| Ⅴ | 取Cu2O固体少量,加入到装有 10 mL 3 mol/L H2SO4 和少量CuSO4 (浅蓝色)的试管中 | 现象同Ⅳ |
| Ⅵ | 重复实验Ⅰ,振荡试管,分为两等份。第一份立刻加入浓硫酸至 c(H2SO4)=3 mol/L;第二份静置 4 h之后,过滤,向固体中加入浓硫酸至 c(H2SO4)=3 mol/L | 第一份加酸后红色固体明显减少,溶液蓝色加深;第二份静置时,固体减少,溶液缓慢变为蓝色,固体加酸后无明显现象。 |
②通过以上实验,臧臧同学得出的结论是
您最近一年使用:0次



