名校
1 . 氢能是一种极具发展潜力的清洁能源。以太阳能为热源,热化学硫碘循环分解水是一种高效、无污染的制氢方法。其反应过程如下图所示:

分析反应I:
反应I: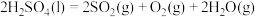

(1)它由两步反应组成:i.

ii. 分解,热化学方程式为
分解,热化学方程式为_______ 。
分析反应II:
(2)反应II的化学方程式是_______ 。
(3)反应II得到的产物用 进行分离。该产物的溶液在过量
进行分离。该产物的溶液在过量 的存在下会分成两层——含低浓度
的存在下会分成两层——含低浓度 的
的 层和高浓度的
层和高浓度的 的
的 层。
层。
①区分两层溶液可加入的试剂为_______ (填序号)。
A.淀粉溶液B.氯化钡溶液(资料: 易溶于水)
易溶于水)
C.硝酸银溶液D.氯化亚铁溶液
②根据上述事实,下列说法正确的是_______ (填序号)。
A.两层溶液的密度存在差异
B.加 前,
前, 溶液和
溶液和 溶液不互溶
溶液不互溶
C. 在
在 溶液中比在
溶液中比在 溶液中易溶
溶液中易溶
③经检测, 层中
层中 。其比值大于2的原因是
。其比值大于2的原因是_______ 。
分析反应Ⅲ:
(4)如表所示的数据是破坏1mol气态物质中的化学键所消耗的能量,请在下图中画出反应Ⅲ: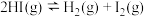 的能量变化示意图
的能量变化示意图_______ (不必标注具体数值)。


分析反应I:
反应I:
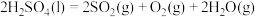

(1)它由两步反应组成:i.


ii.
 分解,热化学方程式为
分解,热化学方程式为分析反应II:
(2)反应II的化学方程式是
(3)反应II得到的产物用
 进行分离。该产物的溶液在过量
进行分离。该产物的溶液在过量 的存在下会分成两层——含低浓度
的存在下会分成两层——含低浓度 的
的 层和高浓度的
层和高浓度的 的
的 层。
层。①区分两层溶液可加入的试剂为
A.淀粉溶液B.氯化钡溶液(资料:
 易溶于水)
易溶于水)C.硝酸银溶液D.氯化亚铁溶液
②根据上述事实,下列说法正确的是
A.两层溶液的密度存在差异
B.加
 前,
前, 溶液和
溶液和 溶液不互溶
溶液不互溶C.
 在
在 溶液中比在
溶液中比在 溶液中易溶
溶液中易溶③经检测,
 层中
层中 。其比值大于2的原因是
。其比值大于2的原因是分析反应Ⅲ:
(4)如表所示的数据是破坏1mol气态物质中的化学键所消耗的能量,请在下图中画出反应Ⅲ:
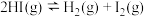 的能量变化示意图
的能量变化示意图
| 物质 |  |  |  |
| 能量(kJ) | 151 | 298 | 436 |
您最近一年使用:0次
名校
解题方法
2 . 工业上利用碳热还原BaSO4制得BaS,进而生产各种含钡化合物。温度对反应后组分的影响如图。

已知:碳热还原BaSO4过程中可能发生下列反应。
i.BaSO4(s)+2C(s)=2CO2(g)+BaS(s) △H1
ii.BaSO4(s)+4C(s)=4CO(g)+BaS(s) △H2=+571.2kJ·mol-1
iii.BaSO4(s)+4CO(g)=4CO2(g)+BaS(s) △H3=-118.8kJ·mol-1
下列关于碳热还原BaSO4过程的说法正确的是

已知:碳热还原BaSO4过程中可能发生下列反应。
i.BaSO4(s)+2C(s)=2CO2(g)+BaS(s) △H1
ii.BaSO4(s)+4C(s)=4CO(g)+BaS(s) △H2=+571.2kJ·mol-1
iii.BaSO4(s)+4CO(g)=4CO2(g)+BaS(s) △H3=-118.8kJ·mol-1
下列关于碳热还原BaSO4过程的说法正确的是
| A.△H1=+113.1kJ·mol-1 |
B.400℃后,反应后组分的变化是由C(s)+CO2(g) 2CO(g)的移动导致的 2CO(g)的移动导致的 |
C.温度升高,C(s)+CO2(g) 2CO(g)的平衡常数K减小 2CO(g)的平衡常数K减小 |
| D.反应过程中,生成的CO2和CO的物质的量之和始终等于投入C的物质的量 |
您最近一年使用:0次
2022-05-15更新
|
1258次组卷
|
7卷引用:北京市海淀区2022届高三二模化学试题
北京市海淀区2022届高三二模化学试题北京市海淀区2021-2022学年高三下学期期末练习化学试题北京市中国人民大学附属中学2023-2024学年高三上学期11月统练三 化学试题(已下线)第七章 化学反应速率和化学平衡(测)-2023年高考化学一轮复习讲练测(全国通用)广东省深圳市蛇口育才教育集团育才中学2023-2024学年高二上学期阶段检测(一)化学试题(已下线)2024届广东省华南师范大学附属中学 广雅中学 深圳中学 广东实验中学高三上学期四校联考化学试题广东省云浮市云安区云安中学2023-2024学年高三下学期3月考试化学试题
21-22高一下·北京西城·期中
名校
3 . 以太阳能为热源,热化学硫碘循环分解水是一种高效、环保的制氢方法,其流程图如下:
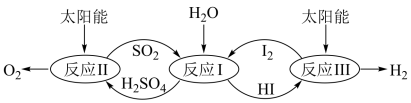
相关反应的热化学方程式为:
反应I:SO2(g)+I2(g)+2H2O(l)=2HI(aq)+H2SO4(aq) △H1=-213kJ·mol-1
反应II:H2SO4(aq)=SO2(g)+H2O(1)+ O2(g) △H2=+327kJ·mol-l
O2(g) △H2=+327kJ·mol-l
反应III:2HI(aq)=H2(g)+I2(g)△H3=+172kJ·mol-1
下列说法不正确的是

相关反应的热化学方程式为:
反应I:SO2(g)+I2(g)+2H2O(l)=2HI(aq)+H2SO4(aq) △H1=-213kJ·mol-1
反应II:H2SO4(aq)=SO2(g)+H2O(1)+
 O2(g) △H2=+327kJ·mol-l
O2(g) △H2=+327kJ·mol-l反应III:2HI(aq)=H2(g)+I2(g)△H3=+172kJ·mol-1
下列说法不正确的是
| A.该过程实现了太阳能到化学能的转化 |
| B.SO2和I2对总反应起到了催化剂的作用 |
| C.总反应的热化学方程式为:2H2O(1)=2H2(g)+O2(g) △H=+286kJ·mol-l |
| D.该过程使水分解制氢分为三步反应,但总反应的△H不变 |
您最近一年使用:0次
名校
4 . 乙烯是一种重要的基本化工原料,乙烯的产量可以衡量一个国家的石油化工发展水平,研究工业制取乙烯有重要的意义。
Ⅰ.工业用 和
和 在一定条件下合成乙烯:
在一定条件下合成乙烯: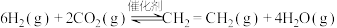

已知:①

②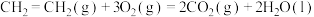

③

(1)
_______ 。
(2)在密闭容器中充入体积比为3:1的 和
和 ,不同温度对
,不同温度对 的平衡转化率和催化剂催化效率的影响如下图所示,下列说法正确的是_______。
的平衡转化率和催化剂催化效率的影响如下图所示,下列说法正确的是_______。

Ⅱ.工业用甲烷催化法制取乙烯:
 ,T℃时,向2L的恒容反应器中充入2mol
,T℃时,向2L的恒容反应器中充入2mol  ,仅发生上述反应,反应过程中
,仅发生上述反应,反应过程中 的物质的量随时间变化如图所示:
的物质的量随时间变化如图所示:

(3)实验测得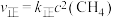 ,
, ,
, 、
、 为速率常数,只与温度有关,T℃时
为速率常数,只与温度有关,T℃时 与
与 的比值为
的比值为_______ (用含x的代数式表示);若将温度升高,速率常数增大的倍数:
_______  (填“>”“=”或“<”)。
(填“>”“=”或“<”)。
Ⅲ.乙烷裂解制乙烯: 。
。
(4)T℃时,将1mol乙烷与1mol氦气混合后,通入体积为1L的密闭容器中发生反应。若平衡时乙烯的体积分数为20%,则T℃时该反应的平衡常数
_______ 。
Ⅳ.电化学法还原二氧化碳制乙烯原理如下图所示。

(5)阴极电极反应式为:_______ 。电路中转移0.3mol电子,两极共收集气体_______ L(标准状况)。
Ⅰ.工业用
 和
和 在一定条件下合成乙烯:
在一定条件下合成乙烯: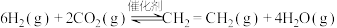

已知:①


②
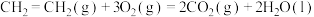

③


(1)

(2)在密闭容器中充入体积比为3:1的
 和
和 ,不同温度对
,不同温度对 的平衡转化率和催化剂催化效率的影响如下图所示,下列说法正确的是_______。
的平衡转化率和催化剂催化效率的影响如下图所示,下列说法正确的是_______。
| A.为了提高乙烯的产率应尽可能选择低温 | B.生成乙烯的速率: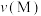 可能小于 可能小于 |
| C.M点时的压强一定小于N点时的压强 | D.平衡常数: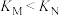 |
Ⅱ.工业用甲烷催化法制取乙烯:

 ,T℃时,向2L的恒容反应器中充入2mol
,T℃时,向2L的恒容反应器中充入2mol  ,仅发生上述反应,反应过程中
,仅发生上述反应,反应过程中 的物质的量随时间变化如图所示:
的物质的量随时间变化如图所示:
(3)实验测得
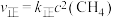 ,
, ,
, 、
、 为速率常数,只与温度有关,T℃时
为速率常数,只与温度有关,T℃时 与
与 的比值为
的比值为
 (填“>”“=”或“<”)。
(填“>”“=”或“<”)。Ⅲ.乙烷裂解制乙烯:
 。
。(4)T℃时,将1mol乙烷与1mol氦气混合后,通入体积为1L的密闭容器中发生反应。若平衡时乙烯的体积分数为20%,则T℃时该反应的平衡常数

Ⅳ.电化学法还原二氧化碳制乙烯原理如下图所示。

(5)阴极电极反应式为:
您最近一年使用:0次
名校
解题方法
5 . 在双碳目标驱动下,大批量氢燃料客车在2022年北京冬奥会上投入使用。稳定氢源的获取是科学研究热点,对以下2种氢源获取方法进行讨论。
Ⅰ.甲醇蒸汽重整制氢
甲醇蒸汽重整制氢过程中有以下化学反应。
资料:产氢率和水碳比(S/C)的定义:
①产氢率=
②水碳比(S/C)表示反应物中H2O和CH3OH的比值,水碳比的变化是以CH3OH不变,改变H2O的物质的量加以控制。
(1)理想产氢率=_______ 。
(2)△H2=_______ kJ·mol-1
(3)针对R1进行讨论:其他条件不变,随着温度升高,n(H2)_______ (填“增大”、“减小”或“不变”),理由是_______ 。
(4)其他条件不变,测得产物摩尔分数(即物质的量分数)随温度的变化如图所示。由图可知,在600-912K时,随着温度升高,氢气的摩尔分数增大,原因是_______ 。

(5)结合资料和图示,提出2条减少积碳的措施_______ 、_______ 。
Ⅱ.电解液氨制氢
氨分子中具有较高的含氢量,因此是制氢的优选原料。使用NaNH2非水电解质研究液氨电解制氢原理,装置示意图如图所示。

资料:2NH3 NH
NH +NH
+NH
(6)①某电极上发生的电极反应为6NH3+6e-=3H2↑+6NH ,该电极为
,该电极为_______ (选填a或b)极。
②写出另一极上发生的电极反应_______ 。
③不考虑其它能量损耗,利用该装置产生1mol氢气时,转移电子的物质的量是_______ mol。
Ⅰ.甲醇蒸汽重整制氢
甲醇蒸汽重整制氢过程中有以下化学反应。
| 编号 | 反应 | 方程式 | △H/kJ·mol-1 |
| R1 | 甲醇蒸汽重整 | CH3OH(g)+H2O(g) CO2(g)+3H2(g) CO2(g)+3H2(g) | △H1=+49.24 |
| R2 | 甲醇分解反应 | CH3OH(g) CO(g)+2H2(g) CO(g)+2H2(g) | △H2 |
| R3 | 水汽反应 | CO(g)+H2O(g) CO2(g)+H2(g) CO2(g)+H2(g) | △H3=-41.17 |
| R4 | 积碳反应 | CO(g)+H2(g) C(s)+H2O(g) C(s)+H2O(g) | △H<0 |
CO2(g)+2H2(g) C(s)+2H2O(g) C(s)+2H2O(g) | △H<0 | ||
2CO(g) C(s)+CO2(g) C(s)+CO2(g) | △H<0 |
资料:产氢率和水碳比(S/C)的定义:
①产氢率=

②水碳比(S/C)表示反应物中H2O和CH3OH的比值,水碳比的变化是以CH3OH不变,改变H2O的物质的量加以控制。
(1)理想产氢率=
(2)△H2=
(3)针对R1进行讨论:其他条件不变,随着温度升高,n(H2)
(4)其他条件不变,测得产物摩尔分数(即物质的量分数)随温度的变化如图所示。由图可知,在600-912K时,随着温度升高,氢气的摩尔分数增大,原因是

(5)结合资料和图示,提出2条减少积碳的措施
Ⅱ.电解液氨制氢
氨分子中具有较高的含氢量,因此是制氢的优选原料。使用NaNH2非水电解质研究液氨电解制氢原理,装置示意图如图所示。

资料:2NH3
 NH
NH +NH
+NH
(6)①某电极上发生的电极反应为6NH3+6e-=3H2↑+6NH
 ,该电极为
,该电极为②写出另一极上发生的电极反应
③不考虑其它能量损耗,利用该装置产生1mol氢气时,转移电子的物质的量是
您最近一年使用:0次
名校
解题方法
6 . 煤的洁净技术(包括固硫技术和脱硫技术两类)可有效降低燃煤废气中SO2的含量,已成为我国解决环境问题的主导技术之一。
I.固硫技术:通过加入固硫剂,将硫元素以固体形式留在煤燃烧的残渣中。石灰石是常用的固硫剂,固硫过程中涉及的部分反应如下:
①CaCO3(s) CaO(s)+CO2(g) △H1=+178.30kJ/mol
CaO(s)+CO2(g) △H1=+178.30kJ/mol
②CaO(s)+SO2(g)+0.5O2(g) CaSO4(s) △H2=-501.92kJ/mol
CaSO4(s) △H2=-501.92kJ/mol
③CO(g)+0.5O2(g) CO2(g) △H3
CO2(g) △H3
④CaSO4(s)+CO(g) CaO(s)+SO2(g)+CO2(g) △H4=+218.92kJ/mol
CaO(s)+SO2(g)+CO2(g) △H4=+218.92kJ/mol
(1)温度升高,反应①的化学平衡常数____ (填“增大”“减小”或“不变”)。
(2)△H3=____ kJ/mol。
(3)在煤燃烧过程中常鼓入稍过量的空气以提高固硫率(燃烧残渣中硫元素的质量占燃煤中硫元素总质量的百分比),结合反应②、③、④分析其原因:____ 。
II.电化学脱硫技术是一种温和的净化技术,其基本原理为利用阳极反应产生的羟基自由基(·OH,氧元素为-1价)将燃煤中的含硫物质氧化除去。
(4)将煤打成煤浆加入电解槽的目的是____ 。
(5)补全用羟基自由基除去煤中二硫化亚铁(FeS2)的反应的离子方程式:____ 。
FeS2+·OH=Fe3++SO +H2O+_____。
+H2O+_____。
(6)对某含FeS2的煤样品进行电解脱硫,测得一定时间内随溶液起始pH的改变脱硫率(溶于水中的硫元素质量占煤样中硫元素总质量的百分比)的变化如图所示。

pH大于1.5后脱硫率下降的可能原因有:随着pH的升高,反应物的氧化性或还原性降低;____ 。
I.固硫技术:通过加入固硫剂,将硫元素以固体形式留在煤燃烧的残渣中。石灰石是常用的固硫剂,固硫过程中涉及的部分反应如下:
①CaCO3(s)
 CaO(s)+CO2(g) △H1=+178.30kJ/mol
CaO(s)+CO2(g) △H1=+178.30kJ/mol②CaO(s)+SO2(g)+0.5O2(g)
 CaSO4(s) △H2=-501.92kJ/mol
CaSO4(s) △H2=-501.92kJ/mol③CO(g)+0.5O2(g)
 CO2(g) △H3
CO2(g) △H3④CaSO4(s)+CO(g)
 CaO(s)+SO2(g)+CO2(g) △H4=+218.92kJ/mol
CaO(s)+SO2(g)+CO2(g) △H4=+218.92kJ/mol(1)温度升高,反应①的化学平衡常数
(2)△H3=
(3)在煤燃烧过程中常鼓入稍过量的空气以提高固硫率(燃烧残渣中硫元素的质量占燃煤中硫元素总质量的百分比),结合反应②、③、④分析其原因:
II.电化学脱硫技术是一种温和的净化技术,其基本原理为利用阳极反应产生的羟基自由基(·OH,氧元素为-1价)将燃煤中的含硫物质氧化除去。
(4)将煤打成煤浆加入电解槽的目的是
(5)补全用羟基自由基除去煤中二硫化亚铁(FeS2)的反应的离子方程式:
FeS2+·OH=Fe3++SO
 +H2O+_____。
+H2O+_____。(6)对某含FeS2的煤样品进行电解脱硫,测得一定时间内随溶液起始pH的改变脱硫率(溶于水中的硫元素质量占煤样中硫元素总质量的百分比)的变化如图所示。

pH大于1.5后脱硫率下降的可能原因有:随着pH的升高,反应物的氧化性或还原性降低;
您最近一年使用:0次
解题方法
7 . “绿水青山就是金山银山”,研究消除氮氧化物污染对建设美丽家乡,打造宜居环境有重要意义。
(1)已知:
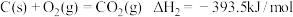

写出C与 反应生成
反应生成 的热化学方程式
的热化学方程式___________ 。
(2)已知: 。在
。在 恒容密闭容器中,投入
恒容密闭容器中,投入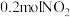 和
和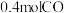 ,经过一段时间后达到平衡状态,测得
,经过一段时间后达到平衡状态,测得 的转化率为
的转化率为 。该温度下,反应的平衡常数为
。该温度下,反应的平衡常数为___________ 。
(3)原煤经热解、冷却得到的煤焦可用于 的脱除。热解温度为
的脱除。热解温度为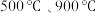 得到的煤焦分别用
得到的煤焦分别用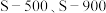 表示,相关信息如下表:
表示,相关信息如下表:
将NO浓度恒定的废气以固定流速通过反应器(图1)。不同温度下,进行多组平行实验,测定相同时间内NO的出口浓度,可得NO的脱除率与温度的关系如图2所示。
[已知: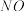 的脱除主要包含吸附和化学还原(
的脱除主要包含吸附和化学还原( )两个过程]
)两个过程]
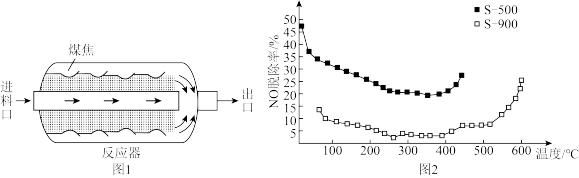
①已知煤焦表面存在的官能团有利于吸附NO,其数量与煤焦中氢碳质量比的值密切相关,比值小,表面官能团少。由图2可知,相同温度下,单位时间内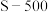 对NO的脱除率比
对NO的脱除率比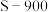 的高,可能原因是
的高,可能原因是___________ 。(答两条)。
② 后,随着温度升高,单位时间内NO的脱除率增大的原因是
后,随着温度升高,单位时间内NO的脱除率增大的原因是___________ 。
(4)电解氧化吸收法:其原理如图3所示:
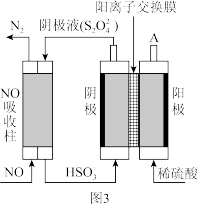
①从A口中出来的物质的是___________ 。
②写出电解池阴极的电极反应式___________ 。
(1)已知:

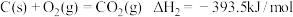

写出C与
 反应生成
反应生成 的热化学方程式
的热化学方程式(2)已知:
 。在
。在 恒容密闭容器中,投入
恒容密闭容器中,投入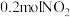 和
和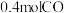 ,经过一段时间后达到平衡状态,测得
,经过一段时间后达到平衡状态,测得 的转化率为
的转化率为 。该温度下,反应的平衡常数为
。该温度下,反应的平衡常数为(3)原煤经热解、冷却得到的煤焦可用于
 的脱除。热解温度为
的脱除。热解温度为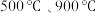 得到的煤焦分别用
得到的煤焦分别用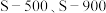 表示,相关信息如下表:
表示,相关信息如下表:| 煤焦 | 元素分析/% | 比表面积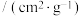 | |
| C | H | ||
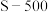 | 80.79 | 2.76 | 105.69 |
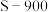 | 84.26 | 0.82 | 8.98 |
[已知:
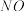 的脱除主要包含吸附和化学还原(
的脱除主要包含吸附和化学还原( )两个过程]
)两个过程]
①已知煤焦表面存在的官能团有利于吸附NO,其数量与煤焦中氢碳质量比的值密切相关,比值小,表面官能团少。由图2可知,相同温度下,单位时间内
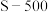 对NO的脱除率比
对NO的脱除率比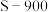 的高,可能原因是
的高,可能原因是②
 后,随着温度升高,单位时间内NO的脱除率增大的原因是
后,随着温度升高,单位时间内NO的脱除率增大的原因是(4)电解氧化吸收法:其原理如图3所示:

①从A口中出来的物质的是
②写出电解池阴极的电极反应式
您最近一年使用:0次
名校
解题方法
8 . 土壤中微生物将大气中的H2S氧化为SO 的变化过程如下图所示。下列说法
的变化过程如下图所示。下列说法不正确 的是

 的变化过程如下图所示。下列说法
的变化过程如下图所示。下列说法
| A.1 mol H2S(g)和1/2mol O2(g)的总能量高于1 mol S(g)和1 mol H2O(g)的总能量 |
B.H2S(g)+ 2O2(g)=SO (aq) +2H+(aq) △H=-806.39kJ/mol (aq) +2H+(aq) △H=-806.39kJ/mol |
C.H2S和SO 中S原子采用的杂化方式不同 中S原子采用的杂化方式不同 |
D.1 mol H2S完全氧化为SO 转移8mol电子 转移8mol电子 |
您最近一年使用:0次
2022-04-16更新
|
447次组卷
|
7卷引用:北京市顺义区2021-2022学年高三下学期4月第二次统练化学试题
北京市顺义区2021-2022学年高三下学期4月第二次统练化学试题(已下线)三轮冲刺卷2-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(北京专用)北京市北京师范大学附属中学2022-2023 学年高三上学期月考2化学试题(已下线)专题08 化学反应中的能量变化(已下线)秘籍15 反应热、盖斯定律应用及图象分析-备战2022年高考化学抢分秘籍(全国通用)(已下线)专项10 化学反应与能量-备战2022年高考化学阶段性新题精选专项特训(全国卷)(4月期)(已下线)热点题型训练 盖斯定律在反应热计算中的应用
名校
解题方法
9 . 烟气脱硫脱硝技术是环境科学研究的热点。某小组模拟 氧化结合
氧化结合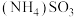 溶液吸收法同时脱除
溶液吸收法同时脱除 和NO的过程示意图如下。
和NO的过程示意图如下。
①已知: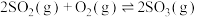
 ,则
,则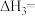
_______ 。
②其他条件不变时,高于150℃,在相同时间内 和NO的转化率均随温度升高而降低,原因是
和NO的转化率均随温度升高而降低,原因是_______ 。
③其他条件不变, 和NO初始的物质的量浓度相等时,经检测装置1分析,在相同时间内,
和NO初始的物质的量浓度相等时,经检测装置1分析,在相同时间内, 和NO的转化率随
和NO的转化率随 的浓度的变化如图。结合数据分析NO的转化率高于
的浓度的变化如图。结合数据分析NO的转化率高于 的原因
的原因_______ 。 和NO初始的物质的量浓度相等时,经检测装置2分析,在相同时间内,
和NO初始的物质的量浓度相等时,经检测装置2分析,在相同时间内, 与NO的物质的量之比对
与NO的物质的量之比对 和NO脱除率的影响如图。
和NO脱除率的影响如图。 溶液显碱性,用化学平衡原理解释:
溶液显碱性,用化学平衡原理解释:_______ 。
② 的浓度很低时,
的浓度很低时, 的脱除率超过97%,原因是
的脱除率超过97%,原因是_______ 。
③在吸收器中, 与
与 反应生成
反应生成 和
和 的离子方程式是
的离子方程式是_______ 。
④在吸收器中,随着吸收过程的进行,部分 被转化为
被转化为 ,反应中
,反应中 和
和 的物质的量之比为1:1,该反应的离子方程式是
的物质的量之比为1:1,该反应的离子方程式是_______ 。
 氧化结合
氧化结合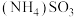 溶液吸收法同时脱除
溶液吸收法同时脱除 和NO的过程示意图如下。
和NO的过程示意图如下。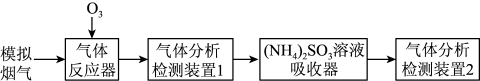
| 反应 | 平衡常数(25℃) | 活化能/(kJ/mol) |
反应a: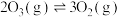 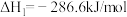 |  | 24.6 |
反应b: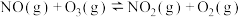 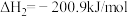 | 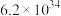 | 3.17 |
反应c:  | 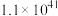 | 58.17 |
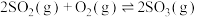
 ,则
,则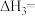
②其他条件不变时,高于150℃,在相同时间内
 和NO的转化率均随温度升高而降低,原因是
和NO的转化率均随温度升高而降低,原因是③其他条件不变,
 和NO初始的物质的量浓度相等时,经检测装置1分析,在相同时间内,
和NO初始的物质的量浓度相等时,经检测装置1分析,在相同时间内, 和NO的转化率随
和NO的转化率随 的浓度的变化如图。结合数据分析NO的转化率高于
的浓度的变化如图。结合数据分析NO的转化率高于 的原因
的原因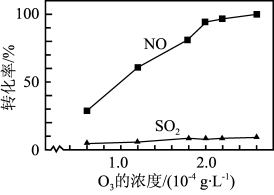
 和NO初始的物质的量浓度相等时,经检测装置2分析,在相同时间内,
和NO初始的物质的量浓度相等时,经检测装置2分析,在相同时间内, 与NO的物质的量之比对
与NO的物质的量之比对 和NO脱除率的影响如图。
和NO脱除率的影响如图。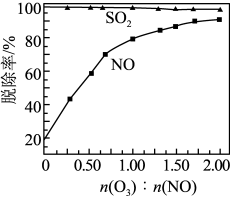
 溶液显碱性,用化学平衡原理解释:
溶液显碱性,用化学平衡原理解释:②
 的浓度很低时,
的浓度很低时, 的脱除率超过97%,原因是
的脱除率超过97%,原因是③在吸收器中,
 与
与 反应生成
反应生成 和
和 的离子方程式是
的离子方程式是④在吸收器中,随着吸收过程的进行,部分
 被转化为
被转化为 ,反应中
,反应中 和
和 的物质的量之比为1:1,该反应的离子方程式是
的物质的量之比为1:1,该反应的离子方程式是
您最近一年使用:0次
2022-04-10更新
|
763次组卷
|
6卷引用:北京市西城区2022届高三一模化学试题
名校
解题方法
10 . CH4联合H2O和CO2制取H2时,发生的主要反应如下:
①CH4(g)+H2O(g) CO(g)+3H2(g) △H1=+206kJ·mol-1
CO(g)+3H2(g) △H1=+206kJ·mol-1
②CH4(g)+CO2(g) 2CO(g)+2H2(g) △H2=+247kJ·mol-1
2CO(g)+2H2(g) △H2=+247kJ·mol-1
将CH4、H2O和CO2按一定比例通入填充有催化剂的恒容反应器,在不同温度下,反应相同时间内(反应均未达到化学平衡状态)测得 的值如图所示。
的值如图所示。
①CH4(g)+H2O(g)
 CO(g)+3H2(g) △H1=+206kJ·mol-1
CO(g)+3H2(g) △H1=+206kJ·mol-1②CH4(g)+CO2(g)
 2CO(g)+2H2(g) △H2=+247kJ·mol-1
2CO(g)+2H2(g) △H2=+247kJ·mol-1将CH4、H2O和CO2按一定比例通入填充有催化剂的恒容反应器,在不同温度下,反应相同时间内(反应均未达到化学平衡状态)测得
 的值如图所示。
的值如图所示。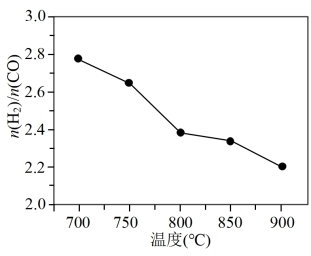
A.由①②可知,CO(g)+H2O(g) CO2(g)+H2(g) △H=+41kJ·mol-1 CO2(g)+H2(g) △H=+41kJ·mol-1 |
| B.反应条件不变,若反应足够长时间,①比②先达到化学平衡状态 |
| C.其他条件不变时,升高温度,①的化学反应速率减小,②的化学反应速率增大 |
D.其他条件不变时,增大原料中H2O的浓度可以提高产物中 的值 的值 |
您最近一年使用:0次
2022-04-09更新
|
1055次组卷
|
11卷引用:北京市东城区2022届高三一模化学试题
北京市东城区2022届高三一模化学试题北京市中关村中学2023-2024学年高三下学期3月月考化学试题北京市中国人民大学附属中学2023-2024学年高三下学期一模模拟化学试题(已下线)化学(北京卷03)-2024年高考押题预测卷(已下线)化学-2022年高考押题预测卷03(福建卷)(已下线)考点25 化学反应速率与平衡图象-备战2023年高考化学一轮复习考点帮(全国通用)湖南省岳阳市第一中学2023届高三下学期第五次月考化学试题湖南省湘潭市第一中学2023届高三上学期第五次月考化学试题天津市新华中学2023届高三下学期第一次统一练习化学试题天津市新华中学2022-2023学年高三第一次模拟考试化学试题(已下线)考点25 化学反应速率与平衡图象(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)



