解题方法
1 . 室温下, 、
、 、
、 。对于以下3种溶液:①0.10
。对于以下3种溶液:①0.10
 溶液;②向0.10
溶液;②向0.10
 溶液中通入少量
溶液中通入少量 所得的溶液;③向20mL 0.10
所得的溶液;③向20mL 0.10
 溶液中逐滴加入10mL等浓度NaOH溶液所得的溶液。下列说法正确的是
溶液中逐滴加入10mL等浓度NaOH溶液所得的溶液。下列说法正确的是
 、
、 、
、 。对于以下3种溶液:①0.10
。对于以下3种溶液:①0.10
 溶液;②向0.10
溶液;②向0.10
 溶液中通入少量
溶液中通入少量 所得的溶液;③向20mL 0.10
所得的溶液;③向20mL 0.10
 溶液中逐滴加入10mL等浓度NaOH溶液所得的溶液。下列说法正确的是
溶液中逐滴加入10mL等浓度NaOH溶液所得的溶液。下列说法正确的是| A.溶液①、③均显酸性 |
B.溶液①中存在: |
C.得到溶液②发生反应的离子方程式: |
D.溶液③中存在: |
您最近一年使用:0次
2 . 常温下,向一定质量的冰醋酸中加水稀释,溶液的导电能力变化如图。已知 ,
, 。下列说法正确的是
。下列说法正确的是
 ,
, 。下列说法正确的是
。下列说法正确的是
| A.a、b、c三点溶液的pH:b>a>c |
| B.a、b、c三点溶液中水的电离程度:a>b>c |
C.b→c过程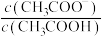 减小 减小 |
| D.向c点溶液中加入等浓度等体积的氮水,所得溶液呈中性 |
您最近一年使用:0次
解题方法
3 . 川西地区盐卤浓度较低,为了降低成本,侯德榜对原有的制碱方法——氨碱法(以食盐、氨气、二氧化碳为原料制取碳酸钠)进行改进。下列说法正确的是

| A.二氧化碳为含极性共价键的非极性分子 |
B.实验室可采用如图所示装置来制取 |
| C.工业上常采用电解饱和食盐水的方法来获得金属钠 |
D. 的 的 溶液中, 溶液中, |
您最近一年使用:0次
名校
解题方法
4 . Ⅰ、按要求回答下列问题:
(1)常温下,有关下列四种溶液的说法正确的是___________。
(2)已知25℃,NH3·H2O的Kb=1.8×10-5,若氨水的浓度为2.0mol·L-1,溶液中的c(OH−)=___________ mol·L−1。
(3)在25℃下,将a mol·L-1的氨水与0.01 mol·L-1的盐酸等体积混合,反应平衡时溶液中c(NH )=c(Cl-),用含a的代数式表示NH3·H2O的电离常数Kb=
)=c(Cl-),用含a的代数式表示NH3·H2O的电离常数Kb=___________ 。
Ⅱ、氢气可以用于合成甲醇的反应为CO(g)+2H2(g) CH3OH(g) ΔH4,在恒压条件下测得H2的平衡转化率与温度和投料比关系如图所示:
CH3OH(g) ΔH4,在恒压条件下测得H2的平衡转化率与温度和投料比关系如图所示:___________ (填“>”“<”或“=”)0。
②写出一条可同时提高反应速率和H2平衡转化率的措施:___________ 。
③保证该压强不变,向T1温度下, =0.5的平衡体系中再加入2molCO、4molH2、2molCH3OH,则化学平衡
=0.5的平衡体系中再加入2molCO、4molH2、2molCH3OH,则化学平衡___________ (填“正向”“逆向”或“不”)移动。
(1)常温下,有关下列四种溶液的说法正确的是___________。
| ① | ② | ③ | ④ |
| 0.1 mol·L-1氨水 | pH=11氨水 | 0.1 mol·L-1盐酸 | pH=3盐酸 |
| A.由水电离出的c(H+):③>① |
| B.①稀释到原来的100倍,pH与②相同 |
C.①与③混合,若溶液pH=7,则溶液中c(NH )>c(Cl-) )>c(Cl-) |
| D.②与④等体积混合,混合溶液的pH>7 |
(3)在25℃下,将a mol·L-1的氨水与0.01 mol·L-1的盐酸等体积混合,反应平衡时溶液中c(NH
 )=c(Cl-),用含a的代数式表示NH3·H2O的电离常数Kb=
)=c(Cl-),用含a的代数式表示NH3·H2O的电离常数Kb=Ⅱ、氢气可以用于合成甲醇的反应为CO(g)+2H2(g)
 CH3OH(g) ΔH4,在恒压条件下测得H2的平衡转化率与温度和投料比关系如图所示:
CH3OH(g) ΔH4,在恒压条件下测得H2的平衡转化率与温度和投料比关系如图所示: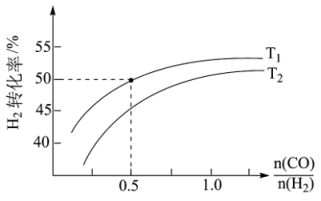
②写出一条可同时提高反应速率和H2平衡转化率的措施:
③保证该压强不变,向T1温度下,
 =0.5的平衡体系中再加入2molCO、4molH2、2molCH3OH,则化学平衡
=0.5的平衡体系中再加入2molCO、4molH2、2molCH3OH,则化学平衡
您最近一年使用:0次
5 . 已知常温下部分弱电解质的电离平衡常数如表:
(1)常温下,pH相同的三种溶液①NaF溶液;②NaClO溶液;③Na2CO3溶液,其物质的量浓度由大到小的顺序是_______ 。(填序号)
(2)向足量的次氯酸钠中通入少量的二氧化碳的离子方程式_______ 。
(3)室温下,经测定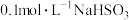 溶液
溶液 ,则
,则
_______  (填“>”、“=”、“<”)。
(填“>”、“=”、“<”)。
(4) 时,将
时,将 的氨水与
的氨水与 的盐酸等体积混合所得溶液中
的盐酸等体积混合所得溶液中 ,则溶液显
,则溶液显_______ (填“酸”“碱”或“中”)性;用含a的代数式表示 的电离平衡常数
的电离平衡常数
_______ 。
(5)将含 的烟气通入该氨水中,当溶液显中性时,溶液中
的烟气通入该氨水中,当溶液显中性时,溶液中
_______ 。
| 化学式 |  |  |  |  |  |
| 电离常数 |  |  |  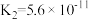 |   |  |
(2)向足量的次氯酸钠中通入少量的二氧化碳的离子方程式
(3)室温下,经测定
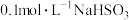 溶液
溶液 ,则
,则
 (填“>”、“=”、“<”)。
(填“>”、“=”、“<”)。(4)
 时,将
时,将 的氨水与
的氨水与 的盐酸等体积混合所得溶液中
的盐酸等体积混合所得溶液中 ,则溶液显
,则溶液显 的电离平衡常数
的电离平衡常数
(5)将含
 的烟气通入该氨水中,当溶液显中性时,溶液中
的烟气通入该氨水中,当溶液显中性时,溶液中
您最近一年使用:0次
名校
6 . 常温下,向 溶液中滴加
溶液中滴加 溶液,得到溶液的
溶液,得到溶液的 与
与 溶液体积的关系曲线如图所示。下列说法错误的是
溶液体积的关系曲线如图所示。下列说法错误的是
 溶液中滴加
溶液中滴加 溶液,得到溶液的
溶液,得到溶液的 与
与 溶液体积的关系曲线如图所示。下列说法错误的是
溶液体积的关系曲线如图所示。下列说法错误的是
A. 溶液中,各离子浓度由大到小的顺序为 溶液中,各离子浓度由大到小的顺序为 |
B. 发生的离子反应为 发生的离子反应为 |
C. 点溶液中, 点溶液中, |
D.常温下, 点溶液中,水电离出的 点溶液中,水电离出的 |
您最近一年使用:0次
名校
7 . 甲基丙烯酸甲酯是合成有机玻璃的单体。
旧法合成的反应:
①
②
新法合成的反应
③
下列说法错误的是
旧法合成的反应:
①

②

新法合成的反应
③

下列说法错误的是
A. 溶液中, 溶液中, |
B. 与 与 的空间结构及VSEPR模型均相同 的空间结构及VSEPR模型均相同 |
| C.旧法合成反应①和新法合成反应③的反应类型均为加成反应 |
D.加热条件下, 与 与 溶液能发生水解反应 溶液能发生水解反应 |
您最近一年使用:0次
解题方法
8 . 常温下,向0.1mol∙L-1二元弱酸H2A溶液中逐滴加入NaOH溶液,H2A、HA-、A2-的物质的量分数[已知 ]。随pH的变化如图所示。下列叙述正确的是
]。随pH的变化如图所示。下列叙述正确的是
 ]。随pH的变化如图所示。下列叙述正确的是
]。随pH的变化如图所示。下列叙述正确的是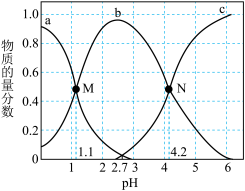
| A.a曲线代表A2-的物质的量分数随pH的变化 |
| B.溶液pH=1时的导电能力强于pH=6时的导电能力 |
| C.H2A第二步电离常数Ka2=10-4.2 |
| D.N点pH=4.2时,c(A2-)=c(HA-),溶液中不存在H2A分子 |
您最近一年使用:0次
解题方法
9 . 根据实验目的设计方案并进行实验,观察到相关现象,其中方案设计或结论不正确的是
实验目的 | 方案设计 | 现象 | 结论 | |
A | 验证NaCl、Na2SO4混合溶液中的Cl- | 取少量混合溶液于试管中,加入过量Ba(NO3)2溶液,静置,向上层清液中滴加稀硝酸酸化AgNO3溶液 | 若上层清液变浑浊 | 则混合溶液中含有Cl- |
B | 探究CF2Cl2分子的极性与非极性 | 用毛皮摩擦过的带电橡胶棒靠近CF2Cl2液流 | 液流方向改变 | CF2Cl2是极性分子 |
C | 比较HCOOH和H2S的酸性 | 分别测等物质的量浓度的HCOONH4和(NH4)2S溶液的pH | 前者的pH小 | 酸性:HCOOH>H2S |
D | 探究SO2和Fe3+的反应{已知[Fe(SO2)6]3+呈红棕色} | 将SO2气体通入FeCl3溶液中 | 溶液先变为红棕色,过一段时间又变成浅绿色 | SO2和Fe3+络合反应速率比氧化还原反应速率快,但氧化还原反应的平衡常数更大 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
10 . 物质在水中可能存在电离平衡、盐的水解平衡和沉淀溶解平衡,请回答:
(1)泡沫灭火剂包括Al2(SO4)3 溶液(约1mol/L ), NaHCO3溶液(约1mol/L )及起泡剂,使用时发生反应的离子方程式为_______ 。
(2)t℃时,某稀硫酸溶液中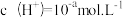 ,
,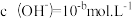 ,已知:
,已知: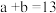 ,该温度下水的离子积常数 KW 的数值为
,该温度下水的离子积常数 KW 的数值为_______ 。
(3)含等物质的量的 NaHC2O4 和 Na 2C2O4 的溶液物料守恒式为_______ 。
(4)已知25℃时部分弱电解质的电离平衡常数数据如下表:
pH 相同的①CH3COONa 溶液、② NaClO溶液、③ NaHCO3溶液、④ NaOH 溶液,其物质的量浓度由大到小的顺序为_______ 。
(5)某溶液只含Cu2+、Fe2+、Fe3+三种金属离子,且三种离子沉淀时的pH 如下表所示:
为制备CuCl2·3H2O,除去Cu2+、Fe2+、Fe3+离子应该先加入_______ ,然后再加入_______ ,调节pH 范围为_______ 。
(1)泡沫灭火剂包括Al2(SO4)3 溶液(约1mol/L ), NaHCO3溶液(约1mol/L )及起泡剂,使用时发生反应的离子方程式为
(2)t℃时,某稀硫酸溶液中
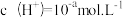 ,
,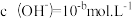 ,已知:
,已知: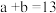 ,该温度下水的离子积常数 KW 的数值为
,该温度下水的离子积常数 KW 的数值为(3)含等物质的量的 NaHC2O4 和 Na 2C2O4 的溶液物料守恒式为
(4)已知25℃时部分弱电解质的电离平衡常数数据如下表:
| 化学式 | CH3COOH | H2CO3 | HClO | |
| 平衡常数 | 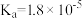 | 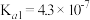 | 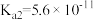 | 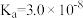 |
(5)某溶液只含Cu2+、Fe2+、Fe3+三种金属离子,且三种离子沉淀时的pH 如下表所示:
| 金属离子 | Fe3+ | Fe2+ | Cu2+ | |
| pH | 氢氧化物开始沉淀 | 1.9 | 7.0 | 4.7 |
| 氢氧化物完全沉淀 | 3.2 | 9.0 | 6.7 | |
您最近一年使用:0次



