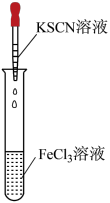名校
解题方法
1 . 乙氨酸( )是一种两性有机物,可与盐酸反应生成盐酸盐(
)是一种两性有机物,可与盐酸反应生成盐酸盐( )。已知
)。已知 水溶液呈酸性,下列叙述正确的是
水溶液呈酸性,下列叙述正确的是
 )是一种两性有机物,可与盐酸反应生成盐酸盐(
)是一种两性有机物,可与盐酸反应生成盐酸盐( )。已知
)。已知 水溶液呈酸性,下列叙述正确的是
水溶液呈酸性,下列叙述正确的是A.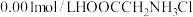 水溶液的pH=3 水溶液的pH=3 |
B.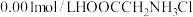 水溶液加水稀释,pH升高 水溶液加水稀释,pH升高 |
C. 在水中的电离方程式为: 在水中的电离方程式为: |
D. 水溶液中: 水溶液中: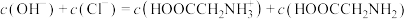 |
您最近半年使用:0次
2 . 为达到下列实验目的,其实验操作正确的是
| 实验目的 | A.验证温度对水解平衡的影响 | B.检查装置的气密性 |
| 实验操作 |
|
|
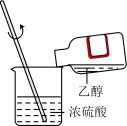
| 实验目的 | C.混合浓硫酸和乙醇 | D.检验溶液的 |
| 实验操作 |
|
|
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
7日内更新
|
82次组卷
|
2卷引用:天津市河北区2023-2024学年高三下学期二模化学试卷
解题方法
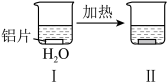
3 . 铝片与 溶液反应的探究实验如下图所示。下列说法错误的是
溶液反应的探究实验如下图所示。下列说法错误的是
 溶液反应的探究实验如下图所示。下列说法错误的是
溶液反应的探究实验如下图所示。下列说法错误的是
|
| |
无明显现象 | 铝片表面产生细小气泡 | 出现白色浑浊,产生大量气泡(经检验为 和 和 ) ) |
A. 溶液中存在水解平衡 溶液中存在水解平衡 |
B.Ⅲ中产生的细小气泡为 ,原因为 ,原因为 溶液显碱性 溶液显碱性 |
C.Ⅲ→Ⅳ的现象可说明加热可促进 的水解 的水解 |
D.Ⅳ中现象的原因为 与 与 相互促进水解产生了 相互促进水解产生了 和 和 |
您最近半年使用:0次
名校
解题方法
4 . 对下列图示实验的描述正确的是
|
|
| A.所示的实验:制取FeCO3 | B.所示的实验:用NaOH溶液滴定盐酸 |
|
|
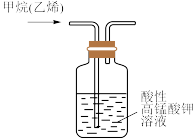
| C.用装置除去甲烷中的乙烯,以得到纯净的甲烷 | D.所示的实验:根据两烧瓶中气体颜色的变化(热水中变深、冰水中变浅)可以判断 的正反应是吸热反应 的正反应是吸热反应 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
5 . 25℃时,向0.1mol/L的氨水中加入少量氯化铵固体,当固体溶解后,测得溶液pH减小,主要原因是(填序号)_______ 。(单项)
A.氨水与氯化铵发生化学反应
B.氯化铵溶液水解显酸性,增加了c(H+)
C.铵根离子浓度增大,抑制了氨水的电离,使c(OH-)减小
A.氨水与氯化铵发生化学反应
B.氯化铵溶液水解显酸性,增加了c(H+)
C.铵根离子浓度增大,抑制了氨水的电离,使c(OH-)减小
您最近半年使用:0次
名校
6 . 已知 时部分弱电解质的电离平衡常数数据如表所示,回答下列问题:
时部分弱电解质的电离平衡常数数据如表所示,回答下列问题:
1.物质的量浓度均为 的下列四种溶液:
的下列四种溶液: 最大是___________。
最大是___________。
2.标准状况下将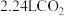 ,通入
,通入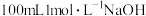 溶液中,用溶液中微粒的浓度符号完成下列等式:
溶液中,用溶液中微粒的浓度符号完成下列等式:
___________ 。
 时部分弱电解质的电离平衡常数数据如表所示,回答下列问题:
时部分弱电解质的电离平衡常数数据如表所示,回答下列问题:| 化学式 |  |  |  |
| 电离平衡常数 |  | 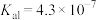  |  |
 的下列四种溶液:
的下列四种溶液: 最大是___________。
最大是___________。A. | B. | C. | D. |
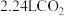 ,通入
,通入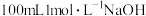 溶液中,用溶液中微粒的浓度符号完成下列等式:
溶液中,用溶液中微粒的浓度符号完成下列等式:
您最近半年使用:0次
7 . 实验是学习化学的基础。已知:[Co(H2O)6]2+呈粉红色,[CoCl4]2-呈蓝色,[ZnCl4]2-呈无色。根据实验操作及现象,下列结论中正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向FeCl3溶液中滴K3[Fe(CN)6]溶液,再加入少量铜粉 | 开始时无明显变化,加入铜粉后产生蓝色沉淀 | 氧化性:Fe3+>Cu2+ |
| B | 将C2H5Br与NaOH溶液共热。冷却后,加入AgNO3溶液 | 没有产生淡黄色沉淀 | C2H5Br没有发生水解反应 |
| C | 将CoCl2固体溶于水,加入适量浓盐酸后,再加入少量ZnCl2固体 | 溶液先由粉红色变为蓝色,再由蓝色变成无色 | 稳定性:[CoCl4]2->[ZnCl4]2- |
| D | 常温下,分别测定1mol/LCH3COONH4溶液和0.1mol/LCH3COONH4溶液的pH | pH都等于7 | 同温下,不同浓度CH3COONH4溶液中水的电离程度相同 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
8 .  用途广泛。某实验小组同学围绕
用途广泛。某实验小组同学围绕 开展如下实验活动。
开展如下实验活动。
 .配制溶液
.配制溶液
(1)配制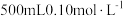 的
的 溶液,需要称量
溶液,需要称量 固体的质量为
固体的质量为___________  。
。
(2)上述配制溶液的过程中,用到的玻璃仪器除玻璃棒、量筒、胶头滴管外,还有___________ (填标号)。 .实验探究
.实验探究
探究温度对 溶液
溶液 的影响,进行如下实验(不考虑水的挥发)。
的影响,进行如下实验(不考虑水的挥发)。
(3) 溶液显碱性的原因是
溶液显碱性的原因是___________ (用离子方程式表示)。
(4)实验1中测得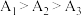 ,可知当
,可知当 时,
时, 溶液的
溶液的 随温度升高而减小,这主要是
随温度升高而减小,这主要是 改变与水解平衡移动共同作用的结果,其中
改变与水解平衡移动共同作用的结果,其中___________ 发挥主导作用。实验1中测得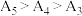 ,且当
,且当 时,实验过程中观察到有气泡产生。
时,实验过程中观察到有气泡产生。
(5)针对(4)中实验现象,小组同学继续开展探究。
查阅资料: 溶液中存在平衡:
溶液中存在平衡: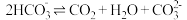 。
。
提出猜想:对于 溶液,当
溶液,当 时,该反应进行程度很小;当
时,该反应进行程度很小;当 时,该反应进行程度明显增大。
时,该反应进行程度明显增大。
实验验证:该小组同学设计如下方案进行实验,进一步验证猜想。补充表格内容。
实验结论:②根据实验1~3的结果,小组同学认为猜想成立,其判断依据是___________ 。
拓展总结:③ 溶液中存在
溶液中存在 的自偶电离平衡:
的自偶电离平衡: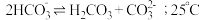 时,
时, 自偶电离的平衡常数为
自偶电离的平衡常数为___________ [保留两位有效数字;已知: 时,
时,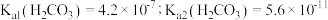 ]。当温度升高时,
]。当温度升高时, 更易分解,
更易分解, 从体系逸出,促进了
从体系逸出,促进了 在溶液中的分解。
在溶液中的分解。
(6)写出 在生产或生活中的一种应用
在生产或生活中的一种应用___________ 。
 用途广泛。某实验小组同学围绕
用途广泛。某实验小组同学围绕 开展如下实验活动。
开展如下实验活动。 .配制溶液
.配制溶液(1)配制
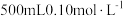 的
的 溶液,需要称量
溶液,需要称量 固体的质量为
固体的质量为 。
。(2)上述配制溶液的过程中,用到的玻璃仪器除玻璃棒、量筒、胶头滴管外,还有
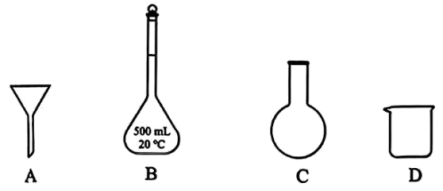
 .实验探究
.实验探究探究温度对
 溶液
溶液 的影响,进行如下实验(不考虑水的挥发)。
的影响,进行如下实验(不考虑水的挥发)。| 实验序号 | 操作 | 测试温度 |  |
| 1 | 采用水浴加热,将 溶液从 溶液从 持续升温至 持续升温至 ,每隔 ,每隔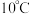 测量并记录溶液 测量并记录溶液 |  |  |
 |  | ||
 |  | ||
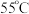 |  | ||
 | 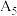 |
 溶液显碱性的原因是
溶液显碱性的原因是(4)实验1中测得
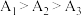 ,可知当
,可知当 时,
时, 溶液的
溶液的 随温度升高而减小,这主要是
随温度升高而减小,这主要是 改变与水解平衡移动共同作用的结果,其中
改变与水解平衡移动共同作用的结果,其中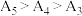 ,且当
,且当 时,实验过程中观察到有气泡产生。
时,实验过程中观察到有气泡产生。(5)针对(4)中实验现象,小组同学继续开展探究。
查阅资料:
 溶液中存在平衡:
溶液中存在平衡: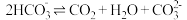 。
。提出猜想:对于
 溶液,当
溶液,当 时,该反应进行程度很小;当
时,该反应进行程度很小;当 时,该反应进行程度明显增大。
时,该反应进行程度明显增大。实验验证:该小组同学设计如下方案进行实验,进一步验证猜想。补充表格内容。
| 实验序号 | 操作 | 测试温度 |  |
| 2 | 采用水浴加热,① ,并记录溶液 ,并记录溶液 |  |  |
| 3 | 采用水浴加热,将 溶液从 溶液从 升温至 升温至 ,然后冷却至 ,然后冷却至 ,并记录溶液 ,并记录溶液 |  |  |
拓展总结:③
 溶液中存在
溶液中存在 的自偶电离平衡:
的自偶电离平衡: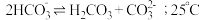 时,
时, 自偶电离的平衡常数为
自偶电离的平衡常数为 时,
时,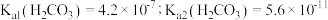 ]。当温度升高时,
]。当温度升高时, 更易分解,
更易分解, 从体系逸出,促进了
从体系逸出,促进了 在溶液中的分解。
在溶液中的分解。(6)写出
 在生产或生活中的一种应用
在生产或生活中的一种应用
您最近半年使用:0次
名校
解题方法
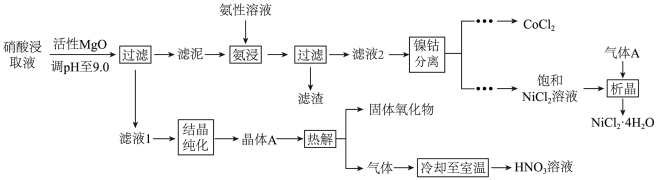
9 . 从处理后的矿石硝酸浸取液(含Ni2+、Co2+、Al3+、Mg2+)中,利用氨浸工艺可提取Ni、Co,并获得高附加值化工产品.工艺流程如下:
(1)Co位于元素周期表中的位置______________ (周期、族);
(2)“氨浸”时,由Co(OH)3转化为[Co(NH3)6]2+的离子方程式为______________________ ;
(3)(NH4)2CO3会使滤泥中的一种胶状物质转化为疏松分布的棒状颗粒物.滤渣的X射线衍射图谱中,出现了NH4Al(OH)2CO3的明锐衍射峰;
①NH4Al(OH)2CO3属于______________ (填“晶体”或“非晶体”);
②(NH4)2CO3提高了Ni、Co的浸取速率,其原因是______________________ ;
(4)“析晶”过程中通入的酸性气体A为______________ .
(5)①“结晶纯化”过程中,没有引入新物质,晶体A含6个结晶水,则所得HNO3溶液中n(HNO3)与n(H2O)的比值,理论上最高为______________ ;
②“热解”对于从矿石提取Ni、Co工艺的意义,在于可重复利用HNO3和___________ (填化学式)。
(1)Co位于元素周期表中的位置
(2)“氨浸”时,由Co(OH)3转化为[Co(NH3)6]2+的离子方程式为
(3)(NH4)2CO3会使滤泥中的一种胶状物质转化为疏松分布的棒状颗粒物.滤渣的X射线衍射图谱中,出现了NH4Al(OH)2CO3的明锐衍射峰;
①NH4Al(OH)2CO3属于
②(NH4)2CO3提高了Ni、Co的浸取速率,其原因是
(4)“析晶”过程中通入的酸性气体A为
(5)①“结晶纯化”过程中,没有引入新物质,晶体A含6个结晶水,则所得HNO3溶液中n(HNO3)与n(H2O)的比值,理论上最高为
②“热解”对于从矿石提取Ni、Co工艺的意义,在于可重复利用HNO3和
您最近半年使用:0次
10 . 下列对实验设计的评价错误的是
| 选项 | 实验设计 | 实验评价 |
| A. | 将含有二氧化硫的气体通入酸性高锰酸钾中,然后加入足量氯化钡溶液。通过测定白色沉淀的质量,可推算二氧化硫的物质的量 | 不合理,酸性高锰酸钾中的稀硫酸会与氯化钡产生沉淀 |
| B. | 实验室用浓硫酸和乙醇制取乙烯时,若要检验所得气体含有CH2=CH2,可将混合气体干燥后,通入溴的四氯化碳溶液中。若溶液褪色,则证明有乙烯 | 合理,混合气体中,只有乙烯可使溴的四氯化碳溶液褪色 |
| C. | 常温下,用pH计分别测定等体积 CH3COONH4溶液和 CH3COONH4溶液和 CH3COONH4溶液的pH.通过比较pH值,探究浓度对水的电离程度的影响 CH3COONH4溶液的pH.通过比较pH值,探究浓度对水的电离程度的影响 | 合理 |
| D. | 探究浓度对反应速率的影响,向2支盛有5mL不同浓度NaHSO3溶液的试管中同时加入2mL5%H2O2溶液。通过观察现象,探究浓度对反应速率的影响 | 不合理,该实验无明显现象 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2024-04-27更新
|
335次组卷
|
2卷引用:2024年辽宁省抚顺市普通高中高三下学期模拟考试化学试卷