名校
1 . 下表列出了13种元素在元素周期表中的位置:
(1)画出这13钟元素中,非金属性最强的元素的原子结构示意图:_______
(2)元素④⑤⑩分别和①形成的气体化合物中,最稳定的是(填化学式,下同)_______ ;⑦⑫⑬形成的简单离子半径由大到小的顺序是_______ 。
(3)这些元素的最高价氧化物对应的水化物中酸性最强的是_______ ,碱性最强的是_______ ,呈两性的氢氧化物是_______ 。写出三者之间两两反应的化学方程式:_______ 。
(4)可以用来证明⑦和⑧两种元素金属性强弱的实验是_______(填字母)
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 一 | ① | |||||||
| 二 | ② | ③ | ④ | ⑤ | ||||
| 三 | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | ⑪ | ||
| 四 | ⑫ | ⑬ |
(1)画出这13钟元素中,非金属性最强的元素的原子结构示意图:
(2)元素④⑤⑩分别和①形成的气体化合物中,最稳定的是(填化学式,下同)
(3)这些元素的最高价氧化物对应的水化物中酸性最强的是
(4)可以用来证明⑦和⑧两种元素金属性强弱的实验是_______(填字母)
| A.将在空气中放置已久的两种元素的块状单质分别放入水中 |
| B.将形状、大小相同的无氧化膜的两种元素的单质分别和同浓度同体积的盐酸反应 |
| C.将形状、大小相同的无氧化膜的两种元素的单质分别和温度相同的热水作用,并滴入酚酞 |
| D.比较两种元素氢化物的热稳定性 |
您最近一年使用:0次
名校
2 . 下表是元素周期表的一部分,用化学用语回答下列问题:
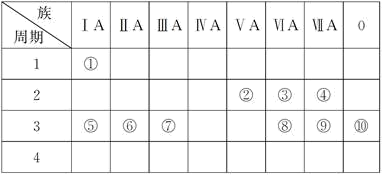
(1)请画出元素⑨阴离子的结构示意图:___________ 。
(2)③⑤⑧的原子半径由小到大的顺序为___________ (填元素符号)。
(3)⑤和⑦的最高价氧化物对应水化物的碱性强弱为___________ >___________ (填化学式)。
(4)③⑤两种元素的原子按1∶1组成的常见化合物的电子式为___________ 。
(5)用电子式表示⑥和⑨形成的化合物的过程:______________________ 。

(1)请画出元素⑨阴离子的结构示意图:
(2)③⑤⑧的原子半径由小到大的顺序为
(3)⑤和⑦的最高价氧化物对应水化物的碱性强弱为
(4)③⑤两种元素的原子按1∶1组成的常见化合物的电子式为
(5)用电子式表示⑥和⑨形成的化合物的过程:
您最近一年使用:0次
2021-06-01更新
|
176次组卷
|
5卷引用:辽宁省沈阳铁路实验中学2018-2019学年高一下学期4月月考化学试题
3 . A、B、C、D、E是前四周期的元素。A、B、C同周期,C、D同主族且原子半径C>D,A的原子结构示意图为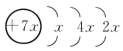 ,B是同周期第一电离能最小的元素,C的最外层有三个未成对电子,E对应的单质是目前用量最大的金属。回答下列问题:
,B是同周期第一电离能最小的元素,C的最外层有三个未成对电子,E对应的单质是目前用量最大的金属。回答下列问题:
(1)写出下列元素的符号:A___________ ,B___________ ,C___________ ,D___________ 。
(2)用元素符号表示D所在周期第一电离能最大的元素是___________ ,电负性最大的元素是___________ 。
(3)E原子价电子排布式是___________ ,E元素在周期表的位置是___________ ,则E元素在___________ 区。
(4)基态D原子的价电子排布图___________ ,元素D的原子最外层共有___________ 种不同运动状态的电子。基态原D子电子占据最高能级的电子云轮廓图为___________ 形。
(5)A、B、C三者原子半径由大到小的顺序为___________ (用元素符号回答)
(6)某同学推断Mg的基态原子的轨道表示式为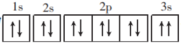 ,该同学所画的轨道表示式违背了
,该同学所画的轨道表示式违背了___________ 。
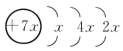 ,B是同周期第一电离能最小的元素,C的最外层有三个未成对电子,E对应的单质是目前用量最大的金属。回答下列问题:
,B是同周期第一电离能最小的元素,C的最外层有三个未成对电子,E对应的单质是目前用量最大的金属。回答下列问题:(1)写出下列元素的符号:A
(2)用元素符号表示D所在周期第一电离能最大的元素是
(3)E原子价电子排布式是
(4)基态D原子的价电子排布图
(5)A、B、C三者原子半径由大到小的顺序为
(6)某同学推断Mg的基态原子的轨道表示式为
 ,该同学所画的轨道表示式违背了
,该同学所画的轨道表示式违背了
您最近一年使用:0次
2021-05-06更新
|
313次组卷
|
4卷引用:辽宁省沈阳市辽中区第一私立高级中学2023-2024学年高二上学期1月期末化学试题
辽宁省沈阳市辽中区第一私立高级中学2023-2024学年高二上学期1月期末化学试题甘肃省酒泉市青海油田第一中学2020-2021学年高二下学期期中考试化学试题(已下线)作业02 原子结构与元素的性质-2021年高二化学暑假作业(人教版2019)黑龙江省牡丹江市海林市朝鲜族中学2021-2022学年高二下学期第一次月考化学试题
名校
4 . 元素周期表短周期的一部分如图所示。回答下列问题:
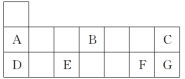
(1)A的元素符号为__________ 。
(2)B位于第二周期第__________ 族,DC为__________ (填“离子”或“共价”)化合物。
(3)G的最高价氧化物的化学式为__________ 。
(4)A、B、D原子半径由大到小的顺序为______________ (填化学式,下同),C、F、G最简单氢化物热稳定性由弱到强的顺序为__________ 。
(5)E的单质与D的最高价氧化物对应的水化物反应的离子方程式为___________________ 。

(1)A的元素符号为
(2)B位于第二周期第
(3)G的最高价氧化物的化学式为
(4)A、B、D原子半径由大到小的顺序为
(5)E的单质与D的最高价氧化物对应的水化物反应的离子方程式为
您最近一年使用:0次
2021-03-09更新
|
287次组卷
|
4卷引用:辽宁省朝阳市凌源市2021-2022学年高一下学期第二次联考化学试题
5 . 下表是周期表中的一部分,数字①~⑧代表八种常见元素在周期表中的位置。

请回答下列问题:
(1)上述元素中化学性质最不活泼的是___ (填元素符号)。写出元素③在周期表中位置___ 。
(2)①、④、⑦三种元素的最高价氧化物的水化物碱性由强到弱的顺序为___ 。(用化学式表示)
(3)非金属性强弱顺序:⑤___ ⑧(填“<”,“>”或“=”),验证该结论的方法为___ (用离子方程式表示)。
(4)②、③、④元素原子半径由大到小的顺序为___ 。(用元素符号表示)
(5)关于元素周期表、周期律,以下说法正确的是___ 。
A.在金属和非金属分界处可以找到半导体材料
B.在过渡元素中寻找制造催化剂和耐高温、耐腐蚀合金的元素
C.通常农药所含有的元素位于元素周期表左下方区域
D.稀有气体原子都满足8电子稳定结构
(6)②的常见单质的电子式___ ;⑦和⑧形成化合物的电子式___ 。

请回答下列问题:
(1)上述元素中化学性质最不活泼的是
(2)①、④、⑦三种元素的最高价氧化物的水化物碱性由强到弱的顺序为
(3)非金属性强弱顺序:⑤
(4)②、③、④元素原子半径由大到小的顺序为
(5)关于元素周期表、周期律,以下说法正确的是
A.在金属和非金属分界处可以找到半导体材料
B.在过渡元素中寻找制造催化剂和耐高温、耐腐蚀合金的元素
C.通常农药所含有的元素位于元素周期表左下方区域
D.稀有气体原子都满足8电子稳定结构
(6)②的常见单质的电子式
您最近一年使用:0次
名校
解题方法
6 . 1869年,俄国化学家门捷列夫制作出了第一张元素周期表,揭示了化学元素间的内在联系,成为化学发展史上的重要里程碑之一。元素周期表与元素周期律在化学学习研究中有很重要的作用。
(1)下表是元素周期表的一部分
i.元素④的过氧化物的电子式为______ ,其最高价氧化物对应的水化物含有的化学键类型为______ ,⑩元素最高价氧化物对应的水化物的化学式是______ 。
ii.元素①、②、③的简单氢化物的稳定性最强的是______ (用化学式表示,下同),②、⑧简单氢化物熔点高的是______ ,④、⑤最高价氧化物的水化物碱性更强的是______ ,④、⑤、⑧、⑨的简单离子半径由大到小的顺序______ 。
(2)最近,德国科学家实现了铷原子气体超流体态与绝缘态的可逆转换,该成果将在量子计算机研究方面带来重大突破。已知铷是37号元素,相对原子质量是85。
i.铷在元素周期表中的位置______ 。
ii.关于铷的下列说法中不正确的是______ (填序号)。
a.与水反应比钠更剧烈
b.Rb2O在空气中易吸收水和二氧化碳
c.Rb2O2与水能剧烈反应并释放出O2
d.单质具有很强的氧化性
e.RbOH的碱性比同浓度的NaOH弱
(1)下表是元素周期表的一部分
| 主族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ③ | |||||
| 三 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ||
| 四 | ⑩ |
i.元素④的过氧化物的电子式为
ii.元素①、②、③的简单氢化物的稳定性最强的是
(2)最近,德国科学家实现了铷原子气体超流体态与绝缘态的可逆转换,该成果将在量子计算机研究方面带来重大突破。已知铷是37号元素,相对原子质量是85。
i.铷在元素周期表中的位置
ii.关于铷的下列说法中不正确的是
a.与水反应比钠更剧烈
b.Rb2O在空气中易吸收水和二氧化碳
c.Rb2O2与水能剧烈反应并释放出O2
d.单质具有很强的氧化性
e.RbOH的碱性比同浓度的NaOH弱
您最近一年使用:0次
2021-01-07更新
|
1365次组卷
|
3卷引用:辽宁省五校联考2020-2021学年高一上学期期末考试化学试题
7 . 下图是元素周期表的一部分(号元素 ,用化学用语回答下列问题:
,用化学用语回答下列问题:

(1)D的基态电子排布式可简写为:___________ ;H代表的元素在周期表中的位置是___________ 。
(2)、G、J、K、M对应的简单离子的半径由大到小的顺序是___________ (用离子符号表示)
(3)在所列元素中,电负性最大的元素是___________ (填元素符号)。
(4)已知某原子的各级电离能如下:I1=577kJ/mol,I2=1817kJ/mol,I3=2745kJ/mol,I4=11578kJ/mol,则该原子在化合物中表现的化合价为___________
(5)元素周期表中位于斜对角线的两种元素及其性质十分相似,称之为对角线规则。根据元素周期表对角线规则,金属铍Be与铝单质及其化合物性质十分相似。Be(OH)2和Mg(OH)2可用试剂NaOH溶液鉴别。涉及的化学方程式为:___________ 。
 ,用化学用语回答下列问题:
,用化学用语回答下列问题:
(1)D的基态电子排布式可简写为:
(2)、G、J、K、M对应的简单离子的半径由大到小的顺序是
(3)在所列元素中,电负性最大的元素是
(4)已知某原子的各级电离能如下:I1=577kJ/mol,I2=1817kJ/mol,I3=2745kJ/mol,I4=11578kJ/mol,则该原子在化合物中表现的化合价为
(5)元素周期表中位于斜对角线的两种元素及其性质十分相似,称之为对角线规则。根据元素周期表对角线规则,金属铍Be与铝单质及其化合物性质十分相似。Be(OH)2和Mg(OH)2可用试剂NaOH溶液鉴别。涉及的化学方程式为:
您最近一年使用:0次
2020-12-15更新
|
1027次组卷
|
5卷引用:辽宁省锦州市义县高级中学2020-2021学年高二12月月考化学试题
辽宁省锦州市义县高级中学2020-2021学年高二12月月考化学试题(已下线)练习18 原子结构与元素的性质-2020-2021学年【补习教材·寒假作业】高二化学(人教版)(已下线)1.2 原子结构与元素的性质(C级检测练)-2020-2021学年高二化学章节分层检测ABC(人教版2019选择性必修2)选择性必修第二册 期末学业水平检测江苏省盐城第一中学2023-2024学年高二上学期第二次学情调研考试(期中)化学(选修)试卷
名校
8 . 下表列出了①~⑥六种元素在周期表中的位置:

请按要求回答下列问题。
(1)元素②的单质电子式是___ 。
(2)元素⑤的原子结构示意图是___ 。
(3)这六种元素中,位于第三周期且原子半径最小的是___ (填元素符号)。
(4)这六种元素的最高价氧化物中,属于两性氧化物的是___ (填化学式)。
(5)这六种元素的最高价氧化物对应的水化物中,属于二元强酸的是___ (填化学式)。
(6)在盛有水的小烧杯中加入元素③的单质,发生反应的离子方程式为___ ;向上述反应后的溶液中再加入元素④的单质,发生反应的化学方程式为___ 。

请按要求回答下列问题。
(1)元素②的单质电子式是
(2)元素⑤的原子结构示意图是
(3)这六种元素中,位于第三周期且原子半径最小的是
(4)这六种元素的最高价氧化物中,属于两性氧化物的是
(5)这六种元素的最高价氧化物对应的水化物中,属于二元强酸的是
(6)在盛有水的小烧杯中加入元素③的单质,发生反应的离子方程式为
您最近一年使用:0次
9 . 下表列出了A~R9种元素在周期表中的位置:
(1)在这9种元素中化学性质最不活泼的是_____
A.E B.D C.R D.H
(2)A、B、C三种元素按原子半径由大到小的顺序排列为_____
A.r(A)>r(B)>r(C) B.r(B)>r(A)>r(C)
C.r(A)>r(C)>r(B) D.r(B)>r(C)>r(A)
(3)F元素氢化物在常温下跟A发生反应所得溶液的pH______ 7
A.< B.> C.= D.无法确定
(4)在此周期表中,9种元素所形成的最高价氧化物对应的水化物,其中酸性最强和碱性最强的化学式是_____
A.H2SO4,NaOH B.H2SO4,KOH
C.HClO4,NaOH D.HClO4,KOH
(5)G元素和H元素两者核电荷数之差是_____
A.8 B.10 C.18 D.26
(6)H元素和A元素形成化合物的化学式以及高温灼烧该化合物时,火焰颜色____
A.NaBr 黄 B.NaCl 黄 C.KBr 紫 D.KCl 紫
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 2 | E | F | ||||||
| 3 | A | C | D | G | R | |||
| 4 | B | H |
A.E B.D C.R D.H
(2)A、B、C三种元素按原子半径由大到小的顺序排列为
A.r(A)>r(B)>r(C) B.r(B)>r(A)>r(C)
C.r(A)>r(C)>r(B) D.r(B)>r(C)>r(A)
(3)F元素氢化物在常温下跟A发生反应所得溶液的pH
A.< B.> C.= D.无法确定
(4)在此周期表中,9种元素所形成的最高价氧化物对应的水化物,其中酸性最强和碱性最强的化学式是
A.H2SO4,NaOH B.H2SO4,KOH
C.HClO4,NaOH D.HClO4,KOH
(5)G元素和H元素两者核电荷数之差是
A.8 B.10 C.18 D.26
(6)H元素和A元素形成化合物的化学式以及高温灼烧该化合物时,火焰颜色
A.NaBr 黄 B.NaCl 黄 C.KBr 紫 D.KCl 紫
您最近一年使用:0次
2020-07-29更新
|
110次组卷
|
2卷引用:辽宁省阜新市第二高级中学2019-2020学年高一下学期期末考试化学试题
解题方法
10 . 根据元素周期表1-18号元素的性质和递变规律,回答下列问题。
(1)属于金属元素的有___ 种,金属性最强的元素与氧反应生成的化合物有___ 、___ (填两种化合物的化学式)。
(2)属于稀有气体的是___ (填元素符号,下同)。
(3)第三周期中,原子半径最大的是___ (稀有气体除外)。
(4)推测Si、N最简单氢化物的稳定性:___ 大于___ (填化学式)。
(1)属于金属元素的有
(2)属于稀有气体的是
(3)第三周期中,原子半径最大的是
(4)推测Si、N最简单氢化物的稳定性:
您最近一年使用:0次



