1 . 下表是元素周期表的一部分。表中所列字母分别代表一种元素。
回答下列问题:
(1)j在元素周期表中的位置是______ 。
(2)e、h、m形成的简单离子其半径由大到小的顺序为________ 。(填写离子符号)
(3)n与g形成的化合物为______ (填写化学式,下同),将该化合物进行焰色反应,火焰呈______ 色。
(4)k、1形成的最高价氧化物的水化物,酸性由强到弱的顺序为______ 。
(5)g的最高价氧化物对应的水化物与i的最高价氧化物对应的水化物反应的离子方程式为______ 。
(6)某同学欲探究元素性质递变规律与原子结构的关系,进行如下实验:
(实验操作)取已除去氧化膜且面积相等的镁条和铝条,分别投入2mL1mol/L盐酸中;
(实验现象)镁与酸反应比铝更剧烈;
(实验结论)①金属性:Mg_____ Al(选填“>”或“<”);
(查阅资料)原子半径(nm)Mg:0.160 Al:0.143;
(思考)②利用元素周期律对上述实验结论进行解释______ 。
| a | b | |||||||
| c | d | e | f | |||||
| g | h | i | j | k | l | m | ||
| n |
(1)j在元素周期表中的位置是
(2)e、h、m形成的简单离子其半径由大到小的顺序为
(3)n与g形成的化合物为
(4)k、1形成的最高价氧化物的水化物,酸性由强到弱的顺序为
(5)g的最高价氧化物对应的水化物与i的最高价氧化物对应的水化物反应的离子方程式为
(6)某同学欲探究元素性质递变规律与原子结构的关系,进行如下实验:
(实验操作)取已除去氧化膜且面积相等的镁条和铝条,分别投入2mL1mol/L盐酸中;
(实验现象)镁与酸反应比铝更剧烈;
(实验结论)①金属性:Mg
(查阅资料)原子半径(nm)Mg:0.160 Al:0.143;
(思考)②利用元素周期律对上述实验结论进行解释
您最近一年使用:0次
2022-01-14更新
|
785次组卷
|
4卷引用:【2023】【高一下】【其他】【杭高卷四-期中复习卷】【高中化学】【刘尼尼收集】
(已下线)【2023】【高一下】【其他】【杭高卷四-期中复习卷】【高中化学】【刘尼尼收集】湖南省怀化市2021-2022学年高一上学期期末考试化学试题(已下线)第四章 物质结构 元素周期律(B卷)-2021-2022学年高一化学优选好题单元专题双测卷(人教版2019必修第一册)湖北省孝感市新高考联考协作体2022-2023学年高二上学期9月联考化学试题
2021高一·全国·专题练习
名校
2 . 下表是元素周期表的一部分,请用化学符号回答有关问题:
(1)表中化学性质最不活泼的元素,其原子结构示意图为___________ 。
(2)②、⑧、⑨、⑩四种元素的简单气态氢化物稳定性由强到弱的顺序是___________ ,最高价氧化物的水化物中酸性最强的是___________ 。
(3)第三周期元素形成的简单离子中半径最小的微粒是___________ ,写出该元素的单质分别与⑥、⑩最高价氧化物的水化物反应的离子方程式___________ 、___________ 。
| 主族 周期 | IA | ⅡA | ⅢA | ⅣA | VA | ⅥA | ⅦA | 0 |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | ⑤ | ||||
| 3 | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(1)表中化学性质最不活泼的元素,其原子结构示意图为
(2)②、⑧、⑨、⑩四种元素的简单气态氢化物稳定性由强到弱的顺序是
(3)第三周期元素形成的简单离子中半径最小的微粒是
您最近一年使用:0次
2021-12-06更新
|
1082次组卷
|
4卷引用:浙江省舟山市舟山中学2021-2022学年高一下学期开学考试化学试题
浙江省舟山市舟山中学2021-2022学年高一下学期开学考试化学试题(已下线)专题4.2.1 元素性质的周期性变化规律(备作业)-【上好课】2021-2022学年高一化学同步备课系列(人教版2019必修第一册)山东省“学情空间”区域教研共同体2022-2023学年高一上学期12月联考(人教版) 化学试题安徽省芜湖市第一中学2022-2023学年高一上学期选科分班考试化学试题
名校
解题方法
3 . 有7种短周期元素,其原子半径及主要化合价如下:
完成下列填空:
(1)A在元素周期表中的位置是_______ 。
(2)上述7种元素形成的简单离子中,离子半径最大是_______ (用离子符号表示)
(3)甲是由G、H两种元素组成的18e-分子,用电子式表示其形成过程_______ 。
(4)用一个化学方程式表示E元素的非金属性比D强_______ 。
| 元素代号 | A | B | D | E | F | G | H |
| 原子半径/nm | 0.186 | 0.143 | 0.104 | 0.099 | 0.070 | 0.066 | 0.032 |
| 主要化合价 | +1 | +3 | +6,-2 | +7,-1 | +5,-3 | -2 | +1 |
完成下列填空:
(1)A在元素周期表中的位置是
(2)上述7种元素形成的简单离子中,离子半径最大是
(3)甲是由G、H两种元素组成的18e-分子,用电子式表示其形成过程
(4)用一个化学方程式表示E元素的非金属性比D强
您最近一年使用:0次
20-21高一下·浙江·阶段练习
解题方法
4 . 按要求回答下列问题:
(1)异丁烷的结构简式为___________ 。
(2)地壳中含量最高的金属元素在元素周期表中的位置___________ 。
(3)NaOH的电子式为___________ 。
(4)二氧化氮溶于水时生成硝酸和一氧化氮,工业上利用这一原理生成硝酸。写出该反应的化学方程式___________ 。
(1)异丁烷的结构简式为
(2)地壳中含量最高的金属元素在元素周期表中的位置
(3)NaOH的电子式为
(4)二氧化氮溶于水时生成硝酸和一氧化氮,工业上利用这一原理生成硝酸。写出该反应的化学方程式
您最近一年使用:0次
20-21高一下·浙江·阶段练习
解题方法
5 . (1)①写出52号元素在元素周期表中的位置___ 。
②用电子式表示MgCl2的形成过程___ 。
(2)现在需配制0.1mol/L的Na2CO3溶液480mL,需要用托盘天平称量Na2CO3固体__ g。
(3)写出碳酸钠溶液和过量盐酸反应的离子方程式___ 。
②用电子式表示MgCl2的形成过程
(2)现在需配制0.1mol/L的Na2CO3溶液480mL,需要用托盘天平称量Na2CO3固体
(3)写出碳酸钠溶液和过量盐酸反应的离子方程式
您最近一年使用:0次
20-21高一下·浙江·阶段练习
解题方法
6 . 1869年,俄国化学家门捷列夫制作出了第一张元素周期表,揭示了化学元素间的内在联系,成为化学发展史上的重要里程碑之一。下表是元素周期表的一部分:
注意:用元素符号或化学式填空。
(1)①到⑩号元素中,所形成的氢化物最稳定的是___________ ,最高价氧化物对应的水化物酸性最强的是___________ 。③号元素在元素周期表中的位置是___________ 。
(2)实验室制备②的气态氢化物的化学方程式为___________ 。
(3)元素⑤的最高价氧化物对应水化物含有的化学键类型为:___________ (选填“离子键”“极性键”“非极性键”),其与⑦的最高价氧化物所对应的水化物能相互反应,反应的离子方程式是:___________ 。
(4)下列说法正确的是___________
A.碱金属单质的金属性很强,均易与氧气发生反应,加热时生成的氧化物为R2O
B.一定条件下,随着核电荷数的增加,卤素单质与H2化合越来越难
C.随着核电荷数的增加,卤族单质的氧化性逐渐增强
D.周期表七行七个周期,18列16族
| ① | ||||||||
| ② | ③ | ④ | ||||||
| ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ||||
| 过渡元素 | ⑩ |
注意:用元素符号或化学式填空。
(1)①到⑩号元素中,所形成的氢化物最稳定的是
(2)实验室制备②的气态氢化物的化学方程式为
(3)元素⑤的最高价氧化物对应水化物含有的化学键类型为:
(4)下列说法正确的是
A.碱金属单质的金属性很强,均易与氧气发生反应,加热时生成的氧化物为R2O
B.一定条件下,随着核电荷数的增加,卤素单质与H2化合越来越难
C.随着核电荷数的增加,卤族单质的氧化性逐渐增强
D.周期表七行七个周期,18列16族
您最近一年使用:0次
21-22高一上·浙江·阶段练习
7 . 1991年,我国著名化学家张青莲精确地测定了铟(In)、锑(Sb)等十种元素的相对原子质量,其中准确测得In的相对原子质量被国际原子量委员会采用为新的标准值。如图是元素周期表的一部分,回答下列问题。
(1)请将In的原子结构示意图补全:
___________ ,Sb的最高正化合价为___________ 。
(2)根据元素周期律,下列关于上表中元素推断正确的是___________ (填序号)。
A.非金属性最强的元素是氟元素
B.原子半径大小: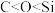
C.氢化物的稳定性: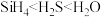
D.可在图中分界线(虚线部分)附近寻找优良的催化剂、合金材料等
(3)写出由上述元素中三个原子组成的直线形分子的结构式:___________ 。
(4)判断非金属强弱:Cl___________ Br(用<、=、>来表示),请用一条化学方程式来解释___________ 。
B | C | N | O | F |
Al | Si | P | S | Cl |
Ga | Ge | As | Se | Br |
In | Sn | Sb | Te | I |
(1)请将In的原子结构示意图补全:

(2)根据元素周期律,下列关于上表中元素推断正确的是
A.非金属性最强的元素是氟元素
B.原子半径大小:
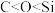
C.氢化物的稳定性:
D.可在图中分界线(虚线部分)附近寻找优良的催化剂、合金材料等
(3)写出由上述元素中三个原子组成的直线形分子的结构式:
(4)判断非金属强弱:Cl
您最近一年使用:0次
20-21高一下·浙江金华·开学考试
解题方法
8 . 根据表中的①~⑧种元素在周期表中的位置,回答下列问题。
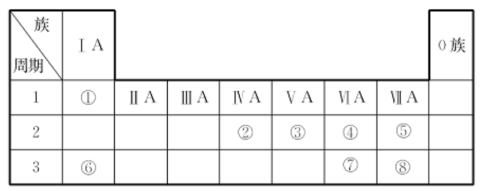
(1)元素⑥、⑦形成的简单的离子,半径大的是_______ (填离子符号)
(2)用电子式表示元素①和⑧的化合物的形成过程:_______ 。
(3)元素②的一种核素可以用来考古,请写该核素的中子数是_______ 。
(4)元素⑤、⑧的简单气态氢化物较稳定的是_______ (填化学式)。

(1)元素⑥、⑦形成的简单的离子,半径大的是
(2)用电子式表示元素①和⑧的化合物的形成过程:
(3)元素②的一种核素可以用来考古,请写该核素的中子数是
(4)元素⑤、⑧的简单气态氢化物较稳定的是
您最近一年使用:0次
21-22高一上·浙江·阶段练习
9 . 下表是元素周期表的一部分,针对表中的①~⑥几种元素,回答以下问题:
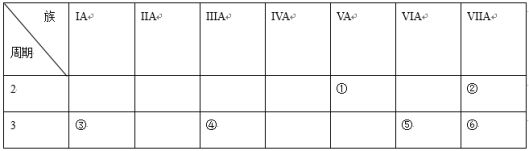
(1)位于第三周期且原子半轻最小元素的原子结构示意图_______ ,其单质与水的化学反应为_______ 。
(2)①②④元素原子形成简单离子的离子半径由大到小的顺序为_______ (填离子符号)。
(3)③④的最高价的氧化物对应的水化物的溶液发生的离子反应为_______ 。
(4)元素③与元素④相比,金属性较强的是_______ (填元素符号),下列表述中能证明这一事实的是_______ (填字母)。
a. ③单质的熔点比④单质低
b. ③单质与水反应比④单质剧烈
c. ③最高价氧化物对应的水化物的碱性比④强
d. ③的化合价比④低
(5)比较⑤⑥气态氢化物的稳定性:_______ >_______ (填化学式),除了可以通过比较⑤⑥气态氢化物的稳定性来验证⑤、⑤的非金属性外,请你再设计一个简单的实验,来验证元素⑤与⑥的非金属性强弱:_______ 。

(1)位于第三周期且原子半轻最小元素的原子结构示意图
(2)①②④元素原子形成简单离子的离子半径由大到小的顺序为
(3)③④的最高价的氧化物对应的水化物的溶液发生的离子反应为
(4)元素③与元素④相比,金属性较强的是
a. ③单质的熔点比④单质低
b. ③单质与水反应比④单质剧烈
c. ③最高价氧化物对应的水化物的碱性比④强
d. ③的化合价比④低
(5)比较⑤⑥气态氢化物的稳定性:
您最近一年使用:0次
21-22高一上·浙江·阶段练习
10 . 下表是元素周期表的一部分,根据表中8种元素,用元素符号等化学用语填空。
(1)①~⑧元素中,金属性最强的是_________ (写元素符号)。
(2)①~⑧元素中,画出最稳定的元素的原子结构示意图_________ 。
(3)①~⑧元素中,最高价氧化物水化物酸性最强的物质是__________ (写化学式)。
(4)②、③、⑥所形成的简单离子,其半径由大到小的顺序是_________ (写离子符号)
| ⅠA族 | ⅡA族 | ⅢA族 | ⅣA族 | ⅤA族 | ⅥA族 | ⅦA族 | 0族 |
2 | ① | ② | ||||||
3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
(1)①~⑧元素中,金属性最强的是
(2)①~⑧元素中,画出最稳定的元素的原子结构示意图
(3)①~⑧元素中,最高价氧化物水化物酸性最强的物质是
(4)②、③、⑥所形成的简单离子,其半径由大到小的顺序是
您最近一年使用:0次