名校
1 . 短周期主族元素A、B、C、D、E、F在元素周期表中的位置如下图所示,其中元素F是同周期元素原子半径最小的;请回答下列问题:
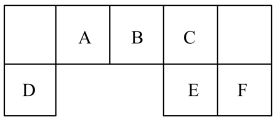
(1)F在周期表中的位置___________ ;
(2)比较B、C、D元素简单离子半径的大小顺序___________ (填写离子符号);
(3)F的氢化物与其最高价氧化物的水化物的钾盐共热能发生反应,生成一种气体单质,反应的化学方程式为_______________________ ;
(4)要比较元素E与F非金属性的强弱,正确合理的实验操作与现象是______________________ ;
(5)用高能射线照射液态水时,一个水分子能释放一个电子,同时产生一种具有较强氧化性阳离子,该阳离子中存在的化学键有______ ,并写出该阳离子与E的氢化物的水溶液反应的离子方程式________________ 。

(1)F在周期表中的位置
(2)比较B、C、D元素简单离子半径的大小顺序
(3)F的氢化物与其最高价氧化物的水化物的钾盐共热能发生反应,生成一种气体单质,反应的化学方程式为
(4)要比较元素E与F非金属性的强弱,正确合理的实验操作与现象是
(5)用高能射线照射液态水时,一个水分子能释放一个电子,同时产生一种具有较强氧化性阳离子,该阳离子中存在的化学键有
您最近一年使用:0次
名校
2 . 肼(N2H4)是重要的化工原料,能与水、乙醇等混溶;它是一种二元弱碱,在水中的电离方式与氨相似,室温下电离常数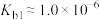 ;在碱性溶液中,N2H4是强还原剂。
;在碱性溶液中,N2H4是强还原剂。
(1)写出N元素在元素周期表中的位置___________ 。
(2)写出N2H4与过量硫酸反应形成的酸式盐的化学式___________ 。
(3)N2H4可通过NH3和NaClO反应制得,总反应主要分为两步,
已知第一步: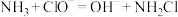
①写出第二步反应的离子方程式___________ 。
②请设计实验,检验总反应中产物的主要阴离子(假设反应物完全反应)___________ 。
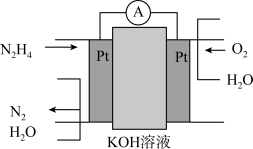
(4)N2H4是一种高能燃料,可用于燃料电池,原理如图,电池的负极反应式为___________ 。
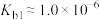 ;在碱性溶液中,N2H4是强还原剂。
;在碱性溶液中,N2H4是强还原剂。(1)写出N元素在元素周期表中的位置
(2)写出N2H4与过量硫酸反应形成的酸式盐的化学式
(3)N2H4可通过NH3和NaClO反应制得,总反应主要分为两步,
已知第一步:
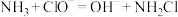
①写出第二步反应的离子方程式
②请设计实验,检验总反应中产物的主要阴离子(假设反应物完全反应)
(4)N2H4是一种高能燃料,可用于燃料电池,原理如图,电池的负极反应式为
您最近一年使用:0次
2023-12-23更新
|
132次组卷
|
2卷引用:浙江省舟山中学2023-2024学年高二上学期11月期中考试化学试题
22-23高一下·浙江·期中
3 . 按要求完成下列填空:
(1)①写出乙烯的电子式_______ ;
②黄铁矿主要成分的化学式_______ 。
(2)写出Si元素在元素周期表中的位置_______ 。
(3)在加热条件下木炭与浓硫酸反应的化学方程式为_______ 。
(1)①写出乙烯的电子式
②黄铁矿主要成分的化学式
(2)写出Si元素在元素周期表中的位置
(3)在加热条件下木炭与浓硫酸反应的化学方程式为
您最近一年使用:0次
解题方法
4 . 按要求回答下列问题。
(1)写出漂白粉有效成分的化学式___________ 。
(2)某元素的一种核素可用于文物的年代测定,写出该元素在周期表中的位置___________ 。
(3)写出稀盐酸与石灰石反应的离子方程式___________ 。
(4)写出红热的铁与水蒸气反应的化学方程式___________ 。
(1)写出漂白粉有效成分的化学式
(2)某元素的一种核素可用于文物的年代测定,写出该元素在周期表中的位置
(3)写出稀盐酸与石灰石反应的离子方程式
(4)写出红热的铁与水蒸气反应的化学方程式
您最近一年使用:0次
23-24高一上·浙江·期末
解题方法
5 . 回答下列问题:
(1)小苏打的化学式:___________ ,CO2的电子式:___________ 。
(2)请写出红热的铁与水蒸气反应的化学方程式:___________ 。
(3)铯和钠属于同主族元素,铯原子核外有6个电子层,铯在元素周期表中的位置___________ 。
(1)小苏打的化学式:
(2)请写出红热的铁与水蒸气反应的化学方程式:
(3)铯和钠属于同主族元素,铯原子核外有6个电子层,铯在元素周期表中的位置
您最近一年使用:0次
23-24高二上·浙江杭州·期末
6 . 氧(O)、硫(S)、硒、碲(Te)、钋(Po)、鉝(Lv)为元素周期表中原子序数依次增大的同主族元素。回答下列问题:
(1)硒_______ (填元素符号);鉝(Lv)_______ (填原子序数);
(2)碲有多种同位素原子,其中的核素是128 Te,它的中子数为_______ ;
(3)还原性:H2O_______ H2S (填">"或"<")
(4)氧常见的氢化物有两种,双氧水(H2O2)和水。双氧水在实验室和实际生产生活都有重要的作用。
①写出H2O2的电子式:_______ 。
②金属Al加到双氧水与NaOH的混合溶液中,金属Al溶解,写出反应的离子方程式_______ ;
③S2Cl2有类似于H2O2的性质,该物质遇水不稳定,生成一种黄色沉淀和无色有刺激性气味的气体,还得到一种强酸溶液,试写出该过程的反应方程式_______ ;
④实验室制氧气有多种方法,下列反应可以用来实验室制氧气的是_______ 。
A.氯酸钾加少量高锰酸钾受热分解
B.双氧水加二氧化锰
C.过氧化钠加水
D.过氧化钠中通二氧化碳
E.次氯酸受热分解
(1)硒
(2)碲有多种同位素原子,其中的核素是128 Te,它的中子数为
(3)还原性:H2O
(4)氧常见的氢化物有两种,双氧水(H2O2)和水。双氧水在实验室和实际生产生活都有重要的作用。
①写出H2O2的电子式:
②金属Al加到双氧水与NaOH的混合溶液中,金属Al溶解,写出反应的离子方程式
③S2Cl2有类似于H2O2的性质,该物质遇水不稳定,生成一种黄色沉淀和无色有刺激性气味的气体,还得到一种强酸溶液,试写出该过程的反应方程式
④实验室制氧气有多种方法,下列反应可以用来实验室制氧气的是
A.氯酸钾加少量高锰酸钾受热分解
B.双氧水加二氧化锰
C.过氧化钠加水
D.过氧化钠中通二氧化碳
E.次氯酸受热分解
您最近一年使用:0次
23-24高二上·浙江·期末
解题方法
7 . 为纪念元素周期表诞生150周年,IUPAC等向世界介绍118位优秀青年化学家,并形成一张“青年化学家元素周期表”。中国学者雷晓光、姜雪峰、刘庄分别成为“N、S、Hg”元素的代言人。回答下列问题:
(1)据汞的原子结构示意图,汞在第_______ 周期。

(2)硒(Se)与硫位于同主族,均是生命必需元素。下列推断不正确的是_______ 。
a.硒元素的最低负化合价为-2
b.二氧化硒(SeO2)具有还原性
c.硒的氧化物对应的水化物属于强酸
(3)氮是自然界各种生物体生命活动不可缺少的重要元素,磷(P)、砷(As)也是氮族元素。
①砷有多种同位素原子,其中稳定的核素是75As,它的中子数为_______ 。
②已知NH4Cl与PH4I的性质相似,则对PH4I性质的推测不正确的是_______ (填序号)。
a.含有离子键和共价键 b.能与NaOH溶液反应
c.与NH4Cl加热充分分解产物的种类完全一样
③下列关于第VA族元素及其化合物的说法不正确的是_______ (填字母)。
a.热稳定性:NH3>PH3
b.酸性:HNO3>H3AsO4
c. As的氧化物的水化物是强碱
d.形成的简单离子半径随着原子序数递增而增大
(1)据汞的原子结构示意图,汞在第

(2)硒(Se)与硫位于同主族,均是生命必需元素。下列推断不正确的是
a.硒元素的最低负化合价为-2
b.二氧化硒(SeO2)具有还原性
c.硒的氧化物对应的水化物属于强酸
(3)氮是自然界各种生物体生命活动不可缺少的重要元素,磷(P)、砷(As)也是氮族元素。
①砷有多种同位素原子,其中稳定的核素是75As,它的中子数为
②已知NH4Cl与PH4I的性质相似,则对PH4I性质的推测不正确的是
a.含有离子键和共价键 b.能与NaOH溶液反应
c.与NH4Cl加热充分分解产物的种类完全一样
③下列关于第VA族元素及其化合物的说法不正确的是
a.热稳定性:NH3>PH3
b.酸性:HNO3>H3AsO4
c. As的氧化物的水化物是强碱
d.形成的简单离子半径随着原子序数递增而增大
您最近一年使用:0次
8 . 元素在周期表中的位置反映了元素的原子结构和性质,矿物白云母是一种重要的化工原料,其化学式的氧化物形式为:K2O·3Al2O3·6SiO2·2H2O。就其组成元素完成下列填空:
(1)Al元素在元素周期表中的位置为_____ ,K2O的电子式为_____ 。
(2)上述元素中(Si、H除外),形成的简单离子的半径最小,该离子与过量氨水反应的离子方程式为_____ 。
(3)根据KH的存在,有人提议可把氢元素放在第ⅦA族,那么根据其最高正价与最低负价的绝对值相等,又可把氢元素放在周期表中的第_____ 族。
(4)某元素R与氧元素同主族,对延长人类寿命起着重要作用,被誉为“生命元素”。已知R元素的原子有4个电子层,则元素R的质子数是_____ 。
(1)Al元素在元素周期表中的位置为
(2)上述元素中(Si、H除外),形成的简单离子的半径最小,该离子与过量氨水反应的离子方程式为
(3)根据KH的存在,有人提议可把氢元素放在第ⅦA族,那么根据其最高正价与最低负价的绝对值相等,又可把氢元素放在周期表中的第
(4)某元素R与氧元素同主族,对延长人类寿命起着重要作用,被誉为“生命元素”。已知R元素的原子有4个电子层,则元素R的质子数是
您最近一年使用:0次
名校
9 . 近年来,我国航空航天事业成果显著,“北斗三号”导航卫星搭载了精密计时的铷(Rb)原子钟。如图为铷元素在元素周期表中的信息和铷的原子结构示意图(如图1)。回答下列问题:
(2)Rb原子第一电子层上电子的能量比最外层上电子的能量_______ (填“低”或“高”)。
(3)如图2中 所示粒子共表示
所示粒子共表示_______ 种元素,铷元素原子的化学性质与如图中_______ (填字母)的化学性质相似。

A.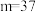 , ,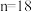 | B.铷是金属元素 |
| C.铷的相对原子质量是85.47 | D.铷原子有5个电子层,最外层有1个电子 |
(3)如图2中
 所示粒子共表示
所示粒子共表示
您最近一年使用:0次
2022-09-07更新
|
410次组卷
|
4卷引用:浙江省金华市曙光学校2022-2023学年高一上学期第一次阶段考试(10月)化学试题
2022高三·全国·专题练习
解题方法
10 . 回答下列问题:
(1)根据“原子序数”推导元素
①56号元素位于第___________ 周期___________ 族。
②114号元素位于第___________ 周期___________ 族。
③35号元素位于第___________ 周期___________ 族。
(2)根据“元素符号”填空(前20号元素)
①主族序数与周期数相同的元素有___________ 。
②主族序数是周期数2倍的元素有___________ ,主族序数是周期数3倍的元素有___________ 。
③周期数是主族序数2倍的元素有___________ ,周期数是主族序数3倍的元素有___________ 。
(3)用“元素符号”填空
①最高正价与最低负价代数和为0的短周期元素是___________ 。
②最高正价是最低负价绝对值3倍的短周期元素是___________ 。
(4)①甲、乙是元素周期表中同一主族的两种元素,若甲的原子序数为x,则乙的原子序数不可能是___________ (填序号)。
A.x+2 B.x+4
C.x+8 D.x+18
②若甲、乙分别是同一周期的ⅡA族和ⅢA族元素,原子序数分别为m和n。则下列关于m和n的关系不正确的是___________ (填序号)。
A.n=m+1 B.n=m+18
C.n=m+25 D.n=m+11
(1)根据“原子序数”推导元素
①56号元素位于第
②114号元素位于第
③35号元素位于第
(2)根据“元素符号”填空(前20号元素)
①主族序数与周期数相同的元素有
②主族序数是周期数2倍的元素有
③周期数是主族序数2倍的元素有
(3)用“元素符号”填空
①最高正价与最低负价代数和为0的短周期元素是
②最高正价是最低负价绝对值3倍的短周期元素是
(4)①甲、乙是元素周期表中同一主族的两种元素,若甲的原子序数为x,则乙的原子序数不可能是
A.x+2 B.x+4
C.x+8 D.x+18
②若甲、乙分别是同一周期的ⅡA族和ⅢA族元素,原子序数分别为m和n。则下列关于m和n的关系不正确的是
A.n=m+1 B.n=m+18
C.n=m+25 D.n=m+11
您最近一年使用:0次



