名校
1 . 下表是元素周期表的一部分,请依据该表回答问题。
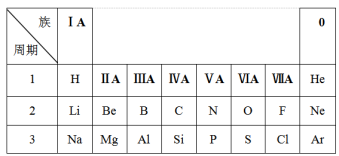
(1)第2周期VIIA族元素的原子结构示意图是___________ ,该元素与同周期IA族元素组成的化合物类型是___________ (填“离子化合物”或“共价化合物”)。
(2)第3周期元素的最高价氧化物对应水化物中,碱性最强的是___________ (填化学式,下同);具有两性的是___________ 。加热时,碳单质能与S的最高价氧化物对应的水化物的浓溶液反应,写出该反应的化学方程式___________ 。
(3)下列判断正确的是___________(填标号)。

(1)第2周期VIIA族元素的原子结构示意图是
(2)第3周期元素的最高价氧化物对应水化物中,碱性最强的是
(3)下列判断正确的是___________(填标号)。
| A.最低负化合价的绝对值:P>S |
| B.非金属性:P>N |
| C.离子半径:Mg2+>O2− |
| D.还原性:S2−>Cl− |
您最近一年使用:0次
名校
2 . 1869年,俄国化学家门捷列夫制作了第一张元素周期表,下表是元素周期表的一部分,表中所列的字母分别代表某一化学元素。
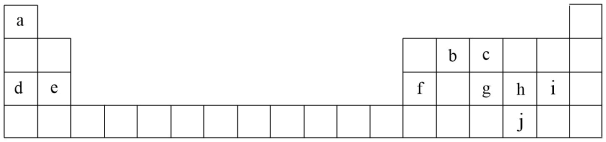
(1)元素c代表的元素是(写元素符号)_______
(2)请写出元素e在元素周期表中所在的位置_______
(3)请画出元素f的简单离子结构示意图_______ 。请写出单质f与d的最高价氧化物对应水化物的离子反应方程式_______ 。
(4)元素a和b能构成最简单的有机化合物(用结构式表示)_______ 。请写出元素a和b构成的最简单有机化合物与i单质发生的第一步化学反应方程式_______ 。
(5)元素h的最高价氧化物对应的水化物呈_______ (酸性、中性或碱性);请写出元素h的最高价氧化物对应的水化物与单质b的化学反应方程式_______ 。

(1)元素c代表的元素是(写元素符号)
(2)请写出元素e在元素周期表中所在的位置
(3)请画出元素f的简单离子结构示意图
(4)元素a和b能构成最简单的有机化合物(用结构式表示)
(5)元素h的最高价氧化物对应的水化物呈
您最近一年使用:0次
2021-09-29更新
|
573次组卷
|
2卷引用:广东省广州市仲元中学2020-2021学年高一下学期期中考试化学试题
名校
解题方法
3 . 下表是元素周期表中的一部分,根据表中给出的10种元素,回答下列问题:
(1)元素f的原子结构示意图为___________ 。
(2)元素g位于元素周期表中第___________ 周期第___________ 族。
(3)元素b有多种同素异形体,写出其中两种的名称___________ 、___________ 。
(4)元素h的最高价氧化物对应水化物的化学式为___________ 。
(5)元素a~j中非金属性最强的是___________ (填元素符号)。
(6)按物质的性质分类,元素i的氧化物属于___________ 氧化物。
(7)e单质和水反应的离子方程式为___________ 。
(8)有3位科学家因在基于a的电池研究方面的成就获得了2019年诺贝尔化学奖。基于e的电池也日益受到重视。下列关于a和e的说法不正确的有___________ (填字母序号)。
A.a的金属性比e强 B.a的原子半径比e大
C.自然界中,e的储量比a高 D.基于a的电池质量轻、易携带
| a | b | c | d | ||||||||||||||
| e | f | g | h | ||||||||||||||
| i | j |
(1)元素f的原子结构示意图为
(2)元素g位于元素周期表中第
(3)元素b有多种同素异形体,写出其中两种的名称
(4)元素h的最高价氧化物对应水化物的化学式为
(5)元素a~j中非金属性最强的是
(6)按物质的性质分类,元素i的氧化物属于
(7)e单质和水反应的离子方程式为
(8)有3位科学家因在基于a的电池研究方面的成就获得了2019年诺贝尔化学奖。基于e的电池也日益受到重视。下列关于a和e的说法不正确的有
A.a的金属性比e强 B.a的原子半径比e大
C.自然界中,e的储量比a高 D.基于a的电池质量轻、易携带
您最近一年使用:0次
名校
4 . 元素周期表短周期的一部分如图所示。回答下列问题:
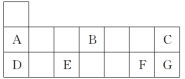
(1)A的元素符号为__________ 。
(2)B位于第二周期第__________ 族,DC为__________ (填“离子”或“共价”)化合物。
(3)G的最高价氧化物的化学式为__________ 。
(4)A、B、D原子半径由大到小的顺序为______________ (填化学式,下同),C、F、G最简单氢化物热稳定性由弱到强的顺序为__________ 。
(5)E的单质与D的最高价氧化物对应的水化物反应的离子方程式为___________________ 。

(1)A的元素符号为
(2)B位于第二周期第
(3)G的最高价氧化物的化学式为
(4)A、B、D原子半径由大到小的顺序为
(5)E的单质与D的最高价氧化物对应的水化物反应的离子方程式为
您最近一年使用:0次
2021-03-09更新
|
287次组卷
|
4卷引用:广东省深圳市翠园中学2020-2021学年高一下学期期中考试化学试卷
5 . 下图是元素周期表的一部分,针对表中①~⑧元素,填写下列空白:
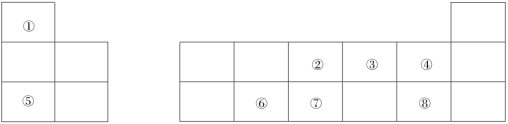
(1)元素⑦在周期表中的位置可表示为第______ 周期第______ 族。
(2)图中8种元素最高价氧化物对应的水化物中,酸性最强的是______ (填化学式,下同),碱性最强的是______ 。
(3)写出由①③元素构成的化合物对应的电子式______ 。(写一种即可)
(4)元素周期表中位于斜对角线的两种元素的化学性质十分相似,称之为“对角线规则”。如金属Be与金属Al的单质及其化合物性质相似。
①写出证明Al2O3是两性氧化物的化学反应的离子方程式:______ ,______ 。
②Be(OH)2和Mg(OH)2可用试剂______ 鉴别。

(1)元素⑦在周期表中的位置可表示为第
(2)图中8种元素最高价氧化物对应的水化物中,酸性最强的是
(3)写出由①③元素构成的化合物对应的电子式
(4)元素周期表中位于斜对角线的两种元素的化学性质十分相似,称之为“对角线规则”。如金属Be与金属Al的单质及其化合物性质相似。
①写出证明Al2O3是两性氧化物的化学反应的离子方程式:
②Be(OH)2和Mg(OH)2可用试剂
您最近一年使用:0次
2021-03-02更新
|
300次组卷
|
3卷引用:广东省汕尾市2020-2021学年高一上学期期末学业质量监测化学试题
6 . 几种主族元素在周期表中的位置如下
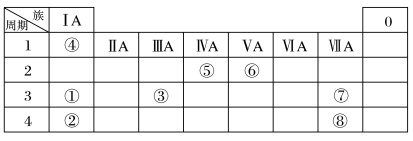
根据上表回答下列问题:
(1)⑥元素的氢化物的电子式是_______ 。
(2)①③⑦三种元素原子半径由大到小的顺序是_______ (用元素符号表示)。
(3)表中某元素原子的核外电子层数是最外层电子数的3倍,该元素的原子结构示意图为_______ ,该元素在周期表中的位置是_______ 。
(4)①②③三种元素最高价氧化物对应水化物碱性最强的是_______ (填化学式),①与③最高价氧化物对应水化物反应的离子方程式为_______ 。
(5)⑦的非金属性强于⑧,从原子结构的角度解释其原因:_______ 。下列表述中能证明这一事实的是_______ (填字母)。
a.⑦的氢化物比⑧的氢化物稳定
b.⑦最高价氧化物对应的水化物的酸性强于 ⑧最高价氧化物对应的水化物的酸性
c.⑦的单质能将⑧从其钠盐溶液中置换出来
d.⑦的氢化物酸性比⑧的氢化物酸性弱
(6)①和④形成的化合物是_______ (填“离子”或“共价”)化合物。

根据上表回答下列问题:
(1)⑥元素的氢化物的电子式是
(2)①③⑦三种元素原子半径由大到小的顺序是
(3)表中某元素原子的核外电子层数是最外层电子数的3倍,该元素的原子结构示意图为
(4)①②③三种元素最高价氧化物对应水化物碱性最强的是
(5)⑦的非金属性强于⑧,从原子结构的角度解释其原因:
a.⑦的氢化物比⑧的氢化物稳定
b.⑦最高价氧化物对应的水化物的酸性强于 ⑧最高价氧化物对应的水化物的酸性
c.⑦的单质能将⑧从其钠盐溶液中置换出来
d.⑦的氢化物酸性比⑧的氢化物酸性弱
(6)①和④形成的化合物是
您最近一年使用:0次
2021-02-23更新
|
1018次组卷
|
3卷引用:广东省汕头市潮阳区2020-2021学年高一上学期期末考试化学试题
广东省汕头市潮阳区2020-2021学年高一上学期期末考试化学试题(已下线)第1章 物质结构 元素周期律(基础过关卷)-2020-2021学年高一化学必修2章末集训必刷卷(人教版)云南省昆明市四川师范大学昆明实验学校安宁校区2020-2021学年高二下学期入学化学试题
解题方法
7 . 联合国大会将2019年定为“化学元素周期表国际年”,显示了元素周期表的重要性。下表列出了a-j 10种元素在周期表中的位置:
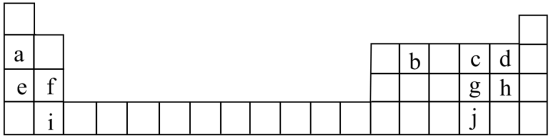
(1)元泰a的原于结构示意图为__________ 。
(2)元素b可以形成多种单质,写出其中的两种____________________ (填名称)。
(3)元素a~j中非金属性最强的是___________ (填元素符号)。
(4)若e单质着火,可用于灭火的物质是___________ (填字母)
A 自来水 B CO2. C 干沙子 D 湿抹布
(5)元素h和i形成的化合物中化学键的类型是___________ 键。h单质与NaOH溶液反应的离子方程式为____________ 。
(6)3位科学家因在基于a的电池研究方面的成就获得了2019年诺贝尔化学奖。基于e的电池也日益受到重视。下列关于a和e的说法正确的有___________ (填字母)。
A a的金属性比e弱 B 自然界中,e的储量比a高
B a的原子半径比e大 D 基于a的电池质量轻、易携带

(1)元泰a的原于结构示意图为
(2)元素b可以形成多种单质,写出其中的两种
(3)元素a~j中非金属性最强的是
(4)若e单质着火,可用于灭火的物质是
A 自来水 B CO2. C 干沙子 D 湿抹布
(5)元素h和i形成的化合物中化学键的类型是
(6)3位科学家因在基于a的电池研究方面的成就获得了2019年诺贝尔化学奖。基于e的电池也日益受到重视。下列关于a和e的说法正确的有
A a的金属性比e弱 B 自然界中,e的储量比a高
B a的原子半径比e大 D 基于a的电池质量轻、易携带
您最近一年使用:0次
2020-12-04更新
|
549次组卷
|
2卷引用:2020年7月广东省普通高中学业水平合格性考试化学试卷
名校
8 . 下表是元素周期表的一部分,回答下列有关问题(用化学符号回答):
(1)写出序号对应的元素符号:①________ ;④__________ ;⑤_________ ;
(2)在①~⑨元素中,最活泼的金属元素是________ ,最活泼的非金属元素是_______ 。
(3)在①~⑨元素的最高价氧化物对应的水化物中,碱性最强的是___________ ,呈两性的是____________ 。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | H | He | ||||||
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(1)写出序号对应的元素符号:①
(2)在①~⑨元素中,最活泼的金属元素是
(3)在①~⑨元素的最高价氧化物对应的水化物中,碱性最强的是
您最近一年使用:0次
2020-12-02更新
|
509次组卷
|
2卷引用:广东省珠海市北京师范大学珠海分校附属外国语学校2020-2021学年高二上学期期中考试化学试题(B卷)
名校
9 . 下表为元素周期表的一部分,请参照元素①一④在表中的位置回答下列问题:
(1)③、⑤、⑥的离子半径由大到小的顺序为____________ '(用离子符号表示)。
(2)写出⑤和⑥的最高价氧化物的水化物相互反应的化学方程式_______________
(3)②的某核素可用于文物年代的测定,该核素有8个中子,该核素的符号是______
(4)比较元素②、⑦和⑧的最高价氧化物的水化物的酸性大小_____
(5)①④两种元素可组成的一种既有极性共价键也有非极性共价键的化合物,写出该物质的电子式______
(6)①和④的单质可组成燃料电池,正极反应物为_____ (用化学式表示,下同),若电解溶液为稀硫酸,写出负极的电极反应__________
族 周期 | IA | 0 | ||||||
| 1 | ① | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ |
(1)③、⑤、⑥的离子半径由大到小的顺序为
(2)写出⑤和⑥的最高价氧化物的水化物相互反应的化学方程式
(3)②的某核素可用于文物年代的测定,该核素有8个中子,该核素的符号是
(4)比较元素②、⑦和⑧的最高价氧化物的水化物的酸性大小
(5)①④两种元素可组成的一种既有极性共价键也有非极性共价键的化合物,写出该物质的电子式
(6)①和④的单质可组成燃料电池,正极反应物为
您最近一年使用:0次
13-14高一·全国·课时练习
名校
解题方法
10 . 结合元素周期表回答下列问题:
(1)下图中的实线是元素周期表的部分边界,请在图中用实线补全元素周期表的边界___________ 。

(2)周期表中所列元素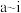 ,属于短周期元素的有
,属于短周期元素的有__________ 种,属于主族元素的有__________ 种;g元素位于第__________ 周期第__________ 族;i元素位于第__________ 周期第__________ 族。
(3)f元素位于第__________ 周期第__________ 族,原子结构示意图为__________ 请在下图方框中按氦元素的式样写出该元素的原子序数,元素符号、元素名称、相对原子质量__________ 。
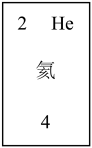

(1)下图中的实线是元素周期表的部分边界,请在图中用实线补全元素周期表的边界

(2)周期表中所列元素
 ,属于短周期元素的有
,属于短周期元素的有(3)f元素位于第


您最近一年使用:0次
2020-10-02更新
|
581次组卷
|
13卷引用:广东省东莞市光明中学2020-2021学年高二上学期期初考试化学试题
广东省东莞市光明中学2020-2021学年高二上学期期初考试化学试题(已下线)2014学年高一化学人教版必修2 1.1.1元素周期表练习卷山东峨山一中2018年3月高一月考(化学试卷)峨山县第一中学2017-2018学年第二学期3月份月考卷(高二化学)2017-2018学年鲁科版高一化学必修二第一章第二节基础题2019—2020学年人教版必修2第一章 第一节《元素周期表》第1课时 《元素周期表》(跟踪训练)苏教版高一化学必修2专题一第一单元第三课时《元素周期表》课时训练(夯实基础)河北深州市长江中学2019-2020学年高一下学期第一次月考化学试题(已下线)4.1.1 原子结构 元素周期表 核素练习(2)——《高中新教材同步备课》(人教版 必修第一册)人教版(2019)高一必修第一册 第四章 物质结构 元素周期律 第一节 原子结构与元素周期表 教材帮(已下线)第8单元 原子结构 元素周期律(A卷 基础过关检测)-2021年高考化学一轮复习单元滚动双测卷(已下线)4.1.2 元素周期表(重点练)-2020-2021学年高一化学上学期十分钟同步课堂专练(人教版2019必修第一册)(已下线)4.1.2 元素周期表-2020-2021学年高一化学同步课堂帮帮帮(人教版2019必修第一册)



