名校
解题方法
1 . 离子液体M的结构如图所示,下列说法错误的是
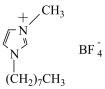

| A.电负性由大到小的顺序是F>N>B |
| B.阴离子的空间结构为正四面体形 |
| C.M因含有机基团而使其熔点较低 |
| D.M分子中C-C键的键能大于C-N键的键能 |
您最近一年使用:0次
名校
解题方法
2 . 铜、镓、硒、硅等元素的化合物是生产第三代太阳能电池的重要材料。请回答:
(1)基态铜原子的电子排布式为_______ 。
(2)硒、硅均能与氢元素形成气态氢化物,则它们形成的组成最简单的氢化物中,分子构型分别为_______ 、_______ ,若“Si—H”中共用电子对偏向氢元素,氢气与硒反应时单质硒是氧化剂,则硒与硅的电负性相对大小为Se_______ Si(填“>”、“<”)。
(3)SeO2常温下为白色晶体,熔点为340~350℃,315℃时升华,则SeO2固体的晶体类型为_______ ;若SeO2类似于SO2是V型分子,则Se原子外层轨道的杂化类型为_______ 。
(4)与镓元素处于同一主族的硼元素具有缺电子性(价电子数少于价层轨道数),其化合物可与具有孤对电子的分子或离子生成配合物,如BF3能与NH3反应生成BF3·NH3,在.BF3·NH3中B原子的杂化轨道类型为_______ ,B与N之间形成_______ 键。
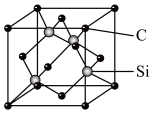
(5)金刚砂(SiC)的硬度为9.5,其晶胞结构如图所示;则金刚砂晶体类型为_______ ,在SiC中,每个C原子周围距离最近且相等的C原子数目为_______ 个;若晶胞的边长为a pm,则金刚砂的密度表达式为_______ g/cm3。
(1)基态铜原子的电子排布式为
(2)硒、硅均能与氢元素形成气态氢化物,则它们形成的组成最简单的氢化物中,分子构型分别为
(3)SeO2常温下为白色晶体,熔点为340~350℃,315℃时升华,则SeO2固体的晶体类型为
(4)与镓元素处于同一主族的硼元素具有缺电子性(价电子数少于价层轨道数),其化合物可与具有孤对电子的分子或离子生成配合物,如BF3能与NH3反应生成BF3·NH3,在.BF3·NH3中B原子的杂化轨道类型为
(5)金刚砂(SiC)的硬度为9.5,其晶胞结构如图所示;则金刚砂晶体类型为

您最近一年使用:0次
名校
解题方法
3 . 下列排序正确的是
A.电负性: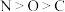 | B.键角: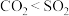 |
C.熔点: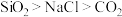 | D.沸点:新戊烷>异戊烷>正戊烷 |
您最近一年使用:0次
解题方法
4 . 铜元素可形成多种重要化合物。回答下列问题:
(1)铜元素位于元素周期表中的_____ 区,其基态原子的价电子排布图为_________ 。
(2)往硫酸铜溶液中加入过量氨水,可形成[Cu(NH3)4]SO4溶液,该溶液可用于溶解纤维素。
①[Cu(NH3)4]SO4中阴离子的立体构型是__________ 。
②在[Cu(NH3)4]SO4中,Cu2+与NH3 之间形成的化学键称为______ ,提供孤电子对的成键原子是_________ 。
③除硫元素外,[Cu(NH3)4]SO4中所含元素的电负性由小到大的顺序为________ 。
④NF3与NH3 的空间构型相同,中心原子的轨道杂化类型均为_________ 。但NF3不易与Cu2+形成化学键,其原因是_______________ 。
(3)一种Hg-Ba-Cu-O高温超导材料的晶胞(长方体)如图所示。
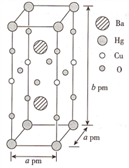
①该物质的化学式为__________ 。
②已知该晶胞中两个Ba2+的间距为c pm.则距离Ba2+最近的Hg+数目为_____ 个,二者的最短距离为_______ pm。(列出计算式即可,下同)
③设该物质的摩尔质量为M,阿伏伽德罗常数的值为NA,则该晶体的密度为______ g·cm-3。
(1)铜元素位于元素周期表中的
(2)往硫酸铜溶液中加入过量氨水,可形成[Cu(NH3)4]SO4溶液,该溶液可用于溶解纤维素。
①[Cu(NH3)4]SO4中阴离子的立体构型是
②在[Cu(NH3)4]SO4中,Cu2+与NH3 之间形成的化学键称为
③除硫元素外,[Cu(NH3)4]SO4中所含元素的电负性由小到大的顺序为
④NF3与NH3 的空间构型相同,中心原子的轨道杂化类型均为
(3)一种Hg-Ba-Cu-O高温超导材料的晶胞(长方体)如图所示。

①该物质的化学式为
②已知该晶胞中两个Ba2+的间距为c pm.则距离Ba2+最近的Hg+数目为
③设该物质的摩尔质量为M,阿伏伽德罗常数的值为NA,则该晶体的密度为
您最近一年使用:0次
2017-12-27更新
|
353次组卷
|
4卷引用:河北省沧州市普通高中高三上学期教学质量监测(联考)化学试题
河北省沧州市普通高中高三上学期教学质量监测(联考)化学试题2020高考化学二轮总复习高分必备 题型专题2 非选择题专练(已下线)考点14 物质结构与性质(选考)-2020年高考化学命题预测与模拟试题分类精编(已下线)2021年高考化学押题预测卷(湖南卷)(01)(含考试版、答题卡、参考答案、全解全析)
5 . A~G是周期表中1~36号的元素,它们的原子序数依次递增且分别位于前四周期的各个周期中。对它们的性质及结构的描述如下:
A的基态原子只有一种形状的电子云,并容易形成共价键;B的基态原子有3个不同的能级,各能级中电子数相等;C与B同周期,其第一电离能高于周期表中与之相邻的元素;D的基态原子2p能级上的未成对电子数与B原子相同;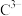 与E2+具有相同的稳定的电子层结构;F元素在周期表中位于C元素的下一周期,其电负性在同周期元素中最大;G元素的基态原子在前四周期中未成对电子数最多。
与E2+具有相同的稳定的电子层结构;F元素在周期表中位于C元素的下一周期,其电负性在同周期元素中最大;G元素的基态原子在前四周期中未成对电子数最多。
(1)A的元素符号为___________ ,基态G原子的电子排布式为___________ ,与G同周期的所有元素的基态原子中最外层电子数与G原子相同的元素有___________ (填元素符号)。
(2)B、C、D三种元素第一电离能从大到小的顺序是___________ ,三种元素的电负性大小顺序为___________ (填元素符号)。
(3)已知元素的电负性C>F,则C元素与F元素形成的化合物CF3中C的化合价为___________ 价,CF3与水发生水解反应的化学方程式为___________ 。
(4)E与C元素形成的化合物的化学式为___________ 。
A的基态原子只有一种形状的电子云,并容易形成共价键;B的基态原子有3个不同的能级,各能级中电子数相等;C与B同周期,其第一电离能高于周期表中与之相邻的元素;D的基态原子2p能级上的未成对电子数与B原子相同;
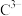 与E2+具有相同的稳定的电子层结构;F元素在周期表中位于C元素的下一周期,其电负性在同周期元素中最大;G元素的基态原子在前四周期中未成对电子数最多。
与E2+具有相同的稳定的电子层结构;F元素在周期表中位于C元素的下一周期,其电负性在同周期元素中最大;G元素的基态原子在前四周期中未成对电子数最多。(1)A的元素符号为
(2)B、C、D三种元素第一电离能从大到小的顺序是
(3)已知元素的电负性C>F,则C元素与F元素形成的化合物CF3中C的化合价为
(4)E与C元素形成的化合物的化学式为
您最近一年使用:0次
6 . 下列有关元素周期表及元素周期律的说法错误的是
| A.N能层的能级数最多为3个 |
| B.Cu元素在元素周期表的ds区 |
| C.F元素在同周期中电负性最大 |
| D.根据对角线规则,铍和铝的化学性质具有相似性 |
您最近一年使用:0次
2017-02-17更新
|
400次组卷
|
7卷引用:2016-2017学年河北省邢台市高二上学期第四次月考化学卷
名校
7 . 由H、C和与C处于同周期的X、Y四种元素组成的穴醚的结构如图,所有原子均满足稳定结构,其空腔直径大约为260~320pm。下列说法正确的是

| 离子 | 直径/pm |
 | 204 |
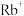 | 304 |
A.电负性: |
| B.简单氢化物的沸点:X>Y |
C.键角: |
D.该穴醚可与 通过配位键形成超分子,对 通过配位键形成超分子,对 进行识别 进行识别 |
您最近一年使用:0次
8 . 下列说法正确的是
| A.由电负性数值:铍—1.5;氯—3.0可推知氯化氨中是离子键 |
| B.根据对角线规可知Li在空气中燃烧会生成Li3N和Li2O |
| C.H—O键能为QkJ/mol,则1molH2分解生成和O2需要吸收2QkJ能量 |
| D.稀有气体一般很难参与反应,是因为其分子内的键能很大,很难断裂 |
您最近一年使用:0次
名校
9 . 下列说法正确的是( )
| A.元素原子的最外层电子数等于元素的最高正化合价 |
| B.多电子原子中,在离核较近的区域内运动的电子能量较高 |
| C.S、Cl的电负性和单质的氧化性均依次增强 |
| D.元素周期表中位于金属元素和非金属元素分界线附近的元素属于过渡元素 |
您最近一年使用:0次
2020-03-26更新
|
93次组卷
|
4卷引用:河北省正定中学2019-2020学年高二3月线上月考化学试题
名校
解题方法
10 .  、
、 、
、 与
与 形成的某种化合物是蛋白质代谢分解的终产物,结构如图所示,工业上常用
形成的某种化合物是蛋白质代谢分解的终产物,结构如图所示,工业上常用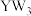 和
和 在一定条件下合成。下列判断错误的是
在一定条件下合成。下列判断错误的是
 、
、 、
、 与
与 形成的某种化合物是蛋白质代谢分解的终产物,结构如图所示,工业上常用
形成的某种化合物是蛋白质代谢分解的终产物,结构如图所示,工业上常用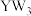 和
和 在一定条件下合成。下列判断错误的是
在一定条件下合成。下列判断错误的是
A.键角: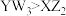 |
B.电负性: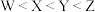 |
C.原子半径: |
D.价电子数: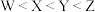 |
您最近一年使用:0次



