名校
解题方法
1 . Fe、Co、Ni是第四周期重要的金属元素,回答下列问题:
(1)基态 的价电子排布图为
的价电子排布图为_______ 。镍易形成 配合物,其熔点为-19.3℃,沸点为43℃,则其晶体类型是
配合物,其熔点为-19.3℃,沸点为43℃,则其晶体类型是_______ ,该配合物中三种元素电负性由大到小的顺序为_______ 。
(2)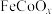 是一种新型光电催化剂,第四电离能大小关系是
是一种新型光电催化剂,第四电离能大小关系是
_______ 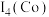 (填“>”、“<”或“=”),原因是
(填“>”、“<”或“=”),原因是_______ 。
(3)二茂铁是一种具有芳香族性质的有机过渡金属化合物,其在工业、农业、医药、航天、节能、环保等行业具有广泛的应用。环戊二烯( )可用于制备二茂铁。
)可用于制备二茂铁。
①环戊二烯中碳原子的杂化方式为_______ 。
②1 mol环戊二烯中有_______ mol  键。
键。
(4) 晶体的晶胞如图甲所示。已知晶胞边长为a nm,阿伏加德罗常数的值为
晶体的晶胞如图甲所示。已知晶胞边长为a nm,阿伏加德罗常数的值为 ,该晶胞中
,该晶胞中 位于
位于 所形成的正八面体的体心,则晶胞密度为
所形成的正八面体的体心,则晶胞密度为_______  。
。
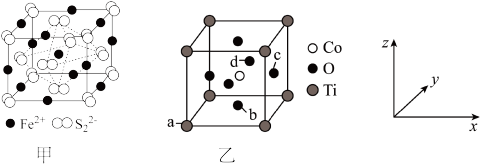
(5)钴的一种化合物晶胞结构如乙图所示。
已知a点的原子坐标参数为 ,b点为
,b点为 ,c点为
,c点为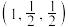 ,则d点的原子坐标参数为
,则d点的原子坐标参数为_______ 。
(1)基态
 的价电子排布图为
的价电子排布图为 配合物,其熔点为-19.3℃,沸点为43℃,则其晶体类型是
配合物,其熔点为-19.3℃,沸点为43℃,则其晶体类型是(2)
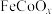 是一种新型光电催化剂,第四电离能大小关系是
是一种新型光电催化剂,第四电离能大小关系是
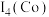 (填“>”、“<”或“=”),原因是
(填“>”、“<”或“=”),原因是(3)二茂铁是一种具有芳香族性质的有机过渡金属化合物,其在工业、农业、医药、航天、节能、环保等行业具有广泛的应用。环戊二烯(
 )可用于制备二茂铁。
)可用于制备二茂铁。①环戊二烯中碳原子的杂化方式为
②1 mol环戊二烯中有
 键。
键。(4)
 晶体的晶胞如图甲所示。已知晶胞边长为a nm,阿伏加德罗常数的值为
晶体的晶胞如图甲所示。已知晶胞边长为a nm,阿伏加德罗常数的值为 ,该晶胞中
,该晶胞中 位于
位于 所形成的正八面体的体心,则晶胞密度为
所形成的正八面体的体心,则晶胞密度为 。
。
(5)钴的一种化合物晶胞结构如乙图所示。
已知a点的原子坐标参数为
 ,b点为
,b点为 ,c点为
,c点为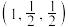 ,则d点的原子坐标参数为
,则d点的原子坐标参数为
您最近一年使用:0次
2 . 填写下列空白:
(1)写出表示含有6个质子、8个中子的原子的化学符号:________ ,该同位素原子在科学研究中有着重要的用途,该用途是_____________
(2)原子序数为113的元素在元素周期表中的位置________ 。
(3)在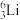 、
、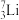 、
、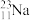 、
、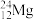 、
、 、
、 中有
中有_______ 种核素
(4)在自然界中许多元素有多种核素,如氧元素存在 、
、 、
、 三种核素,氢元素有
三种核素,氢元素有 、
、  、
、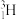 三种核素。
三种核素。
① 、
、 、
、 、
、 四种核数最多可以组成
四种核数最多可以组成______ 种水分子
②请画出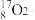 微粒的结构示意图:
微粒的结构示意图:__________________ 。
③现有11g由 和
和 组成的水分子,其中含中子数为
组成的水分子,其中含中子数为_____ mol,电子数为______ 个。
(1)写出表示含有6个质子、8个中子的原子的化学符号:
(2)原子序数为113的元素在元素周期表中的位置
(3)在
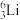 、
、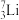 、
、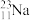 、
、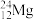 、
、 、
、 中有
中有(4)在自然界中许多元素有多种核素,如氧元素存在
 、
、 、
、 三种核素,氢元素有
三种核素,氢元素有 、
、  、
、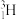 三种核素。
三种核素。①
 、
、 、
、 、
、 四种核数最多可以组成
四种核数最多可以组成②请画出
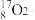 微粒的结构示意图:
微粒的结构示意图:③现有11g由
 和
和 组成的水分子,其中含中子数为
组成的水分子,其中含中子数为
您最近一年使用:0次
名校
解题方法
3 . 金属钛因为其优越的性能被称为“未来金属”,其工业冶炼涉及到的反应如下:TiO2+2C+2Cl2 TiCl4+2CO。回答下列相关问题:
TiCl4+2CO。回答下列相关问题:
(1)基态钛原子的价层电子排布式为____ ,上述反应中非金属元素电负性由大到小是______ ;
(2)已知部分物质熔沸点如下:
自左向右,表中的三种钛的卤化物熔沸点依次升高的原因是__________ 。
(3)配位数为6,组成为TiCl3•6H2O 的晶体有两种:化学式为[TiCl(H2O)5]Cl2•H2O的X呈绿色,定量实验表明,X与AgNO3以1:2物质的量比反应生成沉淀。Y呈紫色,且Y与AgNO3以1:3物质的量之比反应生成沉淀,则Y的化学式为______ 。
(4)钙钛矿是重要的含钛矿物之一。其主要成分Z 的晶胞如图所示。推测Z的化学式为__________ ,Ca填充在O围成的_________ 空隙中。
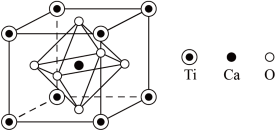
(5)若晶胞参数 a=384.1pm,Z晶体的密度为_________ 列出计算表达式并计算出两位有效数字结果,3.8413≈56.67,阿伏加 德罗常数用 6.0×1023 mol-1)
 TiCl4+2CO。回答下列相关问题:
TiCl4+2CO。回答下列相关问题:(1)基态钛原子的价层电子排布式为
(2)已知部分物质熔沸点如下:
| 名称 | 金红石 | 金刚石 | 四氯化钛 | 四溴化钛 | 四碘化钛 |
| 化学式 | TiO2 | C | TiCl4 | TiBr4 | TiI4 |
| 熔点/℃ | 1830 | 3550 | -24.1 | 38 | 150 |
| 沸点/℃ | 2927 | 4827 | 136.4 | 233.1 | 377.2 |
自左向右,表中的三种钛的卤化物熔沸点依次升高的原因是
(3)配位数为6,组成为TiCl3•6H2O 的晶体有两种:化学式为[TiCl(H2O)5]Cl2•H2O的X呈绿色,定量实验表明,X与AgNO3以1:2物质的量比反应生成沉淀。Y呈紫色,且Y与AgNO3以1:3物质的量之比反应生成沉淀,则Y的化学式为
(4)钙钛矿是重要的含钛矿物之一。其主要成分Z 的晶胞如图所示。推测Z的化学式为

(5)若晶胞参数 a=384.1pm,Z晶体的密度为
您最近一年使用:0次
2020-04-05更新
|
360次组卷
|
2卷引用:陕西省宜川中学2019-2020学年高三4月月考化学试题
名校
解题方法
4 . 对Na、Mg、Al的有关性质的叙述正确的是
| A.碱性:NaOH< Mg(OH)2< Al(OH)3 |
| B.第一电离能:Na< Mg <Al |
| C.电负性:Na> Mg >Al |
| D.熔点:Na< Mg< Al |
您最近一年使用:0次
2019-06-29更新
|
129次组卷
|
2卷引用:陕西省黄陵中学高新部2018-2019学年高二下学期期末考试化学试题
2013·陕西延安·一模
名校
解题方法
5 . 2010年上海世博会场馆,大量的照明材料或屏幕都使用了发光二极管(LED)。目前市售LED品片,材质基本以GaAs(砷化镓)、AlGaInP(磷化铝镓铟)、lnGaN(氮化铟镓)为主。已知镓是铝同族下一周期的元素。砷化镓的晶胞结构如图。试回答:
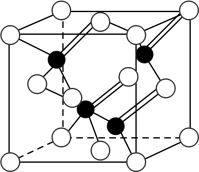
(1)镓的基态原子的电子排布式是_________________ 。
(2)砷化镓晶胞中所包含的砷原子(白色球)个数为___________ ,与同一个镓原子相连的砷原子构成的空间构型为______________ 。
(3)N、P、As处于同一主族,其氢化物沸点由高到低的顺序是________ 。 (用氢化物分子式表示)
(4)砷化镓可由(CH3)3Ga和AsH3在700℃时制得。(CH3)3Ga中镓原子的杂化方式为___________ 。
(5)比较二者的第一电离能:As______ Ga(填“<”、“>”或“=”)。
(6)下列说法正确的是_____________(填字母)。

(1)镓的基态原子的电子排布式是
(2)砷化镓晶胞中所包含的砷原子(白色球)个数为
(3)N、P、As处于同一主族,其氢化物沸点由高到低的顺序是
(4)砷化镓可由(CH3)3Ga和AsH3在700℃时制得。(CH3)3Ga中镓原子的杂化方式为
(5)比较二者的第一电离能:As
(6)下列说法正确的是_____________(填字母)。
| A.砷化镓晶胞结构与NaCl相同 | B.GaP与GaAs互为等电子体 |
| C.电负性:As>Ga | D.砷化镓晶体中含有配位键 |
您最近一年使用:0次
2016-12-09更新
|
996次组卷
|
3卷引用:2013届陕西省延安市秋高考模拟理综化学试卷
(已下线)2013届陕西省延安市秋高考模拟理综化学试卷2016-2017学年高中化学选修3(人教版)第三章 晶体结构与性质 章末检测新疆乌鲁木齐市第四中学2021-2022学年高二下学期期末考试化学试题
9-10高二下·吉林·期中
名校
6 . 下列元素的电负性最大的是:
| A.Na | B.S | C.O | D.C |
您最近一年使用:0次
2016-08-19更新
|
115次组卷
|
12卷引用:陕西省黄陵中学高新部2018-2019学年高二下学期期末考试化学试题
陕西省黄陵中学高新部2018-2019学年高二下学期期末考试化学试题(已下线)2009一2010年度吉林一中下学期高二期中考试化学卷(已下线)2011-2012学年山东省泰安宁阳二中高二下学期期末考试化学试卷(已下线)2012-2013学年云南省芒市中学高二上学期期中考试化学试卷(已下线)2012-2013学年福建省师大附中高二下学期期末考试化学试卷2015-2016学年福建省师大附中高二上期末理化学试卷2015-2016学年四川省雅安市高二上学期期末考试化学试卷2015-2016学年吉林省辽源市田家炳高中高二下期中化学试卷2015-2016学年吉林省汪清六中高二下学期期末化学试卷2015-2016学年辽宁省葫芦岛市六校协作体联考高二下期中化学试卷福建省莆田第八中学2018-2019学年高二下学期期中考试化学试题(已下线)课时54 原子结构与性质-2022年高考化学一轮复习小题多维练(全国通用)



